文档内容
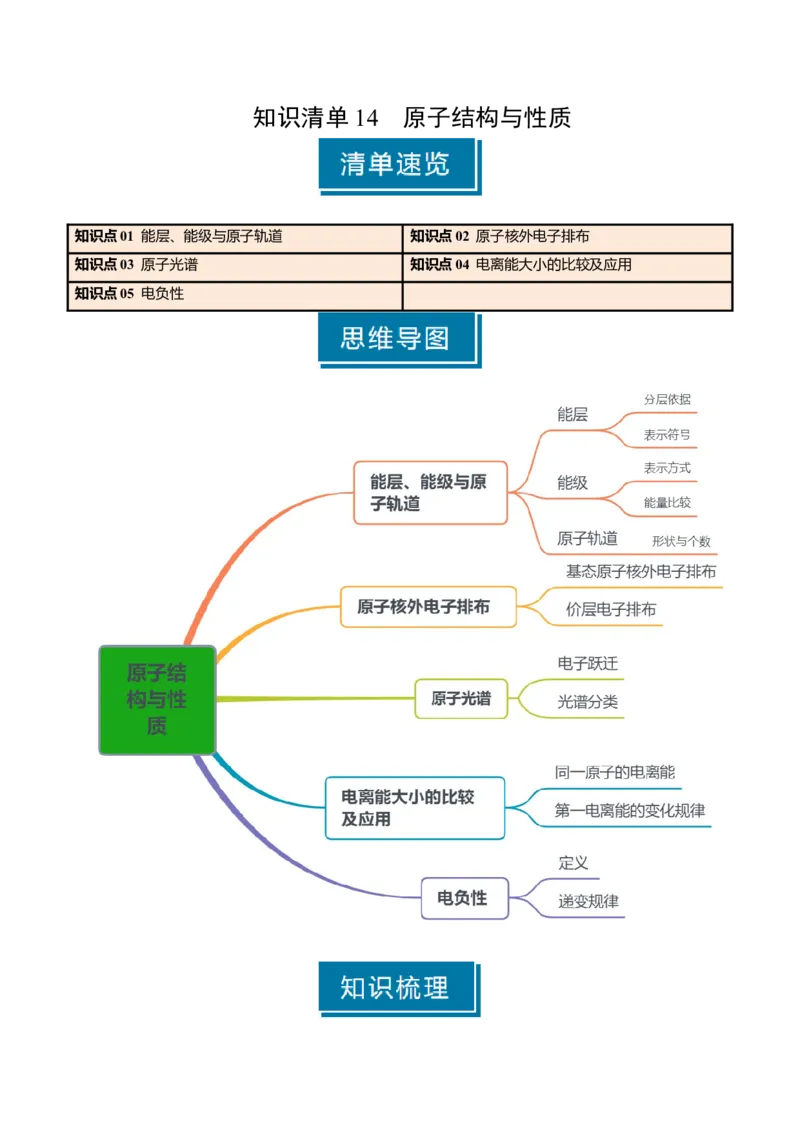
知识清单 14 原子结构与性质
知识点01 能层、能级与原子轨道 知识点02 原子核外电子排布
知识点03 原子光谱 知识点04 电离能大小的比较及应用
知识点05 电负性知识点 01 能层、能级与原子轨道
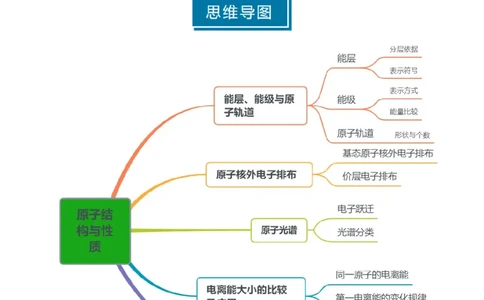
能层、能级与原子轨道的含义
1.能层(n):(又称: )
(1)分层依据:按照电子的 差异
(2)表示符号:K、L、M、N、O、P、Q
2.能级:在多电子原子中,同一能层里电子的_ __也可能不同,又将其分成不同的能级,通常用
等表示,同一能层里,各能级的能量按_ _的顺序依次升高,即_ _。
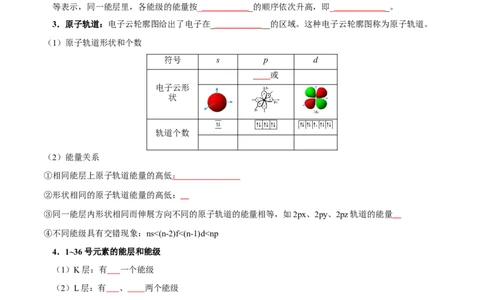
3.原子轨道:电子云轮廓图给出了电子在_ __的区域。这种电子云轮廓图称为原子轨道。
(1)原子轨道形状和个数
符号 s p d
或
电子云形
状
轨道个数
(2)能量关系
①相同能层上原子轨道能量的高低:
②形状相同的原子轨道能量的高低:
③同一能层内形状相同而伸展方向不同的原子轨道的能量相等,如2px、2py、2pz轨道的能量
④不同能级具有交错现象:ns<(n-2)f<(n-1)dO>F>C( )
(2)元素的电负性越大,非金属性越强,第一电离能也越大( )
(3)主族元素的电负性越大,元素原子的第一电离能一定越大( )
(4)第一电离能O>N。( )
(5)钠元素的第一、第二电离能分别小于镁元素的第一、第二电离能。( )
(6)根据元素周期律,原子半径Ga小于As,第一电离能Ga大于As。( )
(7)最外层电子排布为ns2np6(当只有K层时为1s2)的原子第一电离能较大。( )1.填空。
(1)N、O、S的第一电离能 大小为 ,原因是 。
(2)Li及其周期表中相邻元素的第一电离能 如表所示。 ,原因是 。
,原因是 。
520 900 801
Na Mg Al
496 738 578
(3)下列状态的镁中,电离最外层一个电子所需能量最大的是_______(填标号)。
A. B. C. D.
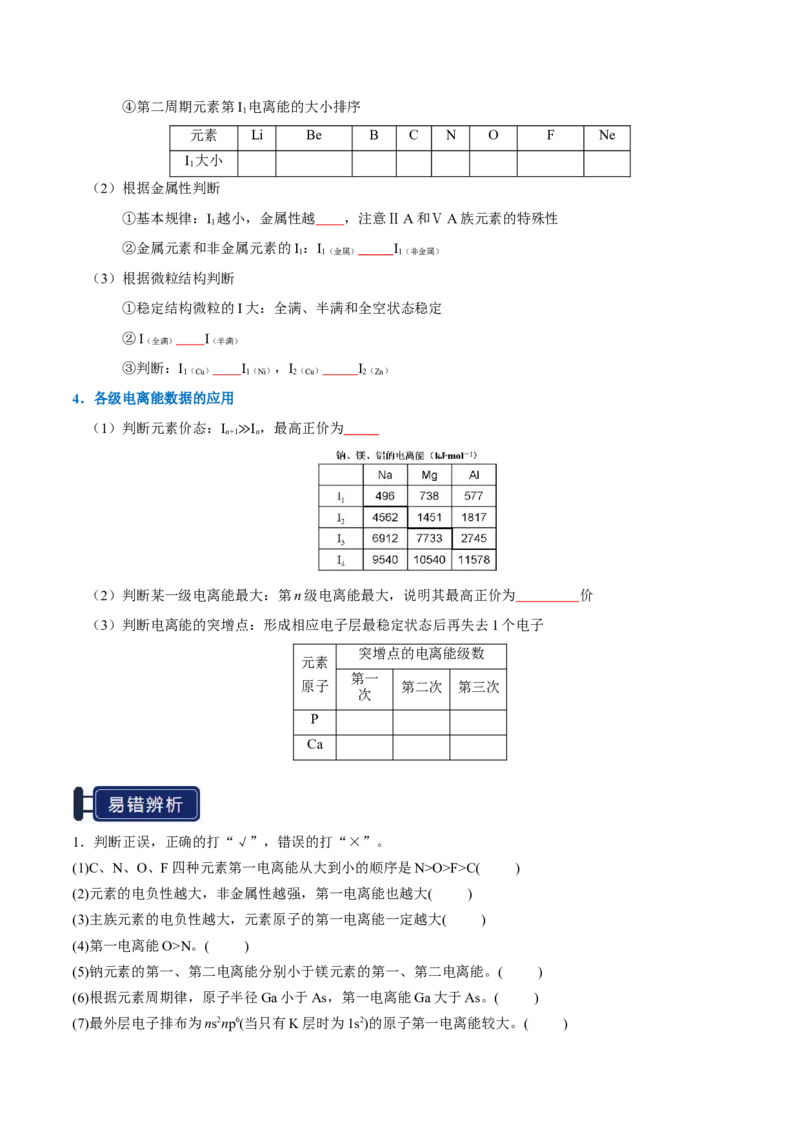
2.图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图
是 (填标号),判断的根据是 ;第三电离能的变化图是 (填标号)。
a. b. c.
知识点 05 电负性1.意义:衡量元素的原子在化合物中 能力
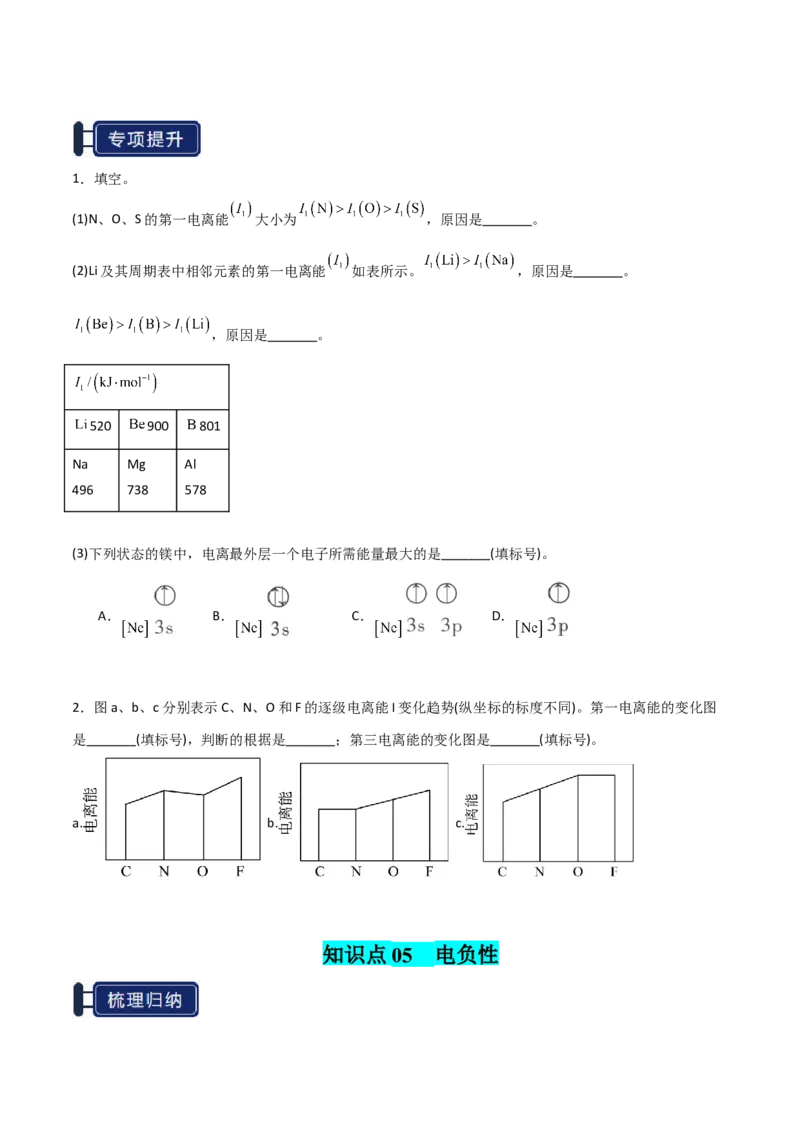
2.递变规律
(1)周期表 角 元素的最大
(2)电负性大小
①电负性最大的前三种元素: > >
②氢元素的电负:C H B;P H Si
3.其他判断方法
(1)根据共用电子对的偏向判断:偏向一方元素的电负性
(2)化合物中化合价的正负判断:显负价元素的电负性
(3)根据元素的非金属性判断
①最高价氧化物对应水化物的酸性越强,电负性越
②单质与氢气越容易化合,电负性越
③气态氢化物越稳定,电负性越
4.判断化合物的类型
(1)差值:|△X|>1.7, 化合物
(2)差值:|△X|<1.7, 化合物
5.根据电负性写水解方程式
(1)水解原理
①电负性大的原子显 ,结合水中的
②电负性小的原子显 ,结合水中的
(2)实例
①BrI
②NCl :
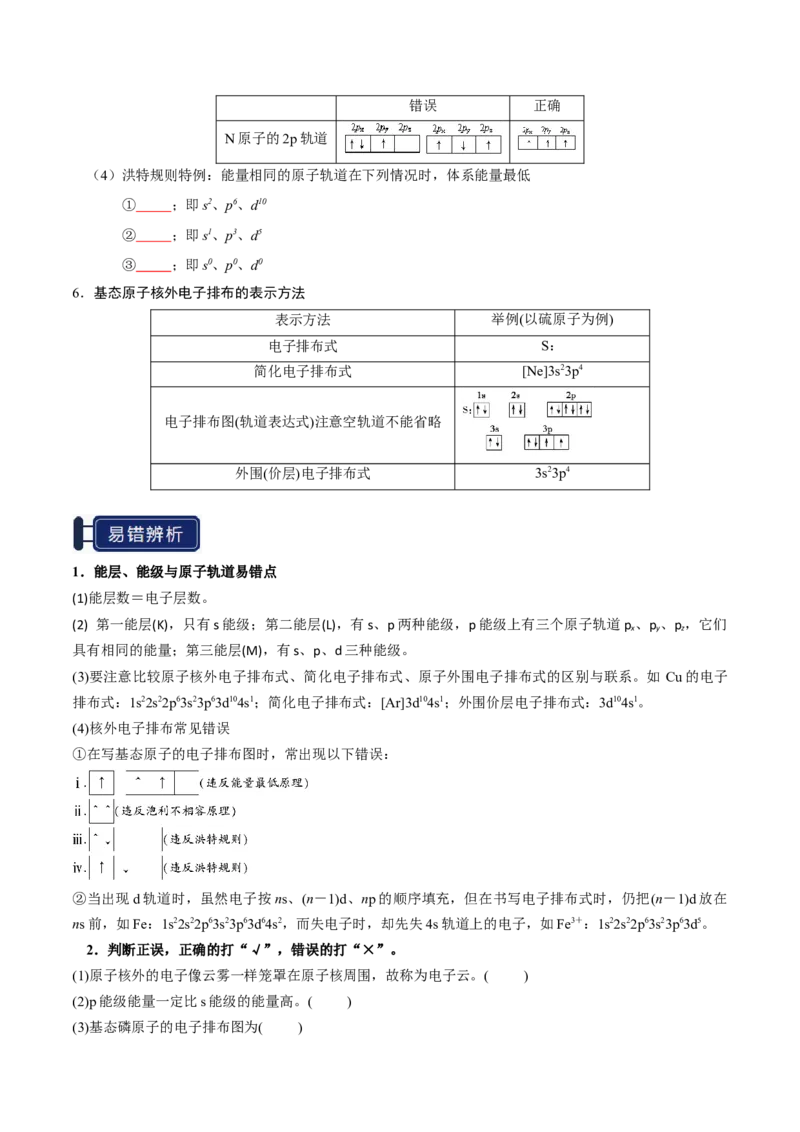
31.判断正误,正确的打“√”,错误的打“×”。
(1)B和N相比,电负性较大的是N( )
(2)元素的电负性越大,非金属性越强,第一电离能也越大( )
(3)电负性大的元素非金属性强( )
(4)主族元素的电负性越大,元素原子的第一电离能一定越大( )
(5)在元素周期表中,同周期元素电负性从左到右越来越大( )
(6)金属元素电负性一定小于非金属元素电负性( )
(7)在形成化合物时,电负性越小的元素越容易显示正价。( )
1.侯氏制碱法工艺流程中的主反应为 ,其中W、X、Y、Z、Q、R分
别代表相关化学元素。下列说法正确的是
A.原子半径: B.第一电离能:
C.单质沸点: D.电负性:
2.Ga、As、Se位于元素周期表第四周期。下列说法正确的是
A.原子半径:
B.第一电离能:
C.元素电负性:
D.可在周期表中Se附近寻找优良的催化剂材料