文档内容
第 1 讲 物质的量 气体摩尔体积(练)
第一部分:高考真题感悟
1.(2022·广东·高考真题)我国科学家进行了如图所示的碳循环研究。下列说法正确的是
A.淀粉是多糖,在一定条件下能水解成葡萄糖
B.葡萄糖与果糖互为同分异构体,都属于烃类
C. 中含有 个电子
D. 被还原生成
2.(2022·浙江·高考真题)设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.在25℃时,1LpH为12的Ba(OH) 溶液中含有OH-数目为0.01N
2 A
B.1.8g重水(D O)中所含质子数为N
2 A
C.足量的浓盐酸与8.7gMnO 反应,转移电子的数目为0.4N
2 A
D.32g甲醇的分子中含有C—H键的数目为4N
A
3.(2022·全国·高考真题) 为阿伏加德罗常数的值,下列说法正确的是
A.25℃, 下, 氢气中质子的数目为
B. 溶液中, 的数目为
C. 苯甲酸完全燃烧,生成 的数目为
D.电解熔融 ,阴极增重 ,外电路中通过电子的数目为
4.(2022·浙江·高考真题)设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.在25℃时,1LpH为12的Ba(OH) 溶液中含有OH-数目为0.01N
2 A
B.1.8g重水(D O)中所含质子数为N
2 AC.足量的浓盐酸与8.7gMnO 反应,转移电子的数目为0.4N
2 A
D.32g甲醇的分子中含有C—H键的数目为4N
A
5.(2021·湖北·高考真题)N 为阿伏加德罗常数的值。下列说法错误的是
A
A.23gCHCHOH中sp3杂化的原子数为N
3 2 A
B.0.5molXeF 中氙的价层电子对数为3N
4 A
C.1mol[Cu(H O) ]2+中配位键的个数为4N
2 4 A
D.标准状况下,11.2LCO和H 的混合气体中分子数为0.5N
2 A
6.(2021·广东·高考真题)设 为阿伏加德罗常数的值。下列说法正确的是
A. 含有 键的数目为
B. 的盐酸含有阴离子总数为
C. 与 混合后的分子数目为
D. 与足量 反应生成的 分子数目为
7.(2021·浙江·高考真题)设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.1 mol NH F晶体中含有的共价键数目为3N
4 A
B.CH 和C H 混合气体2.24L(标准状况)完全燃烧,则消耗O 分子数目为0.25N
4 2 4 2 A
C.向100mL 0.10mol·L-1FeCl 溶液中加入足量Cu粉充分反应,转移电子数目为0.01N
3 A
D.0.1 mol CH COOH与足量CHCHOH充分反应生成的CHCOOCH CH 分子数目为0.1N
3 3 2 3 2 3 A
8.(2021·河北·高考真题)N 是阿伏加德罗常数的值,下列说法错误的是
A
A.22.4L(标准状况)氟气所含的质子数为18N
A
B.1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2N
A
C.电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为N
A
D.1L1mol•L-1溴化铵水溶液中NH 与H+离子数之和大于N
A
9.(2021·湖南·高考真题) 为阿伏加德罗常数的值。下列说法正确的是
A. 含有的中子数为
B. 溶液中含有的 数为C. 与 在密闭容器中充分反应后的分子数为
D. 和 (均为标准状况)在光照下充分反应后的分子数为
10.(2021·浙江·高考真题)设 为阿伏加德罗常数的值,下列说法不正确的是
A.标准状况下, 中含有中子数为
B. (分子结构: )中的共价键数目为
C. 的 水溶液中含有氧原子数为
D. 三肽 (相对分子质量:189)中的肽键数目为
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2022·广西·一模)N 为阿伏加德罗常数的值,下列说法正确的是
A
A.lmol NO与0.5mol O 充分反应后,混合气体分子中氮原子数目为1N
2 A
B.常温下,100mL 0.1 mol·L-1 Na CO 溶液中阴离子总数目为0.01 N
2 3 A
C.常温下,5.6g Fe与足量浓硝酸完全反应,转移电子数目为0. 3 N
A
D.等物质的量的乙烷(C H) 与乙醛(C HO)分子中含共用电子对数目均为7 N
2 6 2 4 A
2.(2022·上海·模拟预测)常温常压下,往某密闭容器中充入两种气体后不久,测得容器内最终气体平均
式量为49,则充入的气体可能为( )
A.C H 和O B.NO和O C.NH 和HCl D.SO 和HS
3 8 2 2 3 2 2
3.(2021·陕西省洛南中学一模)下列叙述正确的是
A.24 g 镁与27 g铝中,含有相同的质子数
B.同等质量的氧气和臭氧中,电子数相同
C.1 mol重水与1 mol水中,中子数比为2∶1
D.1 mol乙烷和1 mol乙烯中,化学键数相同
4.(2021·山东·模拟预测)下列说法正确的是
A.在标准状况下,1 mol氧气和1 mol氦气的体积相同,含有原子数也相同
B.同温同压下,等质量的CO和NO体积相同C.同温同压,相同体积的CO和N,则二者含有的原子数相同
2
D.同温同体积的条件下,等质量的SO 和O 的压强比为2∶1
2 2
5.(2021·山东·模拟预测)下列情况中,气体分子数不一定相同的是
A.相同体积的CO和CO
2
B.同温同压下1 L CO和1 L CO
2
C.常温常压下1 g CO和1 g N
2
D.同温同压下,同容积的两个容器,一个盛有NO,另一个盛有N 和O,两容器内的气体一定具有相同
2 2
的分子总数
6.(2022·上海·模拟预测)某固体物质A在一定条件下发生分解: ,测得生成
的混合气体对氢气的相对密度为d,则A的相对分子质量为
A.8d B.7d C.6d D.5d
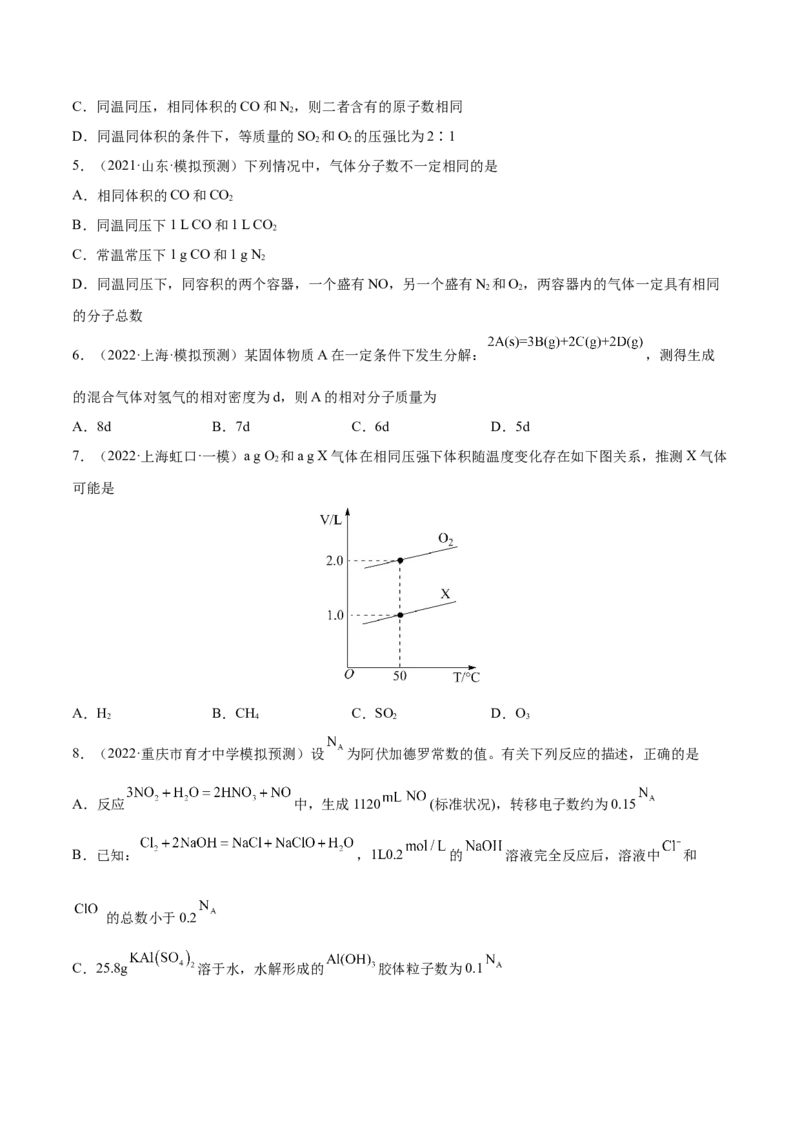
7.(2022·上海虹口·一模)a g O 和a g X气体在相同压强下体积随温度变化存在如下图关系,推测X气体
2
可能是
A.H B.CH C.SO D.O
2 4 2 3
8.(2022·重庆市育才中学模拟预测)设 为阿伏加德罗常数的值。有关下列反应的描述,正确的是
A.反应 中,生成1120 (标准状况),转移电子数约为0.15
B.已知: ,1L0.2 的 溶液完全反应后,溶液中 和
的总数小于0.2
C.25.8g 溶于水,水解形成的 胶体粒子数为0.1D.密闭容器中,1 和1 反应后分子总数小于2
9.(2022·湖北·武汉二中模拟预测)N 为阿伏加德罗常数的值,下列说法正确的是
A
A.标准状况下,11.2LCHCl 分子数为0.5N
2 2 A
B.1molXeF 分子中价层电子对数为5N
2 A
C.pH=2的盐酸中,H+数目为0.01N
A
D.120gNaHSO 晶体中SO 的数目为N
4 A
10.(2022·辽宁·鞍山一中模拟预测)下列有关N 的说法正确的是
A
A.1mol熔融的KHSO 中含有离子总数为3N
4 A
B.40 g SiC(与金刚石结构类似)中Si-C键的数目为4N
A
C.锌与足量的稀硫酸反应生成22.4LH ,转移电子数为2N
2 A
D.0.1 mol Na O 与足量SO 反应时,转移电子数为0.1N
2 2 2 A
11.(2021·江西上饶市·高三一模)设N 为阿伏伽德罗常数的值,下列有关叙述正确的是
A
A.2HS+SO=3S↓+2H O反应中,每生成1mol氧化产物时转移电子数为N
2 2 2 A
B.物质的量相等的重水与水相差2N 个中子
A
C.乙烯和丙烯组成的28g 混合气体中含氢原子数为4N
A
D.pH=13的1LBa(OH) 溶液中所含有OH-数目为0.2N
2 A
12.(2021·福建高三零模)已知N 是阿伏加德罗常数的值,下列说法正确的是
A
A.0.1mol·L-1KNO 溶液中离子总数大于0.2N
3 A
B.D18O和TO的混合物1.1 g, 含有的质子数为0. 5N
2 2 A
C.5.6g Fe与足量的S反应转移的电子数为0.3N
A
D.0.1 mol H 和0.2 mol I 充分反应后分子总数小于0.3N
2 2 A
二、主观题(共4小题,共40分)
13.(8分)如图所示,在相同温度下,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO
和O,且恰好使两容器内气体密度相同。打开活塞,使NO与O 充分反应。(不考虑NO 与NO 的转化)
2 2 2 2 4
(1)开始时左右两室分子数__________(填“相同”或“不相同”)。
(2)反应前后NO室压强______(填“增大”或“减小”)。
(3)最终容器内密度与原来__________(填“相同”或“不相同”)。(4)最终容器内__________(填“有”或“无”)O 存在。
2
14.(10分)长征系列运载火箭的燃料之一是某液体化合物XY。16 g XY 在一定量的 O 中恰好完全燃烧,
2 4 2 4 2
反应的化学方程式为XY(l)+O (g)==X (g)+2YO(l)。冷却后标准状况下测得生成物 X 的体积为11.2 L,其
2 4 2 2 2 2
密度为1.25 g·L-1,则:
(1)反应前O 的体积(标准状况下)为________,其物质的量为________mol。
2
(2)X 的摩尔质量为________,Y元素的名称是______________________。
2
(3)若反应生成0.1 mol X,则转移电子的物质的量为________mol。
2
15.(12分)物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)0.2 g H 含有________个氢原子。
2
(2)标准状况下,含有相同氧原子数的CO和CO 的体积之比为________。
2
(3)100 mL硫酸铝溶液中n(Al3+)=0.20 mol(不考虑水解因素),则其中c(SO 2-)=________。
4
(4)在9.5 g某二价金属的氯化物中含有0.2 mol Cl-,此氯化物的摩尔质量为________,该金属元素的相对原
子质量为________。
(5)6.72 L CO(标准状况)与一定量的Fe O 恰好完全反应(生成Fe与CO)后,生成Fe的质量为________g。
2 3 2
16.(10分)(1)30 g 12C18O 和 28 g 14N 所含的分子数之比为________。
2
(2)同温同压下,12C18O和14N 两种气体的密度之比为________。
2
(3)同温同压同体积的12C18O和 14N 具有电子数之比为________。
2
(4)28 g14N 所含的原子数为________N 。
2 A
(5)将乙烯、CO、N 三种气体分别盛放在三个相同容器中,若三个容器的温度和质量相等,则三个容器的
2
气体压强之比为________。