文档内容
第 09 讲 无机非金属材料
1.广东作为中国南大门,保存着不少国宝级文物。下列国宝级文物主要由陶瓷制成的是
A.元青花人物图玉壶春瓶 B.南宋鎏金腰带
C.清象牙雕空雕八仙福寿提梁盒 D.北宋木雕罗汉像
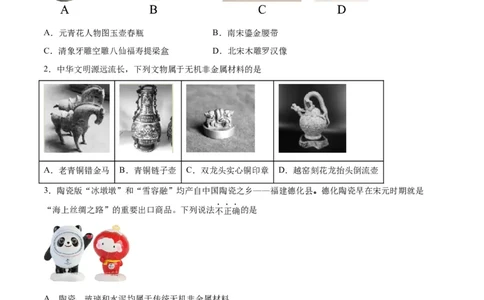
2.中华文明源远流长,下列文物属于无机非金属材料的是
A.老青铜错金马 B.青铜链子壶 C.双龙头实心铜印章 D.越窑刻花龙抬头倒流壶
3.陶瓷版“冰墩墩”和“雪容融”均产自中国陶瓷之乡——福建德化县。德化陶瓷早在宋元时期就是
“海上丝绸之路”的重要出口商品。下列说法不正确的是
A.陶瓷、玻璃和水泥均属于传统无机非金属材料
B.陶瓷版“冰墩墩”上黑色涂料的主要成分为Fe O
2 3
C.高温结构陶瓷具有耐高温、耐氧化、耐磨蚀等优良性能
D.陶瓷是以粘土及天然矿物岩为原料,经加工烧制而成
4.航天科技的发展与化学密切相关。2013年12月15日,“玉兔号”成为我国登陆月球的第一辆月球
车。2022年11月29日,神舟十五号载人飞船成功发射,首次实现6名航天员太空会师。中国航天科技集
团计划2023年安排60余次宇航发射任务。下列说法中错误的是
A.碳化硅 可用作宇宙飞船的耐热材料
B.肼 可作火箭燃料,可用 作氧化剂
C.二氧化硅可用作航天器太阳能电池板的材料
D.电解水产生氧气是宇航员供氧的主要来源
5.下列有关硅及其化合物的说法不正确的是
A.因为高温时SiO 与NaCO 反应放出CO,所以HSiO 酸性比HCO 强
2 2 3 2 2 3 2 3
B.SiO 晶体是由Si与O按照1∶2的比例形成的立体网状结构, 硅氧四面体不仅存在于SiO 晶体中,而且
2 2
存在于硅酸盐矿石中
C.水晶镜片、石英钟表、玛瑙手镯的主要成分为SiO
2
D.青花瓷胎体的原料为高岭土[AlSi O(OH) ],若以氧化物形式可表示为:Al O·2SiO·2H O
2 2 5 4 2 3 2 2
6.沙子的主要成分是SiO,SiO 属于酸性氧化物,部分性质与CO、SO 类似。下列关于SiO 性质的预测
2 2 2 2 2
错误的是
A.SiO 能与氢氧化钠溶液反应生成NaSiO 和HO
2 2 3 2
B.SiO 高温下能与CaO反应生成CaSiO
2 3
C.SiO 能与水反应生成硅酸
2
D.SiO 可以用作建筑材料
2
7.化学与社会、生活密切相关。对下列现象或事实的解释正确的是
选项 现象或事实 解释
A 用氢氟酸刻蚀玻璃 二氧化硅是碱性氧化物
豆科植物的根瘤菌将氮气转化成
B 这是一个自然固氮的过程
氨
过氧化钠可作呼吸面具中氧气来
C 过氧化钠能氧化二氧化碳
源
D 用硅制光导纤维 硅是良好的半导体材料8.在给定条件下,下列选项所示的物质间转化均能一步实现的是
A.
B.
C.
D.
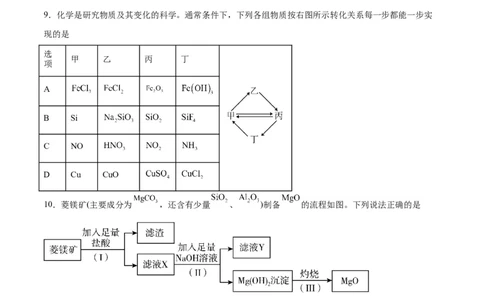
9.化学是研究物质及其变化的科学。通常条件下,下列各组物质按右图所示转化关系每一步都能一步实
现的是
选
甲 乙 丙 丁
项
A
B Si
C NO
D Cu CuO
10.菱镁矿(主要成分为 ,还含有少量 、 )制备 的流程如图。下列说法正确的是
A.步骤(Ⅰ)得到的滤渣主要成分为 B.步骤(Ⅱ)发生的反应有2个
C.步骤(Ⅲ)操作可在蒸发皿中进行 D.滤液Y中加入足量氨水可得到白色沉淀
11.在给定条件下,下列物质间转化不能实现的是
A.黄铁矿
B.石英砂 粗硅 高纯硅C.
D.
12.铁橄榄石 [Fe (SiO)]是嫦娥五号月壤的主要含铁矿物之一,我国科学家发现陨石撞击过程的高温高压
2 4
可引发铁橄榄石发生熔融产生 , 发生反应形成 与 ,下列相关选项错误的是
A.铁橄榄石是一种硅酸盐,可改写为
B.该反应的方程式为:
C.铁橄榄石熔融产生自由移动的 属于化学变化
D.该研究证明了月壤中存在歧化成因的单质铁
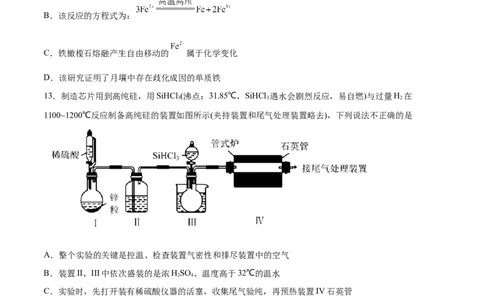
13.制造芯片用到高纯硅,用SiHCl (沸点:31.85℃,SiHCl 遇水会剧烈反应,易自燃)与过量H 在
3 3 2
1100~1200℃反应制备高纯硅的装置如图所示(夹持装置和尾气处理装置略去),下列说法不正确的是
A.整个实验的关键是控温、检查装置气密性和排尽装置中的空气
B.装置II、III中依次盛装的是浓HSO 、温度高于32℃的温水
2 4
C.实验时,先打开装有稀硫酸仪器的活塞,收集尾气验纯,再预热装置IV石英管
D.尾气处理可直接通入NaOH溶液中
14.以叶蛇纹石[主要成分是 ,含少量Fe O、FeO、Al O 等]为原料提取高纯硅的流程
2 3 2 3
如下:
叶蛇纹石 SiO 粗硅 SiHCl 高纯硅
2 3
下列说法错误的是
A.反应2的副产物可作燃料B.反应3和反应4的副产物可循环利用
C.反应1、2、3、4都是氧化还原反应
D.上述流程中反应3和反应4不可在同一容器中进行
15.黄铜矿主要成分是 ,还含有 ,以该黄铜矿为原料制备胆矾的流程如下:
下列说法正确的是
A.方案Ⅰ中,“浸取”时使用98%浓硫酸
B.滤渣Ⅱ中含 和S
C.可用氯水和KSCN溶液检验滤液Ⅰ和滤液Ⅱ中是否含
D.方案Ⅰ更符合环保要求
16.根据“玉兔二号”提供的一个暗绿色闪光的石块信息进行分析,发现石块主要由约 的斜长石(
)、 的辉石 ( 、 为单核离子, )和 的橄榄石( , 为
、 )组成。下列关于上述“三石”的说法正确的是
A.既是硅酸盐材料,又是金属材料
B.斜长石( )不稳定易水解
C.若辉石中 、 为 时, 可能是
D.橄榄石的氧化物形式一定为
17.将过量的CO 分别通入下列溶液中:①CaCl 溶液②NaSiO 溶液③Ca(ClO) 溶液④饱和NaCO 溶
2 2 2 3 2 2 3
液,最终溶液中有白色沉淀析出的是
A.①②③④ B.②④ C.①②③ D.②③④18.某废催化剂含SiO、ZnS、CuS及少量的Fe O 某实验小组以该废催化剂为原料,回收锌和铜,设计实
2 3 4.
验流程如图:
下列说法正确的是
A.步骤①操作中,生成的气体可用CuSO 溶液吸收
4
B.检验滤液1中是否含有Fe2+,可以选用KSCN和新制的氯水
C.步骤②操作中,应先加6% H O,然后加入1.0mol·L -1HSO
2 2 2 4
D.滤渣1和滤渣2均含有HSiO 胶体,进一步加工可获得硅胶
2 3
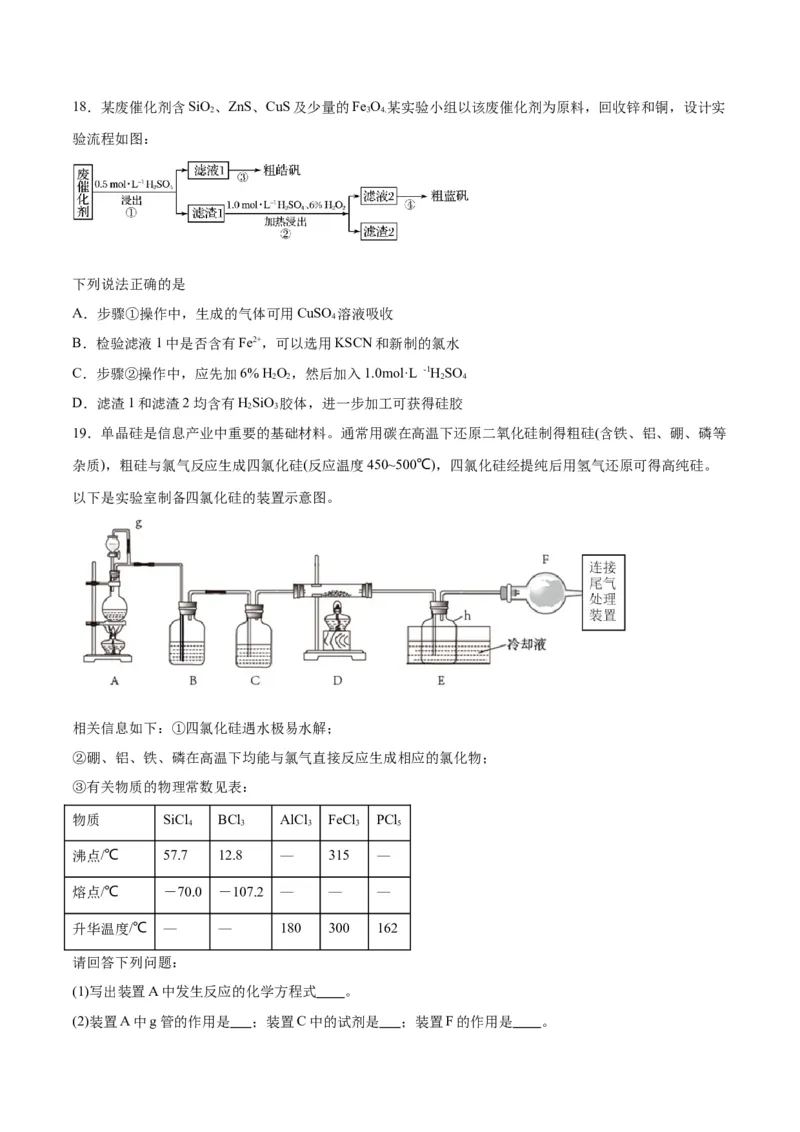
19.单晶硅是信息产业中重要的基础材料。通常用碳在高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等
杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500℃),四氯化硅经提纯后用氢气还原可得高纯硅。
以下是实验室制备四氯化硅的装置示意图。
相关信息如下:①四氯化硅遇水极易水解;
②硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
③有关物质的物理常数见表:
物质 SiCl BCl AlCl FeCl PCl
4 3 3 3 5
沸点/℃ 57.7 12.8 — 315 —
熔点/℃ -70.0 -107.2 — — —
升华温度/℃ — — 180 300 162
请回答下列问题:
(1)写出装置A中发生反应的化学方程式 。
(2)装置A中g管的作用是 ;装置C中的试剂是 ;装置F的作用是 。(3)常用强碱溶液吸收尾气,反应的离子方程式为 。
(4)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,除
铁元素外可能还含有的元素是 (填写元素符号)。
(5)为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO 标准溶液在酸
4
性条件下进行氧化还原滴定,反应的离子方程式是 。
20.高纯硅是制作光伏电池的关键材料,如图是一种生产高纯硅的工艺流程示意图:
已知:①流化床反应器主反应: ;
②还原炉主反应: ;
③ 极易水解: 。
回答下列问题:
(1)石英砂的主要成分为 , 是一种酸性氧化物,能与烧碱反应生成盐和水,下列物质中也能与烧
碱反应生成盐和水的是 (填标号)
A. B. C. D.
还能在一种常见的酸中溶解,生成一种气态含硅物质,这种酸的电子式为 。
(2)电弧炉中生成粗硅,反应的化学方程式为 。若电弧炉中焦炭过量,还会有 生成,石英
砂和焦炭生成 的反应中,氧化剂和还原剂的物质的量之比为 。
(3)整个操作流程都需隔绝空气,原因是 (答出两条即可)。
(4)流化床反应器中除 外,还可能发生副反应,生成其他含硅化合物(如 、 、
等),可以用分馏的方法加以分离,该操作方法的理论依据是 。
(5)上述操作流程中可以循环利用的物质是 。