文档内容
第 12 讲 氯及其化合物
(模拟精练+真题演练)
完卷时间:50分钟
可能用到的相对原子质量:O 16 Na23 Cl35.5 Ca 40
一、选择题(每小题只有一个正确选项,共12×5分)
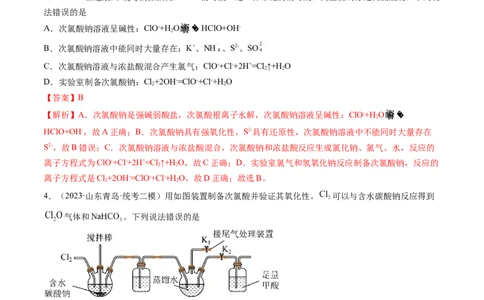
1.(2022·广东深圳·统考一模)某实验小组利用下图装置进行实验。下列说法不正确的是
A.滴加浓盐酸时需将分液漏斗上端玻璃塞上的凹槽对准漏斗上的小孔
B.蘸有淀粉KI溶液的棉花变蓝,说明氯气的氧化性强于碘
C.蘸有品红溶液的棉花褪色,说明氯气具有漂白性
D.蘸有紫色石蕊溶液的棉花上出现的现象是棉花先变红后褪色
【答案】C
【解析】A.滴加浓盐酸时需将分液漏斗上端玻璃塞上的凹槽对准漏斗上的小孔,A正确;B.蘸有淀粉
KI溶液的棉花变蓝,说明Cl 与KI溶液发生了反应:Cl+2KI=2KCl+I ,I 遇淀粉溶液变为蓝色。在该反应
2 2 2 2
中Cl 为氧化剂,I 为氧化产物,所以氯气的氧化性强于碘,B正确;C.氯气本身没有漂白性,氯气与水
2 2
反应生成的次氯酸具有漂白性,能够使品红溶液褪色,C错误;D.浓盐酸与KMnO 溶液反应产生Cl,
4 2
Cl 溶于蘸有紫色石蕊溶液中,反应产生HCl、HClO,酸使紫色石蕊试液变为红色,HClO同时具有强氧化
2
性,又将红色物质氧化变为无色,因此看到蘸有紫色石蕊溶液的棉花上出现的现象是先变红后褪色,D正
确;故合理选项是C。
2.(2023·全国·模拟预测)实验室以 和浓盐酸为原料,制备 并获得漂白粉。下列图示装置和原
理能达到实验目的的是
A.制备 B.收集氯气 C.制备漂白粉 D.尾气处理【答案】B
【分析】本题以 及漂白粉的制备为背景考查化学实验基础知识,具体考查氯气的制备和收集、漂白粉
的制备、尾气处理等,意在考查考生对化学实验基础知识的掌握及应用能力。
【解析】A.实验室利用浓盐酸和 制备 时需要加热,A不符合题意;B. 的密度比空气的大,
应选用向上排空气法收集 ,B符合题意;C.石灰水中 的浓度较小,应利用石灰乳与 反应
制备漂白粉,C不符合题意;D. 在饱和NaCl溶液中的溶解度很小,应用NaOH溶液吸收尾气,D不
符合题意。故选B。
3.(2023·福建泉州·统考模拟预测)“84消毒液”是一种常见的消毒剂,其主要成分是次氯酸钠。下列说
法错误的是
A.次氯酸钠溶液呈碱性:ClO-+H O HClO+OH-
2
B.次氯酸钠溶液中能同时大量存在:K+、NH 、S2-、SO
C.次氯酸钠溶液与浓盐酸混合产生氯气:ClO-+Cl-+2H+=Cl↑+H O
2 2
D.实验室制备次氯酸钠:Cl+2OH-=ClO-+Cl-+H O
2 2
【答案】B
【解析】A.次氯酸钠是强碱弱酸盐,次氯酸根离子水解,次氯酸钠溶液呈碱性:ClO-+H O
2
HClO+OH-,故A正确;B.次氯酸钠具有强氧化性,S2-具有还原性,次氯酸钠溶液中不能同时大量存在
S2-,故B错误;C.次氯酸钠溶液与浓盐酸混合,次氯酸钠和浓盐酸反应生成氯化钠、氯气、水,反应的
离子方程式为ClO-+Cl-+2H+=Cl↑+H O,故C正确;D.实验室氯气和氢氧化钠反应制备次氯酸钠,反应的
2 2
离子方程式是Cl+2OH-=ClO-+Cl-+H O,故D正确;故选B。
2 2
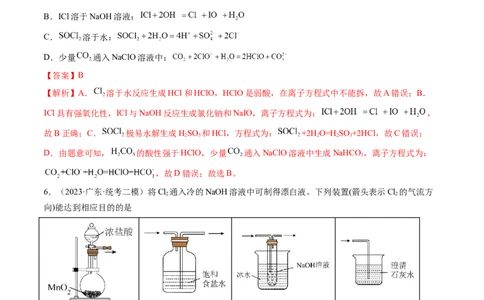
4.(2023·山东青岛·统考二模)用如图装置制备次氯酸并验证其氧化性。 可以与含水碳酸钠反应得到
气体和 。下列说法错误的是
A.装置甲中每生成16.8g碳酸氢钠同时生成标准状况下
B.装置乙中盛装的是浓硫酸
C.将装置丙中次氯酸溶液转移到装置丁中的具体操作是打开 关闭
D.装置丁中溶液酸性显著增强可证明次氯酸的氧化性
【答案】B
【解析】A.装置甲中发生氧化还原反应:2Cl+2Na CO+H O=Cl O+2NaHCO +2NaCl,每生成
2 2 3 2 2 3
16.8g(0.2mol)碳酸氢钠则生成0.1molCl O,标准状况下的体积为2.24L,A项正确;B.装置乙的作用是吸
2收多余的Cl,防止干扰后续氧化性的验证,浓硫酸不能除去多余Cl,故装置乙中盛装的不是浓硫酸,B
2 2
项错误;C.打开 K 关闭 K,则利用压强能将装置丙中液体压入装置丁,C项正确;D.装置丁中溶液
2 1
酸性显著则说明发生了HClO+HCOOH=HCl+CO ↑+H O,可证明次氯酸的氧化性,D项正确。答案选B。
2 2
5.(2023·江苏盐城·统考三模)周期表中VIIA元素及其化合物应用广泛。氢氟酸可用作雕刻玻璃;
可溶于苯、 等有机溶剂,极易水解;卤素互化物(如ICl、 )具有强氧化性;卤化银具有感光
性( 的电离平衡常数分别为: 、 ;HClO的电离平衡常数为:
)。下列化学反应表示正确的是
A. 溶于水:
B.ICl溶于NaOH溶液:
C. 溶于水:
D.少量 通入NaClO溶液中:
【答案】B
【解析】A. 溶于水反应生成HCl和HClO,HClO是弱酸,在离子方程式中不能拆,故A错误;B.
ICl具有强氧化性,ICl与NaOH反应生成氯化钠和NaIO,离子方程式为: ,
故B正确;C. 极易水解生成HSO 和HCl,方程式为: +2H O=HSO +2HCl,故C错误;
2 3 2 2 3
D.由题意可知, 的酸性强于HClO,少量 通入NaClO溶液中生成NaHCO ,离子方程式为:
3
,故D错误;故选B。
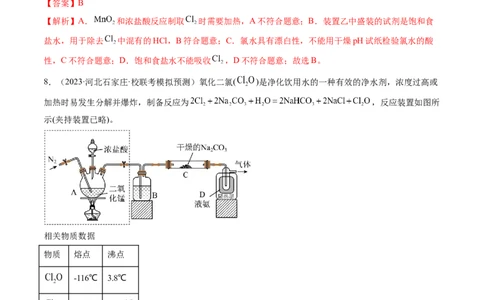
6.(2023·广东·统考二模)将Cl 通入冷的NaOH溶液中可制得漂白液。下列装置(箭头表示Cl 的气流方
2 2
向)能达到相应目的的是
A.制备Cl B.除去Cl 中的HCl C.制备漂白液 D.尾气处理
2 2
【答案】C
【解析】A.二氧化锰和浓盐酸反应需要加热,故A错误;B.用饱和食盐水除去Cl 中的HCl,气体导气
2
管应该“长进短出”,故B错误;C.氯气和氢氧化钠在较低温度下反应生成氯化钠和次氯酸钠,故C正
确;D.石灰水的浓度太小,石灰水吸收氯气的量少,应该用氢氧化钠溶液吸收氯气,故D错误;选C。
7.(2023·全国·模拟预测)实验室欲制取少量Cl 的水溶液并探究其性质,有关实验装置、试剂和操作能
2
达到实验目的的是A.用装置甲制取Cl B.装置乙中盛装的试剂是饱和食盐水
2
C.用干燥pH试纸检验装置丙中氯水的酸性 D.用装置丁吸收尾气中的Cl
2
【答案】B
【解析】A. 和浓盐酸反应制取 时需要加热,A不符合题意;B.装置乙中盛装的试剂是饱和食
盐水,用于除去 中混有的HCl,B符合题意;C.氯水具有漂白性,不能用干燥pH试纸检验氯水的酸
性,C不符合题意;D.饱和食盐水不能吸收 ,D不符合题意;故选B。
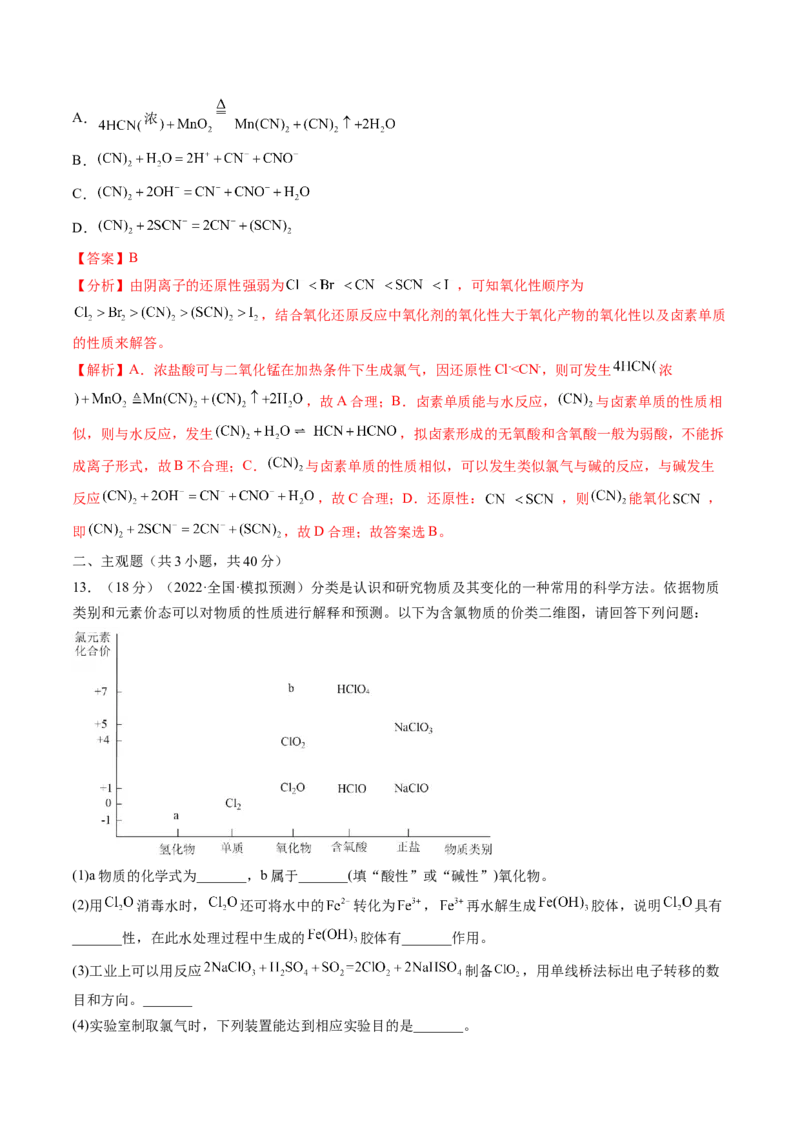
8.(2023·河北石家庄·校联考模拟预测)氧化二氯( )是净化饮用水的一种有效的净水剂,浓度过高或
加热时易发生分解并爆炸,制备反应为 ,反应装置如图所
示(夹持装置已略)。
相关物质数据
物质 熔点 沸点
-116℃ 3.8℃
— -34.6℃
液氨 — -33.5℃
下列说法错误的是
A.检查虚框中装置气密性可用液差法 B.装置B中试剂是浓硫酸
C.装置D收集ClO D.通入 可降低爆炸风险
2
【答案】B
【分析】本实验目的是制备ClO,实验原理是 ,A装置中
2制备氯气,氯气中混有HCl,为防止HCl干扰实验,需要除去,即装置B盛放饱和食盐水,C装置为发生
装置,D装置为收集装置;
【解析】A.虚框中装置气密性检验,可用液差法,将止水夹夹住装置A两端橡胶管,打开分液漏斗活塞,
加水,一段时间后,水不能顺利流下,则气密性良好,故A说法正确;B.因反应
,需要有水参与,不能用浓硫酸除去水,装置B中试剂应
是饱和食盐水,除去HCl,故B说法错误;C.根据ClO的沸点,并且在液氨中冷凝,所以装置D为收集
2
装置,故C说法正确;D.ClO浓度过高易发生分解并爆炸,通入N 可稀释ClO,降低爆炸风险,故D
2 2 2
说法正确;答案为B。
9.(2023·上海黄浦·统考二模)一定条件下,在水溶液中1molClO ;(x=0,1,2,3,4)的相对能量(kJ)
大小如图所示。下列有关说法正确的是
A.上述离子中最稳定的是C
B.B→A+D反应的热化学方程式为3ClO-(aq)=2Cl-(aq)+ClO (aq)+116kJ
C.上述离子中结合H+能力最强的是E
D.一定温度下,Cl 与NaOH溶液反应产物中有A、B、D,则三者的浓度之比可能为10∶1∶2
2
【答案】B
【分析】由图可知A为Cl-,B为ClO-,C为 ,D为 ,E为 ,据此作答。
【解析】A.物质具有的能量越低越稳定,由图可知,最稳定的是A,A错误;B.B→A+D反应的化学方
程式为 ,生成物的总能量减去反应物的总能量=
,故放出116kJ能量,B正确;C.酸越弱,酸根离子结合氢离子能
力越强,同种元素的含氧酸,化合价越高,酸性越强,故酸性HClO>HClO >HClO,结合氢离子能力ClO-
3 2
最强,即结合氢离子能力最强的B,C错误;D. 一定温度下,Cl 与NaOH溶液反应产物中有Cl-,
2
ClO-, ,若三者浓度之比为10:1:2,得失电子比=10:(2+2×5)=5:6,得失电子不守恒,D错误;故选B。
10.(2023·湖南永州·统考二模)正高碘酸 是白色结晶性粉末,溶于水,主要用作氧化剂和分析试
剂。由 制取 的实验流程如图所示:下列说法错误的是
A.“反应1”是为了将 转化为
B.“反应2”中发生的反应是
C.“反应3”的滤液中含有大量的 等
D.“反应4”得到的无色气体可能是氧气
【答案】C
【分析】电解NaI溶液生成NaIO ,往NaIO 溶液中加入NaOH溶液和通入氯气,反应生成不溶于水的
3 3
NaHIO ,过滤得到NaHIO ,加入硝酸银溶液生成不溶于水的黑色Ag IO ,过滤得到黑色Ag IO ,通入
2 3 6 2 3 6 5 6 5 6
氯气和加入水发生反应 ,过滤得到HIO ,以此解答。
5 6
【解析】A.“反应1”中,电解NaI溶液生成NaIO ,目的是将 转化为 ,A正确;B.“反应2”中,
3
往NaIO 溶液中加入NaOH溶液和通入氯气,反应生成不溶于水的NaHIO ,反应的化学方程式为
3 2 3 6
,B正确;C.由分析可知,“反应3”中NaHIO 加入硝酸银溶
2 3 6
液生成不溶于水的黑色Ag IO ,同时生成NaNO 和HNO,C错误;D.“反应4”中发生的反应为
5 6 3 3
,因此生成的无色气体可能是氧气,D正确;故选C。
11.卤素间形成的化合物如“ 、 、 ”等称为卤素互化物,化学性质与卤素单质类似,则下列关
于卤素互化物的性质的描述及发生的相关反应不正确的是( )
A. 是一种化合物 B.
C. 的氧化性强于 D. 可以与 溶液反应生成2种盐
【答案】B
【分析】化合物是由两种元素组成的纯净物;氧化性Fe3+>I,氧化剂的氧化性大于氧化产物;Cl、Br的
2
非金属性比I强,BrCl的氧化性强于I;卤素间形成的化合物称为卤素互化物,化学性质与卤素单质类似,
2
故 可以看作是氯气。
【解析】A. 由碘和氟两种元素组成,是化合物,故A正确;B.氧化性Fe3+>I,IBr与铁反应生成
2
FeI,故B错误;C.Cl、Br的非金属性比I强,BrCl的氧化性强于I,介于氯气和溴之间,故C正确;
2 2
D.IBr可以与NaOH溶液生成NaIO和NaBr,故D正确;答案选B。
12.氰 ,硫氰 等称为拟卤素,与卤素单质性质相似,它们的阴离子与也卤素阴离子性质相似,
阴离子的还原性顺序为: ,又知,拟卤素形成的无氧酸和含氧酸一般为弱酸,
下列反应中,不合理的是( )A. 浓
B.
C.
D.
【答案】B
【分析】由阴离子的还原性强弱为 ,可知氧化性顺序为
,结合氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性以及卤素单质
的性质来解答。
【解析】A.浓盐酸可与二氧化锰在加热条件下生成氯气,因还原性Cl-历程Ⅰ
D.历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:
【答案】C
【分析】对比两个历程可知,历程Ⅱ中增加了催化剂,降低了反应的活化能,加快了反应速率。
【解析】A.催化剂能降低活化能,但是不能改变反应的焓变,因此 ,A正确;B.已知
的相对能量为0,对比两个历程可知, 的相对能量为 ,则 键能为,B正确;C.催化剂不能改变反应的平衡转化率,因此相同条件下, 的平衡转化率:
历程Ⅱ=历程Ⅰ,C错误;D.活化能越低,反应速率越快,由图像可知,历程Ⅱ中第二步反应的活化能最
低,所以速率最快的一步反应的热化学方程式为: ,D
正确;故答案为:C。
6.(2022·浙江·统考高考真题)下列说法正确的是
A.工业上通过电解六水合氯化镁制取金属镁
B.接触法制硫酸时,煅烧黄铁矿以得到三氧化硫
C.浓硝酸与铁在常温下不能反应,所以可用铁质容器贮运浓硝酸
D.“洁厕灵”(主要成分为盐酸)和“84消毒液”(主要成分为次氯酸钠)不能混用
【答案】D
【解析】A.六水合氯化镁没有自由移动的离子,不能导电,工业上通过电解熔融的无水氯化镁制取金属
镁,A不正确;B.接触法制硫酸时,煅烧黄铁矿只能得到二氧化硫,二氧化硫在接触室经催化氧化才能
转化为三氧化硫,B不正确;C.在常温下铁与浓硝酸发生钝化反应,在铁表面生成一层致密的氧化物薄
膜并阻止反应继续发生,所以可用铁质容器贮运浓硝酸,C不正确;D.“洁厕灵”(主要成分为盐酸)和
“84消毒液”(主要成分为次氯酸钠)不能混用,若两者混用会发生归中反应生成氯气,不仅达不到各自预
期的作用效果,还会污染环境,D正确;综上所述,本题选D。
7.(2022·浙江·统考高考真题)关于化合物 的性质,下列推测不合理的是
A.与稀盐酸反应生成 、 、
B.隔绝空气加热分解生成FeO、 、
C.溶于氢碘酸(HI),再加 萃取,有机层呈紫红色
D.在空气中,与 高温反应能生成
【答案】B
【分析】已知化合物 中Fe的化合价为+3价,CHO-带一个单位负电荷。
3
【解析】A.由分析可知,化合物 中Fe的化合价为+3价,故其与稀盐酸反应生成 、
、 ,反应原理为:FeO(OCH)+3HCl=FeCl +H O+CHOH,A不合题意;B.由分析可知,化
3 3 2 3
合物 中Fe的化合价为+3价,C为-2,若隔绝空气加热分解生成FeO、 、 则得失电子
总数不相等,不符合氧化还原反应规律,即不可能生成FeO、 、 ,B符合题意;C.由分析可知,
化合物 中Fe的化合价为+3价,故其溶于氢碘酸(HI)生成的Fe3+能将I-氧化为I,反应原理为:
2
2FeO(OCH)+6HI=2FeI +I +2H O+2CHOH,再加 萃取,有机层呈紫红色,C不合题意;D.化合物
3 2 2 2 3
在空气中高温将生成Fe O、CO 和HO,然后Fe O 为碱性氧化物,SiO 为酸性氧化物,故化
2 3 2 2 2 3 2
合物 与 高温反应能生成 ,D不合题意;故答案为:B。8.(2023·山东·统考高考真题)卤素可形成许多结构和性质特殊的化合物。回答下列问题:
(1) 时, 与冰反应生成 利 。常温常压下, 为无色气体,固态 的晶体类型为
_____, 水解反应的产物为_____(填化学式)。
(2) 中心原子为 , 中心原子为 ,二者均为 形结构,但 中存在大 键 。 中
原子的轨道杂化方式_____;为 键角_____ 键角(填“>”“ <”或“=”)。比较 与
中 键的键长并说明原因_____。
(3)一定条件下, 和 反应生成 和化合物 。已知 属于四方晶系,晶胞结构如图所示(晶胞
参数 ),其中 化合价为 。上述反应的化学方程式为_____。若阿伏加德罗常数
的值为 ,化合物 的密度 _____ (用含 的代数式表示)。
【答案】(1)分子晶体 HF 、 和
(2) > 分子中 键的键长小于 中 键的键长,其原因是: 分子中既存在σ键,
又存在大 键,原子轨道重叠的程度较大,因此其中 键的键长较小,而 只存在普通的σ键。
(3)
【解析】(1)常温常压下, 为无色气体,则 的沸点较低,因此,固态HOF的晶体类型为分子
晶体。 分子中F显-1价,其水解时结合 电离的 生成HF,则 结合 电离的 ,两者
反应生成 , 不稳定,其分解生成 ,因此, 水解反应的产物为HF 、 和 。
(2) 中心原子为 , 中心原子为 ,二者均为V形结构,但 中存在大 键( )。由 中
存在 可以推断,其中 原子只能提供1对电子,有一个 原子提供1个电子,另一个 原子提供1对电
子,这5个电子处于互相平行的 轨道中形成大 键, 提供孤电子对与其中一个 形成配位键,与另一
个 形成的是普通的共价键(σ键,这个 只提供了一个电子参与形成大 键), 的价层电子对数为
3,则 原子的轨道杂化方式为 ; 中心原子为 ,根据价层电子对的计算公式可知 ,
因此, 的杂化方式为 ;根据价层电子对互斥理论可知, 时,价电子对的几何构型为正四面体,
时,价电子对的几何构型平面正三角形, 杂化的键角一定大于 的,因此,虽然 和 均
为 形结构,但 键角大于 键角,孤电子对对成键电子对的排斥作用也改变不了这个结论。 分子中 键的键长小于 中 键的键长,其原因是: 分子中既存在σ键,又存在
大 键,原子轨道重叠的程度较大,因此其中 键的键长较小,而 只存在普通的σ键。
(3)一定条件下, 、 和 反应生成 和化合物X。已知X属于四方晶系,其中Cu化合价为
+2。由晶胞结构图可知,该晶胞中含有黑球的个数为 、白球的个数为 、灰
色球的个数为 ,则X中含有3种元素,其个数比为1:2:4,由于其中Cu化合价为+2、 的化合价
为-1、K的化合价为+1,根据化合价代数和为0,可以推断X为 ,上述反应的化学方程式为
。若阿伏加德罗富数的值为 ,晶胞的质量为 ,晶胞的体积为
,化合物X的密度 。