文档内容
第 17 讲 电解池 金属的腐蚀与防护
1.理解电解池的构成、工作原理及应用,能书写电极反应和总反应方程式。
2.了解金属发生电化学腐蚀的原因、金属腐蚀的危害以及防止金属腐蚀的措施。
【核心素养分析】
变化观念与平衡思想:认识化学变化的本质是有新物质生成,并伴有能量的转化;能多角度、动态地
分析电解池中发生的反应,并运用电解原理解决实际问题。
证据推理与模型认知:利用电解池装置,分析电解原理,建立解答电解池问题的思维模型,并利用模
型揭示其本质及规律。
科学态度与社会责任:肯定电解原理对社会发展的重大贫献,具有可持续发展意识和绿色化学观念,
能对与电解有关的社会热点问题做出正确的价值判断。
知识点一 电解的原理
1.电解和电解池
(1)电解:在电流作用下,电解质在两个电极上分别发生氧化反应和还原反应的过程。
(2)电解池:电能转化为化学能的装置。
(3)电解池的构成
①有与电源相连的两个电极。
②电解质溶液(或熔融电解质)。
③形成闭合回路。
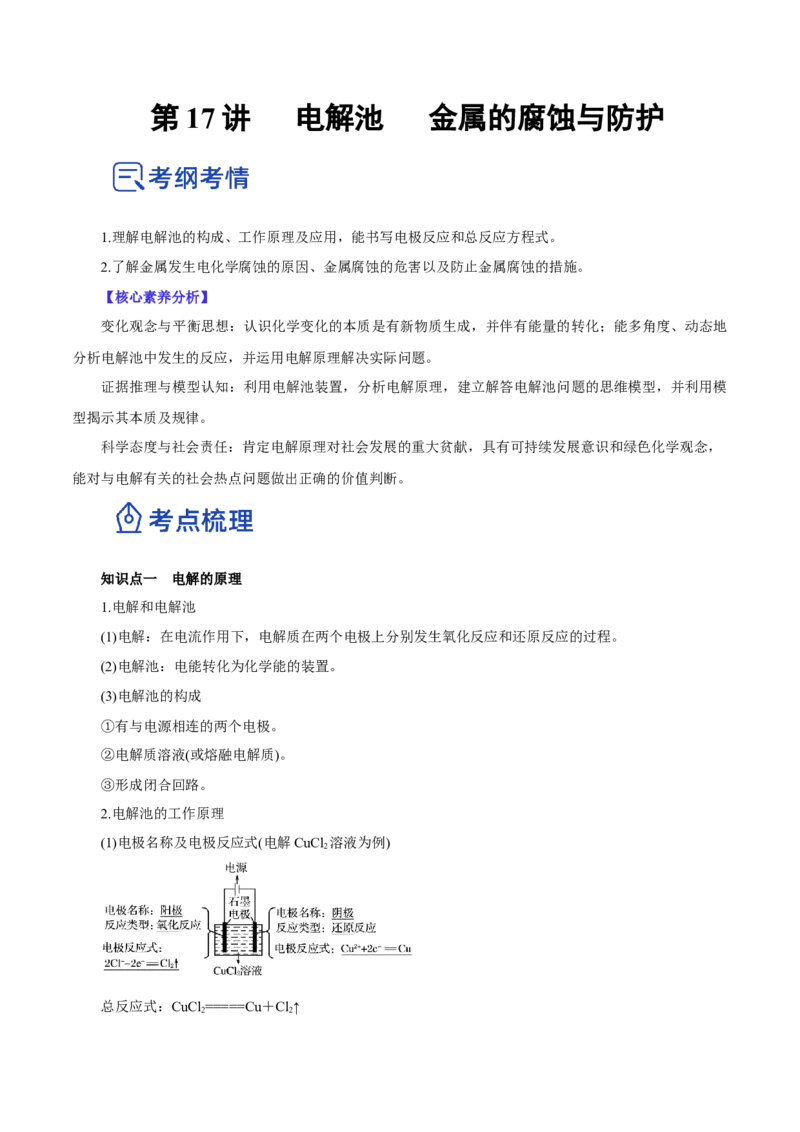
2.电解池的工作原理
(1)电极名称及电极反应式(电解CuCl 溶液为例)
2
总反应式:CuCl =====Cu+Cl↑
2 2(2)电子和离子的移动方向
①电子:从电源负极流出后,流向电解池阴极;从电解池的阳极流出后流向电源的正极。
②离子:阳离子移向电解池的阴极,阴离子移向电解池的阳极。
3.阴阳两极上放电顺序
(1)阴极:(与电极材料无关)。氧化性强的先放电,放电顺序:
(2)阳极:若是活性电极作阳极,则活性电极首先失电子,发生氧化反应。
若是惰性电极作阳极,放电顺序为
注意 ①阴极不管是什么材料,电极本身都不反应,一定是溶液(或熔融电解质)中的阳离子放电。②
最常用、最重要的放电顺序为阳极:Cl->OH-;阴极:Ag+>Cu2+>H+。③电解水溶液时,K+~Al3+不可
能在阴极放电,即不可能用电解水溶液的方法得到K、Ca、Na、Mg、Al等金属。
4.用惰性电极电解电解质溶液的规律
4.用惰性电极电解电解质溶液的规律
类型 实例 电极反应特点或反应式 电解产物 溶液pH变化 溶液复原
含氧酸 HSO 溶液中的H+和OH 减小
2 4
-分别在阴阳两极放
强碱 NaOH 增大
电:
H
电解 2
阴极:4H++4e- 水
水型
活泼金属的 KNO ===2H 2 ↑ O 2 不变
含氧酸盐 3
阳极: 4OH--4e-
===2HO+O↑
2 2
无氧酸(氢 电解质电离的阴阳
HCl H Cl 增大 HCl
电解 氟酸除外) 离子分别在两极放电: 2 2
电解
质型 不活泼金属 阳极:2Cl--2e-
CuCl Cu Cl CuCl
的无氧酸盐 2 ===Cl ↑ 2 2
2
放氢 阴极水电离的H+ 阴极:H
活泼金属的 2
生碱 NaCl 放电,阳极电解质电离 增大 HCl
无氧酸盐
型 的阴离子放电 阳极:Cl 2
阳极水电离的OH-放
放氧 不活泼金属 电,阴极电解质的阳离 Ag阳
生酸 的含氧酸盐 AgNO 3 子放电 极:O 减小 Ag 2 O
性 2
阴极:Ag++e-===Ag
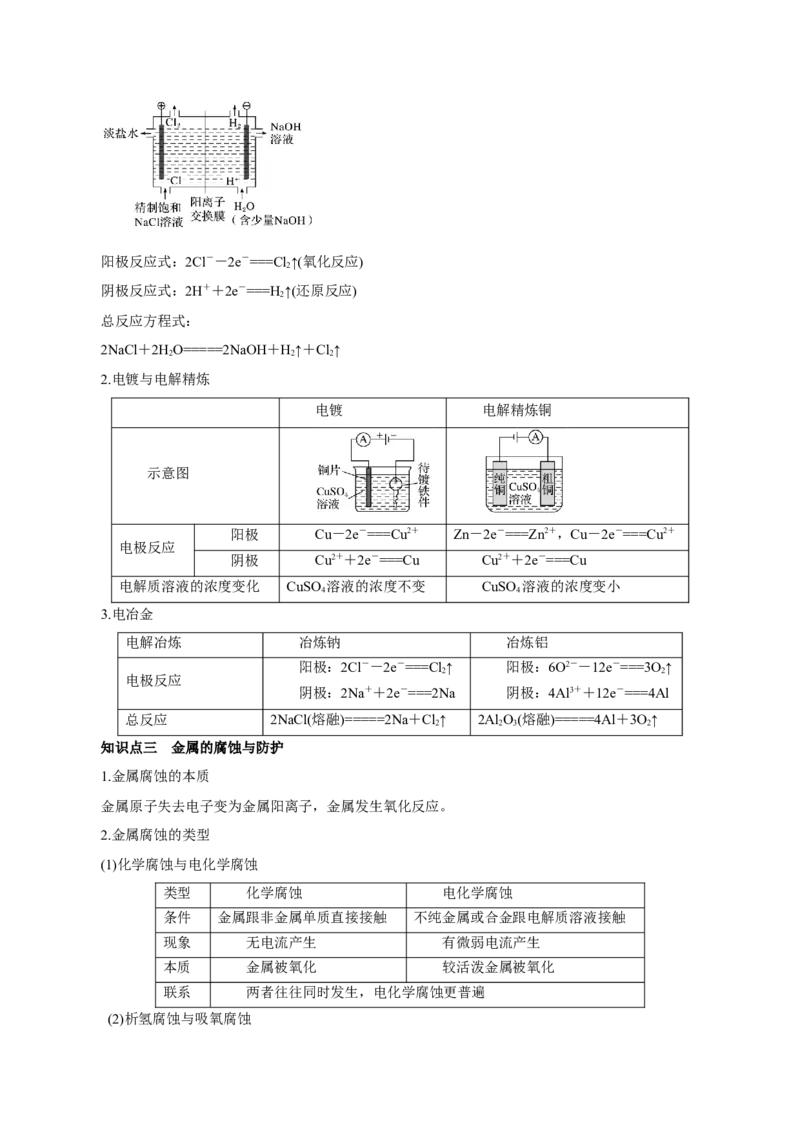
知识点二 电解原理的应用
1.氯碱工业阳极反应式:2Cl--2e-===Cl ↑(氧化反应)
2
阴极反应式:2H++2e-===H↑(还原反应)
2
总反应方程式:
2NaCl+2HO=====2NaOH+H↑+Cl↑
2 2 2
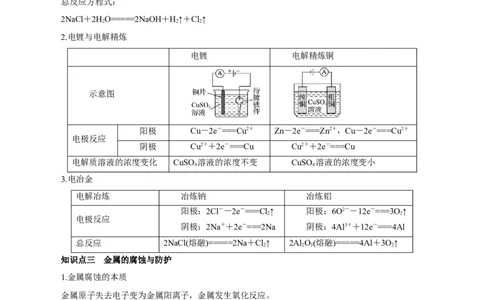
2.电镀与电解精炼
电镀 电解精炼铜
示意图
阳极 Cu-2e-===Cu2+ Zn-2e-===Zn2+,Cu-2e-===Cu2+
电极反应
阴极 Cu2++2e-===Cu Cu2++2e-===Cu
电解质溶液的浓度变化 CuSO 溶液的浓度不变 CuSO 溶液的浓度变小
4 4
3.电冶金
电解冶炼 冶炼钠 冶炼铝
阳极:2Cl--2e-===Cl ↑ 阳极:6O2--12e-===3O↑
2 2
电极反应
阴极:2Na++2e-===2Na 阴极:4Al3++12e-===4Al
总反应 2NaCl(熔融)=====2Na+Cl↑ 2Al O(熔融)=====4Al+3O↑
2 2 3 2
知识点三 金属的腐蚀与防护
1.金属腐蚀的本质
金属原子失去电子变为金属阳离子,金属发生氧化反应。
2.金属腐蚀的类型
(1)化学腐蚀与电化学腐蚀
类型 化学腐蚀 电化学腐蚀
条件 金属跟非金属单质直接接触 不纯金属或合金跟电解质溶液接触
现象 无电流产生 有微弱电流产生
本质 金属被氧化 较活泼金属被氧化
联系 两者往往同时发生,电化学腐蚀更普遍
(2)析氢腐蚀与吸氧腐蚀以钢铁的腐蚀为例进行分析:
类型 析氢腐蚀 吸氧腐蚀
条件 水膜酸性较强(pH≤4.3) 水膜酸性很弱或呈中性
负极 Fe-2e-===Fe2+
电极反应
正极 2H++2e-===H↑ O+2HO+4e-===4OH-
2 2 2
总反应式 Fe+2H+===Fe2++H↑ 2Fe+O+2HO===2Fe(OH)
2 2 2 2
联系 吸氧腐蚀更普遍
3.金属的防护
(1)电化学防护
①牺牲阳极的阴极保护法——原电池原理
a.负极:比被保护金属活泼的金属;
b.正极:被保护的金属设备。
②外加电流的阴极保护法——电解原理
a.阴极:被保护的金属设备;
b.阳极:惰性金属或石墨。
(2)改变金属的内部结构,如制成合金、不锈钢等。
(3)加防护层,如在金属表面喷油漆、涂油脂、电镀、喷镀或表面钝化等方法。
高频考点一 电解原理
【例1】(2022·广东卷)以熔融盐为电解液,以含 和 等的铝合金废料为阳极进行电解,
实现 的再生。该过程中
A. 阴极发生的反应为 B. 阴极上 被氧化
C. 在电解槽底部产生含 的阳极泥 D. 阳极和阴极的质量变化相等
【答案】C
【解析】根据电解原理可知,电解池中阳极发生失电子的氧化反应,阴极发生得电子的还原反应,该
题中以熔融盐为电解液,含Cu、Mg和Si等的铝合金废料为阳极进行电解,通过控制一定的条件,从而可
使阳极区Mg和Al发生失电子的氧化反应,分别生成Mg2+和Al3+,Cu和Si不参与反应,阴极区Al3+得电
子生成Al单质,从而实现Al的再生,据此分析解答。阴极应该发生得电子的还原反应,实际上Mg在阳
极失电子生成Mg2+,A错误;Al在阳极上被氧化生成Al3+,B错误;阳极材料中Cu和Si不参与氧化反应,在电解槽底部可形成阳极泥,C正确;因为阳极除了铝参与电子转移,镁也参与了电子转移,且还会形成
阳极泥,而阴极只有铝离子得电子生成铝单质,根据电子转移数守恒及元素守恒可知,阳极与阴极的质量
变化不相等,D错误;故选C。
【变式探究】(2021·全国乙卷)沿海电厂采用海水为冷却水,但在排水管中生物的附着和滋生会阻碍
冷却水排放并降低冷却效率。为解决这一问题,通常在管道口设置一对惰性电极(如图所示),通入一定的
电流。下列叙述错误的是( )
A.阳极发生将海水中的Cl-氧化生成Cl 的反应
2
B.管道中可以生成氧化灭杀附着生物的NaClO
C.阴极生成的H 应及时通风稀释安全地排入大气
2
D.阳极表面形成的Mg(OH) 等积垢需要定期清理
2
【答案】D
【解析】海水中存在大量的Cl-,在阳极Cl-放电生成Cl ,A叙述正确;阴极HO放电生成H 和OH
2 2 2
-,OH-与Cl 反应生成ClO-,因此管道中存在一定量的NaClO,B叙述正确;因为H 为可燃性气体,所
2 2
以阴极生成的H 应及时通风稀释安全地排入大气,C叙述正确;阴极产生OH-,因此会在阴极表面形成
2
Mg(OH) 等积垢,需定期清理以保持良好的导电性,D叙述错误。
2
【变式探究】(2020·山东卷)采用惰性电极,以去离子水和氧气为原料通过电解法制备双氧水的装置
如图所示。忽略温度变化的影响,下列说法错误的是( )
A.阳极反应为2HO-4e-===4H++O↑
2 2
B.电解一段时间后,阳极室的pH未变
C.电解过程中,H+由a极区向b极区迁移
D.电解一段时间后,a极生成的O 与b极反应的O 等量
2 2
【答案】D
【解析】根据图像可知,b极由O 反应生成了HO ,在这个过程中,氧元素化合价降低,发生了得电
2 2 2子的还原反应,因此b极是电解池的阴极,可推出阴极的电极反应式为 O +2e-+2H+===H O ;则a极为
2 2 2
电解池的阳极,发生失电子的氧化反应,根据图像可知阳极生成了氧气,则阳极反应为2HO-4e-===4H+
2
+O↑,故A正确;根据阳极的电极反应可知,阳极生成了氢离子,但同时生成的氢离子全部从阳极室移
2
向阴极室,故电解一段时间后,阳极室的pH未变,故B正确;电解池的电解质溶液中,阳离子会移向阴
极,故氢离子由a极区向b极区迁移,故C正确;阳极的电极反应式为2HO-4e-===4H++O↑,保持阴
2 2
极和阳极电极反应的得失电子数一致,可得阴极的电极反应为2O +4e-+4H+===2H O ,同一个电路中阳
2 2 2
极的失电子总数和阴极的得电子总数在相同情况下是一样的,故电解一段时间后,a极生成的氧气与b极
反应的氧气的物质的量之比为1∶2,不相等,故D错误。
高频考点二 电极反应式的书写与判断
【例2】(2022·浙江卷)通过电解废旧锂电池中的 可获得难溶性的 和 ,电解
示意图如下(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不计)。
下列说法不正确的是
A.电极A为阴极,发生还原反应
B.电极B的电极发应:
C.电解一段时间后溶液中 浓度保持不变
D.电解结束,可通过调节 除去 ,再加入 溶液以获得
【答案】C
【解析】由电解示意图可知,电极B上Mn2+转化为了MnO ,锰元素化合价升高,失电子,则电极B
2
为阳极,电极A为阴极,得电子,发生还原反应,A正确;由电解示意图可知,电极B上Mn2+失电子转化
为了MnO ,电极反应式为:2HO+Mn2+-2e-=MnO+4H+,B正确;电极A为阴极,LiMn O 得电子,电极
2 2 2 2 4
反应式为:2LiMn O+6e-+16H+=2Li++4Mn2++8H O,依据得失电子守恒,电解池总反应为:
2 4 2
2LiMn O+4H+=2Li++Mn2++3MnO+2H O,反应生成了Mn2+,Mn2+浓度增大,C错误;电解池总反应为:
2 4 2 2
2LiMn O+4H+=2Li++Mn2++3MnO+2H O,电解结束后,可通过调节溶液pH将锰离子转化为沉淀除去,然
2 4 2 2后再加入碳酸钠溶液,从而获得碳酸锂,D正确;故选C。
【方法技巧】①书写电解池的电极反应式时,可以用实际放电的离子表示,但书写电解池的总反应时,
弱电解质要写成分子式。
如用惰性电极电解食盐水时,阴极反应式为2H++2e-===H↑(或2HO+2e-===H↑+2OH-);总反应
2 2 2
离子方程式为2Cl-+2HO=====2OH-+H↑+Cl↑。
2 2 2
②电解水溶液时,应注意放电顺序,位于H+、OH-之后的离子一般不参与放电。
③Fe3+在阴极上放电时生成Fe2+而不是得到单质Fe。
【变式探究】(2021·广东卷)钴(Co)的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶
液中电解制备金属钴的装置示意图。下列说法正确的是( )
A.工作时,Ⅰ室和Ⅱ室溶液的pH均增大
B.生成1 mol Co,Ⅰ室溶液质量理论上减少16 g
C.移除两交换膜后,石墨电极上发生的反应不变
D.电解总反应:2Co2++2HO=====2Co+O↑+4H+
2 2
【答案】D
【解析】石墨电极为阳极,电极反应式为2HO-4e-===O ↑+4H+,H+通过阳离子交换膜由Ⅰ室进入
2 2
Ⅱ室,右侧Co电极为阴极,电极反应式为Co2++2e-===Co,Cl-通过阴离子交换膜由Ⅲ室进入Ⅱ室,与
H+结合生成盐酸。由上述分析知,Ⅰ室中水放电使硫酸浓度增大,Ⅱ室中生成盐酸,故Ⅰ室和Ⅱ室溶液的
pH均减小,A错误;生成1 mol Co时,转移2 mol电子,Ⅰ室有0.5 mol O(即16 g)逸出,有2 mol H+(即2
2
g)通过阳离子交换膜进入Ⅱ室,则Ⅰ室溶液质量理论上减少18 g,B错误;移除两交换膜后,石墨电极上
的电极反应式为2Cl--2e-===Cl↑,C错误;根据上述分析可知,电解时生成了O、Co、H+,则电解总
2 2
反应为2Co2++2HO=====2Co+O↑+4H+,D正确。
2 2
高频考点三 电子守恒在电化学计算中的应用
【例3】(2022·山东卷)设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐
生成 ,将废旧锂离子电池的正极材料 转化为 ,工作时保持厌氧环境,并定时将乙室
溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是A. 装置工作时,甲室溶液pH逐渐增大
B. 装置工作一段时间后,乙室应补充盐酸
C. 乙室电极反应式为
D. 若甲室 减少 ,乙室 增加 ,则此时已进行过溶液转移
【答案】BD
【解析】由于乙室中两个电极的电势差比甲室大,所以乙室是原电池,甲室是电解池,然后根据原电
池、电解池反应原理分析解答。电池工作时,甲室中细菌上乙酸盐的阴离子失去电子被氧化为CO 气体,
2
Co2+在另一个电极上得到电子,被还原产生Co单质,CHCOO-失去电子后,Na+通过阳膜进入阴极室,溶
3
液变为NaCl溶液,溶液由碱性变为中性,溶液pH减小,A错误;对于乙室,正极上LiCoO 得到电子,被
2
还原为Co2+,同时得到Li+,其中的O与溶液中的H+结合HO,因此电池工作一段时间后应该补充盐酸,B
2
正确;电解质溶液为酸性,不可能大量存在OH-,乙室电极反应式为:LiCoO +e-+4H+=Li++Co2++2H O,C
2 2
错误;若甲室Co2+减少200 mg,电子转移物质的量为n(e-)= ,乙室Co2+增加300
mg,转移电子的物质的量为n(e-)= ,说明此时已进行过溶液转移,D正确;故选
BD。
【方法技巧】电化学综合计算的三种常用方法
(1)根据总反应式计算
先写出电极反应式,再写出总反应式,最后根据总反应式列出比例式计算。
(2)根据电子守恒计算
①用于串联电路中阴阳两极产物、正负两极产物、相同电量等类型的计算,其依据是电路中转移的电
子数相等。②用于混合溶液中电解的分阶段计算。
(3)根据关系式计算
根据得失电子守恒定律建立起已知量与未知量之间的桥梁,构建计算所需的关系式。
【变式探究】(2021·全国甲卷)乙醛酸是一种重要的化工中间体,可采用如下图所示的电化学装置合成。
图中的双极膜中间层中的HO解离为H+和OH-,并在直流电场作用下分别向两极迁移。下列说法正确的
2
是( )
A.KBr在上述电化学合成过程中只起电解质的作用
C.制得2 mol乙醛酸,理论上外电路中迁移了1 mol电子
D.双极膜中间层中的H+在外电场作用下向铅电极方向迁移
【答案】D
【解析】由题图可知,在铅电极乙二酸变成乙醛酸是去氧的过程,发生还原反应,则铅电极是电解装
置的阴极,石墨电极发生氧化反应,反应为2Br--2e-===Br ,是电解装置的阳极。由上述分析可知,Br-
2
起到还原剂的作用,A错误;阳极上的反应式为2Br--2e-===Br ,B错误;制得2 mol乙醛酸,实际上是
2
左、右两侧各制得1 mol乙醛酸,共转移2 mol电子,故理论上外电路中迁移的电子为2 mol,C错误;电
解装置中,阳离子移向阴极(即铅电极),D正确。
【变式探究】按如图1所示装置进行电解,A、B、C、D均为铂电极,回答下列问题。(1)甲槽电解的是200 mL一定浓度的NaCl与CuSO 的混合溶液,理论上两极所得气体的体积随时间变
4
化的关系如图2所示(气体体积已换算成标准状况下的体积,电解前后溶液的体积变化忽略不计)。
①原混合溶液中NaCl的物质的量浓度为_____mol·L-1,CuSO 的物质的量浓度为______mol·L-1。
4
②t 时所得溶液的pH=________。
2
(2)乙槽为200 mL CuSO 溶液,乙槽内电解的总离子方程式:_____________________:
4
①当C极析出0.64 g物质时,乙槽溶液中生成的HSO 为________mol。电解后,若使乙槽内的溶液完
2 4
全复原,可向乙槽中加入________(填字母)。
A.Cu(OH) B.CuO
2
C.CuCO D.Cu (OH) CO
3 2 2 3
②若通电一段时间后,向所得的乙槽溶液中加入0.2 mol的Cu(OH) 才能恰好恢复到电解前的浓度,则
2
电解过程中转移的电子数为________。
【解析】(1)①A、B、C、D均为惰性电极Pt,甲槽电解NaCl和CuSO 的混合液,阳极上离子放电顺
4
序为Cl->OH->SO,阴极上离子放电顺序为Cu2+>H+>Na+,开始阶段阴极上析出Cu,阳极上产生
Cl,则题图2中曲线Ⅰ代表阴极产生气体体积的变化,曲线Ⅱ代表阳极产生气体体积的变化。阳极上发生
2
的反应依次为2Cl--2e-===Cl ↑、4OH--4e-===2HO+O↑,由曲线Ⅱ可知,Cl-放电完全时生成224 mL
2 2 2
Cl,根据Cl原子守恒可知,溶液中c(NaCl)==0.1 mol·L-1;阴极上发生的反应依次为Cu2++2e-
2
===Cu、2H++2e-===H↑,由曲线Ⅱ可知Cu2+放电完全时,阳极上产生224 mL Cl 和112 mL O,则电路
2 2 2
中转移电子的物质的量为0.01 mol×2+0.005 mol×4=0.04 mol,据得失电子守恒可知n(Cu2+)=0.04 mol×=
0.02 mol,故混合液中c(CuSO )==0.1 mol·L-1。②0~t 时间内相当于电解CuCl ,电解反应式为
4 1 2
CuCl =====Cu+Cl↑,t~t 时间内相当于电解CuSO ,而电解CuSO 溶液的离子反应为2Cu2++
2 2 1 2 4 4
2HO=====2Cu+O↑+4H+,则生成H+的物质的量为0.005 mol×4=0.02 mol,则有c(H+)==0.1 mol·L-
2 2
1,故溶液的pH=1。(2)电解CuSO 溶液时,Cu2+在阴极放电,水电离的OH-在阳极放电,电解的总离子
4
方程式为2Cu2++2HO=====2Cu+O↑+4H+。①C极为阴极,电极反应式为Cu2++2e-===Cu,析出0.64
2 2
g Cu(即0.01 mol)时,生成HSO 的物质的量也为0.01 mol。电解CuSO 溶液时,阴极析出Cu,阳极上产生
2 4 4
O,故可向电解质溶液中加入CuO、CuCO 等使电解质溶液完全复原。②加入0.2 mol Cu(OH) 相当于加入
2 3 2
0.2 mol CuO和0.2 mol HO,则电解过程中转移电子的物质的量为0.2 mol×2+0.2 mol×2=0.8 mol,即
2
0.8N 个电子。
A
【答案】(1)①0.1 0.1 ②1
(2)2Cu2++2HO=====2Cu+O↑+4H+ ①0.01 BC ②0.8N
2 2 A
高频考点四 电解原理的应用【例4】 (2022·北京卷)利用下图装置进行铁上电镀铜的实验探究。
序
装置示意图 电解质溶液 实验现象
号
阴极表面有无色气体,一段时间
① 后阴极表面有红色固体,气体减
少。经检验电解液中有
阴极表面未观察到气体,一段时
② 间后阴极表面有致密红色固体。
经检验电解液中无 元素
下列说法不正确的是
A. ①中气体减少,推测是由于溶液中 减少,且 覆盖铁电极,阻碍 与铁接触
B. ①中检测到 ,推测可能发生反应:
C. 随阴极析出 ,推测②中溶液 减少, 平衡逆移
D. ②中 生成 ,使得 比①中溶液的小, 缓慢析出,镀层更致密
【答案】C
【解析】由实验现象可知,实验①时,铁做电镀池的阴极,铁会先与溶液中的氢离子、铜离子反应生
成亚铁离子、氢气和铜,一段时间后,铜离子在阴极失去电子发生还原反应生成铜;实验②中铜离子与过
量氨水反应生成四氨合铜离子,四氨合铜离子在阴极得到电子缓慢发生还原反应生成铜,在铁表面得到比
实验①更致密的镀层。由分析可知,实验①时,铁会先与溶液中的氢离子、铜离子反应,当溶液中氢离子
浓度减小,反应和放电生成的铜覆盖铁电极,阻碍氢离子与铁接触,导致产生的气体减少,故A正确;由
分析可知,实验①时,铁做电镀池的阴极,铁会先与溶液中的氢离子、铜离子反应生成亚铁离子、氢气和
铜,可能发生的反应为 ,故B正确;由分析可知,四氨合铜离子在
阴极得到电子缓慢发生还原反应生成铜,随阴极析出铜,四氨合铜离子浓度减小,
平衡向正反应方向移动,故C错误;由分析可知,实验②中铜离子与过量
氨水反应生成四氨合铜离子,四氨合铜离子在阴极得到电子缓慢发生还原反应生成铜,在铁表面得到比实
验①更致密的镀层,故D正确;故选C。
【变式探究】(2021·广东卷)环氧乙烷(C HO)常用于医用消毒,一种制备方法为:使用惰性电极电解
2 4KCl溶液,用Cl-交换膜将电解液分为阴极区和阳极区,其中一区持续通入乙烯;电解结束,移出交换膜,
两区混合反应: HOCH CHCl+OH-===Cl-+HO+C HO。下列说法错误的是( )
2 2 2 2 4
A.乙烯应通入阴极区
B.移出交换膜前存在反应Cl+HOHCl+HClO
2 2
C.使用Cl- 交换膜阻止OH- 通过,可使Cl 生成区的pH逐渐减小
2
D.制备过程的总反应为HC===CH +HO===H ↑+C HO
2 2 2 2 2 4
【答案】A
【解析】环氧乙烷的制备原理:Cl-在阳极被氧化生成Cl,Cl 与水发生反应Cl+HOHCl+
2 2 2 2
HClO,HClO与乙烯发生加成反应生成HOCH CHCl;阴极区水电离出的氢离子放电生成氢气,同时产生
2 2
氢氧根离子,电解结束,移出交换膜,两区混合反应: HOCH CHCl+OH-===Cl-+HO+C HO。阳极
2 2 2 2 4
区产生HClO,所以乙烯通入阳极区,故A错误;根据分析可知阳极氧化生成的氯气会与水发生反应Cl+
2
HOHCl+HClO,故B正确;根据分析可知阳极区会产生HCl,使用Cl- 交换膜阻止OH- 通过,HCl
2
的浓度不断增大,pH逐渐减小,故C正确;根据分析可知该反应过程中KCl并没有被消耗,实际上是水、
乙烯反应,总反应为HC===CH +HO===H ↑+C HO,故D正确。
2 2 2 2 2 4
【举一反三】(2020·全国Ⅱ卷)电致变色器件可智能调控太阳光透过率,从而实现节能。下图是某电致
变色器件的示意图。当通电时,Ag+注入到无色WO 薄膜中,生成AgWO,器件呈现蓝色,对于该变化
3 x 3
过程,下列叙述错误的是( )
A.Ag为阳极
B.Ag+由银电极向变色层迁移
C.W元素的化合价升高
D.总反应为WO+xAg===AgWO
3 x 3
【答案】C
【解析】该装置是电解池,通电时银失去电子被氧化为Ag+,因此,银电极为阳极,A项正确;电解
池工作时,Ag+向阴极移动,即Ag+由银电极向变色层迁移,B项正确;WO 在阴极发生还原反应,即W
3
元素的化合价降低,C项错误;电池总反应为WO+xAg===AgWO,D项正确。
3 x 3
【变式探究】(2020·全国卷Ⅱ节选)(1)氯气是制备系列含氯化合物的主要原料,可采用如图所示的装置
来制取。装置中的离子膜只允许________离子通过,氯气的逸出口是________(填标号)。(2)(2020·全国卷Ⅱ节选)CH 和CO 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合
4 2
转化,其原理如图所示:
①阴极上的反应式为_____________________________________________________。
②若生成的乙烯和乙烷的体积比为2∶1,则消耗的CH 和CO 体积比为________。
4 2
【解析】(1)结合题图电解装置,可知阴极上水电离出的H+得电子生成H ,Na+从左侧通过离子膜向
2
阴极移动,即该装置中的离子膜只允许Na+通过;电解时阳极上Cl-失去电子,Cl 在a出口逸出。(2)①结
2
合图示可知CO 在阴极发生还原反应生成 CO,即阴极上的反应式为 CO +2e-===CO+O2-。②设生成
2 2
C H 和C H 的物质的量分别为2 mol和1 mol,则反应中转移电子的物质的量为4 mol×2+2 mol×1=10
2 4 2 6
mol,根据碳原子守恒,可知反应的CH 为6 mol;则由CO→CO转移10 mol电子,需消耗5 mol CO ,则
4 2 2
反应中消耗CH 和CO 的体积比为6∶5。
4 2
【答案】(1)Na+ a (2) ①CO+2e-===CO+O2- ②6∶5
2
高频考点五 金属腐蚀与防护
【例5】(2022·广东卷)为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀锌铁片
放入酸化的 溶液中。一段时间后,取溶液分别实验,能说明铁片没有被腐蚀的是
A. 加入 溶液产生沉淀 B. 加入淀粉碘化钾溶液无蓝色出现
C. 加入 溶液无红色出现 D. 加入 溶液无蓝色沉淀生成
【答案】D
【解析】镀层有破损的镀锌铁片被腐蚀,则将其放入到酸化的3%NaCl溶液中,会构成原电池,由于
锌比铁活泼,作原电池的负极,而铁片作正极,溶液中破损的位置会变大,铁也会继续和酸化的氯化钠溶液反应产生氢气,溶液中会有亚铁离子生成,据此分析解答。氯化钠溶液中始终存在氯离子,所以加入硝
酸银溶液后,不管铁片是否被腐蚀,均会出现白色沉淀,故A不符合题意;淀粉碘化钾溶液可检测氧化性
物质,但不论铁片是否被腐蚀,均无氧化性物质可碘化钾发生反应,故B不符合题意;KSCN溶液可检测
铁离子的存在,上述现象中不会出现铁离子,所以无论铁片是否被腐蚀,加入KSCN溶液后,均无红色出
现,故C不符合题意;K[Fe(CN) ]是用于检测Fe2+的试剂,若铁片没有被腐蚀,则溶液中不会生成亚铁离
3 6
子,则加入K[Fe(CN) ]溶液就不会出现蓝色沉淀,故D符合题意。综上所述,答案为D。
3 6
【方法技巧】判断金属腐蚀快慢的规律
(1)对同一电解质溶液来说,腐蚀速率的快慢:电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀
>有防护措施的腐蚀。
(2)对同一金属来说,在不同溶液中腐蚀速率的快慢:强电解质溶液中>弱电解质溶液中>非电解质溶液
中。
(3)活动性不同的两种金属,活动性差别越大,腐蚀速率越快。
(4)对同一种电解质溶液来说,电解质浓度越大,金属腐蚀越快。
【变式探究】(2020·江苏卷)将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。在题
图所示的情境中,下列有关说法正确的是
A. 阴极的电极反应式为
B. 金属M的活动性比Fe的活动性弱
C. 钢铁设施表面因积累大量电子而被保护
D. 钢铁设施在河水中的腐蚀速率比在海水中的快
【答案】C
【解析】该装置为原电池原理的金属防护措施,为牺牲阳极的阴极保护法,金属M作负极,钢铁设备
作正极,据此分析解答。阴极的钢铁设施实际作原电池的正极,正极金属被保护不失电子,故A错误;阳
极金属M实际为原电池装置的负极,电子流出,原电池中负极金属比正极活泼,因此M活动性比Fe的活
动性强,故B错误;金属M失电子,电子经导线流入钢铁设备,从而使钢铁设施表面积累大量电子,自身
金属不再失电子从而被保护,故C正确;海水中的离子浓度大于河水中的离子浓度,离子浓度越大,溶液
的导电性越强,因此钢铁设施在海水中的腐蚀速率比在河水中快,故D错误;故选C。【变式探究】[2019·江苏卷]将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图所示装置中,进
行铁的电化学腐蚀实验。下列有关该实验的说法正确的是
A.铁被氧化的电极反应式为Fe−3e−===Fe3+
B.铁腐蚀过程中化学能全部转化为电能
C.活性炭的存在会加速铁的腐蚀
D.以水代替NaCl溶液,铁不能发生吸氧腐蚀
【答案】C
【解析】在铁的电化学腐蚀中,铁单质失去电子转化为二价铁离子,即负极反应为:Fe−2e−=Fe2+,故
A错误;铁的腐蚀过程中化学能除了转化为电能,还有一部分转化为热能,故B错误;活性炭与铁混合,
在氯化钠溶液中构成了许多微小的原电池,加速了铁的腐蚀,故C正确;以水代替氯化钠溶液,水也呈中
性,铁在中性或碱性条件下易发生吸氧腐蚀,故D错误。