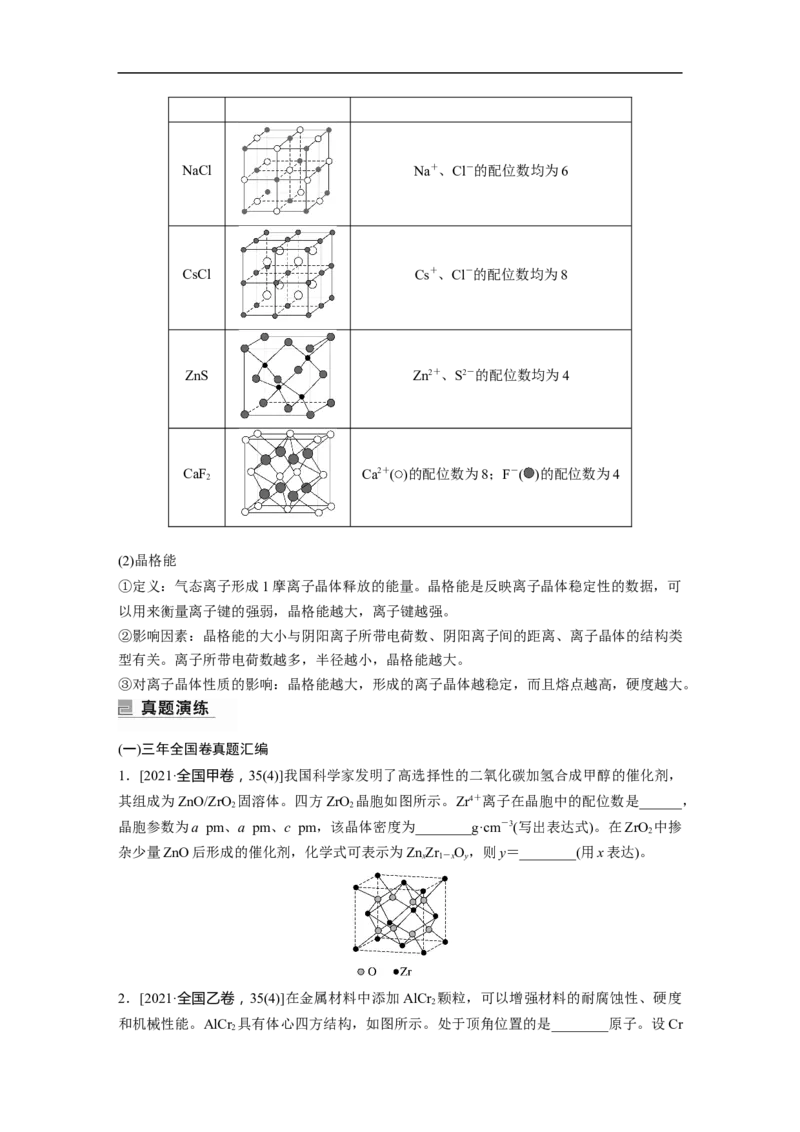
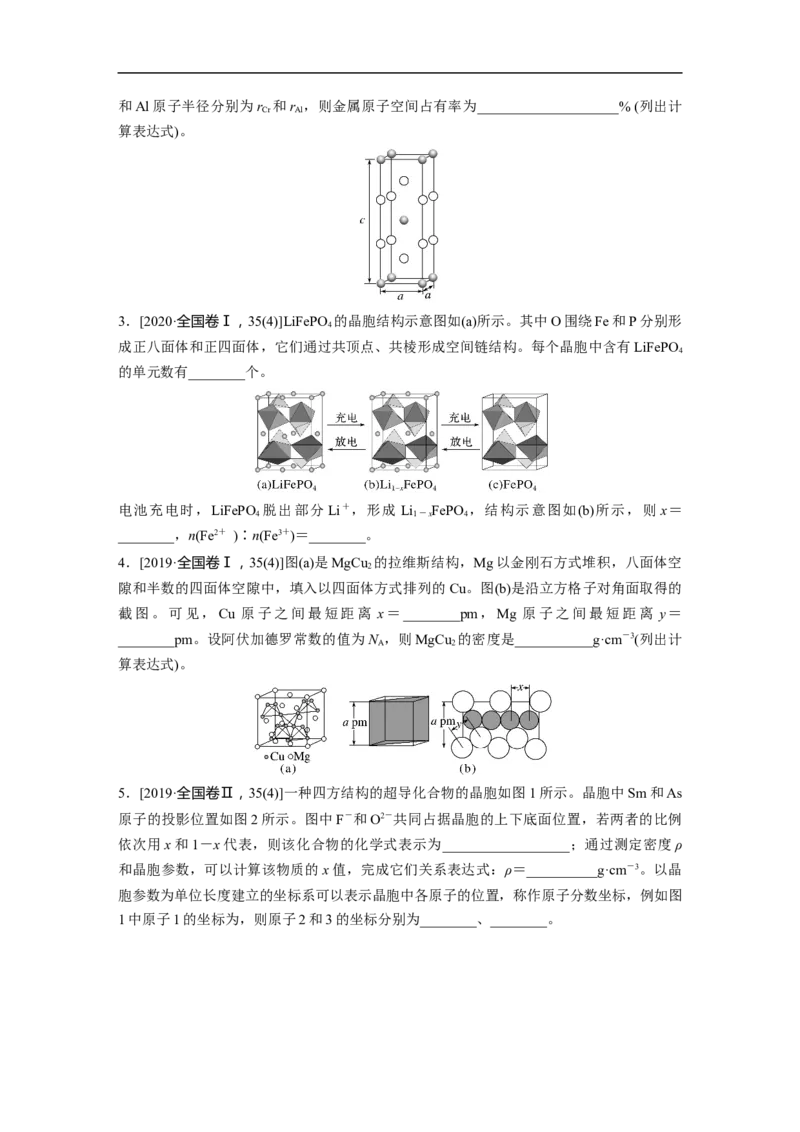
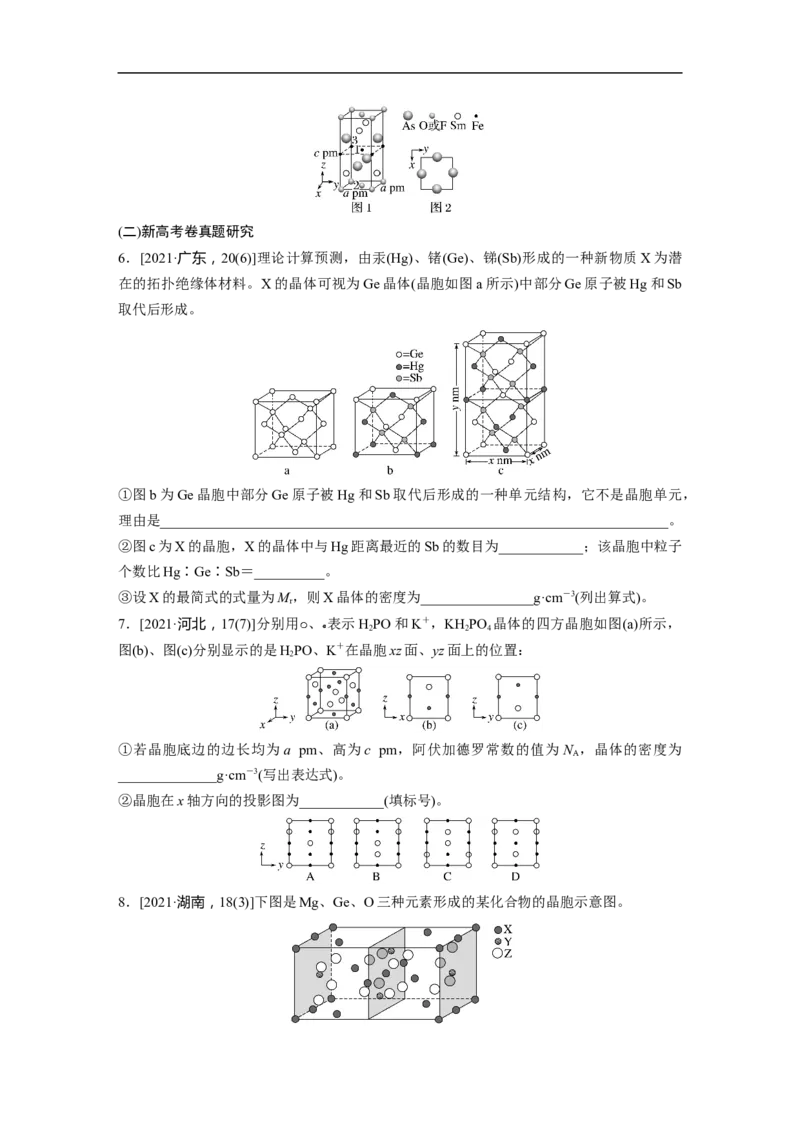
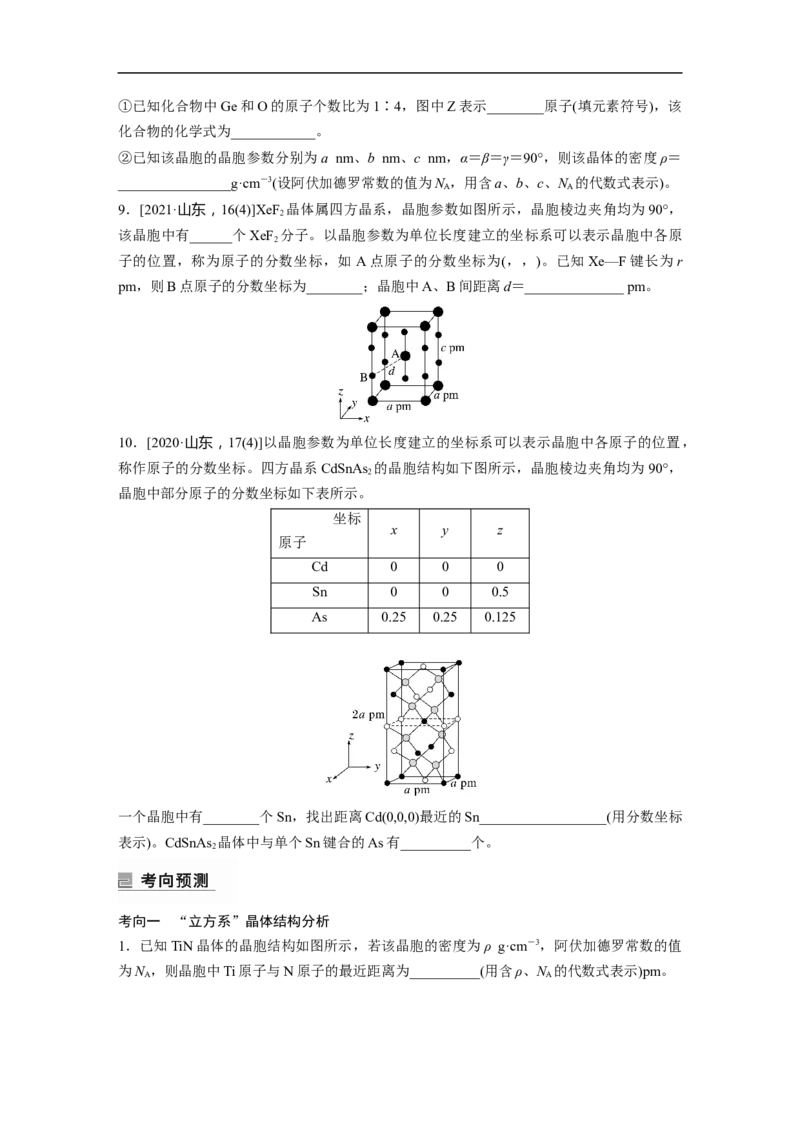
文档内容
[复习目标] 1.掌握常见的晶体类型及微粒间相互作用。2.掌握常见晶体的结构及相关计算。
考点一 晶体类型与微粒间相互作用力
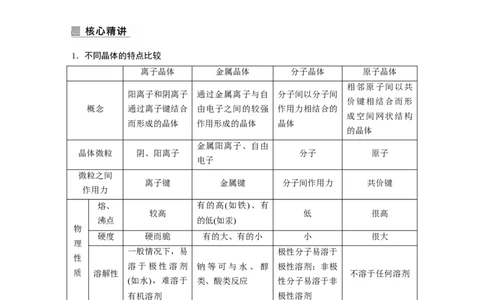
1.不同晶体的特点比较
离子晶体 金属晶体 分子晶体 原子晶体
相邻原子间以共
阳离子和阴离子 通过金属离子与自 分子间以分子间
价键相结合而形
概念 通过离子键结合 由电子之间的较强 作用力相结合的
成空间网状结构
而形成的晶体 作用形成的晶体 晶体
的晶体
金属阳离子、自由
晶体微粒 阴、阳离子 分子 原子
电子
微粒之间
离子键 金属键 分子间作用力 共价键
作用力
熔、 有的高(如铁)、有
较高 低 很高
沸点 的低(如汞)
物
硬度 硬而脆 有的大、有的小 小 很大
理
一般情况下,易 极性分子易溶于
性
溶于极性溶剂 钠等可与水、醇 极性溶剂;非极
质 溶解性 不溶于任何溶剂
(如水),难溶于 类、酸类反应 性分子易溶于非
有机溶剂 极性溶剂
2.晶体类别的判断方法
(1)依据构成晶体的微粒和微粒间作用力判断
由阴、阳离子形成的离子键构成的晶体为离子晶体;由原子形成的共价键构成的晶体为原子
晶体;由分子依靠分子间作用力形成的晶体为分子晶体;由金属阳离子、自由电子以金属键
构成的晶体为金属晶体。
(2)依据物质的分类判断
①活泼金属氧化物和过氧化物(如KO、NaO 等)、强碱(如NaOH、KOH等)、绝大多数的盐
2 2 2是离子晶体。
②部分非金属单质、所有非金属氢化物、部分非金属氧化物、几乎所有的酸、绝大多数有机
物的晶体是分子晶体。
③常见的单质类原子晶体有金刚石、晶体硅、晶体硼等,常见的化合物类原子晶体有SiC、
SiO、AlN、BP、GaAs等。
2
④金属单质、合金是金属晶体。
(3)依据晶体的熔点判断
不同类型晶体熔点大小的一般规律:原子晶体>离子晶体>分子晶体。金属晶体的熔点差别
很大,如钨、铂等熔点很高,铯等熔点很低。
(4)依据导电性判断
①离子晶体溶于水和熔融状态时均能导电。
②原子晶体一般为非导体。
③分子晶体为非导体,但分子晶体中的电解质(主要是酸和强极性非金属氢化物)溶于水时,
分子内的化学键断裂形成自由移动的离子,也能导电。
④金属晶体是电的良导体。
(5)依据硬度和机械性能判断
一般情况下,硬度:原子晶体>离子晶体>分子晶体。金属晶体多数硬度大,但也有较小的,
且具有较好的延展性。
3.晶体熔、沸点的比较
(1)原子晶体
→→→
如熔点:金刚石>碳化硅>晶体硅。
(2)离子晶体
一般地说,阴、阳离子的电荷数越多,离子半径越小,离子间的作用力就越强,离子晶体的
熔、沸点就越高,如熔点:MgO>NaCl>CsCl。
(3)分子晶体
①分子间作用力越大,物质的熔、沸点越高;具有分子间氢键的分子晶体熔、沸点反常得高,
如沸点:HO>HTe>HSe>H S。
2 2 2 2
②组成和结构相似的分子晶体,相对分子质量越大,熔、沸点越高,如熔、沸点:
SnH >GeH>SiH >CH 。
4 4 4 4
③组成和结构不相似的物质(相对分子质量接近),分子的极性越大,其熔、沸点越高,如熔、
沸点:CO>N。
2
④在同分异构体中,一般支链越多,熔、沸点越低,如熔、沸点:正戊烷>异戊烷。
(4)金属晶体
金属离子半径越小,所带电荷数越多,其金属键越强,熔、沸点就越高,如熔、沸点:
Na