文档内容
第 23 讲 电解池 金属的腐蚀与防护
(模拟精练+真题演练)
完卷时间:50分钟
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Cu 64
一、选择题(每小题只有一个正确选项,共12×5分)
1.(2023·河南安阳·统考三模)二氧化氯(ClO )是一种安全的绿色消毒剂,实验室可用下列方法制备:
2
①电解NH Cl的盐酸溶液制得NCl (N元素为-3价)溶液;②将NCl 溶液与NaClO 溶液混合制得ClO 。
4 3 3 2 2
下列说法正确的是
A.①中在电解池的阴极得到NCl
3
B.组成①中的电解池除需要有电源、导线和大烧杯等,还必须有两个不同材质的电极
C.②中反应的氧化剂与还原剂的物质的量之比是6:1
D.②中反应后的溶液中主要存在的阳离子是Na+
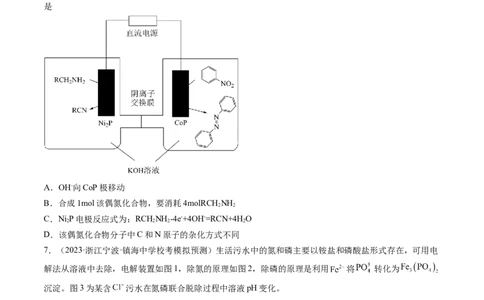
2.(2023·浙江·校联考一模)利用电解池原理可将 转化为燃料或者化学品。下图通过将 与辛胺反
应耦合,实现了两电极体系中产物的高选择性合成。
下列说法正确的是
A.装置中b电极为阴极,发生还原反应
B.电极a的电极反应可能为:
C.中间的离子交换膜一定是质子交换膜
D.电解过程中,a、b两极反应物物质的量之比为2∶1
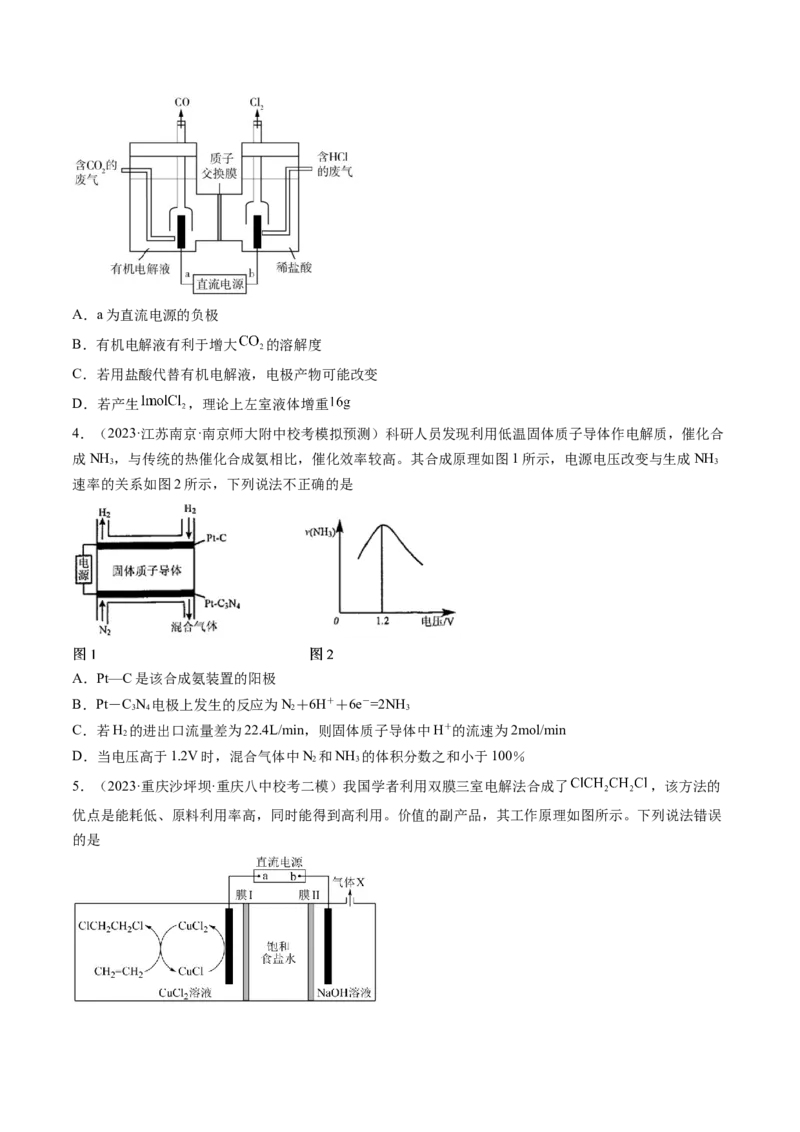
3.(2023·河北·校联考模拟预测)利用 和 废气作原料,通过电化学原理制备光气原料气的装置如
图所示。下列说法错误的是A.a为直流电源的负极
B.有机电解液有利于增大 的溶解度
C.若用盐酸代替有机电解液,电极产物可能改变
D.若产生 ,理论上左室液体增重
4.(2023·江苏南京·南京师大附中校考模拟预测)科研人员发现利用低温固体质子导体作电解质,催化合
成NH ,与传统的热催化合成氨相比,催化效率较高。其合成原理如图1所示,电源电压改变与生成NH
3 3
速率的关系如图2所示,下列说法不正确的是
A.Pt—C是该合成氨装置的阳极
B.Pt-C N 电极上发生的反应为N+6H++6e-=2NH
3 4 2 3
C.若H 的进出口流量差为22.4L/min,则固体质子导体中H+的流速为2mol/min
2
D.当电压高于1.2V时,混合气体中N 和NH 的体积分数之和小于100%
2 3
5.(2023·重庆沙坪坝·重庆八中校考二模)我国学者利用双膜三室电解法合成了 ,该方法的
优点是能耗低、原料利用率高,同时能得到高利用。价值的副产品,其工作原理如图所示。下列说法错误
的是A.b为电源负极,气体X为
B.膜I、膜Ⅱ依次适合选用阴离子交换膜、阳离子交换膜
C.电解过程中需及时补充NaCl
D.制得 的同时NaOH溶液质量增加80g
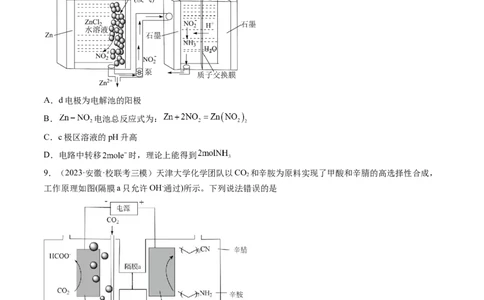
6.(2023·安徽芜湖·统考二模)下图为合成偶氮化合物 的电化学装置,有关说法正确的
是
A.OH-向CoP极移动
B.合成1mol该偶氮化合物,要消耗4molRCH NH
2 2
C.Ni P电极反应式为:RCHNH -4e-+4OH-=RCN+4H O
2 2 2 2
D.该偶氮化合物分子中C和N原子的杂化方式不同
7.(2023·浙江宁波·镇海中学校考模拟预测)生活污水中的氮和磷主要以铵盐和磷酸盐形式存在,可用电
解法从溶液中去除,电解装置如图1,除氮的原理如图2,除磷的原理是利用 将 转化为
沉淀。图3为某含 污水在氮磷联合脱除过程中溶液pH变化。
下列说法不正确的是A.产生 的主要过程是:
B.除磷时阴极产物主要是
C.脱氮过程中阳极主要发生的反应为
D.在0-20min时脱除的元素是氮元素
8.(2023·福建南平·统考三模)西北工业大学推出一种新型 电池。该电池能有效地捕获 ,
将其转化为 ,再将产生的 电解制氨,过程如图所示。下列说法错误的是
A.d电极为电解池的阳极
B. 电池总反应式为:
C.c极区溶液的pH升高
D.电路中转移 时,理论上能得到
9.(2023·安徽·校联考三模)天津大学化学团队以CO 和辛胺为原料实现了甲酸和辛腈的高选择性合成,
2
工作原理如图(隔膜a只允许OH-通过)所示。下列说法错误的是
A.Ni P电极的电势比In/In O 电极的高
2 2 3-x
B.In/In O 电极上可能有副产物H 生成
2 3-x 2
C.电解过程中,OH-由In/In O 电极区向Ni P电极区迁移
2 3-x 2
D.电路中转移2mol电子时,阴极区溶液质量增加44g(不考虑气体的溶解)
10.(2023·陕西榆林·统考模拟预测)电解HF和熔融KHF 的混合物(熔融混合物中常加入少量LiF或
2
AlF)制备单质氟,以电解槽内壁(镍铜合金)和石墨为电极,总反应为2KHF =2KF+F ↑+H ↑。下列有关电
3 2 2 2
解制备单质氟的说法正确的是A.电解过程中,电解槽内壁与电源的正极相连
B.石墨电极发生的电极反应为2F- +2e- =F↑
2
C.电解过程中加入少量LiF或AlF 可以降低混合物的熔点,增强导电性
3
D.电解一段时间后,加入一定量的固体KHF 可还原混合物的组成
2
11.(2023·湖南长沙·长郡中学校考一模)“乌铜走银”是云南特有的中国传统铜制工艺品。它以铜为胎,
在胎上雕刻各种花纹图案,然后将熔化的银(或金)水填入花纹图案中,完成制作后需经常用汗湿的手摩擦
器物,使铜胎变为乌黑,透出银(或金)纹图案。下列有关该工艺的说法错误的是
A.用铜和少量的贵金属熔炼成的铜胎仍具有金属性能
B.熔化银(或金)时需破坏金属键
C.铜胎变乌黑的原因是汗液中存在氧化性物质使铜变成了氧化铜
D.“乌铜走银”工艺品最终呈现出黑白(或黑黄)分明的装饰效果
12.(2023·辽宁鞍山·鞍山一中校考模拟预测)近日,清华大学王保国教授团队设计出了一种双极膜(将
解离成 和 )电解合成 的反应器,其简化模型如图所示,已知:法拉第常数 Cmol
(法拉第常数的物理意义:每摩尔电子携带的电荷量)。下列说法错误的是 ⋅
A.M极电势低于N极电势
B.电解合成过程中,N极附近电解质溶液的pH减小
C.阴极的电极反应式为
D.理论上产生0.02mol 时,外电路流过的电量为1930C
二、主观题(共3小题,共40分)
13.(14分)钢铁工业是国家工业的基础,钢铁生锈现象却随处可见,为此每年国家损失大量资金。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的正极电极反应式为:
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用图①所示的方案,其中焊接在铁闸门上的固体材料R
可以采用 。
A.铜 B.钠 C.锌 D.石墨(3)图②所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的 极。
(4)钢铁的防护除了用电化学保护方法之外,在钢铁制品表面镀铜也可以有效地防止其腐蚀,电镀的装置如
图所示:
①电镀装置图的“直流电源”中, 填“a”或“b” 是正极。Fe电极反应式为 ;
②接通电源前,装置图中的铜、铁两个电极质量相等,电镀完成后,将两个电极取出,用水小心冲洗干净、
烘干,然后称量,二者质量之差为5.12g,由此计算电镀过程中电路中通过电子的物质的量为 。
③上述铁镀件破损后,铁更容易被腐蚀。请简要说明镀铜铁镀件破损后,铁更容易被腐蚀的原因:
。
14.(14分)Ⅰ.高铁酸盐在能源、环保等方面有着广泛的用途。高铁酸钾(K FeO)不仅是一种理想的水处
2 4
理剂,而且高铁电池的研制也在进行中。如图是高铁电池的模拟实验装置:
(1)该电池放电时正极的电极反应式为 。
(2)盐桥中盛有饱和KCl溶液,此盐桥中氯离子向 (填“左”或“右”)移动;若用阳离子交换膜代替盐桥,
则钾离子向 (填“左”或“右”)移动。
(3)如图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有 。
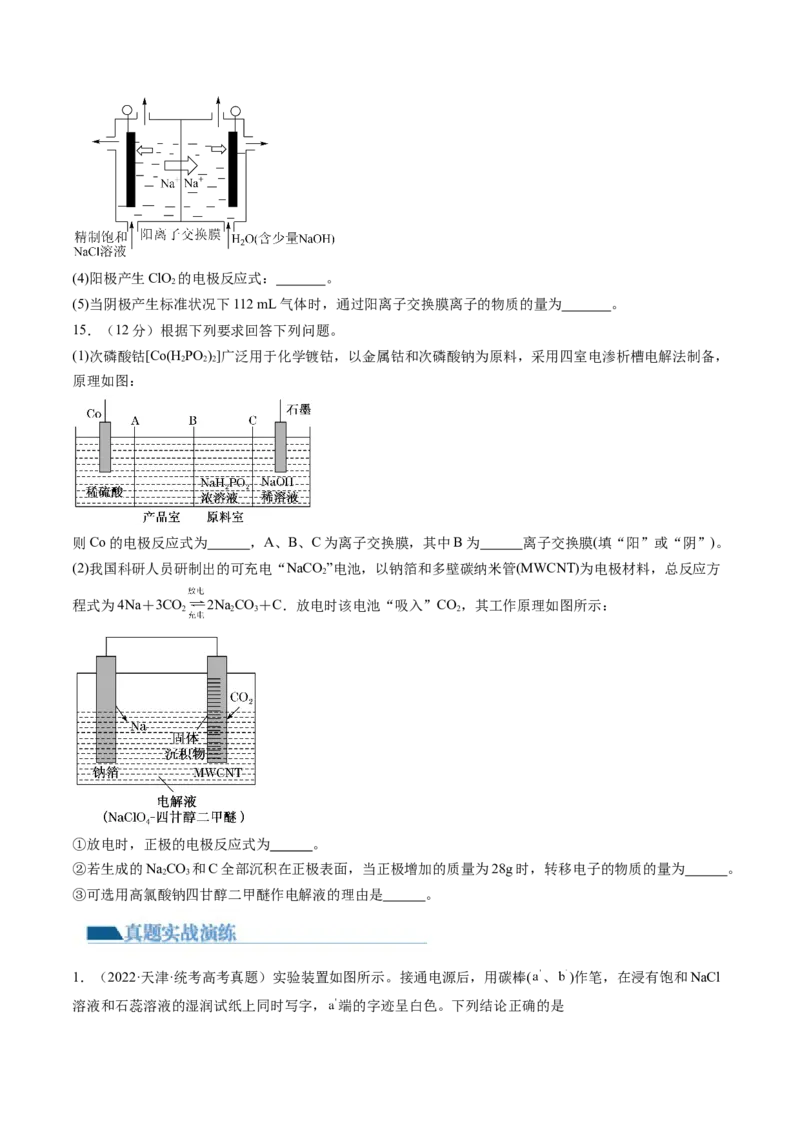
Ⅱ.二氧化氯(ClO )为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。如图是目
2
前已开发出用电解法制取ClO 的新工艺。
2(4)阳极产生ClO 的电极反应式: 。
2
(5)当阴极产生标准状况下112 mL气体时,通过阳离子交换膜离子的物质的量为 。
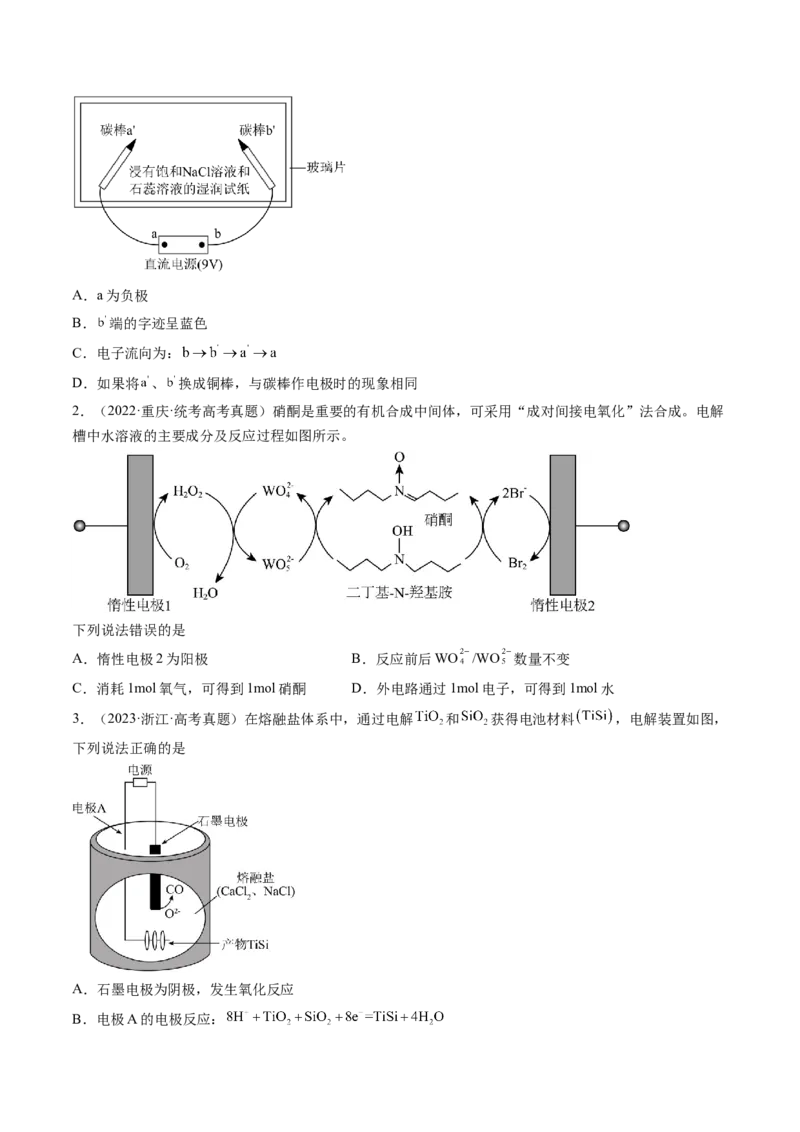
15.(12分)根据下列要求回答下列问题。
(1)次磷酸钴[Co(H PO )]广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,
2 2 2
原理如图:
则Co的电极反应式为 ,A、B、C为离子交换膜,其中B为 离子交换膜(填“阳”或“阴”)。
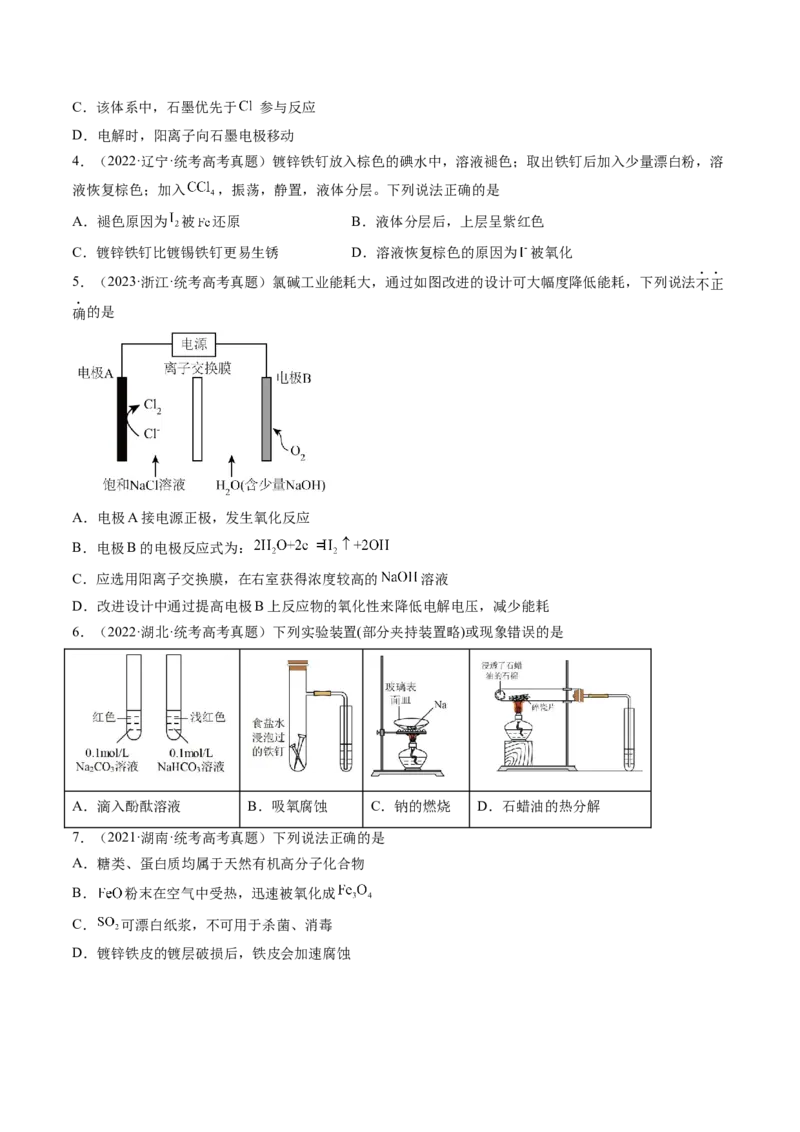
(2)我国科研人员研制出的可充电“NaCO”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应方
2
程式为4Na+3CO 2NaCO+C.放电时该电池“吸入”CO,其工作原理如图所示:
2 2 3 2
①放电时,正极的电极反应式为 。
②若生成的NaCO 和C全部沉积在正极表面,当正极增加的质量为28g时,转移电子的物质的量为 。
2 3
③可选用高氯酸钠四甘醇二甲醚作电解液的理由是 。
1.(2022·天津·统考高考真题)实验装置如图所示。接通电源后,用碳棒( 、 )作笔,在浸有饱和NaCl
溶液和石蕊溶液的湿润试纸上同时写字, 端的字迹呈白色。下列结论正确的是A.a为负极
B. 端的字迹呈蓝色
C.电子流向为:
D.如果将 、 换成铜棒,与碳棒作电极时的现象相同
2.(2022·重庆·统考高考真题)硝酮是重要的有机合成中间体,可采用“成对间接电氧化”法合成。电解
槽中水溶液的主要成分及反应过程如图所示。
下列说法错误的是
A.惰性电极2为阳极 B.反应前后WO /WO 数量不变
C.消耗1mol氧气,可得到1mol硝酮 D.外电路通过1mol电子,可得到1mol水
3.(2023·浙江·高考真题)在熔融盐体系中,通过电解 和 获得电池材料 ,电解装置如图,
下列说法正确的是
A.石墨电极为阴极,发生氧化反应
B.电极A的电极反应:C.该体系中,石墨优先于 参与反应
D.电解时,阳离子向石墨电极移动
4.(2022·辽宁·统考高考真题)镀锌铁钉放入棕色的碘水中,溶液褪色;取出铁钉后加入少量漂白粉,溶
液恢复棕色;加入 ,振荡,静置,液体分层。下列说法正确的是
A.褪色原因为 被 还原 B.液体分层后,上层呈紫红色
C.镀锌铁钉比镀锡铁钉更易生锈 D.溶液恢复棕色的原因为 被氧化
5.(2023·浙江·统考高考真题)氯碱工业能耗大,通过如图改进的设计可大幅度降低能耗,下列说法不正
确的是
A.电极A接电源正极,发生氧化反应
B.电极B的电极反应式为:
C.应选用阳离子交换膜,在右室获得浓度较高的 溶液
D.改进设计中通过提高电极B上反应物的氧化性来降低电解电压,减少能耗
6.(2022·湖北·统考高考真题)下列实验装置(部分夹持装置略)或现象错误的是
A.滴入酚酞溶液 B.吸氧腐蚀 C.钠的燃烧 D.石蜡油的热分解
7.(2021·湖南·统考高考真题)下列说法正确的是
A.糖类、蛋白质均属于天然有机高分子化合物
B. 粉末在空气中受热,迅速被氧化成
C. 可漂白纸浆,不可用于杀菌、消毒
D.镀锌铁皮的镀层破损后,铁皮会加速腐蚀