文档内容
专题 11 水溶液中的离子反应与平衡
第 32 练 盐类的水解
1. 下列物质的水溶液因水解而呈碱性的是( )
A.NaCO B.AlCl C.Ca(OH) D.NaNO
2 3 3 2 3
2.(2020•浙江7月选考)水溶液呈酸性的是( )
A.NaCl B.NaHSO C.HCOONa D.NaHCO
4 3
3.下列物质的水溶液因水解而呈碱性的是( )
A.NH NO B.NaCO C.NaCl D.Al (SO )
4 3 2 3 2 4 3
4.把下列物质的水溶液加热蒸干后,能得到原溶质的是( )
A.NaHCO B.AlCl C.NH HCO D.Fe (SO )
3 3 4 3 2 4 3
5.下列方程式属于水解反应方程式的是( )
A.HCO HCO -+H+ B.HCO -+H O HO++CO 2-
2 3 3 3 2 3 3
C.HCO -+OH-=H O+CO2- D.CO2-+ H O HCO -+ OH-
3 2 3 3 2 3
6.下列用于解释事实的化学用语中,不正确的是( )
A.NaS溶液显碱性: S2-+ 2HO HS + 2OH-
2 2 2
B.KCr O 溶液中含有CrO2-:Cr O2- + HO 2CrO2- + 2H+
2 2 7 4 2 7 2 4
C.盛放NaOH 溶液的试剂瓶不能用玻璃塞: 2OH-+ SiO=SiO 2-+ HO
2 3 2
D.红热木炭遇浓硫酸产生刺激性气味气体: 2HSO ( 浓)+C CO↑+2SO↑+2H O
2 4 2 2 2
7.配制下列溶液时常需加入少量括号内的物质,其中不是为了抑制离子水解的是( )
A.FeSO (Fe) B.CuCl (HCl) C.FeCl (HCl) D.CHCOONa (NaOH)
4 2 3 3
8.下列根据反应原理设计的应用,不正确的是( )
A.CO+HO HCO+OH- 用热的纯碱溶液清洗油污
2
B.Al3++3HO Al(OH) (胶体)+3H+ 明矾净水
2 3
C.TiCl +(x+2)H O(过量) TiO·xHO↓+4HCl 制备TiO 纳米粉
4 2 2 2 2
D.SnCl +HO Sn(OH)Cl↓+HCl 配制氯化亚锡溶液时加入氢氧化钠
2 2
9.将下列固体物质溶于水,再将其溶液加热,蒸发结晶、再灼烧,得到化学组成与原固体物质相同
的是( )
①胆矾 ②氯化铝 ③硫酸铝 ④氯化铜
A.③ B.①④ C.①②③ D.全部10.下列关于盐类水解的说法错误的是( )
A.在纯水中加入能水解的盐一定促进水的电离
B.同温时,等浓度的NaHCO 和NaCO 溶液,NaHCO 溶液的pH大
3 2 3 3
C.在NH Cl溶液中加入稀HNO 能抑制NH水解
4 3
D.加热CHCOONa溶液,溶液中 的值将减小 ( )
3
11.下列操作会促进HO的电离,且使溶液pH>7的是( )
2
A.将纯水加热到90 ℃ B.向水中加少量NaOH溶液
C.向水中加少量NaCO 溶液 D.向水中加少量FeCl 溶液
2 3 3
12.有①NaCO 溶液 ②CHCOONa溶液 ③NaOH溶液各25 mL,物质的量浓度均为0.1 mol·L-
2 3 3
1,下列说法正确的是( )
A.3种溶液pH的大小顺序是 ③>②>①
B.若将3种溶液稀释相同倍数,pH变化最大的是②
C.若分别加入25 mL 0.1 mol·L-1盐酸后,pH最大的是①
D.若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>②
13.合理利用某些盐能水解的性质,能解决许多生产、生活中的问题,下列叙述的事实与盐类水解的
性质无关的是( )
A.金属焊接时可用NH Cl溶液做除锈剂
4
B.配制FeSO 溶液时,加入一定量Fe粉
4
C.长期施用铵态氮肥会使土壤酸化
D.向FeCl 溶液中加入CaCO 粉末后有气泡产生
3 3
14.对滴有酚酞溶液的下列溶液,操作后颜色变深的是( )
A.明矾溶液加热
B.CHCOONa溶液加热
3
C.氨水中加入少量NH Cl固体
4
D.小苏打溶液中加入少量NaCl固体
15.下列关于盐类水解的应用中,说法正确的是( )
A.加热蒸干NaCO 溶液,最后可以得到NaOH和NaCO 的混合固体
2 3 2 3
B.除去MgCl 中的Fe3+,可以加入NaOH固体
2
C.明矾净水的反应:Al3++3HO Al(OH) (胶体)+3H+
2 3
D.加热蒸干KCl溶液,最后得到KOH固体(不考虑CO 的反应)
2
1.在一定条件下,NaCO 溶液存在水解平衡:CO2-+HO HCO -+OH-。下列说法正确的是(
2 3 3 2 3
)A. 稀释溶液,水解平衡常数增大
B. 加入少量NH Cl固体,平衡朝正反应方向移动
4
C. 升高温度, 减小
D. 加入NaOH固体,溶液pH减小
2.(2021•广东选择性考试)鸟嘌呤(G)是一种有机弱碱,可与盐酸反应生成盐酸盐(用GHCl表示)。已知
GHCl水溶液呈酸性,下列叙述正确的是( )
A.0.001mol·L-1GHCl水溶液的pH=3
B.0.001mol·L-1GHCl水溶液加水稀释,pH升高
C.GHCl在水中的电离方程式为:GHCl=G+HCl
D.GHCl水溶液中:c(OH-)+c(Cl-)=c(GH+)+c(G)
3.下列实验操作不能达到实验目的的是( )
实验目的 实验操作
A 实验室配制FeCl 水溶液 将FeCl 溶于少量浓盐酸中,再加水稀释
3 3
B 由MgCl 溶液制备无水MgCl 将MgCl 溶液加热蒸干
2 2 2
将0.1mol·L-1MgSO 溶液滴入NaOH溶液
证明Cu(OH) 的溶度积比 4
C 2 至不再有沉淀产生,再滴加
Mg(OH) 的小
2 0.1mol·L-1CuSO 溶液
4
D 除去MgCl 酸性溶液中的Fe3+ 加入过量MgO充分搅拌,过滤
2
4.(2020•浙江 7 月选考)常温下,用 0.1 mol·L−1氨水滴定 10 mL 浓度均为 0.1 mol·L−1的 HCl 和
CHCOOH的混合液,下列说法不正确的是( )
3
A.在氨水滴定前,HCl和CHCOOH的混合液中c(Cl−)>c(CHCOO−)
3 3
B.当滴入氨水10 mL时,c(NH)+c(NH ·H O)=c(CHCOO−)+c(CHCOOH)
3 2 3 3
C.当滴入氨水20 mL时,c(CHCOOH)+c(H+)=c(NH ·H O)+c(OH−)
3 3 2
D.当溶液呈中性时,氨水滴入量大于20 mL,c(NH)<c(Cl−)
5.将标准状况下1.68LCO 通入含有2gNaOH的水溶液中,完全反应并得到2L碱性溶液。则对于该溶
2
液表述正确的是( )
A.2c(Na+)=3[c(HCO-)+c(CO 2-)+c(H CO)]
3 3 2 3
B.c(Na+)+c(H+)=c(HCO-)+2c(CO 2-)+c(OH-)
3 3
C.HCO -的电离程度大于HCO -的水解程度
3 3
D.存在的平衡体系只有:HCO -+H O HCO+OH-,HCO - H++ CO2-
3 2 2 3 3 36.下列溶液中粒子的物质的量浓度关系正确的是( )
A.0.1 mol·L-1 NaHCO 溶液与0.1 mol·L-1 NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO)>
3
c(HCO)>c(OH-)
B.20 mL 0.1 mol·L-1 CHCOONa溶液与10 mL 0.1 mol·L-1 HCl溶液混合后溶液呈酸性,所得溶液中:
3
c(CHCOO-)>c(Cl-)>c(CHCOOH)>c(H+)
3 3
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH)+c(OH
-)
D.0.1 mol·L-1 CHCOOH溶液与0.1 mol·L-1 NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)
3
+c(CHCOOH)
3
7.在一定条件下,NaCO 溶液存在水解平衡:CO2-+HO HCO -+OH-。下列说法正确的是(
2 3 3 2 3
)
A.稀释溶液,水解平衡向逆反应方向移动,水解程度减小
B.通入CO,平衡向正反应方向移动
2
C.升高温度,c(HCO -)/c(CO2-)减小
3 3
D.加入NaOH固体,溶液pH减小
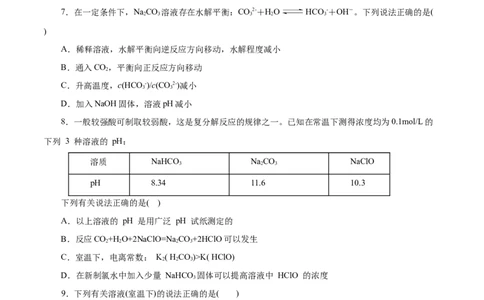
8.一般较强酸可制取较弱酸,这是复分解反应的规律之一。已知在常温下测得浓度均为0.1mol/L的
下列 3 种溶液的 pH:
溶质 NaHCO NaCO NaClO
3 2 3
pH 8.34 11.6 10.3
下列有关说法正确的是( )
A.以上溶液的 pH 是用广泛 pH 试纸测定的
B.反应CO+H O+2NaClO=Na CO+2HClO可以发生
2 2 2 3
C.室温下,电离常数: K( H CO)>K( HClO)
2 2 3
D.在新制氯水中加入少量 NaHCO 固体可以提高溶液中 HClO 的浓度
3
9.下列有关溶液(室温下)的说法正确的是( )
A.NaCO 和NaHCO 形成的混合溶液中:2c(Na+)=3[c(CO 2-)+c(HCO-)+c(H CO)]
2 3 3 3 3 2 3
B.0.10mol•L-1NaHSO 溶液中通入NH 至溶液pH=7:c(Na+)>c(NH+)>c(SO2-)
3 3 4 3
C.物质的量浓度相等的①(NH )SO 溶液、②NH HCO 溶液、③NH Cl溶液、④(NH )Fe(SO ) 溶液
4 2 4 4 3 4 4 2 4 2
中,c(NH +)的大小关系:④>①>②>③
4
D.0.10mol•L-1CHCOONa溶液中通入HCl至溶液pH=7:c(Na+)>c(CH COOH)>c(Cl-)
3 3
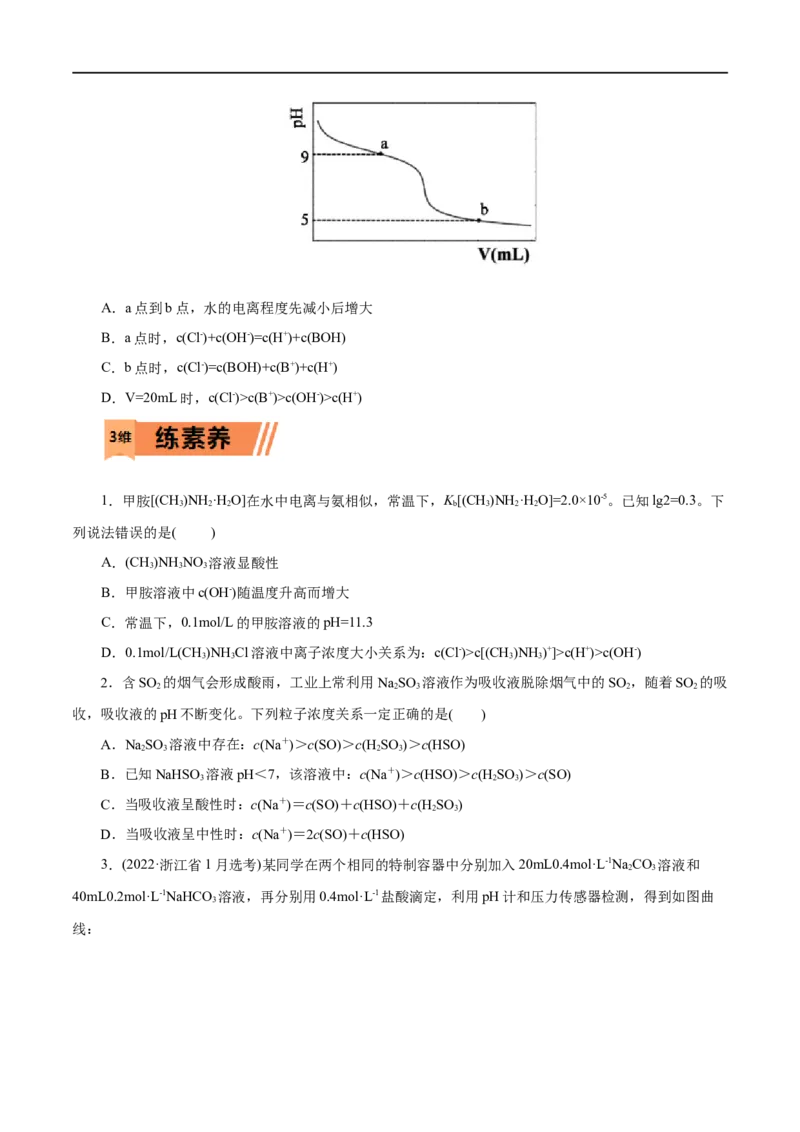
10.25℃,向20mL0.1mol•L-1的弱碱BOH溶液(K =1.0×10-5)中逐滴加入0.1mol•L-1盐酸,pH~V曲线
b
如图所示,下列说法正确的是A.a点到b点,水的电离程度先减小后增大
B.a点时,c(Cl-)+c(OH-)=c(H+)+c(BOH)
C.b点时,c(Cl-)=c(BOH)+c(B+)+c(H+)
D.V=20mL时,c(Cl-)>c(B+)>c(OH-)>c(H+)
1.甲胺[(CH )NH ·H O]在水中电离与氨相似,常温下,K [(CH )NH ·H O]=2.0×10-5。已知lg2=0.3。下
3 2 2 b 3 2 2
列说法错误的是( )
A.(CH)NH NO 溶液显酸性
3 3 3
B.甲胺溶液中c(OH-)随温度升高而增大
C.常温下,0.1mol/L的甲胺溶液的pH=11.3
D.0.1mol/L(CH )NH Cl溶液中离子浓度大小关系为:c(Cl-)>c[(CH )NH )+]>c(H+)>c(OH-)
3 3 3 3
2.含SO 的烟气会形成酸雨,工业上常利用NaSO 溶液作为吸收液脱除烟气中的SO ,随着SO 的吸
2 2 3 2 2
收,吸收液的pH不断变化。下列粒子浓度关系一定正确的是( )
A.NaSO 溶液中存在:c(Na+)>c(SO)>c(H SO )>c(HSO)
2 3 2 3
B.已知NaHSO 溶液pH<7,该溶液中:c(Na+)>c(HSO)>c(H SO )>c(SO)
3 2 3
C.当吸收液呈酸性时:c(Na+)=c(SO)+c(HSO)+c(H SO )
2 3
D.当吸收液呈中性时:c(Na+)=2c(SO)+c(HSO)
3.(2022·浙江省1月选考)某同学在两个相同的特制容器中分别加入20mL0.4mol·L-1NaCO 溶液和
2 3
40mL0.2mol·L-1NaHCO 溶液,再分别用0.4mol·L-1盐酸滴定,利用pH计和压力传感器检测,得到如图曲
3
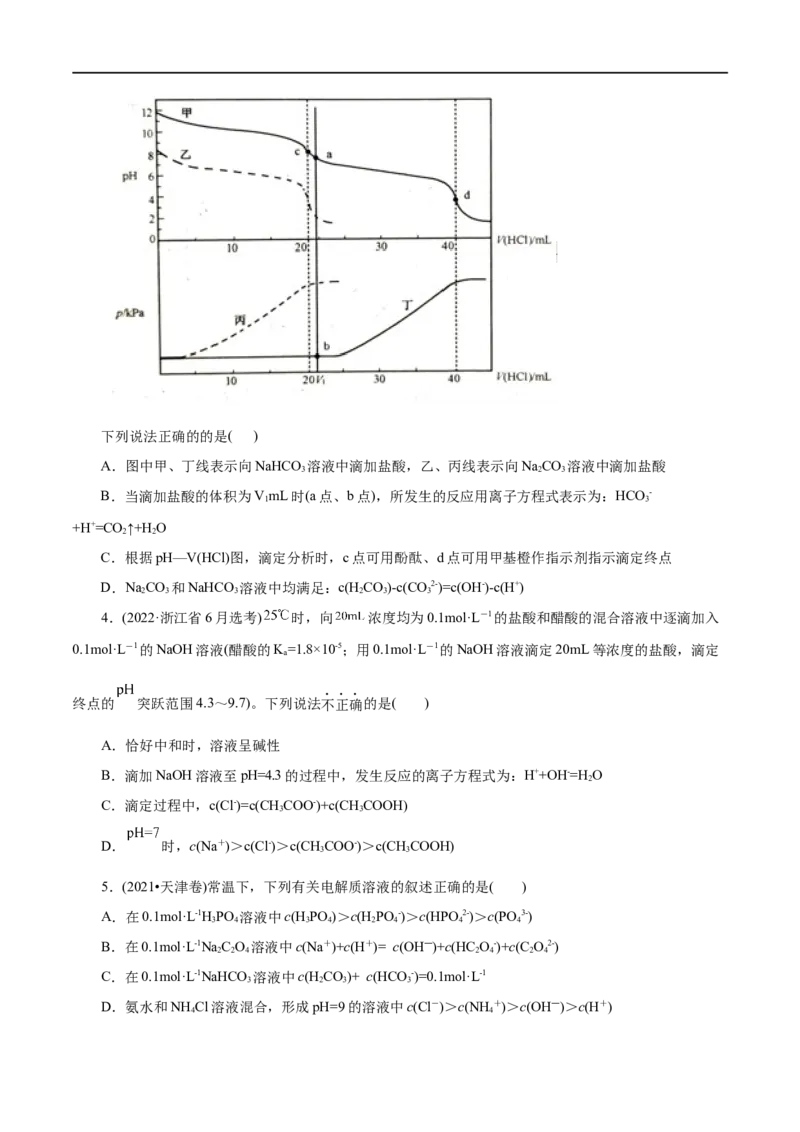
线:下列说法正确的的是( )
A.图中甲、丁线表示向NaHCO 溶液中滴加盐酸,乙、丙线表示向NaCO 溶液中滴加盐酸
3 2 3
B.当滴加盐酸的体积为VmL时(a点、b点),所发生的反应用离子方程式表示为:HCO -
1 3
+H+=CO ↑+H O
2 2
C.根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点
D.NaCO 和NaHCO 溶液中均满足:c(HCO)-c(CO2-)=c(OH-)-c(H+)
2 3 3 2 3 3
4.(2022·浙江省6月选考) 时,向 浓度均为0.1mol·L-1的盐酸和醋酸的混合溶液中逐滴加入
0.1mol·L-1的NaOH溶液(醋酸的K=1.8×10-5;用0.1mol·L-1的NaOH溶液滴定20mL等浓度的盐酸,滴定
a
终点的 突跃范围4.3~9.7)。下列说法不正确的是( )
A.恰好中和时,溶液呈碱性
B.滴加NaOH溶液至pH=4.3的过程中,发生反应的离子方程式为:H++OH-=H O
2
C.滴定过程中,c(Cl-)=c(CH COO-)+c(CH COOH)
3 3
D. 时,c(Na+)>c(Cl-)>c(CHCOO-)>c(CHCOOH)
3 3
5.(2021•天津卷)常温下,下列有关电解质溶液的叙述正确的是( )
A.在0.1mol·L-1HPO 溶液中c(H PO )>c(H PO -)>c(HPO 2-)>c(PO 3-)
3 4 3 4 2 4 4 4
B.在0.1mol·L-1NaC O 溶液中c(Na+)+c(H+)= c(OH―)+c(HC O-)+c(C O2-)
2 2 4 2 4 2 4
C.在0.1mol·L-1NaHCO 溶液中c(H CO)+ c(HCO -)=0.1mol·L-1
3 2 3 3
D.氨水和NH Cl溶液混合,形成pH=9的溶液中c(Cl-)>c(NH +)>c(OH―)>c(H+)
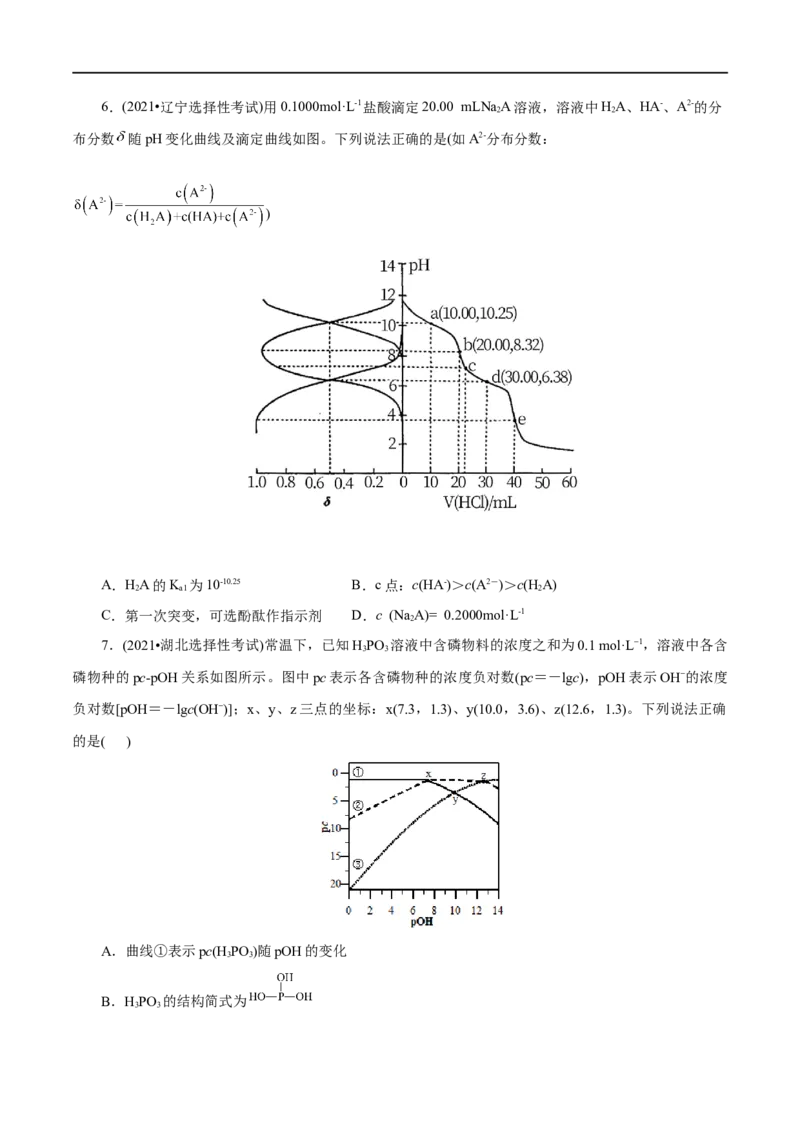
4 46.(2021•辽宁选择性考试)用0.1000mol·L-1盐酸滴定20.00 mLNa A溶液,溶液中HA、HA-、A2-的分
2 2
布分数 随pH变化曲线及滴定曲线如图。下列说法正确的是(如A2-分布分数:
)
A.HA的K 为10-10.25 B.c点:c(HA-)>c(A2-)>c(H A)
2 a1 2
C.第一次突变,可选酚酞作指示剂 D.c (NaA)= 0.2000mol·L-1
2
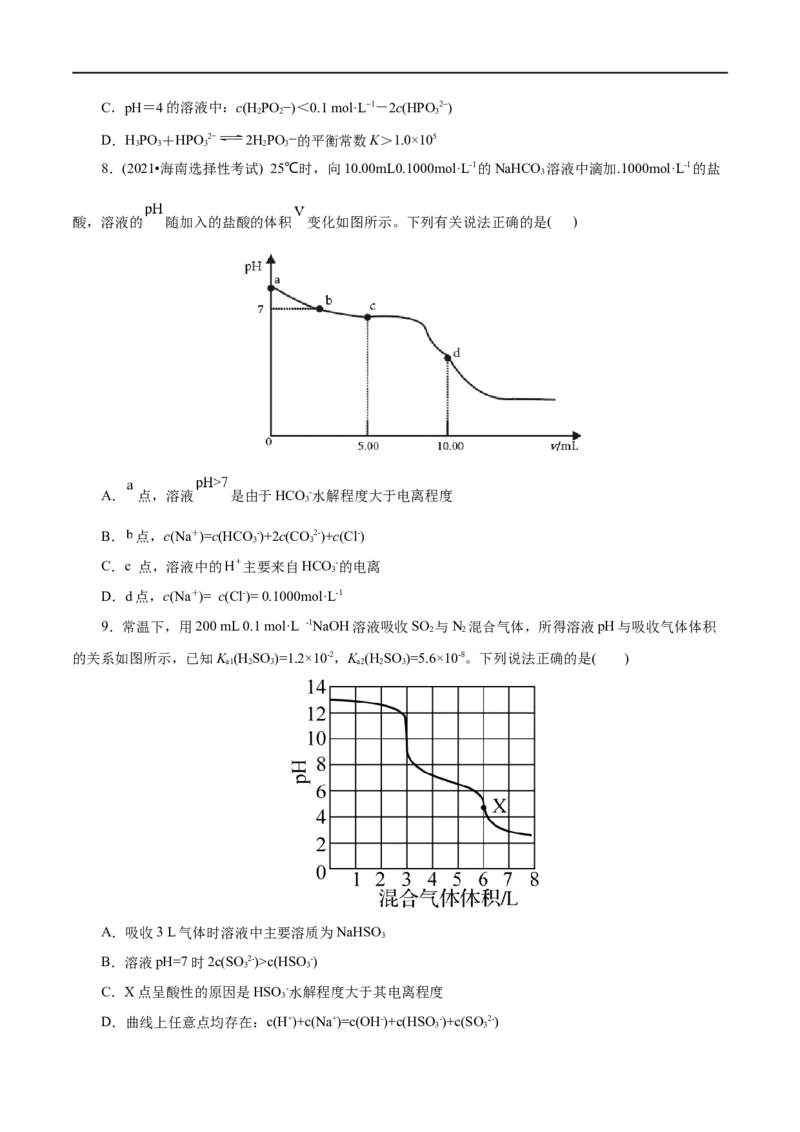
7.(2021•湖北选择性考试)常温下,已知HPO 溶液中含磷物料的浓度之和为0.1 mol·L1,溶液中各含
3 3
磷物种的pc-pOH关系如图所示。图中pc表示各含磷物种的浓度负对数(pc=-lgc),pOH表示OH的浓度
负对数[pOH=-lgc(OH)];x、y、z三点的坐标:x(7.3,1.3)、y(10.0,3.6)、z(12.6,1.3)。下列说法正确
的是( )
A.曲线①表示pc(H PO )随pOH的变化
3 3
B.HPO 的结构简式为
3 3C.pH=4的溶液中:c(H PO )<0.1 mol·L1-2c(HPO 2)
2 2 3
D.HPO +HPO 2 2 HPO 的平衡常数K>1.0×105
3 3 3 2 3
8.(2021•海南选择性考试) 25℃时,向10.00mL0.1000mol·L-1的NaHCO 溶液中滴加.1000mol·L-1的盐
3
酸,溶液的 随加入的盐酸的体积 变化如图所示。下列有关说法正确的是( )
A. 点,溶液 是由于HCO -水解程度大于电离程度
3
B. 点,c(Na+)=c(HCO -)+2c(CO2-)+c(Cl-)
3 3
C.c 点,溶液中的 主要来自HCO -的电离
3
D.d点,c(Na+)= c(Cl-)= 0.1000mol·L-1
9.常温下,用200 mL 0.1 mol·L -1NaOH溶液吸收SO 与N 混合气体,所得溶液pH与吸收气体体积
2 2
的关系如图所示,已知K (H SO )=1.2×10-2,K (H SO )=5.6×10-8。下列说法正确的是( )
a1 2 3 a2 2 3
A.吸收3 L气体时溶液中主要溶质为NaHSO
3
B.溶液pH=7时2c(SO 2-)>c(HSO -)
3 3
C.X点呈酸性的原因是HSO -水解程度大于其电离程度
3
D.曲线上任意点均存在:c(H+)+c(Na+)=c(OH-)+c(HSO -)+c(SO2-)
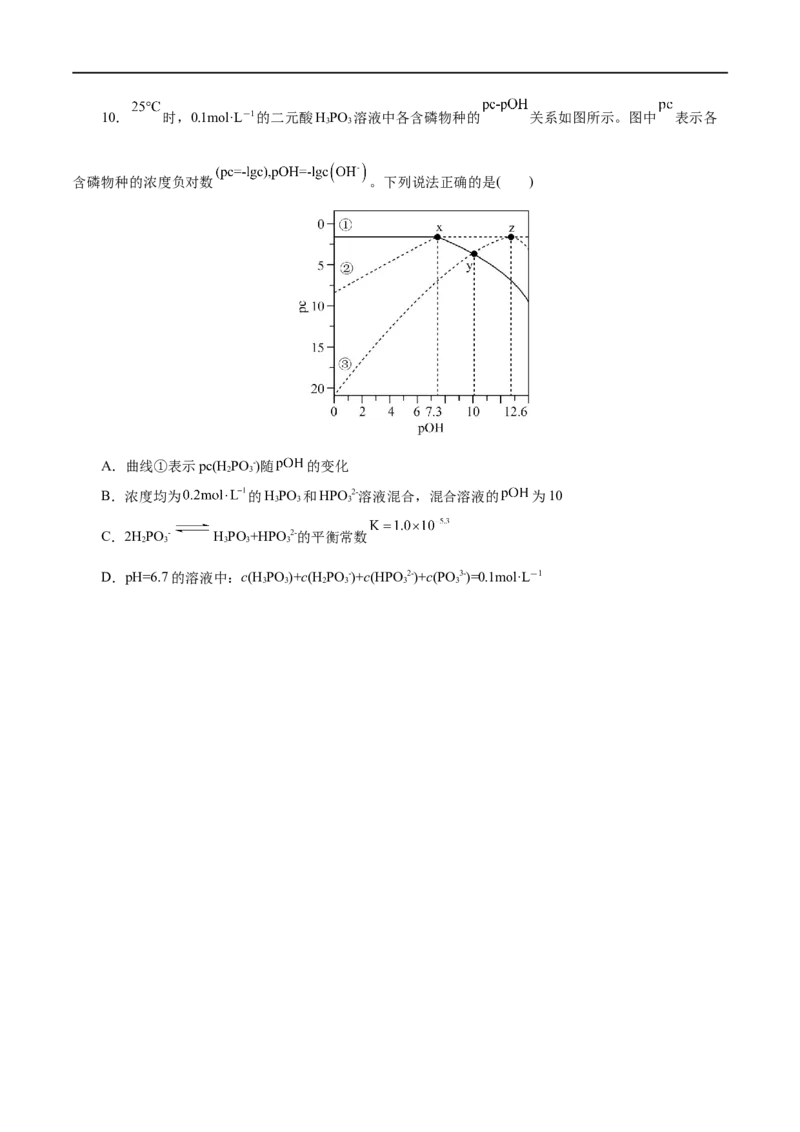
3 310. 时,0.1mol·L-1的二元酸HPO 溶液中各含磷物种的 关系如图所示。图中 表示各
3 3
含磷物种的浓度负对数 。下列说法正确的是( )
A.曲线①表示pc(HPO -)随 的变化
2 3
B.浓度均为 的HPO 和HPO 2-溶液混合,混合溶液的 为10
3 3 3
C.2HPO - HPO +HPO 2-的平衡常数
2 3 3 3 3
D.pH=6.7的溶液中:c(H PO )+c(H PO -)+c(HPO 2-)+c(PO 3-)=0.1mol·L-1
3 3 2 3 3 3