文档内容
第3课时 必备知识——电解质和离子反应
[基本概念]①电解质和非电解质;②强电解质和弱电解质;③电离;④离子反应;⑤
知识清单 氧化还原反应;⑥氧化剂和还原剂;⑦氧化性和还原性
[基本规律]①离子反应规律;②氧化还原反应基本规律
知识点1 电解质及其电离
1.电解质
(1)电解质及其分类
答案 ①电离 ②强电解质 ③强酸 ④强碱 ⑤弱电解质 ⑥弱酸 ⑦弱碱 ⑧水
溶液 ⑨熔融
(2)电解质和非电解质
前提条件 实验条件 现象 实质 范围
电 水溶液或 自身电离
酸、碱、盐、大部分金
解 熔融状态 能导电 出自由移
属氧化物、水等
质 下 动离子
都必须是
非
化合物 水溶液和 大多数非金属氧化物
电 不能 自身不
熔融状态 和 氢 化物 、大多数有
解 导电 能电离
下 机物等
质
①电解质和非电解质都必须是化合物,单质、混合物既不是电解质,也不是非电
解质;②本身电离而导电的混合物才是电解质,有些化合物的水溶液虽然能导电,但溶液中
导电的离子不是其自身电离产生的,这些化合物属于非电物质。例如:SO 、NH (因溶于水分
2 3
别生成的HSO 、NH ·HO能电离出自由移动的离子而导电)等;③电解质不一定能导电,如
2 3 3 2
固态NaCl、液态HCl等,能导电的物质不一定是电解质,如铜、稀硫酸等;④区分电解质和电
解质溶液,HCl是电解质,盐酸是HCl的水溶液,属于混合物,是电解质溶液。
(3)强电解质和弱电解质
强电解质 弱电解质
概念 在水溶液中能完全电离的电解质 在水溶液中只能部分电离的电解质
溶液中
离子、水分子 离子、水分子和弱电解质分子
存在微粒种类
电离 电离过程不可逆,不存在电离平
可逆,存在电离平衡
过程 衡
①强酸:HCl、HSO 、HNO、
2 4 3
①弱酸:CHCOOH、HF、HS、
3 2
HClO、HBr 、HI等;
4
包含 HCO、HSO 等;
2 3 2 3
②强碱:KOH、NaOH、Ca(OH) 、
2
范围 ②弱碱:NH ·H O、Cu(OH) 等;
3 2 2
Ba(OH) 等;
2
③水(H O)
2
③绝大部分盐:BaSO、BaCl 等
4 2
①电解质强弱与物质溶解性无关,溶解度小的物质易被误认为是弱电解质。如
BaSO、AgCl、CaCO 等在水溶液中溶解度很小,但溶解部分是完全电离的,因此属于强电解
4 3
质;②溶液导电性强弱与自由离子的浓度及离子所带的电荷数有关,与电解质强弱无直接关
系。
2.电解质的电离
(1)电离及其条件
电解质在水溶液中或熔融状态下,离解成自由移动离子的过程。电解质的电离条件是溶
于水或受热熔化。
(2)从电离的角度认识酸、碱、盐
电离特征及产生离子
电离出的阳离子全部是H+的化合物是酸,分为强酸与弱酸、含氧酸与无氧酸等;但能
酸
电离出H+的物质不一定是酸,如NaHSO 是一种盐
4
碱 电离出的阴离子全部是OH-的化合物是碱,分为强碱与弱碱、可溶性碱与难溶性碱等
由金属阳离子(或铵根离子)与酸根离子构成的化合物是盐, 分为可溶性盐与难溶性
盐
盐,酸式盐、碱式盐与正盐等
(3)电离方程式
①强电解质:全部电离,用“===”连接。例如,KSO :KSO === 2K + + SO 。
2 4 2 4
②弱电解质:部分电离,用“ ”表示。
⇌
多元弱酸分步电离,分步书写且电离程度逐步减弱,以第一步电离为主。例如,
HSO 的电离:HSO H + + HSO 、HSO H++SO
2 3 2 3
弱电 多元弱碱分步电离,但一步写出。例如,Fe(OH) 的电离:Fe(OH) Fe 3 + +
3 3
解质 3OH -
两性氢氧化物的电离,例如Al(OH) 的电离:
3
H + + AlO + H O(酸式电离) Al(OH) Al 3 + + 3OH - (碱式电离)
2 3
在水中强酸的酸式盐完全电离,但受热熔化电离产生阳离子和酸式根离子。例
酸式 如,NaHSO 在水溶液中电离:NaHSO=== Na + + H + + SO ,在熔融状态下的电
4 4
盐 离:NaHSO=== Na + + HSO
4
多元弱酸酸式盐,第一步完全电离,其余部分电离。例如,NaHCO 的电离:
3NaHCO === Na + + HCO 、HCO H++CO
3
[通关1] (易错排查)判断正误
(1)金属铝和NaCl溶液都能导电,故都属于电解质(×)
(2)CO 、NH 的水溶液能导电,故CO、NH 均是电解质(×)
2 3 2 3
(3)强电解质都是离子化合物,弱电解质都是共价化合物(×)
(4)强电解质溶液的导电性比弱电解质溶液的导电性强(×)
(5)(2019·北京卷)CH
3
COOH在水中电离(如图):CH
3
COOH⇌CH
3
COO-+H+(√)
[通关2] (2020.7·浙江选考)下列物质在熔融状态下不导电的是( )
A.NaOH B.CaCl
2
C.HCl D.KSO
2 4
C [NaOH、CaCl 、KSO 为离子化合物,熔融状态下均能够导电,HCl为共价化合物,液
2 2 4
态HCl不导电,C项正确。]
[通关3] (2019.4·浙江选考)下列属于强电解质的是( )
A.硫酸钡 B.食盐水
C.二氧化硅 D.醋酸
A [BaSO 是难溶于水的盐,属于强电解质,A项正确;食盐水是NaCl溶液,属于混合
4
物,是强电解质溶液,B项错误;SiO 是非金属氧化物,属于非电解质,C项错误;醋酸是弱酸,
2
属于弱电解质,D项错误。]
[通关4] (人教必修1·P34,4题改编)下列电离方程式中,正确的是( )
A.HSO ===H++SO
2 4
B.Ca(OH) ===Ca2++OH
2
C.Fe (SO )===2Fe3++3SO
2 4 3
D.NH ·H O===NH+OH-
3 2
C [H SO 溶于水电离产生H+和SO,正确应为HSO ===2H++SO,A项错误;Ca(OH)
2 4 2 4 2
电离产生Ca2+和OH-,正确应为Ca(OH) ===Ca2++2OH-,B项错误;Fe (SO ) 电离产生Fe3
2 2 4 3
+和SO,符合离子配比关系,C项正确;NH ·HO是弱电解质,部分电离,正确应为
3 2
NH
3
·H
2
O⇌NH+OH-,D项错误。]
[通关5] (深度思考)现有8种物质:①铜;②稀硫酸;③HCl;④乙醇;⑤NaCl;⑥HS;
2
⑦CaCO ;⑧蔗糖。
3
(1)属于非电解质的有____________(填序号,下同)。
(2)属于电解质,但液态时不能导电的是________。(3)既不是电解质,也不是非电解质,但本身能导电的是__________。
(4)分别写出③、⑥的电离方程式:
________________________________________________________________________、
________________________________________________________________________。
答案 (1)④⑧ (2)③⑥ (3)①② (4)HCl===H++Cl- H
2
S⇌HS-+H+、HS- ⇌S2-+
H+
知识点2 离子反应与离子方程式
1.离子反应
(1)概念:有离子参加或离子生成的化学反应。
(2)条件
生成难溶的物质,例如Cu(OH) 、BaSO 等
2 4
复分解
生成难电离的物质,例如弱酸、弱碱、水等
反应型
生成易挥发的物质,例如CO、SO 、NH 等
2 2 3
氧化还原
强氧化性与强还原性微粒发生反应,如Fe3+与I-、S2-等反应
反应型
(3)本质:溶液中离子的种类或浓度减小。
2.离子方程式
(1)概念:用实际参加反应的离子符号来表示反应的式子。
(2)意义:离子方程式不仅可以表示某一个具体的化学反应,还可以表示同一类型的离子
反应。
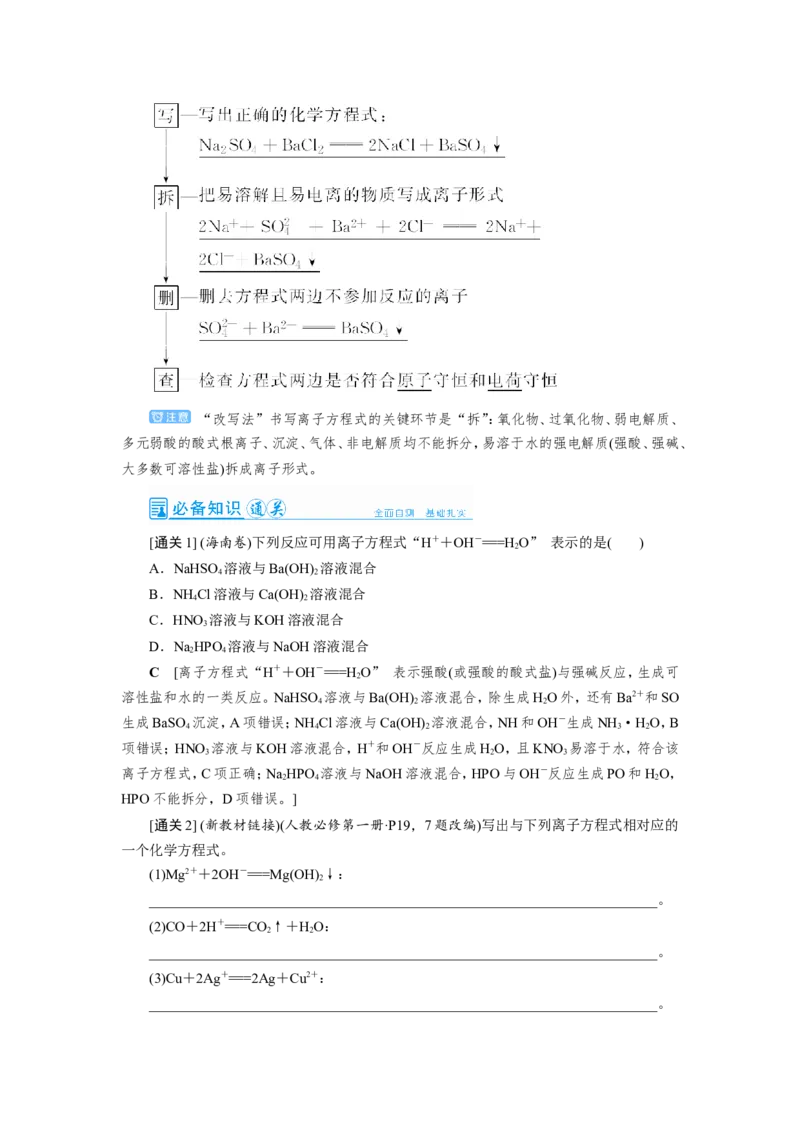
(3)书写方法——“改写法”(以NaSO 溶液和BaCl 溶液的反应为例)
2 4 2“改写法”书写离子方程式的关键环节是“拆”:氧化物、过氧化物、弱电解质、
多元弱酸的酸式根离子、沉淀、气体、非电解质均不能拆分,易溶于水的强电解质(强酸、强碱、
大多数可溶性盐)拆成离子形式。
[通关1] (海南卷)下列反应可用离子方程式“H++OH-===H O” 表示的是( )
2
A.NaHSO 溶液与Ba(OH) 溶液混合
4 2
B.NH Cl溶液与Ca(OH) 溶液混合
4 2
C.HNO 溶液与KOH溶液混合
3
D.NaHPO 溶液与NaOH溶液混合
2 4
C [离子方程式“H++OH-===H O” 表示强酸(或强酸的酸式盐)与强碱反应,生成可
2
溶性盐和水的一类反应。NaHSO 溶液与Ba(OH) 溶液混合,除生成HO外,还有Ba2+和SO
4 2 2
生成BaSO 沉淀,A项错误;NH Cl溶液与Ca(OH) 溶液混合,NH和OH-生成NH ·HO,B
4 4 2 3 2
项错误;HNO 溶液与KOH溶液混合,H+和OH-反应生成HO,且KNO 易溶于水,符合该
3 2 3
离子方程式,C项正确;NaHPO 溶液与NaOH溶液混合,HPO与OH-反应生成PO和HO,
2 4 2
HPO不能拆分,D项错误。]
[通关2] (新教材链接)(人教必修第一册·P19,7题改编)写出与下列离子方程式相对应的
一个化学方程式。
(1)Mg2++2OH-===Mg(OH) ↓:
2
________________________________________________________________________。
(2)CO+2H+===CO ↑+HO:
2 2
________________________________________________________________________。
(3)Cu+2Ag+===2Ag+Cu2+:
________________________________________________________________________。(4)Fe O+6H+===2Fe3++3HO:
2 3 2
________________________________________________________________________。
答案 (1)MgCl +2NaOH===Mg(OH) ↓+2NaCl(其他合理答案均可,下同)
2 2
(2)Na CO+2HCl===2NaCl+CO↑+HO
2 3 2 2
(3)Cu+2AgNO===2Ag+Cu(NO )
3 3 2
(4)Fe O+6HCl===2FeCl +3HO
2 3 3 2
[通关3] (深度思考)完成下列反应的离子方程式:
(1)氧化铜溶于稀硫酸:
________________________________________________________________________。
(2)澄清石灰水中加入稀盐酸:
________________________________________________________________________。
(3)石灰乳与NaCO 溶液反应:
2 3
________________________________________________________________________。
(4)Na CO 溶液与AgNO 溶液混合:
2 3 3
________________________________________________________________________。
(5)用MnO 与浓盐酸共热制Cl:
2 2
________________________________________________________________________。
(6)铜与稀硝酸反应制取NO:
________________________________________________________________________。
(7)向Al (SO ) 溶液中加入过量氨水:
2 4 3
________________________________________________________________________。
(8)向NaAlO 溶液中通入足量CO:
2 2
________________________________________________________________________。
答案 (1)CuO+2H+===Cu2++HO
2
(2)OH-+H+===H O
2
(3)Ca(OH) +CO===CaCO +2OH-
2 3
(4)CO+2Ag+===Ag CO↓
2 3
(5)MnO +4H++2Cl-=====Mn2++Cl↑+2HO
2 2 2
(6)3Cu+8H++2NO===3Cu2++2NO↑+4HO
2
(7)Al3++3NH ·H O===Al(OH) ↓+3NH
3 2 3
(8)AlO+2HO+CO===Al(OH) ↓+HCO
2 2 3训练(六) 电解质和离子反应
1.(2021·山东师大附中检测)有如下物质:①NaCl溶液;②熔融MgCl ;③CuSO ·5H O
2 4 2
晶体;④NaOH固体;⑤金属铜;⑥蔗糖。有关它们的说法正确的是( )
A.属于非电解质的有①⑤⑥
B.属于电解质的有①②③④
C.不能导电的有③④⑥
D.属于混合物的有①②③⑥
C [NaCl溶液是混合物,铜是单质,二者既不是电解质也不是非电解质,A项错误;
NaCl溶液是电解质溶液,并非电解质,B项错误;CuSO ·5HO和NaOH固体均为电解质,
4 2
但固态时不导电,蔗糖是非电解质,不导电,C项正确;熔融MgCl 、CuSO ·5HO和蔗糖都
2 4 2
是纯净物,D项错误。]
2.(2021·北京师大附中检测)下图是NaCl加入水中溶解并电离的示意图,观察该图可得
到的结论是( )
A.该过程通常表示为NaCl===Na++Cl-
B.NaCl只有在水分子的作用下才能形成Na+
C.NaCl的水溶液是电解质
D.NaCl只有在水溶液中才能导电
A [NaCl溶于水或受热熔化时,均发生电离,其电离过程可表示为NaCl===Na++Cl-;
NaCl的水溶液是混合物,是电解质溶液,而不是电解质,NaCl为电解质,在水溶液中或熔融
状态下均能够导电。]
3.下列物质在水中的电离方程式中正确的是( )
A.NaHCO ===Na++H++CO
3
B.NaHSO===Na++HSO
4
C.MgCl ===Mg2++2Cl-
2
D.HS===2H++S2-
2
C [NaHCO 是弱酸的酸式盐,溶于水电离生成 Na+和 HCO,电离方程式为
3
NaHCO ===Na++HCO,A 项错误;NaHSO 在水中电离出 Na+、H+和 SO,应为
3 4
NaHSO===Na++H++SO,B项错误;MgCl 是易溶于水的强电解质,电离产生Mg2+和Cl-,
4 2
C项正确;HS是弱电解质,存在电离平衡,且分步电离,D项错误。]
2
4.(2020·湖北沙市中学模拟)下列离子方程式的书写中,正确的是( )A.碳酸氢钙溶液跟盐酸反应:Ca(HCO )+2H+===Ca2++2HO+2CO↑
3 2 2 2
B.“84消毒液”(有效成分NaClO)和“洁厕灵”(主要成分盐酸)混合使用放出氯气:
ClO-+Cl-+2H+===Cl↑+HO
2 2
C.将少量SO 通入NaClO溶液:SO +HO+2ClO-===SO+2HClO
2 2 2
D.向碳酸氢铵溶液中加入足量石灰水:Ca2++HCO+OH-===CaCO ↓+HO
3 2
B [碳酸氢钙易溶于水,要用离子符号表示,应为HCO+H+===CO ↑+HO,A项错误;
2 2
“84消毒液”和“洁厕灵”混合时发生氧化还原反应生成Cl,符合反应事实及守恒规律,
2
B项正确;SO 通入NaClO溶液中发生氧化还原反应,应为SO +ClO-+HO===SO+Cl-+
2 2 2
2H+,C项错误;漏写NH与OH-发生的反应,应为NH+HCO+Ca2++2OH-===CaCO ↓+
3
NH ·HO+HO,D项错误。]
3 2 2
5.(2021·安徽六校联考)在电解质的导电性装置(如图所示)中,若向某一电解质溶液中逐
滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )
A.盐酸中逐滴加入食盐溶液
B.硫酸中逐滴加入氢氧化钠溶液
C.石灰乳中逐滴加入稀盐酸
D.硫酸中逐滴加入氢氧化钡溶液
D [盐酸滴加到食盐溶液中,不发生反应,溶液的导电性变化不大,灯泡的明亮程度变
化不大,A错误;硫酸滴加到NaOH溶液中,二者发生反应生成NaSO 和HO,NaSO 在水
2 4 2 2 4
中电离产生Na+和SO,溶液的导电性变化不大,灯泡的明亮程度变化不大,B错误;石灰乳
中Ca(OH) 达到过饱和状态,导电能力较弱,逐滴加入稀盐酸,二者反应生成CaCl 和HO,
2 2 2
溶液的导电能力增大,灯泡变亮,C错误;硫酸逐滴加入氢氧化钡溶液中,二者反应生成
BaSO 沉淀和HO,BaSO 难溶于水,而水几乎不导电,溶液的导电能力逐渐减弱,二者恰好
4 2 4
完全反应时,灯泡熄灭,当硫酸过量时,灯泡逐渐变亮,D正确。]
6.(2021·安徽“江南十校”联考)下列离子方程式正确的是( )
A.在AgNO 溶液中加入过量氨水:Ag++NH ·H O===AgOH↓+NH
3 3 2
B.HSO 与Ba(OH) 溶液反应:Ba2++OH-+H++SO===BaSO ↓+HO
2 4 2 4 2
C.在强碱溶液中NaClO与Fe(OH) 反应生成NaFeO:3ClO-+2Fe(OH) ===2FeO+3Cl
3 2 4 3
-+4H++HO
2
D.等体积、等浓度的 Ba(OH) 溶液与 NH HCO 溶液混合:Ba2++2OH-+NH+
2 4 3
HCO===BaCO ↓+NH ·H O+HO
3 3 2 2
D [AgOH溶于过量氨水,正确应为Ag++2NH ·HO===Ag(NH )+2HO,A项错误;
3 2 3 2不符合离子配比关系,正确应为Ba2++2OH-+2H++SO===BaSO ↓+2HO,B项错误;强
4 2
碱性溶液中不能生成H+,正确应为3ClO-+2Fe(OH) +4OH-===2FeO+3Cl-+5HO,C项
3 2
错误;符合反应事实及守恒规律,D项正确。]
7.(2021·黑龙江哈尔滨模拟)在下图点滴板上进行四个溶液之间反应的小实验,其对应
反应的离子方程式书写正确的是( )
A.a反应:Fe2++2H++HO===Fe3++2HO
2 2 2
B.b反应:CO+H+===HCO
C.c反应:H++OH-===H O
2
D.Al3++3NH ·H O===Al(OH) ↓+3NH
3 2 3
D [a中反应的离子方程式不符合电荷守恒,A项错误;忽视反应物的量对产物的影响,
正确应为CO+2H+===CO ↑+HO,B项错误;CHCOOH是弱酸,书写离子方程式时要用
2 2 3
化学式表示,C项错误。]
8.下列物质:①液态 HCl ② NaHCO ③ NaCl 溶液 ④ CO ⑤蔗糖晶体
3 2
⑥Ba(OH) ⑦红褐色的氢氧化铁胶体 ⑧NH ·H O ⑨空气 ⑩Al (SO )
2 3 2 2 4 3
(1)上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为 H++OH-
===H O,该反应的化学方程式为________________________________。
2
(2)⑩在水中的电离方程式为
___________________________________________________
________________________________________________________________________。
(3)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打
(NaHCO ) , 能 治 疗 胃 酸 过 多 , 请 写 出 其 反 应 的 离 子 方 程 式 :
3
______________________________________;如果病人同时患胃溃疡,为防胃壁穿孔,不能
服用小苏打,此时最好用含Al(OH) 的胃药(如胃舒平),它与胃酸反应的离子方程式为
3
________________________________________。
(4)向Ba(OH) 溶液中通入过量的CO 的离子方程式:
2 2
________________________________________________________________________。
解析 (1)可溶性的强酸和强碱反应生成可溶性盐,可用离子方程式H++OH-===H O
2
表示,则化学方程式为Ba(OH) +2HCl===BaCl +2HO。
2 2 2
(2)Al(SO ) 是强电解质,在水中发生完全电离,电离方程式为 Al (SO )===2Al3++
2 4 3 2 4 3
3SO。(3)胃液中含有盐酸,盐酸与小苏打反应生成二氧化碳和水,反应的离子方程式为HCO+H+===H O+CO↑;Al(OH) 与HCl发生酸碱中和反应,由于Al(OH) 是难溶物,故书写离
2 2 3 3
子方程式时不拆分,该反应的离子方程式为Al(OH) +3H+===3H O+Al3+。
3 2
(4)向Ba(OH) 溶液中通入过量的CO,生成Ba(HCO ),反应的离子方程式为CO+OH
2 2 3 2 2
-===HCO。
答案 (1)Ba(OH) +2HCl===BaCl +2HO
2 2 2
(2)Al(SO )===2Al3++3SO
2 4 3
(3)HCO+H+===H O+CO↑ Al(OH) +3H+===3H O+Al3+
2 2 3 2
(4)CO +OH-===HCO
2