文档内容
专题 14 分子结构与性质
第 40 练 分子的空间结构
1.利用红外光谱对有机化合物分子进行测试并记录,可初步判断该有机物分子拥有的( )
A.同分异构体数 B.原子个数
C.化学键和官能团种类 D.有机化合物的分子式
2.下列有关价层电子对互斥理论的描述正确的是( )
A.价层电子对就是σ键电子对
B.孤电子对数由分子式来确定
C.分子的立体构型是价层电子对互斥的结果
D.孤电子对数等于π键数
3.用价层电子对互斥理论预测HO和NO的立体结构,两个结论都正确的是( )
2
A.直线形;三角锥形 B.V形;三角锥形
C.直线形;平面三角形 D.V形;平面三角形
4.乙炔分子中的碳原子采取的杂化方式是( )
A.sp1杂化 B.sp2杂化 C.sp3杂化 D.无法确定
5.在 中,中间的碳原子和两边的碳原子分别采用的杂化方式是( )
A.sp2 sp2 B.sp3 sp3 C.sp2 sp3 D.sp1 sp3
6.下列各物质中的中心原子不是采用sp3杂化的是( )
A.NH B.HO C.CO D.CCl
3 2 2 4
7.s轨道和p轨道杂化的类型不可能有( )
A.sp1杂化 B.sp2杂化 C.sp3杂化 D.sp4杂化
8.在BrCH==CHBr分子中,C和Br成键采用的轨道是( )
A.spp B.sp2s C.sp2p D.sp3p
9.sp3杂化形成的AB 型分子的立体构型为( )
4
A.平面四边形 B.正四面体形C.四角锥形 D.平面三角形
10.四氯化碳(CCl )是一种很重要的化学试剂,可以作为溶剂和防火剂。下列关于四氯化碳分子的几
4
何构型和中心原子(C)采取杂化方式的说法正确的是( )
A.三角锥型、sp3 B.正四面体形、sp3
C.平面三角形、sp2 D.三角锥型、sp2
11.鲍林是两位获得诺贝尔奖不同奖项的人之一,杂化轨道是鲍林为了解释分子的立体结构提出的。
下列对sp3、sp2、sp杂化轨道的夹角的比较,得出结论正确的是( )
A.sp杂化轨道的夹角最大 B.sp2杂化轨道的夹角最大
C.sp3杂化轨道的夹角最大 D.sp3、sp2、sp杂化轨道的夹角相等
1.下列说法中正确的是( )
A.NO 、SO 、BF、NCl 分子中没有一个分子中原子的最外层电子都满足了8电子稳定结构
2 2 3 3
B.P 和CH 都是正四面体形分子且键角都为109°28′
4 4
C.NH的电子式为 ,离子呈平面正方形结构
D.NH 分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强
3
2.下列有关键角与分子立体构型的说法不正确的是( )
A.键角为180°的分子,立体构型是直线形
B.键角为120°的分子,立体构型是平面三角形
C.键角为60°的分子,立体构型可能是正四面体形
D.键角为90°~109°28′之间的分子,立体构型可能是V形
3.下列分子或离子中,中心原子价层电子对的立体构型为正四面体形且分子或离子的立体构型为V
形的是( )
A.NH B.PH
3
C.HO+ D.OF
3 2
4.在白磷分子中,四个P原子分别处于正四面体的四个顶点上,结合有关P原子的成键特点,下列
有关白磷的说法正确的是( )
A.白磷分子的键角为109°28′ B.分子中共有4对共用电子对
C.白磷分子的键角为60° D.分子中有6对孤电子对
5.已知在CH 中,C—H键间的键角为109°28′,NH 中,N—H键间的键角为107°,HO中O—H键
4 3 2
间的键角为105°,则下列说法中正确的是( )
A.孤电子对与成键电子对间的斥力大于成键电子对与成键电子对间的斥力
B.孤电子对与成键电子对间的斥力小于成键电子对与成键电子对间的斥力
C.孤电子对与成键电子对间的斥力等于成键电子对与成键电子对间的斥力D.题干中的数据不能说明孤电子对与成键电子对间的斥力同成键电子对与成键电子对间的斥力之间
的大小关系
6.下列有关sp2杂化轨道的说法错误的是( )
A.由同一能层上的s轨道与p轨道杂化而成
B.共有3个能量相同的杂化轨道
C.每个sp2杂化轨道中s能级成分占三分之一
D.sp2杂化轨道最多可形成2个σ键
7.下列关于杂化轨道的叙述中,不正确的是( )
A.分子中中心原子通过sp3杂化轨道成键时,该分子不一定为正四面体结构
B.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对
C.NH 和CH 两个分子中中心原子N和C都是通过sp3杂化轨道成键
3 4
D.杂化轨道理论与VSEPR模型分析分子的空间构型结果常常相互矛盾
8.在乙烯分子中有5个σ键、一个π键,它们分别是( )
A.sp2杂化轨道形成σ键、未杂化的2p轨道形成π键
B.sp2杂化轨道形成π键、未杂化的2p轨道形成σ键
C.C—H之间是sp2形成的σ键,C—C之间是未参加杂化的2p轨道形成的π键
D.C—C之间是sp2形成的σ键,C—H之间是未参加杂化的2p轨道形成的π键
9.了解有机物分子中化学键特征以及成键方式是研究有机物性质的基础。下列关于有机物分子成键
方式的描述不正确的是( )
A.烷烃分子中碳原子均采取sp3杂化成键
B.炔烃分子中的碳碳三键由1个σ键、2个π键组成
C.苯分子中所有碳原子均采取sp2杂化成键,苯环中存在6个碳原子共有的大π键
D.甲苯分子中所有碳原子均采取sp2杂化成键
10.CH、—CH、CH都是重要的有机反应中间体,有关它们的说法正确的是( )
3
A.它们互为等电子体,碳原子均采取sp2杂化
B.CH与NH 、HO+互为等电子体,中心原子均为sp3杂化,几何构型均为正四面体形
3 3
C.CH中的碳原子采取sp2杂化,所有原子共平面
D.CH中的碳原子采取sp3杂化,所有原子均共面
11.推理是学习化学知识的一种重要方法。下列推理合理的是( )
A.SO 中硫原子采取sp2杂化,则CO 中碳原子也采取sp2杂化
2 2
B.NH 分子的空间结构是三角锥形,则NCl 分子的空间结构也是三角锥形
3 3
C.H O分子的键角是105°,则HS分子的键角也是105°
2 2
D.PCl 分子中每个原子最外层达到8电子稳定结构,则BF 分子中每个原子最外层也能达到8电子稳
3 3
定结构
12.下列有关苯分子中的化学键描述正确的是( )A.每个碳原子的sp2杂化轨道中的其中一个形成大π键
B.每个碳原子的未参加杂化的2p轨道形成大π键
C.碳原子的三个sp2杂化轨道与其他原子形成三个π键
D.碳原子的未参加杂化的2p轨道与其他原子形成σ键
13.了解有机物分子中化学键特征以及成键方式是研究有机物性质的基础。下列关于有机物分子成键
方式的描述不正确的是( )
A.烷烃分子中碳原子均采取sp3杂化成键
B.炔烃分子中的碳碳三键由1个σ键、2个π键组成
C.苯分子中所有碳原子均采取sp2杂化成键,苯环中存在6个碳原子共有的大π键
D.甲苯分子中所有碳原子均采取sp2杂化成键
1.已知次氯酸分子的结构式为H—O—Cl,下列有关说法正确的是( )
A.O原子发生sp1杂化
B.O原子与H、Cl都形成σ键
C.该分子为直线形分子
D.该分子电子式是
2.多核离子所带电荷可以认为是中心原子得到或失去电子导致,根据VSEPR模型,下列离子中所有
原子都在同一平面的一组是( )
A.NO -和NH - B.HO+和ClO - C.NO -和CH- D.PO 3-和SO 2-
2 2 3 3 3 3 4 4
3.下列对应关系不正确的是( )
选项 A B C D
中心原子所在族 ⅣA ⅤA ⅣA ⅥA
分子通式 AB AB AB AB
4 3 2 2
立体结构 正四面体形 平面三角形 直线形 Ⅴ形4.有X、Y两种活性反应中间体微粒,均含有1个碳原子和3个氢原子,其球棍模型如图所示:
(X), (Y)。下列说法错误的是( )
A.X的组成为CH B.Y的组成为CH
C.X的价层电子对数为4 D.Y中键角小于120°
5.下列叙述正确的是( )
A.NH 是极性分子,分子中N原子处在3个H原子所组成的三角形的中心
3
B.CC1 是非极性分子,分子中C原子处在4个C1原子所组成的正方形的中心
4
C.HO是极性分子,分子中O原子处在2个H原子所连成的直线的中央
2
D.CO 是非极性分子,分子中C原子处在2个O原子所连成的直线的中央
2
6.了解有机物分子中化学键特征以及成键方式是研究有机物性质的基础。下列关于有机物分子的成
键方式的描述不正确的是( )
A.烷烃分子中碳原子均采用sp3杂化成键
B.炔烃分子中的碳碳叁键由1个σ键、2个π键组成
C.苯分子中所有碳原子均采用sp2杂化成键,苯环中存在6个碳原子共有的大π键
D.甲苯分子中所有碳原子均采用sp2杂化成键
7.有几种阴离子的信息如下:
阴离子 ClO - ClO - M ClO-
4 3
中心元素化合价 +5 +3 +1
中心原子杂化类型 sp3 sp3
下列推断不正确的是( )
A.ClO -和CO2-的价电子总数相同 B.M的化学式为ClO -
3 3 2
C.ClO -、ClO-中氯原子的杂化类型都为sp3 D.M的空间结构为V形
3
8.短周期元素X、Y、Z原子序数依次增大,X元素基态原子有2个未成对电子,Y元素基态原子的
核外p电子数比s电子数少1个,Z的一种“超原子”(Z -)具有40个价电子,下列说法错误的是( )
13
A.简单离子半径:Y<Z B.XO 2-的空间构型为平面三角形
3
C.YO -中心原子的杂化方式为sp2杂化 D.X、Y、Z的电负性:Y>X>Z
3
9.X、Y、Z、Q、E、M六种元素中,X的原子的基态价电子排布式为2s2,Y的基态原子核外有5种运动状态不同的电子,Z元素的两种同位素原子通常作为示踪原子研究生物化学反应和测定文物的年代,
Q是元素周期表中电负性最大的元素,E的阳离子通常存在于硝石、明矾和草木灰中,M的原子序数比E
大1。下列说法正确的是( )
A.EYQ 中阴离子中心原子的杂化方式为sp2杂化
4
B.X、Y元素的第一电离能大小关系:X<Y
C.ZO2-的空间构型为平面三角形
3
D.MZ 仅含离子键,可用于制备乙炔
2
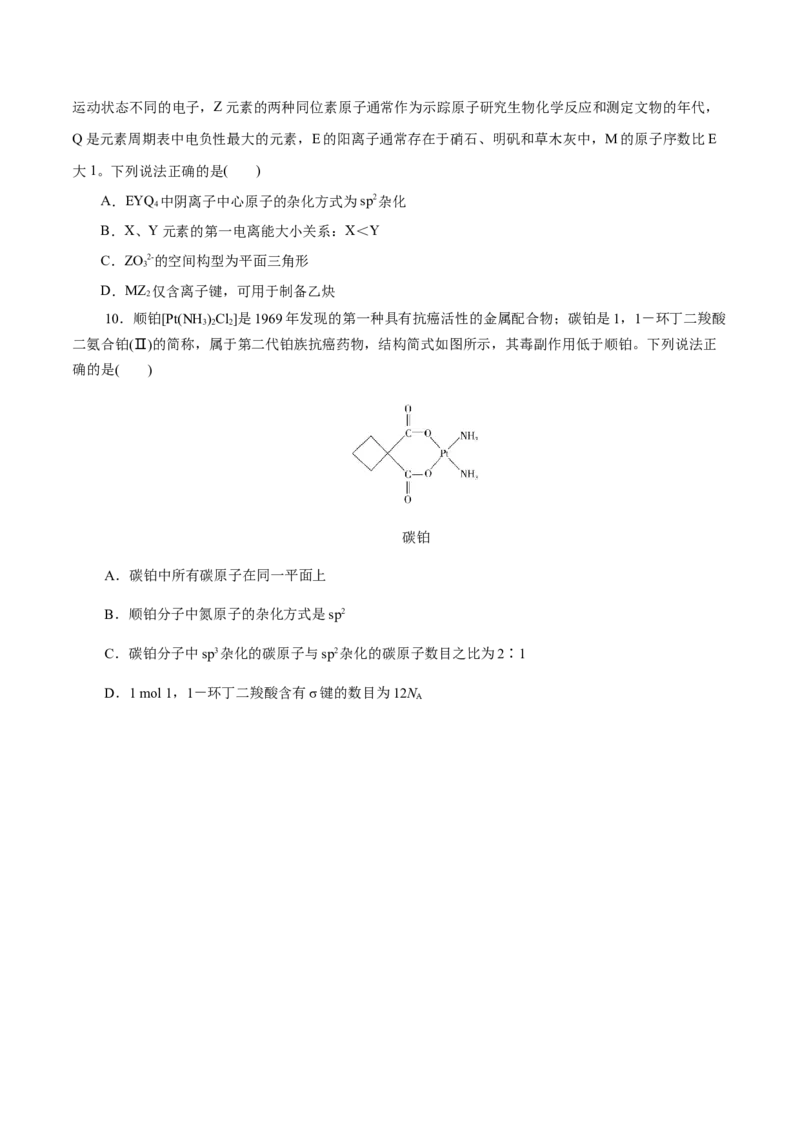
10.顺铂[Pt(NH )Cl]是1969年发现的第一种具有抗癌活性的金属配合物;碳铂是1,1-环丁二羧酸
3 2 2
二氨合铂(Ⅱ)的简称,属于第二代铂族抗癌药物,结构简式如图所示,其毒副作用低于顺铂。下列说法正
确的是( )
碳铂
A.碳铂中所有碳原子在同一平面上
B.顺铂分子中氮原子的杂化方式是sp2
C.碳铂分子中sp3杂化的碳原子与sp2杂化的碳原子数目之比为2∶1
D.1 mol 1,1-环丁二羧酸含有σ键的数目为12N
A