文档内容
专题 15 晶体结构与性质
第 42 练 物质的聚集状态与晶体的常识
1.下列物质中,不属于非晶体的是( )
A.玻璃 B.石蜡和沥青 C.塑料 D.干冰
【答案】D
【解析】干冰属于分子晶体,玻璃、石蜡、沥青、塑料均属于非晶体,故选D。
2.红磷是巨型共价分子,无定型结构,下列方法能证明红磷是非晶体的是
A.质谱法 B.原子发射光谱法 C.核磁共振谱 D.X射线衍射法
【答案】D
【解析】区别晶体和非晶体最有效的方法是进行X射线衍射实验,故选D。
3.下列各组物质中,化学键类型相同,晶体类型也相同的是
A.金刚石和二氧化碳 B.NaBr和HBr C.氯气和KCl D.甲烷和
【答案】D
【解析】A项,金刚石是由共价键结合的原子晶体,干冰是含有共价键的分子晶体,故A不符合题意;
B项,NaBr是离子晶体含有离子键,HBr是分子晶体含有共价键,故B不符合题意;C项,氯气是分子晶
体,含有共价键,KCl是离子晶体含有离子键,故C不符合题意;D项,甲烷和HO都是分子晶体,都只
2
含共价键,故D符合题意;故选D。
4.区分晶体和非晶体最可靠的科学方法是( )
A.测定熔点、沸点 B.观察外形
C.对固体进行X射线衍射实验 D.通过比较硬度确定
【答案】C
【解析】从外形和某些物理性质可以初步鉴别晶体和非晶体,但并不一定可靠。区分晶体和非晶体最
可靠的科学方法是对固体进行X射线衍射实验,所以只有C选项正确。
5.仔细观察下图,它表示( )A.晶体 B.晶体或非晶体 C.非晶体 D.不能确定
【答案】C
【解析】观察最右侧一个空隙中有2个大球,而左上角一个空隙中有1个大球,因此此固体的构成微
粒排列无序,为非晶体。
6.下列物质具有自范性、各向异性的是( )
A.钢化玻璃 B.塑料 C.水晶 D.陶瓷
【答案】C
【解析】晶体具有自范性和各向异性,钢化玻璃、塑料、陶瓷均不属于晶体。
7.下列不属于晶体特性的是( )
A.具有规则的几何外形 B.具有各向异性
C.具有对称性 D.没有固定的熔点
【答案】D
【解析】晶体具有规则的几何外形、各向异性、自范性、对称性等特征,且晶体有固定的熔点。
8.下列不属于晶体的特点的是( )
A.一定有固定的几何外形 B.一定有各向异性
C.一定有固定的熔点 D.一定是无色透明的固体
【答案】D
【解析】晶体的特点有:有规则的几何外形(由晶体的自范性决定)、固定的熔点及各向异性,但不一
定是无色透明的固体,如紫黑色的碘晶体、蓝色的硫酸铜晶体。
9.整块晶体可以看作是数量巨大的晶胞“无隙并置”而成。对这句话的理解错误的是( )
A.相邻晶胞之间没有任何间隙
B.晶体是晶胞简单、随意堆积而成
C.晶胞排列时,取向相同
D.“并置”是指所有晶胞都是平行排列的
【答案】B
【解析】晶体并不是晶胞简单、随意堆积而成,而是晶胞平行排列而成的,且相邻晶胞之间没有任何
间隙。
10.下列有关晶胞的说法正确的是( )
A.晶胞是晶体中最小的结构单元 B.晶胞中所有的粒子都为几个晶胞共用C.晶胞均为长方体 D.不同晶体的晶胞不一定相同
【答案】D
【解析】A项,晶胞是晶体的最小重复单元,但不一定是最小结构单元,故A项错误;B项,晶胞中
有些粒子为晶胞独自拥有,故B项错误;C项,晶胞多数为平行六面体,不一定为长方体,故C项错误;
D项,不同晶体的晶胞可能相同,也可能不相同,故D项正确;故选D。
11.下列有关晶胞的说法正确的是( )
A.晶胞是晶体中最小的结构单元 B.晶胞中所有的粒子都为几个晶胞共用
C.晶胞均为长方体 D.不同晶体的晶胞不一定相同
【答案】D
【解析】A项,晶胞是晶体的最小重复单元,但不一定是最小结构单元,故A项错误;B项,晶胞中
有些粒子为晶胞独自拥有,故B项错误;C项,晶胞多数为平行六面体,不一定为长方体,故C项错误;
D项,不同晶体的晶胞可能相同,也可能不相同,故D项正确;故选D。
12.下列关于NaCl晶体结构的说法中正确的是( )
A.NaCl晶体中,每个 周围吸引的 与每个 周围吸引的 数目相等
B.NaCl晶体中,每个 周围吸引1个
C.NaCl晶胞中的质点代表一个NaCl
D.NaC1晶体中存在单个的NaCl分子
【答案】A
【解析】A项,氯化钠晶体中,每个Na+周围吸引6个Cl-,而每个Cl-周围吸引6个Na+,数目相等,
A正确;B项,氯化钠晶体中,每个Na+周围吸引6个Cl-,而每个Cl-周围吸引6个Na+,B错误;C项,
NaCl晶体中的质点表示Na+或Cl-,C错误;D项,NaCl晶体中不存在单个NaCl分子,D错误。故选A。
1.下列说法不正确的是 ( )
A.晶体具有固定的熔、沸点,而非晶体没有固定的熔、沸点
B.晶体与非晶体具有相同的性质
C.部分电子表、电脑的显示器是由液晶材料制成的
D.等离子体是一种很好的导电体,在信息产业等领域有非常好的应用前景
【答案】B
【解析】A项,晶体有固定的熔点,自范性、各向异性,非晶体无固定的熔点,故A项正确;B项,晶体与非晶体内部结构不同,故表现的性质不同,故B项错误;C项,部分电子表、电脑的显示器是由液
晶材料制成的,需要的驱动电压很低,故C正项确;D项,等离子体是一种很好的导电体,在信息产业等
领域有非常好的应用前景,等离子体技术在新能源行业、聚合物薄膜、材料防腐蚀等方面前景可观,故D
项正确;故选B。
2.下列关于特殊聚集状态的应用的描述中,错误的是( )
A.运用等离子束切割金属
B.晶体合金的硬度和强度均比非晶体合金的硬度和强度高
C.液晶用于各种显示仪器上
D.化妆品中加入纳米颗粒可使其具备防紫外线的功能
【答案】B
【解析】A项,运用等离子束切割金属,是利用高温等离子电弧的热量使工件切口处的金属部分或局
部熔化,故A项正确;B项,某些非晶体合金的硬度和强度比晶体合金的硬度和强度高,故B项错误;C
项,液晶用于各种显示仪器上,液晶具有显著的电光特性,故C项正确;D项,纳米颗粒具有极强的紫外
线屏蔽能力,化妆品中加入纳米颗粒可使其具备防紫外线的功能,故D项正确;故选B。
3.普通玻璃和水晶的根本区别在于( )
A.外形不一样
B.普通玻璃的基本构成粒子无规则地排列,水晶的基本构成粒子按一定规律做周期性重复排列
C.水晶有固定的熔点,普通玻璃无固定的熔点
D.水晶可用于能量转换,普通玻璃不能用于能量转换
【答案】B
【解析】晶体和非晶体的本质区别就是粒子(原子、离子或分子)在微观空间里是否呈现周期性的有序
排列。
4.将晶体划分为离子晶体、金属晶体、共价晶体和分子晶体的本质标准是( )
A.基本构成微粒种类
B.晶体中最小重复结构单元的种类
C.微观粒子的密堆积种类
D.晶体内部微粒的种类及微粒间相互作用的种类
【答案】D
【解析】根据晶体内部微粒的种类和微粒间的相互作用的不同,可将晶体分为离子晶体、金属晶体、
共价晶体和分子晶体。
5.下列关于晶体的说法正确的是( )
A.将饱和硫酸铜溶液降温,析出的固体不是晶体
B.石蜡和玻璃都是非晶体,但它们都有固定的熔点C.假宝石往往是玻璃仿造的,可以用划痕的方法鉴别宝石和玻璃制品
D.蓝宝石在不同方向上的硬度一定相同
【答案】C
【解析】A项,得到晶体一般有三条途径:①熔融态物质凝固;②气态物质冷却不经液态直接凝固(凝
华);③溶质从溶液中析出,所以将饱和硫酸铜溶液降温,析出的固体是晶体,A项错误;B项,晶体具有
固定的熔沸点,而非晶体没有固定熔沸点,而是在一定温度范围内熔化,石蜡和玻璃都是非晶体,故它们
都没有固定的熔点,B项错误;C项,硬度是衡量固体软硬程度的指标,一般宝石的硬度较大,玻璃制品
的硬度较小,故可以用划痕的方法鉴别宝石和玻璃制品,C项正确;D项,晶体具有各向异性的性质,蓝
宝石属于晶体,在不同方向上硬度有一些差异,D项错误;故选C。
6.玻璃是常见的非晶体,在生产、生活中有着广泛的应用,有关玻璃的说法错误的是( )
A.玻璃内部微粒排列是长程无序和短程有序的
B.玻璃熔化时吸热,温度不断上升
C.水晶和玻璃都是非晶体
D.利用X射线衍射实验可以鉴别玻璃和水晶
【答案】C
【解析】根据玻璃是非晶体知,构成玻璃的粒子在空间的排列是长程无序和短程有序的,没有固定的
熔点,A、B项正确;区分晶体与非晶体最科学的方法是对固体进行 X射线衍射实验,D项正确。故选
C。
7.关于晶体的自范性,下列叙述正确的是( )
A.破损的晶体能够在固态时自动变成规则的多面体
B.缺角的氯化钠晶体在饱和NaCl溶液中慢慢变为完美的立方体晶块
C.圆形容器中结出的冰是圆形的,体现了晶体的自范性
D.由玻璃制成规则的玻璃球,体现了晶体的自范性
【答案】B
【解析】晶体的自范性指的是在适宜条件下,晶体能够自发呈现规则的几何外形的性质。A选项所述
过程不可能实现;C选项中的圆形并不是晶体冰本身自发形成的,而是受容器的限制形成的;D选项中玻
璃属于非晶体;氯化钠属于晶体,从饱和溶液中析出是形成晶体的途径之一,其发生的原因是晶体的自范
性,故B选项正确。
8.下列关于晶体的说法正确的是( )
A.将饱和硫酸铜溶液降温,析出的固体不是晶体B.假宝石往往是玻璃仿造的,可以用划痕的方法鉴别宝石和玻璃制品
C.石蜡和玻璃都是非晶体,但它们都有固定的熔点
D.蓝宝石在不同方向上的硬度一定相同
【答案】B
【解析】选项A,将饱和CuSO 溶液降温可析出胆矾,胆矾属于晶体。选项B,宝石的硬度较大,玻
4
璃制品的硬度较小,可以根据有无划痕来鉴别。选项C,非晶体没有固定熔点。选项D,晶体的各向异性
导致蓝宝石在不同方向上的硬度有些差异。
9.云母属晶体,是单斜晶系一族层状结构的硅酸盐矿物的总称。用烧热了的针去接触涂有薄薄一层
石蜡的云母片的反面时,熔化了的石蜡呈现椭圆形,这是因为( )
A.云母是热的不良导体,传热不均匀
B.石蜡是热的不良导体,传热不均匀
C.石蜡具有各向异性,不同的方向导热性不同
D.云母具有各向异性,不同的方向导热性不同
【答案】D
【解析】云母属晶体,晶体具有各向异性。
10.下列关于晶体的性质叙述中,不正确的是( )
A.晶体的自范性指的是在适宜条件下晶体能够自发地呈现封闭规则的多面体几何外形
B.晶体的各向异性和对称性是矛盾的
C.晶体的对称性是微观粒子按一定规律做周期性重复排列的必然结果
D.晶体的各向异性直接取决于微观粒子的排列具有特定的方向性
【答案】B
【解析】晶体的各向异性取决于微观粒子的排列具有特定的方向性,而对称性是微观粒子按一定规律
做周期性重复排列的必然结果,B项的说法错误。
11.下列途径不能得到晶体的是( )
A.熔融态SiO 快速冷却 B.熔融态SiO 热液缓慢冷却
2 2
C.FeCl 蒸气冷凝 D.CuSO 饱和溶液蒸发浓缩后冷却
3 4
【答案】A
【解析】晶体呈现自范性是需要一定条件的,即晶体生长的速率要适当。熔融态物质快速冷却时不能
得到晶体,如熔融态SiO 快速冷却得到看不到晶体外形的玛瑙,热液缓慢冷却则形成水晶。FeCl 、AlCl
2 3 3
等固体均易升华,其蒸气凝华则得到晶体。D项析出胆矾晶体(CuSO ·5H O)。
4 2
12.下列途径不能得到晶体的是( )
A.FeCl 蒸气冷凝 B.熔融态SiO 热液缓慢冷却
3 2C.熔融态SiO 快速冷却 D.CuSO 饱和溶液蒸发浓缩后冷却
2 4
【答案】C
【解析】得到晶体一般有三条途径:①熔融态物质凝固;②气态物质冷却不经液态直接凝固(凝华);
③溶质从溶液中析出。A项,FeCl 蒸气冷凝得到氯化铁晶体,A项不符合题意;B项,熔融态SiO 热液缓
3 2
慢冷却可以得到SiO 晶体,B项不符合题意C项,熔融态物质急速冷却得到玻璃态物质,不属于晶体,C
2
项符合题意;D项,硫酸不挥发,所以CuSO 饱和溶液蒸发浓缩后冷却可以得到硫酸晶体,D项不符合题
4
意;故选C。
13.下列有关晶胞的叙述中正确的是( )
A.晶胞的结构是晶体的结构
B.不同的晶体中,晶胞的大小和形状都相同
C.晶胞中的任何一个粒子都完全属于该晶胞
D.已知晶胞的组成就可推知晶体的组成
【答案】D
【解析】由晶胞的定义可知A项错误;相同晶体中晶胞的大小和形状完全相同,不同晶体中,晶胞的
大小和形状不一定相同,B项错误;晶体中的大部分粒子被若干个晶胞所共有,不完全属于某个晶胞,C
项错误;知道晶胞的组成,利用“均摊法”即可推知晶体的组成,D项正确。
1.水的状态除了气、液和固态外,还有玻璃态。它是由液态水急速冷却到165 K时形成的。玻璃态的
水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述中正确的是(
)
A.水由液态变为玻璃态,体积缩小
B.水由液态变为玻璃态,体积膨胀
C.玻璃态是水的一种特殊状态
D.在玻璃态水的X射线图谱上有分立的斑点或明锐的衍射峰
【答案】C
【解析】玻璃态水无固定形状,不存在晶体结构,故玻璃态水不是晶体,不能在其 X射线图谱上有分
立的斑点或明锐的衍射峰;因密度与普通水相同,故水由液态变为玻璃态时体积不变。故选C。
2.物质的非晶体能自动转变为晶体,而晶体却不能自动地转变为非晶体,这说明( )
A.非晶体是不稳定的,处于非晶体时能量大
B.晶体是稳定的,处于晶体时能量大
C.非晶体是不稳定的,处于非晶体时能量小D.晶体是不稳定的,处于非晶体时能量小
【答案】A
【解析】根据“非晶体能自动转变为晶体”可知,非晶体不稳定,晶体较稳定,能量越低越稳定,说
明非晶体是处于高能量状态,转变为晶体后趋向于低能量的稳定状态,故选A。
3.下面有关晶体的叙述中,正确的是( )
A.在晶体中只要有阳离子就一定有阴离子
B.离子晶体中只有离子键没有共价键,分子晶体中只有分子间作用力没有共价键
C.分子晶体中分子间作用力越大,分子越稳定
D.共价晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性
【答案】D
【解析】A项,金属晶体由金属阳离子和自由电子构成,所以晶体中有阳离子不一定存在阴离子,故
A错误;B项,离子晶体中一定存在离子键,可能有共价键,如NaOH中既有离子键又有共价键,分子晶
体中肯定有分子间作用力,大多数有共价键,少数没有(如稀有气体),故B错误;C项,分子的稳定性属
于化学性质,与共价键有关,分子间作用力与稳定性无关,故C错误;D项,共价晶体中原子以共价键结
合,共价键的键能较大,所以共价晶体的熔点高、硬度大,故D正确。故选D。
4.下列有关晶体的叙述中,正确的是
A.晶体与非晶体的本质区别在于固体是否具有规则的几何外形
B.红外光谱不仅可以用于晶体和非晶体的鉴别,还可测定分子中官能团和化学键的信息
C.SiO 属于共价晶体,其中Si采取sp3杂化与4个O相连,形成正四面体结构单元
2
D.第三周期主族元素形成的氧化物的晶体中,NaO是纯粹的离子晶体,SiO 是纯粹的共价晶体
2 2
【答案】C
【解析】A项,晶体与非晶体的根本区别在于其内部粒子在空间上是否按一定规律做周期性重复排列,
不是在于是否具有规则的几何外形,A错误;B项,红外光谱是反映有机物分子中含有的化学键或官能团
的信息,而不是用于鉴别晶体和非晶体,B错误;C项,SiO 属于共价晶体,Si原子与4个O原子形成4
2
个共价键,因此其中Si采取sp3杂化与4个O相连,形成与Si原子相连的4个O原子形成正四面体结构单
元,C正确;D项,NaO、SiO 中既有共价键成分又有离子键成分,前者离子键的百分数大于50%,偏向
2 2
于离子键,对应晶体偏向于离子晶体;后者离子键的百分数小于50%,偏向于共价键,对应晶体偏向于共
价晶体,D错误;故选C。
5.科学研究表明,宇宙中90%以上的物质以等离子体状态存在,其原因是大部分发光星球的内部温
度和压力都很高。下列说法中正确的是( )A.只有在宇宙发光星球上才存在等离子体
B.等离子体能吸收电磁波
C.有些难以发生的化学反应,在等离子体中也不能发生
D.等离子体是一种自然现象,不能人工得到
【答案】B
【解析】在我们周围,等离子体也常常存在,如日光灯和霓虹灯的灯管里存在等离子体,A项错误;
等离子体因含带电微粒而能吸收电磁波,因能量很高而能使一些难以发生的化学反应迅速发生,B项正确,
C项错误;等离子体可以通过人工得到,D项错误。故选B。
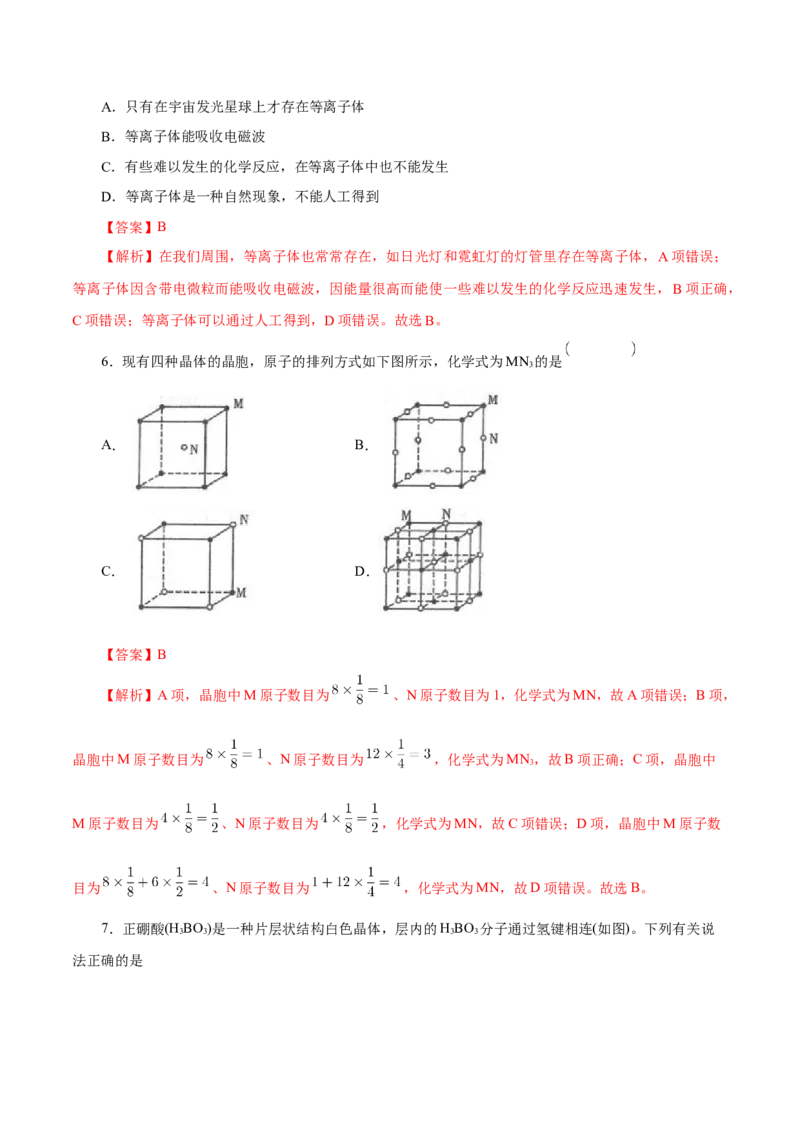
6.现有四种晶体的晶胞,原子的排列方式如下图所示,化学式为MN 的是
3
A. B.
C. D.
【答案】B
【解析】A项,晶胞中M原子数目为 、N原子数目为1,化学式为MN,故A项错误;B项,
晶胞中M原子数目为 、N原子数目为 ,化学式为MN ,故B项正确;C项,晶胞中
3
M原子数目为 、N原子数目为 ,化学式为MN,故C项错误;D项,晶胞中M原子数
目为 、N原子数目为 ,化学式为MN,故D项错误。故选B。
7.正硼酸(H BO)是一种片层状结构白色晶体,层内的HBO 分子通过氢键相连(如图)。下列有关说
3 3 3 3
法正确的是A.正硼酸晶体属于共价晶体
B.HBO 分子的稳定性与氢键有关
3 3
C.分子中硼原子最外层为8电子稳定结构
D.1molH BO 晶体中含有3mol氢键
3 3
【答案】D
【解析】A项,正硼酸晶体是HBO 分子通过氢键相连,属于分子晶体,故A错误;B项,HBO 分
3 3 3 3
子的稳定性与氢键无关,氢键与熔沸点有关,故B错误;C项,根据HBO 分子的结构得到分子中硼原子
3 3
最外层是6电子,故C错误;D项,HBO 晶体中每个—OH中的氧和氢分别与另外的—OH的H和另外的
3 3
—OH的O形成氢键,因此1molH BO 晶体中含有3mol氢键,故D正确。故选D。
3 3
8.F 和Xe在一定条件下可生成XeF 、XeF 和XeF 三种氟化氙,它们都是极强的氧化剂(其氧化性依
2 2 4 6
次递增),都极易与水反应。其中6XeF +12HO===2XeO+4Xe↑+24HF+3O↑,下列推测正确的是( )
4 2 3 2
黑球表示氙原子 白球表示氟原子
A.XeF 分子中各原子均达到八电子的稳定结构
2
B.某种氟化氙的晶体结构单元如上图所示,可推知其化学式为XeF
6
C.XeF 按已知方式水解,每生成2 mol Xe转移8 mol电子
4
D.XeF 加入水中,在水分子的作用下,将重新生成Xe和F
2 2
【答案】C
【解析】Xe原子已经达到8电子稳定,故XeF 不可能具有8电子稳定结构,A不正确;根据平行六面
2
体规律:Xe为8×1/8+1=2,F为8×1/4+2=4,故该晶体的化学式为XeF ,B项不正确;由于F的非金属
2
性最强,在XeF 中Xe的化合价为+4价,生成2 mol Xe转移电子数为8 mol,C项正确;F 有强的氧化性,
4 2
能够与水反应,故XeF 与水反应不可能生成F,D项不正确。
2 2
9.下列各项是晶体结构中具有代表性的最小重复单元(晶胞)的排列方式,图中:○—X,●—Y,⊗—
Z。其中对应的化学式不正确的是( )【答案】B
【解析】A项中 X、Y的位置、数目完全等同,化学式为 XY,正确;B项中 X、Y的个数比为
1∶(8×)=1∶1,化学式为XY,错误;C项中X的数目:4×+1=,Y的数目:4×=,化学式为XY,正确;
3
D项中X的数目:8×=1,Y的数目:6×=3,Z位于体心,数目为1,化学式为XY Z,正确。
3
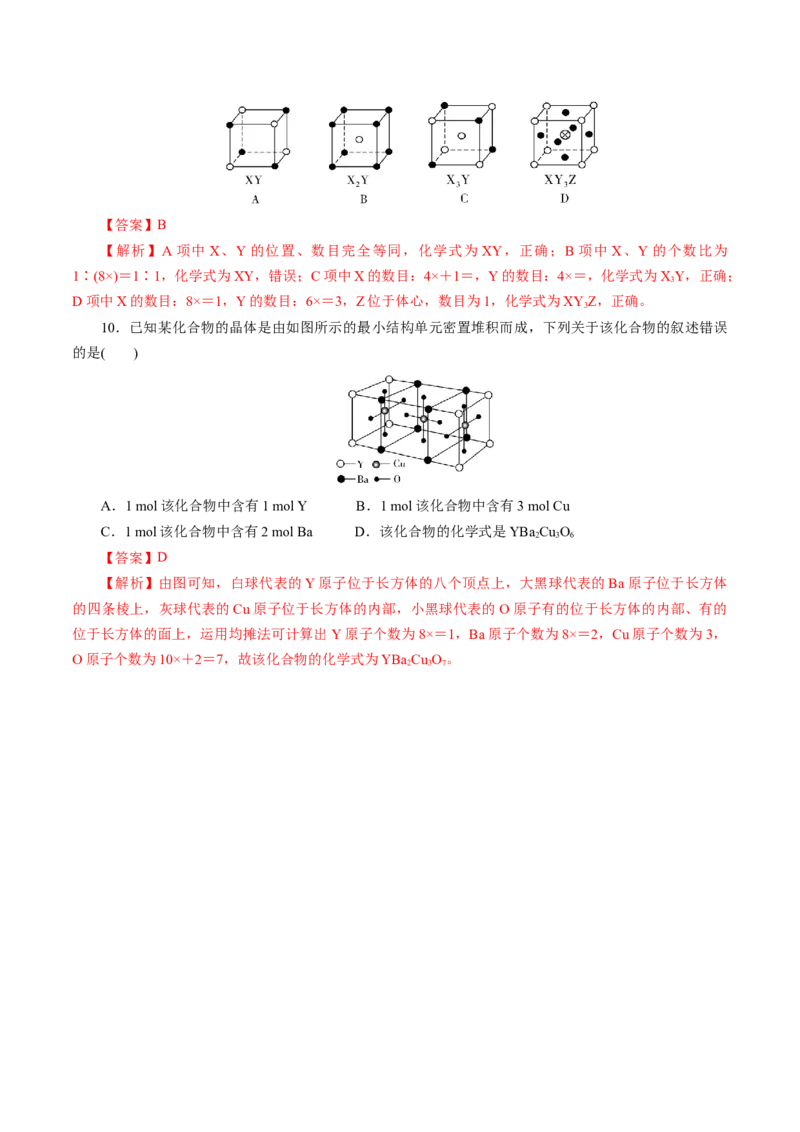
10.已知某化合物的晶体是由如图所示的最小结构单元密置堆积而成,下列关于该化合物的叙述错误
的是( )
A.1 mol该化合物中含有1 mol Y B.1 mol该化合物中含有3 mol Cu
C.1 mol该化合物中含有2 mol Ba D.该化合物的化学式是YBa Cu O
2 3 6
【答案】D
【解析】由图可知,白球代表的Y原子位于长方体的八个顶点上,大黑球代表的Ba原子位于长方体
的四条棱上,灰球代表的Cu原子位于长方体的内部,小黑球代表的O原子有的位于长方体的内部、有的
位于长方体的面上,运用均摊法可计算出Y原子个数为8×=1,Ba原子个数为8×=2,Cu原子个数为3,
O原子个数为10×+2=7,故该化合物的化学式为YBa Cu O。
2 3 7