文档内容
第4课时 关键能力——离子方程式的判断及书写
离子方程式的判断及书写是高考常考题型之一,在选择题中考查离子方程式的正误判
断,在非选择题中结合题给信息考查离子方程式的书写。此类试题以常见元素及其化合物知
识为载体,突出考查考生的理解与辨析能力、分析与推测能力、归纳与论证能力,要求考生掌
握基础知识(元素及其化合物的性质)、辨析基本概念(离子反应、氧化还原反应)、获取有关信
息,并在此基础上判断物质结构、分析物质性质、推断反应结果、归纳总结规律、用化学语言
合理表达等。离子方程式的判断及书写体现《中国高考评价体系》中实践操作能力、思维认知
能力等。
考向1 离子方程式的正误判断(分析与推测能力)
近几年,全国卷较少考查离子方程式的正误判断,但北京、江苏、天津、海南等地方卷中
考查频率较高,此类问题设置“陷阱”的角度主要有不符合反应原理、化学式拆分不当、不
符合守恒规律、忽视反应物用量对产物的影响等。要求考生能够阅读和理解各种主要文本、
基本符号,能够客观全面地获取相关信息,能够准确概括和描述学科所涉及基本现象的特征
及其相互关系,能够透过现象看到本质,发现隐含的规律或原理,并作出合理的分析、推测及
判断。
角度1 考虑是否符合反应原理
下列离子方程式中,书写正确的是( )
A.(2020·全国卷Ⅲ)向CaCl 溶液中通入CO:Ca2++HO+CO===CaCO ↓+2H+
2 2 2 2 3
B.(2020·全国卷Ⅲ)向HO 溶液中滴加少量FeCl :2Fe3++HO===O ↑+2H++2Fe2+
2 2 3 2 2 2
C.(2019·江苏卷)室温下用稀HNO 溶解铜:Cu+2NO+2H+===Cu2++2NO ↑+HO
3 2 2
D.(2019·江苏卷)室温下用稀NaOH溶液吸收Cl:Cl+2OH-===ClO-+Cl-+HO
2 2 2
D [由于HCl的酸性强于HCO,CO 通入氯化钙溶液时,二氧化碳与氯化钙不反应,A
2 3 2
项错误;HO 溶液中加入FeCl 溶液时,FeCl 作HO 分解的催化剂,B项错误;室温下用稀
2 2 3 3 2 2
HNO 溶解铜产生NO,正确应为:3Cu+2NO+8H+===3Cu2++2NO↑+4HO,C项错误。]
3 2[强化1] 下列离子方程式中,书写正确的是( )
A.(2019·海南卷)向碘化钾溶液中加入少量双氧水:2HO+I-===IO+3HO
2 2 2
B.(2019·天津卷)氧化亚铁溶于稀硝酸:FeO+2H+===Fe2++HO
2
C.(2019·天津卷)向沸水中滴加饱和氯化铁溶液得到红褐色液体:Fe3++3HO===
2
Fe(OH) ↓+3H+
3
D.(2017·江苏卷)电解饱和食盐水获取烧碱和氯气:2Cl-+2HO=====H↑+Cl↑+
2 2 2
2OH-
D [KI溶液中加入少量双氧水,反应生成I,正确应为HO+2I-===I +2OH-,A项错
2 2 2 2
误;FeO与稀硝酸发生氧化还原反应,正确应为3FeO+10H++NO===3Fe3++NO↑+5HO,
2
B项错误;向沸水中滴加饱和氯化铁溶液得到红褐色液体,得不到沉淀,正确应为Fe3++
3HO===== Fe(OH) (胶体)+3H+,C项错误。]
2 3
角度2 考虑化学式是否拆分得当
下列离子方程式中,书写正确的是( )
A.(2020.7·浙江选考)CuSO 溶液中滴加稀氨水:Cu2++2OH-===Cu(OH) ↓
4 2
B.(2020·天津卷)CaCO 与稀硝酸反应:CO+2H+===H O+CO↑
3 2 2
C.(2019·江苏卷)向NaSiO 溶液中滴加稀盐酸:NaSiO+2H+===H SiO↓+2Na+
2 3 2 3 2 3
D.(2019·天津卷)向氢氧化镁悬浊液中滴加氯化铵溶液,沉淀溶解:Mg(OH) +
2
2NH===Mg2++2NH ·H O
3 2
D [一水合氨是弱碱,书写离子方程式用化学式NH ·HO表示,A项错误;碳酸钙难
3 2
溶于水,要用化学式CaCO 表示,B项错误;NaSiO 为易溶于水的盐,应写成离子形式,正确
3 2 3应为SiO+2H+===H SiO↓,C项错误。]
2 3
[强化2] 下列离子方程式中正确的是( )
A.(2019·北京卷)HC O 有还原性:2MnO+5C O+16H+===2Mn2++10CO↑+8HO
2 2 4 2 2 2
B.(2018·江苏卷)电解饱和食盐水:2Cl-+2H+=====Cl↑+H↑
2 2
C.(2018·江苏卷)饱和Na
2
CO
3
溶液与CaSO
4
固体反应:CO+CaSO 4⇌CaCO
3
+SO
D.(2020·江苏卷)0.1 mol·L-1 AgNO 溶液中加入过量浓氨水:Ag++NH +
3 3
HO===AgOH↓+NH
2
C [H C O 是弱酸,书写离子方程式要用化学式表示,正确应为2MnO+5HC O+6H+
2 2 4 2 2 4
===2Mn2++10CO↑+8HO,A项错误;电解饱和食盐水,阴极上水电离产生的H+放电生成
2 2
H,水不能写成H+,正确应为2Cl-+2HO=====Cl↑+H↑+2OH-,B项错误;AgOH会
2 2 2 2
溶于过量的浓氨水,生成Ag(NH)OH,D项错误。]
3 2
角度3 考虑是否符合守恒规律
下列离子方程式中,正确的是( )
A.(2020·天津卷)FeSO 溶液与溴水反应:2Fe2++Br ===2Fe3++2Br-
4 2
B.(2019·江苏卷)用铝粉和NaOH溶液反应制取少量H:Al+2OH-===AlO+H↑
2 2
C.(2019·天津卷)二氧化硫使酸性高锰酸钾溶液褪色:3SO +2MnO+4H+===3SO+
2
2Mn2++2HO
2
D.(2018·江苏卷)酸化NaIO 和NaI的混合溶液:I-+IO+6H+===I +3HO
3 2 2A [Br 具有较强氧化性,可将Fe2+氧化成Fe3+,A项正确;不符合电荷守恒及得失电子
2
守恒,正确应为2Al+2OH-+2HO===2AlO+3H↑,B项错误;不符合得失电子守恒,正确
2 2
应为5SO +2MnO+2HO===5SO+2Mn2++4H+,C项错误;不符合电荷守恒和得失电子守
2 2
恒,正确应为5I-+IO+6H+===3I +3HO,D项错误。]
2 2
[强化3] 下列离子方程式中正确的是( )
A.(2020·天津卷)C HONa溶液中通入少量CO 2C HO-+CO +HO===2C HOH+
6 5 2∶ 6 5 2 2 6 5
CO
B.(2020·全国卷Ⅲ)同浓度同体积 NH HSO 溶液与 NaOH 溶液混合:NH+OH-
4 4
===NH·H O
3 2
C.(2017·海南卷)用氢氧化钠溶液吸收工业废气中的NO 2NO +2OH-===NO+NO+
2∶ 2
HO
2
D.(2017·江苏卷)钠与水反应:Na+2HO===Na++2OH-+H↑
2 2
C [酸性:HCO>C HOH>HCO,在苯酚钠溶液中无论通入多少CO,只能生成HCO,
2 3 6 5 2
A项错误;同体积同浓度的 NH HSO 溶液与 NaOH 溶液混合时,发生反应 H++OH-
4 4
===H O,B项错误;符合反应事实及守恒规律,C项正确;不符合电荷守恒规律,正确应为
2
2Na+2HO===2Na++2OH-+H↑,D项错误。]
2 2
角度4 考虑是否忽视反应物的用量对产物的影响
下列离子方程式中不正确的是( )
A.(2020·天津卷)NaOH溶液与过量HC O 溶液反应:HC O+2OH-===C O+2HO
2 2 4 2 2 4 2 2
B.(2020·全国卷Ⅲ)用NaSO 溶液吸收少量Cl:3SO+Cl+HO===2HSO+2Cl-+SO
2 3 2 2 2
C.(2019·海南卷)向碳酸钠溶液中通入少量CO:CO+CO+HO===2HCO
2 2 2
D.(2019·海南卷)向硫化钠溶液中通入过量SO :2S2-+5SO +2HO===3S↓+4HSO
2 2 2A [NaOH与过量的HC O 生成酸式盐NaHC O,A项错误;亚硫酸钠具有强还原性,
2 2 4 2 4
而氯气具有强氧化性,二者会发生氧化还原反应,生成硫酸钠和盐酸,当参加反应的氯气量
较少时,反应生成的盐酸会与亚硫酸钠反应生成亚硫酸氢钠,B项正确;碳酸钠溶液中通入
少量CO ,反应生成NaHCO ,C项正确;硫化钠溶液中通入过量 SO ,反应生成S和
2 3 2
NaHSO,D项正确。]
3
[强化4] 下列离子方程式中书写正确的是( )
A.CuSO 溶液与过量浓氨水反应的离子方程式:Cu2++2NH ·H O===Cu(OH) ↓+2NH
4 3 2 2
B.向FeI 溶液中通入少量Cl:2Fe2++Cl===2Fe3++2Cl-
2 2 2
C.向NaAlO 溶液中通入少量CO:2AlO+CO+3HO===2Al(OH) ↓+CO
2 2 2 2 3
D.等体积、等浓度的NH HSO 溶液与NaOH溶液混合:NH+HSO+2OH-===NH·H O
4 3 3 2
+SO+HO
2
C [Cu(OH) 溶于过量氨水,正确应为Cu2++4NH ·H O===Cu(NH)+4HO,A项错误;
2 3 2 3 2
I-的还原性强于Fe2+,向FeI 溶液中通入少量Cl,只将I-氧化生成I,B项错误;等体积、等
2 2 2
浓度的NH HSO 溶液与NaOH溶液混合,溶质的物质的量之比为1∶1,NaOH完全反应,只
4 3
发生反应:HSO+OH-===SO+HO,D项错误。]
2
考向2 特殊离子方程式的书写(实践与操作能力)
近几年,高考重点考查了新情境下的离子方程式的书写,大多出现在Ⅱ卷的化工流程题
或综合实验题中,要求考生从试题提供的新信息中,准确地提取实质性内容,并经与已有知
识块整合,重组为新知识块,进行学以致用的学科认知操作和行动操作,用于分析、解决实际
问题,侧重考查考生的阅读理解能力、信息搜索能力、信息整理能力、动手操作能力、语言表
达能力等。
角度5 “配比型”离子方程式的书写——“少定多变法”
书写酸式盐与碱反应的离子方程式,常采用“少定多变法”,具体思路如下:(1)将少量物质定为“1 mol”,若少量物质有两种或两种以上离子参加反应,则参加反应
离子的物质的量之比与物质组成之比相符。
(2)依据少量物质中离子的物质的量,确定过量物质中实际参加反应的离子的物质的量。
(3)依据“先中和后沉淀”的思路书写。
按要求写出下列反应的离子方程式。
(1)向Ca(HCO ) 溶液中加入足量NaOH溶液:
3 2
________________________________________________________________________。
(2)向NaHCO 溶液中加入少量Ba(OH) 溶液:
3 2
________________________________________________________________________。
(3)向NaHCO 溶液中加入足量Ba(OH) 溶液:
3 2
________________________________________________________________________。
(4) 等 体 积 、 等 浓 度 的 Ba(OH) 溶 液 与 NaHSO 溶 液 混 合 :
2 4
________________________________________________________________________。
解析 (1)采用“少定多变法”分析向Ca(HCO ) 溶液中加入足量NaOH溶液:
3 2
(2)向NaHCO 溶液中加入少量Ba(OH) 溶液,Ba(OH) 完全反应,将其定为1 mol,拆分
3 2 2
成1 mol Ba2+和2 mol OH-;NaHCO 足量,2 mol OH-消耗2 mol HCO,生成2 mol CO和2
3
mol HO,其中1 mol CO与Ba2+结合生成BaCO 沉淀:Ba2++2HCO+2OH-===BaCO ↓+
2 3 3
CO+2HO。
2
(3)向NaHCO 溶液中加入足量Ba(OH) 溶液,NaHCO 完全反应,将其定为1 mol,写出
3 2 3
离子方程式:Ba2++HCO+OH-===BaCO ↓+HO
3 2
(4)等体积、等浓度的Ba(OH) 溶液与NaHSO 溶液混合,二者的物质的量之比为1∶1,
2 4
OH-与H+生成水后还剩余,按NaHSO 书写离子方程式:Ba2++OH-+H++SO===BaSO ↓
4 4
+HO。
2
答案 (1)Ca2++2HCO+2OH-===CaCO ↓+CO+2HO
3 2
(2)Ba2++2HCO+2OH-===BaCO ↓+CO+2HO
3 2
(3)Ba2++HCO+OH-===BaCO ↓+HO
3 2
(4)Ba2++OH-+H++SO===BaSO ↓+HO
4 2[强化5] 写出下列反应的离子方程式:
(1)少量Ca(OH) 溶液和NaHCO 溶液反应:
2 3
________________________________________________________________________。
(2)过量硫酸氢钠溶液与氢氧化钡溶液反应:
________________________________________________________________________。
(3)将SO 通入到过量NaClO溶液中:
2
________________________________________________________________________。
(4)Mg(HCO ) 溶液与足量的NaOH溶液反应:
3 2
________________________________________________________________________。
答案 (1)Ca2++2OH-+2HCO===CaCO ↓+CO+2HO
3 2
(2)Ba2++2OH-+SO+2H+===BaSO ↓+2HO
4 2
(3)SO +ClO-+HO===Cl-+SO+2H+
2 2
(4)Mg2++2HCO+4OH-===Mg(OH) ↓+2CO+2HO
2 2
角度6 “顺序型”离子方程式的书写——“先分后总法”
“连续型”离子反应中,生成的物质(或离子)与过量的某种离子继续反应,导致其离子
方程式与反应物的用量有关。书写“连续型”离子方程式,常采用“先分后总法”,具体思路
如下:
(1)分析反应物的用量,判断物质过量与否,确定反应物是恰好反应,还是某种物质过量。
(2)若某物质过量,考虑生成的物质(或离子)与过量物质之间的反应。
(3)依据“先分后总”的思路书写总反应的离子方程式。
按要求写出下列反应的离子方程式。
(1)向水玻璃中通入足量CO:
2
________________________________________________________________________。
(2)向NaAlO 溶液中滴加盐酸至过量:
2
________________________________________________________________________。(3)向AlCl 溶液中滴加NaOH溶液至过量:
3
________________________________________________________________________。
(4)向NaCO 溶液中滴加稀盐酸至过量:
2 3
________________________________________________________________________。
解析 (1)向水玻璃中通入足量 CO ,先反应生成 HSiO 和 NaCO :SiO+HO+
2 2 3 2 3 2
CO===H SiO↓+CO;继续通入CO ,NaCO 与CO 、HO生成NaHCO :CO+CO +
2 2 3 2 2 3 2 2 3 2
HO===2HCO,综合上述两式可得:SiO+2HO+2CO===H SiO↓+2HCO。
2 2 2 2 3
(2)向NaAlO 溶液中滴加盐酸至过量,先发生反应:AlO+HO+H+===Al(OH) ↓,生成
2 2 3
的Al(OH) 与过量盐酸发生反应:Al(OH) +3H+===Al3++3HO,综合上述两式可得:AlO+
3 3 2
4H+=== Al3++2HO。
2
(3)向AlCl 溶液中滴加NaOH溶液至过量,先发生反应:Al3++3OH-=== Al(OH) ↓,生
3 3
成的Al(OH) 与过量NaOH溶液发生反应:Al(OH) +OH-===AlO+2HO,综合上述两式可
3 3 2
得:Al3++4OH-=== AlO+2HO。
2
(4)向NaCO 溶液中滴加稀盐酸至过量,先发生反应:CO+H+===HCO,盐酸过量时发
2 3
生反应:HCO+H+===CO ↑+HO,综合上述两式可得:CO+2H+=== CO↑+HO。
2 2 2 2
答案 (1)SiO+2HO+2CO===H SiO↓+2HCO
2 2 2 3
(2)AlO+4H+=== Al3++2HO
2
(3)Al3++4OH-=== AlO+2HO
2
(4)CO+2H+=== CO↑+HO
2 2
[强化6] 写出下列反应的离子方程式:
(1)将铁粉加入足量稀硝酸中:
________________________________________________________________________。
(2)向NaOH溶液中通入足量SO 气体:
2________________________________________________________________________。
(3)向HS溶液中加入足量NaOH溶液:
2
________________________________________________________________________。
(4)向FeCl 溶液中加入足量锌粉:
3
________________________________________________________________________。
答案 (1)Fe+NO+4H+===Fe3++NO↑+2HO
2
(2)SO +OH-===HSO
2
(3)H S+2OH-===S2-+2HO
2 2
(4)2Fe3++3Zn===3Zn2++2Fe
角度7 “竞争型”离子方程式的书写——“先强后弱法”
一种反应物电离产生的两种或两种以上的组成离子,都能跟另一种反应物反应,但反应
相互竞争,当另一种反应物不足时,要考虑反应的先后顺序。
(1)氧化还原型的离子反应
对于氧化还原反应,按“先强后弱”的顺序书写,即氧化性(或还原性)强的优先发生反
应,氧化性(或还原性)弱的后发生反应。具体思路如下:
①确定反应的先后顺序,如氧化性:HNO>Fe3+,还原性:I->Fe2+>Br-。例如,向FeI
3 2
溶液中通入Cl,I-先与Cl 发生反应。
2 2
②根据反应物的量判断反应发生的情况,确定是部分还是全部离子反应。例如,足量Cl
2
与FeI 溶液反应时,I-、Fe2+均与Cl 发生反应:2Fe2++4I-+3Cl===2Fe3++2I+6Cl-。
2 2 2 2
(2)非氧化还原型的离子反应
①与OH-反应的先后顺序:H+>金属阳离子(如Fe3+、Cu2+等)>HCO>NH等。
②与H+反应的先后顺序:OH->AlO>CO>HCO等。
按要求写出下列反应的离子方程式。
(1)向FeBr 溶液中通入少量Cl:
2 2
________________________________________________________________________。
(2)向NH Al(SO) 溶液中加入少量NaOH溶液:
4 4 2
________________________________________________________________________。
(3)NH HCO 溶液与足量澄清石灰水混合:
4 3
________________________________________________________________________。
(4)1 mol·L - 1 的 NaAlO 溶 液 和 2.5 mol·L - 1 的 HCl 溶 液 等 体 积 混 合 :
2
________________________________________________________________________。
解析 (1)向FeBr 溶液中通入少量Cl,由于还原性:Fe2+>Br-,Cl 只氧化Fe2+生成Fe3
2 2 2+:2Fe2++Cl===2Fe3++2Cl-。
2
(2)向NH Al(SO) 溶液中加入少量NaOH溶液,OH-先与Al3+反应生成Al(OH) ,离子
4 4 2 3
方程式为:Al3++3OH-===Al(OH) ↓。
3
(3)NH HCO 溶液与足量澄清石灰水混合,NH、HCO均与OH-反应,离子方程式为:NH
4 3
+HCO+2OH-+Ca2+===CaCO ↓+NH ·HO+HO。
3 3 2 2
(4)1 mol·L-1的NaAlO 溶液和2.5 mol·L-1的HCl溶液等体积混合,NaAlO 和HCl的物
2 2
质的量之比为2∶5,反应生成Al3+、Al(OH) ,离子方程式为2AlO+5H+===Al3++Al(OH) ↓
3 3
+HO。
2
答案 (1)2Fe2++Cl===2Fe3++2Cl-
2
(2)Al3++3OH-===Al(OH) ↓
3
(3)NH+HCO+2OH-+Ca2+===CaCO ↓+NH ·H O+HO
3 3 2 2
(4)2AlO+5H+===Al3++Al(OH) ↓+HO
3 2
[强化7] (原创题)写出下列反应的离子方程式:
(1) 向 含 有 0.4 mol FeBr 的 溶 液 中 通 入 0.3 mol Cl 充 分 反 应 :
2 2
________________________________________________________________________。
(2) 向 含 0.1 mol FeBr 和 0.1 mol FeI 的 混 合 液 中 通 入 0.2 mol Cl :
2 2 2
________________________________________________________________________。
(3)向 NH HSO 稀溶液中 逐滴加入 Ba(OH) 稀溶液至 SO 刚好沉淀 完全 :
4 4 2
________________________________________________________________________。
(4)0.1 mol·L - 1NH Al(SO ) 溶 液 与 0.2 mol·L - 1Ba(OH) 溶 液 等 体 积 混 合 :
4 4 2 2
________________________________________________________________________
________________________________________________________________________。
答案 (1)4Fe2++2Br-+3Cl===4Fe3++6Cl-+Br
2 2
(2)2Fe2++2I-+2Cl===2Fe3++I+4Cl-
2 2
(3)Ba2++2OH-+NH+H++SO===BaSO ↓+NH ·H O+HO
4 3 2 2
(4)NH+Al3++2SO+2Ba2++4OH-===Al(OH) ↓+2BaSO↓+NH ·H O
3 4 3 2角度8 “情境型”离子方程式的书写——“守恒规律法”
书写新情境下的离子方程式,可采用“守恒规律法”,巧妙利用原子、得失电子及电荷守
恒进行书写,具体思路如下[以NaClO溶液与SO 的反应为例]:
2
(1)依据物质的氧化性和还原性,找出发生氧化还原反应的粒子:ClO-和SO 。
2
(2)根据氧化还原反应中价态转化规律,判断反应的产物:ClO-+SO +…―→Cl-+SO
2
+…。
(3)配电子:依据得失电子守恒配平氧化剂和还原剂、氧化产物和还原产物的化学计量数:
ClO-+SO +…―→Cl-+SO+…。
2
(4)配原子:依据质量守恒配平未参与氧化还原反应的原子:ClO-+SO +HO―→Cl-+
2 2
SO+H+。
(5)配电荷:依据电荷守恒,配平各微粒的化学计量数:ClO-+SO +HO===Cl-+SO+
2 2
2H+。
非氧化还原反应型离子方程式的书写,只需要配原子和电荷,不需要配电子。
(1)(2020·全国卷Ⅲ,27题节选)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用
作镍镉电池正极材料的NiOOH,写出该反应的离子方程式:
_____________________________
________________________________________________________________________。
(2)(2019·全国卷Ⅱ,26题节选)立德粉ZnS·BaSO(也称锌钡白),是一种常用白色颜料:
4
, 沉 淀 器 中 反 应 的 离 子 方 程 式 为
________________________________________________________________________。
(3)(2019·全国卷Ⅲ,26题节选)含MnSO 的溶液 ,写出“沉
4
锰”的离子方程式_______________________________________________________________
________________________________________________________________________。
解析 (1)Ni2+被ClO-氧化为NiOOH,ClO-被还原为Cl-,根据电子守恒可配平得2Ni2+
+ClO-―→2NiOOH↓+Cl-,再依据电荷守恒可配平得 2Ni2++ClO-+4OH-
―→2NiOOH↓+Cl-,最后依据质量守恒可配平得2Ni2++ClO-+4OH-===2NiOOH↓+Cl
-+HO。
2
(2)“沉淀器”中净化的BaS溶液加入ZnSO ,反应生成难溶于水的立德粉,反应物是
4BaS、ZnSO,生成物是ZnS·BaSO,离子方程式为Ba2++S2-+Zn2++SO=== ZnS·BaSO↓。
4 4 4
(3)“沉锰”时,含MnSO 的溶液中加入NH HCO ,生成MnCO 沉淀,Mn2+与HCO电
4 4 3 3
离产生的CO结合生成MnCO 沉淀,部分HCO结合H+生成CO 和HO,离子方程式为Mn2
3 2 2
++2HCO===MnCO↓+CO↑+HO。
3 2 2
答案 (1)2Ni2++ClO-+4OH-===2NiOOH↓+Cl-+HO
2
(2)Ba2++S2-+Zn2++SO=== ZnS·BaSO↓
4
(3)Mn2++2HCO===MnCO↓+CO↑+HO
3 2 2
[强化8] 根据题给信息,回答相关问题:
(1)(2018·全国卷Ⅱ,26题节选)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离
子方程式为___________________________________________________________________
________________________________________________________________________。
(2)(2018·天津卷,9题节选)NO被HO 氧化为NO的离子方程式是_______________
2 2
________________________________________________________________________。
(3)(2018·海南卷,14题节选)电子工业使用FeCl 溶液刻蚀印刷电路板铜箔,写出该过程
3
的离子方程式__________________________________________________________________
________________________________________________________________________。
(4)(2017·全国卷Ⅰ,27题节选)LiTi O 和LiFePO 都是锂离子电池的电极材料,可利用
4 3 12 4
钛铁矿(主要成分为FeTiO,还含有少量MgO、SiO 等杂质)来制备。钛铁矿加入盐酸“酸浸”,
3 2
“ 酸 浸 ” 后 , 钛 主 要 以 TiOCl 形 式 存 在 , 写 出 相 应 反 应 的 离 子 方 程 式 :
________________________________________________________________________________________________________________________________________________。
解析 (1)溶液中的Cd2+可用锌粉除去,锌是活泼金属,发生置换反应,离子方程式为Zn
+Cd2+===Cd+Zn2+。
(2)NO被HO 氧化为NO,则被还原为HO,据此可得:NO+HO +…→NO+HO
2 2 2 2 2 2
+…,结合得失电子守恒、原子守恒和电荷守恒配平:2NO+3HO===2NO+2H++2HO。
2 2 2
(3)用FeCl 溶液刻蚀印刷电路板铜箔,发生反应:2Fe3++Cu===2Fe2++Cu2+。
3
(4)钛铁矿的主要成分为FeTiO,加入盐酸“酸浸”,“酸浸”后,钛主要以TiOCl形式存
3
在,则有FeTiO+H++Cl-―→Fe2++TiOCl+…,结合原子守恒和电荷守恒配平该离子方程
3
式。
答案 (1)Zn+Cd2+===Cd+Zn2+
(2)2NO+3HO===2NO+2H++2HO
2 2 2
(3)2Fe3++Cu===2Fe2++Cu2+
(4)FeTiO+4H++4Cl-===Fe2++TiOCl+2HO
3 2
训练(七) 离子方程式的判断及书写
1.(2021·清华大学附中一模)下列实验对应的离子方程式正确的是( )
A.铝溶解在NaOH溶液中: 2Al+2OH-===2AlO+3H↑
2
B.向溴水中通入 SO 后褪色: SO +Br +2HO===SO+2Br-+4H+
2 2 2 2
C.白醋与 84 消毒液混合产生黄绿色气体:Cl-+ClO-+2H+===Cl↑+HO
2 2
D.少量铁溶于过量稀硝酸中:3Fe+8H++2NO===3Fe2++2NO↑+4HO
2
B [不符合原子守恒,正确应为2Al+2OH-+2HO===2AlO+3H↑,A错误;醋酸是弱
2 2
酸,书写离子方程式时,要用化学式CHCOOH,C错误;少量铁溶于过量稀硝酸生成
3
Fe(NO ),正确应为Fe+4H++NO===Fe3++NO↑+2HO,D错误。]
3 3 2
2.(2021·天津和平区一模)能正确表示下列反应的离子方程式为( )
A.向FeBr 溶液中通入过量Cl:2Fe2++Cl===2Fe3++2Cl-
2 2 2
B.向饱和碳酸钠溶液中通入足量CO:CO+2CO+HO===2HCO
2 2 2
C.向碘化钾溶液中加入少量酸性双氧水:3HO+I-===IO+3HO
2 2 2
D.向CuSO 溶液中通入HS:HS+Cu2+===CuS↓+2H+
4 2 2
D [Fe2+、Br-都能被过量Cl 氧化,正确应为2Fe2++4Br-+3Cl===2Fe3++2Br +6Cl
2 2 2
-,A错误;饱和NaCO 溶液中通入足量CO,析出NaHCO 晶体,正确应为2Na++CO+CO
2 3 2 3 2
+HO===2NaHCO↓,B错误;KI溶液中加入少量双氧水,反应生成I,正确应为2I-+HO
2 3 2 2 2
+2H+===I +2HO,C错误。]
2 2
3.(2021·吉林松原检测)下列离子方程式正确的是( )
A.KClO碱性溶液与Fe(OH) 反应:3ClO-+2Fe(OH) ===2FeO+3Cl-+4H++HO
3 3 2
B.用稀硫酸除去硫酸钠溶液中少量的硫代硫酸钠:SO+2H+===SO↑+S↓+HO
2 2 2
C.铝粉加入NaOH溶液中产生无色气体:2Al+2OH-===2AlO+H↑
2D.向碳酸氢铵溶液中加入足量Ba(OH) 溶液:Ba2++HCO+OH-===BaCO ↓+HO
2 3 2
B [在强碱性溶液中不可能生成H+,应为3ClO-+2Fe(OH) +4OH-===2FeO+3Cl-+
3
5HO, A项错误;用稀硫酸除去硫酸钠溶液中少量的NaSO,反应生成二氧化硫和硫:SO
2 2 2 3 2
+2H+===SO↑+S↓+HO, B项正确;Al与NaOH溶液反应生成NaAlO 和H,正确应为
2 2 2 2
2Al+2OH-+2HO===2AlO+3H↑,C项错误;向碳酸氢铵溶液中加入足量Ba(OH) 溶液,
2 2 2
NH、HCO均与OH-反应,生成的CO与Ba2+结合生成BaCO 沉淀,正确应为Ba2++HCO+
3
NH+2OH-===BaCO ↓+NH ·HO+HO,D项错误。]
3 3 2 2
4.(2021·山东青岛检测)下列指定反应的离子方程式正确的是( )
A.钠与水反应:Na+2HO===Na++2OH-+H↑
2 2
B.用CHCOOH溶解CaCO :CaCO +2H+===Ca2++HO+CO↑
3 3 3 2 2
C.向FeCl 溶液中加入少量KSCN溶液:Fe3++3SCN-===Fe(SCN)
3 3
D.NaHSO 溶液与Ba(OH) 溶液反应至中性:H++SO+Ba2++OH-===BaSO ↓+HO
4 2 4 2
C [不符合电荷守恒规律,应为2Na+2HO===2Na++2OH-+H↑,A项错误;醋酸为
2 2
弱电解质,要用化学式表示,应为CaCO +2CHCOOH===Ca2++CO↑+2CHCOO-+
3 3 2 3
HO,B项错误; FeCl 溶液加入少量KSCN溶液,反应生成弱电解质Fe(SCN) ,符合反应事
2 3 3
实及守恒规律,C项正确;不符合反应物的离子配比关系,应为2H++SO+Ba2++2OH-
===BaSO ↓+2HO,D项错误。]
4 2
5.(2021·北京海淀区一模)下列反应的离子方程式不正确的是( )
A.NaOH溶液腐蚀玻璃瓶塞:SiO+2OH-=== SiO+2HO
2 2
B.实验室制Cl:MnO +4HCl(浓)=====Mn2++2Cl-+2HO+Cl↑
2 2 2 2
C.向Mg(OH) 悬浊液中加入FeCl 溶液:2Fe3++3Mg(OH) ===2 Fe(OH) +3Mg2+
2 3 2 3
D.向Ba(OH) 溶液中加入少量NaHSO 溶液: HSO+Ba2++OH-===BaSO ↓+HO
2 3 3 2
B [盐酸是强酸,书写离子方程式要用离子式表示,正确应为MnO +4H++2Cl-
2
=====Mn2++2HO+Cl↑,B错误。]
2 2
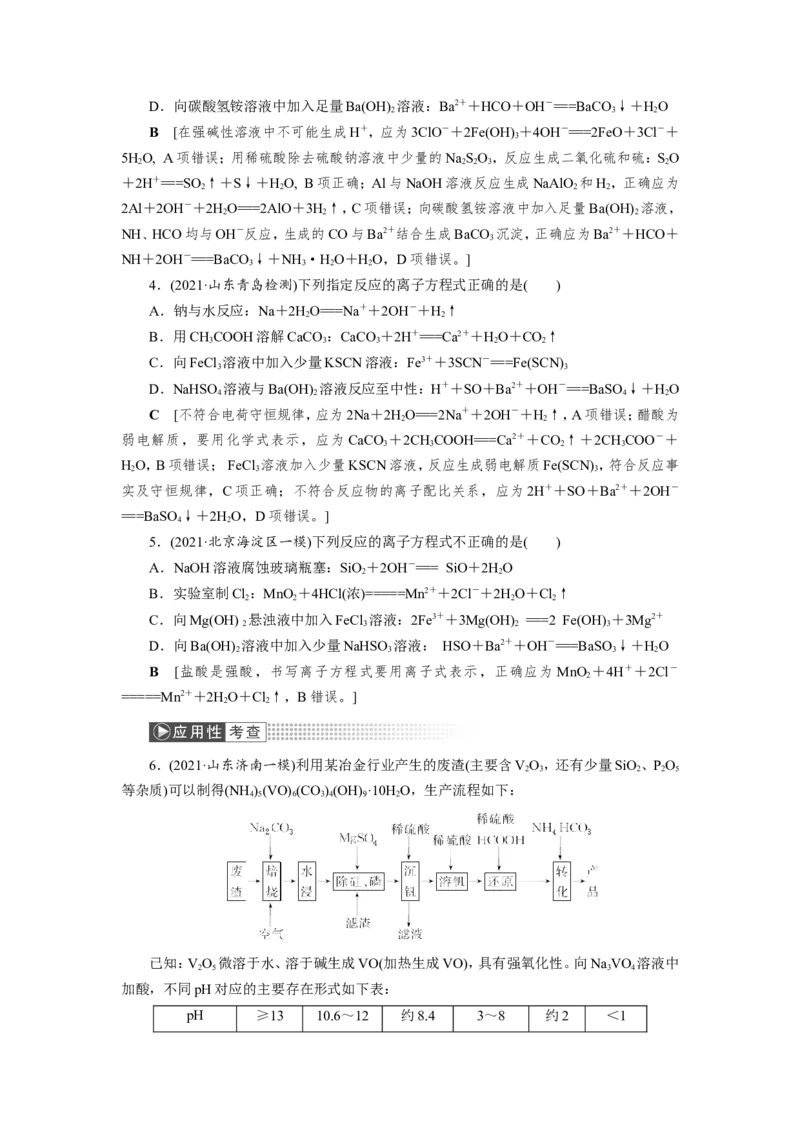
6.(2021·山东济南一模)利用某冶金行业产生的废渣(主要含VO,还有少量SiO、PO
2 3 2 2 5
等杂质)可以制得(NH )(VO) (CO)(OH) ·10H O,生产流程如下:
4 5 6 3 4 9 2
已知:VO 微溶于水、溶于碱生成VO(加热生成VO),具有强氧化性。向NaVO 溶液中
2 5 3 4
加酸,不同pH对应的主要存在形式如下表:
pH ≥13 10.6~12 约8.4 3~8 约2 <1存在形式 VO VO VO V O VO VO
2 3 10 2 5
回答下列问题:
(1)“焙烧”后V元素转化为NaVO ,Si元素转化为________(写化学式)。
3
(2)“沉钒”过程中,pH由8.5到5.0发生反应的离子方程式为:_____________________
最终需 要控制 pH 约为________;“沉钒”最终 得到的 主要含钒 物质是
______________(写化学式)。
(3)“还原”和“转化”过程中主要反应的离子方程式分别为
________________________________________________________________________、
________________________________________________________________________。
答案 (1)Na SiO
2 3
(2)10V O+12H+===3V O+6HO 2 VO
3 10 2 2 5
(3)2VO+HCOOH+2H+===2VO2++CO↑+2HO
2 2
5NH+6VO2++17HCO+6HO===(NH )(VO) (CO)(OH) ·10H O+13CO↑
2 4 5 6 3 4 9 2 2
或5NH+6VO2++17HCO+19HO===(NH )(VO) (CO)(OH) ·10H O+13HCO
2 4 5 6 3 4 9 2 2 3
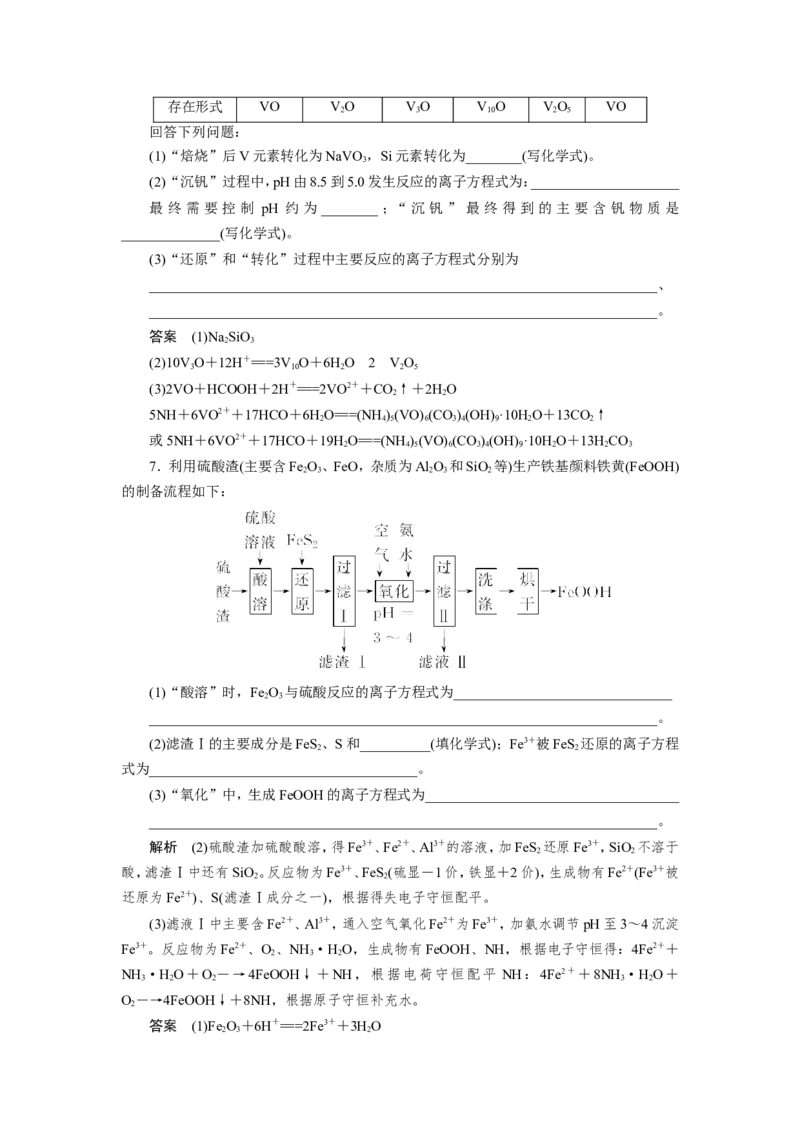
7.利用硫酸渣(主要含Fe O、FeO,杂质为Al O 和SiO 等)生产铁基颜料铁黄(FeOOH)
2 3 2 3 2
的制备流程如下:
(1)“酸溶”时,Fe O 与硫酸反应的离子方程式为_______________________________
2 3
________________________________________________________________________。
(2)滤渣Ⅰ的主要成分是FeS、S和__________(填化学式);Fe3+被FeS 还原的离子方程
2 2
式为______________________________________。
(3)“氧化”中,生成FeOOH的离子方程式为____________________________________
________________________________________________________________________。
解析 (2)硫酸渣加硫酸酸溶,得Fe3+、Fe2+、Al3+的溶液,加FeS 还原Fe3+,SiO 不溶于
2 2
酸,滤渣Ⅰ中还有SiO。反应物为Fe3+、FeS(硫显-1价,铁显+2价),生成物有Fe2+(Fe3+被
2 2
还原为Fe2+)、S(滤渣Ⅰ成分之一),根据得失电子守恒配平。
(3)滤液Ⅰ中主要含Fe2+、Al3+,通入空气氧化Fe2+为Fe3+,加氨水调节pH至3~4沉淀
Fe3+。反应物为Fe2+、O、NH ·HO,生成物有FeOOH、NH,根据电子守恒得:4Fe2++
2 3 2
NH ·HO+O―→4FeOOH↓+NH,根据电荷守恒配平 NH:4Fe2++8NH ·HO+
3 2 2 3 2
O―→4FeOOH↓+8NH,根据原子守恒补充水。
2
答案 (1)Fe O+6H+===2Fe3++3HO
2 3 2(2)SiO 2Fe3++FeS===3Fe2++2S
2 2
(3)4Fe2++8NH ·H O+O===4FeOOH↓+8NH+2HO
3 2 2 2