文档内容
训练(七) 离子方程式的判断及书写
1.(2021·清华大学附中一模)下列实验对应的离子方程式正确的是( )
A.铝溶解在NaOH溶液中: 2Al+2OH-===2AlO+3H↑
2
B.向溴水中通入 SO 后褪色: SO +Br +2HO===SO+2Br-+4H+
2 2 2 2
C.白醋与 84 消毒液混合产生黄绿色气体:Cl-+ClO-+2H+===Cl↑+HO
2 2
D.少量铁溶于过量稀硝酸中:3Fe+8H++2NO===3Fe2++2NO↑+4HO
2
B [不符合原子守恒,正确应为2Al+2OH-+2HO===2AlO+3H↑,A错误;醋酸是弱
2 2
酸,书写离子方程式时,要用化学式CHCOOH,C错误;少量铁溶于过量稀硝酸生成
3
Fe(NO ),正确应为Fe+4H++NO===Fe3++NO↑+2HO,D错误。]
3 3 2
2.(2021·天津和平区一模)能正确表示下列反应的离子方程式为( )
A.向FeBr 溶液中通入过量Cl:2Fe2++Cl===2Fe3++2Cl-
2 2 2
B.向饱和碳酸钠溶液中通入足量CO:CO+2CO+HO===2HCO
2 2 2
C.向碘化钾溶液中加入少量酸性双氧水:3HO+I-===IO+3HO
2 2 2
D.向CuSO 溶液中通入HS:HS+Cu2+===CuS↓+2H+
4 2 2
D [Fe2+、Br-都能被过量Cl 氧化,正确应为2Fe2++4Br-+3Cl===2Fe3++2Br +6Cl
2 2 2
-,A错误;饱和NaCO 溶液中通入足量CO,析出NaHCO 晶体,正确应为2Na++CO+CO
2 3 2 3 2
+HO===2NaHCO↓,B错误;KI溶液中加入少量双氧水,反应生成I,正确应为2I-+HO
2 3 2 2 2
+2H+===I +2HO,C错误。]
2 2
3.(2021·吉林松原检测)下列离子方程式正确的是( )
A.KClO碱性溶液与Fe(OH) 反应:3ClO-+2Fe(OH) ===2FeO+3Cl-+4H++HO
3 3 2
B.用稀硫酸除去硫酸钠溶液中少量的硫代硫酸钠:SO+2H+===SO↑+S↓+HO
2 2 2
C.铝粉加入NaOH溶液中产生无色气体:2Al+2OH-===2AlO+H↑
2
D.向碳酸氢铵溶液中加入足量Ba(OH) 溶液:Ba2++HCO+OH-===BaCO ↓+HO
2 3 2
B [在强碱性溶液中不可能生成H+,应为3ClO-+2Fe(OH) +4OH-===2FeO+3Cl-+
3
5HO, A项错误;用稀硫酸除去硫酸钠溶液中少量的NaSO,反应生成二氧化硫和硫:SO
2 2 2 3 2
+2H+===SO↑+S↓+HO, B项正确;Al与NaOH溶液反应生成NaAlO 和H,正确应为
2 2 2 2
2Al+2OH-+2HO===2AlO+3H↑,C项错误;向碳酸氢铵溶液中加入足量Ba(OH) 溶液,
2 2 2
NH、HCO均与OH-反应,生成的CO与Ba2+结合生成BaCO 沉淀,正确应为Ba2++HCO+
3
NH+2OH-===BaCO ↓+NH ·HO+HO,D项错误。]
3 3 2 2
4.(2021·山东青岛检测)下列指定反应的离子方程式正确的是( )
A.钠与水反应:Na+2HO===Na++2OH-+H↑
2 2
B.用CHCOOH溶解CaCO :CaCO +2H+===Ca2++HO+CO↑
3 3 3 2 2
C.向FeCl 溶液中加入少量KSCN溶液:Fe3++3SCN-===Fe(SCN)
3 3
D.NaHSO 溶液与Ba(OH) 溶液反应至中性:H++SO+Ba2++OH-===BaSO ↓+HO
4 2 4 2
C [不符合电荷守恒规律,应为2Na+2HO===2Na++2OH-+H↑,A项错误;醋酸为
2 2弱电解质,要用化学式表示,应为CaCO +2CHCOOH===Ca2++CO↑+2CHCOO-+
3 3 2 3
HO,B项错误; FeCl 溶液加入少量KSCN溶液,反应生成弱电解质Fe(SCN) ,符合反应事
2 3 3
实及守恒规律,C项正确;不符合反应物的离子配比关系,应为2H++SO+Ba2++2OH-
===BaSO ↓+2HO,D项错误。]
4 2
5.(2021·北京海淀区一模)下列反应的离子方程式不正确的是( )
A.NaOH溶液腐蚀玻璃瓶塞:SiO+2OH-=== SiO+HO
2 2
B.实验室制Cl:MnO +4HCl(浓)=====Mn2++2Cl-+2HO+Cl↑
2 2 2 2
C.向Mg(OH) 悬浊液中加入FeCl 溶液:2Fe3++3Mg(OH) ===2 Fe(OH) +3Mg2+
2 3 2 3
D.向Ba(OH) 溶液中加入少量NaHSO 溶液: HSO+Ba2++OH-===BaSO ↓+HO
2 3 3 2
B [盐酸是强酸,书写离子方程式要用离子式表示,正确应为MnO +4H++2Cl-
2
=====Mn2++2HO+Cl↑,B错误。]
2 2
6.(2021·山东济南一模)利用某冶金行业产生的废渣(主要含VO,还有少量SiO、PO
2 3 2 2 5
等杂质)可以制得(NH )(VO) (CO)(OH) ·10H O,生产流程如下:
4 5 6 3 4 9 2
已知:VO 微溶于水、溶于碱生成VO(加热生成VO),具有强氧化性。向NaVO 溶液中
2 5 3 4
加酸,不同pH对应的主要存在形式如下表:
pH ≥13 10.6~12 约8.4 3~8 约2 <1
存在形式 VO VO VO V O VO VO
2 3 10 2 5
回答下列问题:
(1)“焙烧”后V元素转化为NaVO ,Si元素转化为________(写化学式)。
3
(2)“沉钒”过程中,pH由8.5到5.0发生反应的离子方程式为:_____________________
最终需要控制 pH 约为 ________;“沉钒 ”最终得到的主要含钒物质是
______________(写化学式)。
(3)“还原”和“转化”过程中主要反应的离子方程式分别为
________________________________________________________________________、
________________________________________________________________________。
答案 (1)Na SiO
2 3
(2)10V O+12H+===3V O+6HO 2 VO
3 10 2 2 5
(3)2VO+HCOOH+2H+===2VO2++CO↑+2HO
2 2
5NH+6VO2++17HCO+6HO===(NH )(VO) (CO)(OH) ·10H O+13CO↑
2 4 5 6 3 4 9 2 2或5NH+6VO2++17HCO+19HO===(NH )(VO) (CO)(OH) ·10H O+13HCO
2 4 5 6 3 4 9 2 2 3
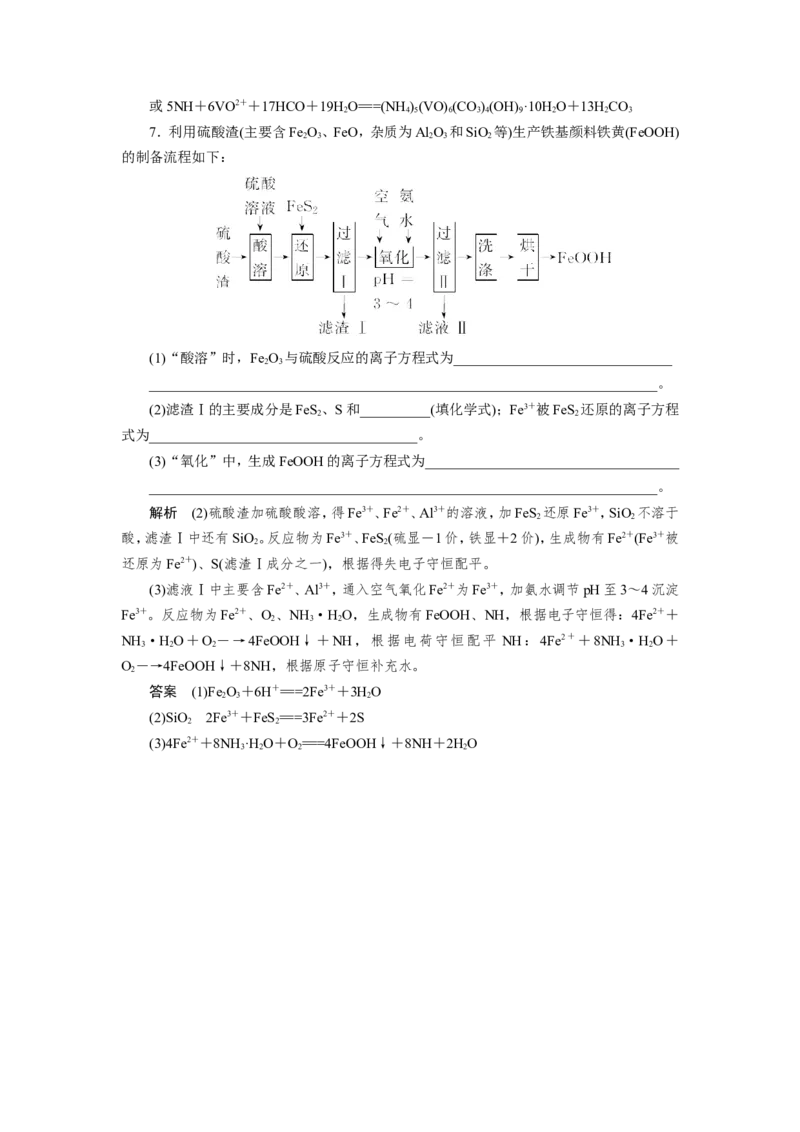
7.利用硫酸渣(主要含Fe O、FeO,杂质为Al O 和SiO 等)生产铁基颜料铁黄(FeOOH)
2 3 2 3 2
的制备流程如下:
(1)“酸溶”时,Fe O 与硫酸反应的离子方程式为_______________________________
2 3
________________________________________________________________________。
(2)滤渣Ⅰ的主要成分是FeS、S和__________(填化学式);Fe3+被FeS 还原的离子方程
2 2
式为______________________________________。
(3)“氧化”中,生成FeOOH的离子方程式为____________________________________
________________________________________________________________________。
解析 (2)硫酸渣加硫酸酸溶,得Fe3+、Fe2+、Al3+的溶液,加FeS 还原Fe3+,SiO 不溶于
2 2
酸,滤渣Ⅰ中还有SiO。反应物为Fe3+、FeS(硫显-1价,铁显+2价),生成物有Fe2+(Fe3+被
2 2
还原为Fe2+)、S(滤渣Ⅰ成分之一),根据得失电子守恒配平。
(3)滤液Ⅰ中主要含Fe2+、Al3+,通入空气氧化Fe2+为Fe3+,加氨水调节pH至3~4沉淀
Fe3+。反应物为Fe2+、O、NH ·HO,生成物有FeOOH、NH,根据电子守恒得:4Fe2++
2 3 2
NH ·HO+O―→4FeOOH↓+NH,根据电荷守恒配平 NH:4Fe2++8NH ·HO+
3 2 2 3 2
O―→4FeOOH↓+8NH,根据原子守恒补充水。
2
答案 (1)Fe O+6H+===2Fe3++3HO
2 3 2
(2)SiO 2Fe3++FeS===3Fe2++2S
2 2
(3)4Fe2++8NH ·H O+O===4FeOOH↓+8NH+2HO
3 2 2 2