文档内容
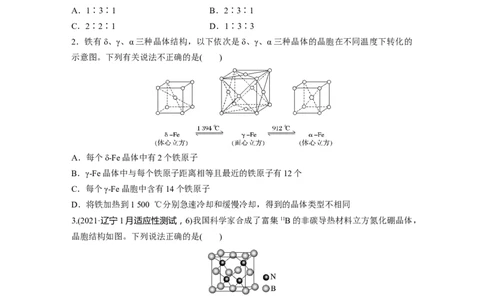
1.(2022·青岛模拟)某物质的晶体中含有A、B、C三种元素,其排列方式如图所示(其中前后
两面面心中的B元素的原子未能画出)。则晶体中A、B、C的原子个数比为( )
A.1∶3∶1 B.2∶3∶1
C.2∶2∶1 D.1∶3∶3
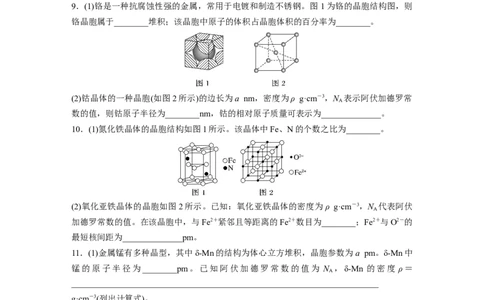
2.铁有δ、γ、α三种晶体结构,以下依次是δ、γ、α三种晶体的晶胞在不同温度下转化的
示意图。下列有关说法不正确的是( )
A.每个δ-Fe晶体中有2个铁原子
B.γ-Fe晶体中与每个铁原子距离相等且最近的铁原子有12个
C.每个γ-Fe晶胞中含有14个铁原子
D.将铁加热到1 500 ℃分别急速冷却和缓慢冷却,得到的晶体类型不相同
3.(2021·辽宁1月适应性测试,6)我国科学家合成了富集11B的非碳导热材料立方氮化硼晶体,
晶胞结构如图。下列说法正确的是( )
A.11BN和10BN的性质无差异
B.该晶体具有良好的导电性
C.该晶胞中含有14个B原子,4个N原子
D.N原子周围等距且最近的N原子数为12
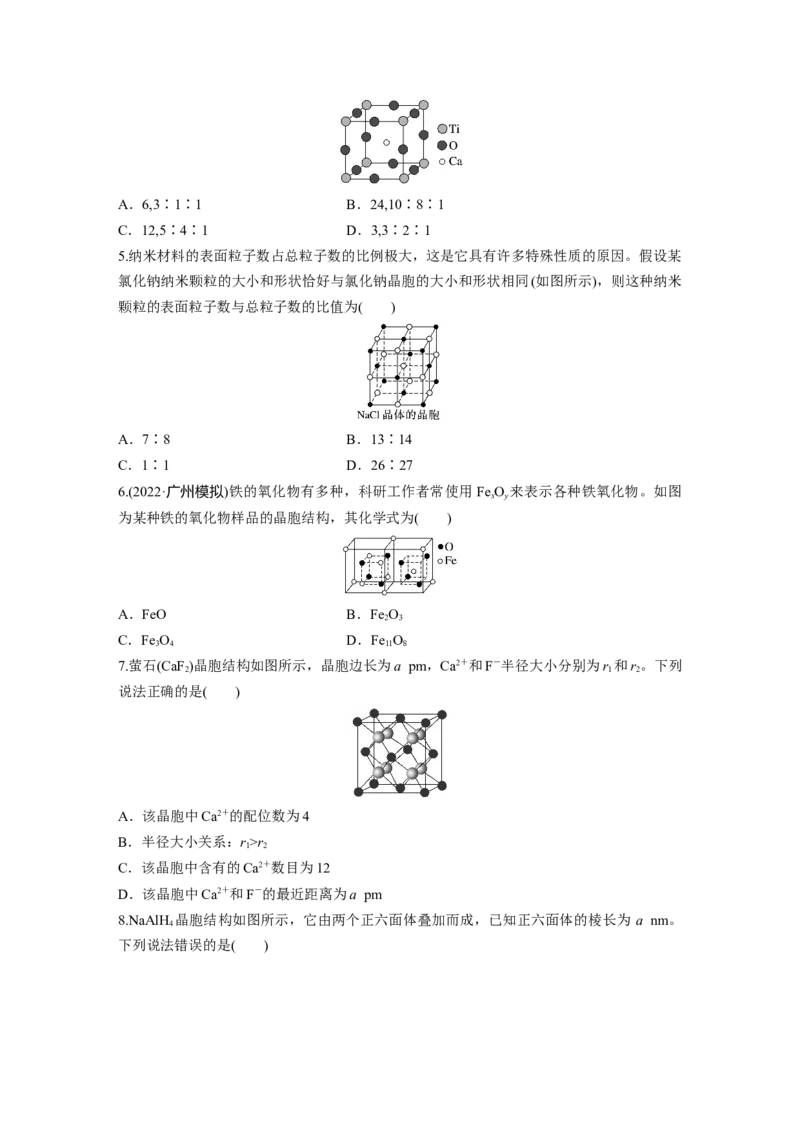
4.如图为高温超导领域里的一种化合物(钙钛矿)结构中的最小重复单元。该化合物中,每个
钛离子周围与它最接近且距离相等的钛离子有a个,元素氧、钛、钙的原子个数比为b。则
a、b是( )A.6,3∶1∶1 B.24,10∶8∶1
C.12,5∶4∶1 D.3,3∶2∶1
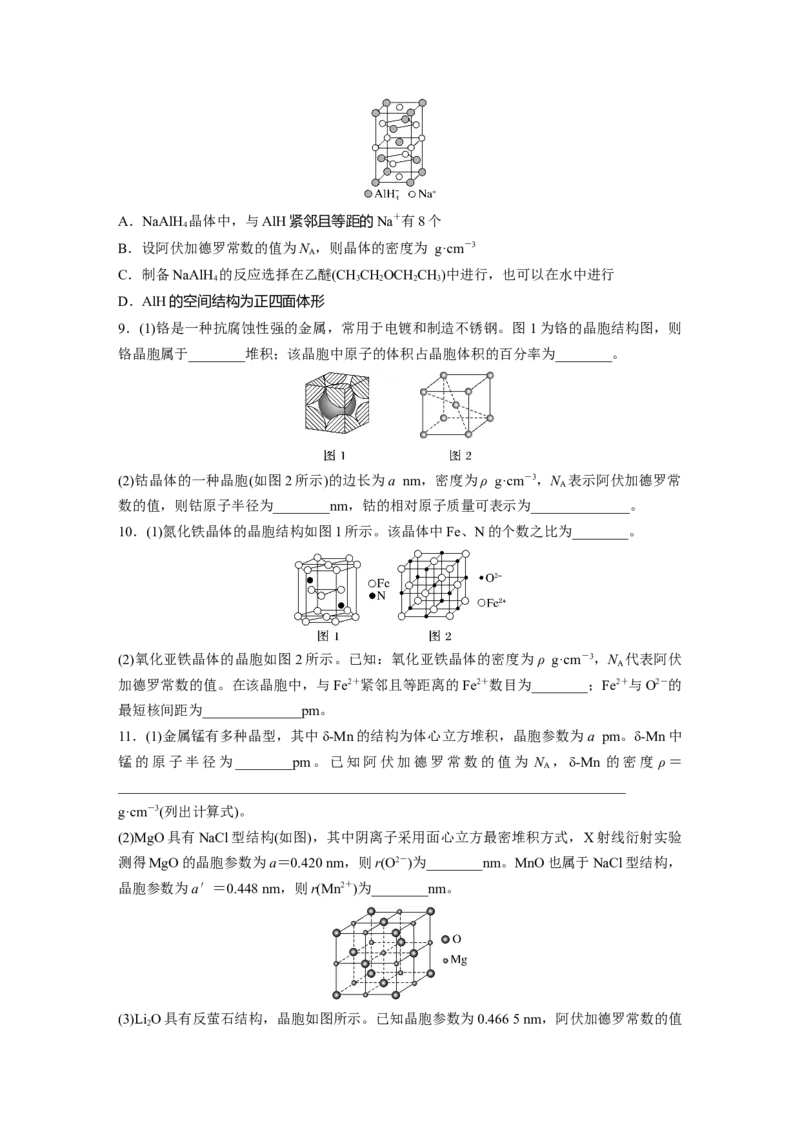
5.纳米材料的表面粒子数占总粒子数的比例极大,这是它具有许多特殊性质的原因。假设某
氯化钠纳米颗粒的大小和形状恰好与氯化钠晶胞的大小和形状相同(如图所示),则这种纳米
颗粒的表面粒子数与总粒子数的比值为( )
A.7∶8 B.13∶14
C.1∶1 D.26∶27
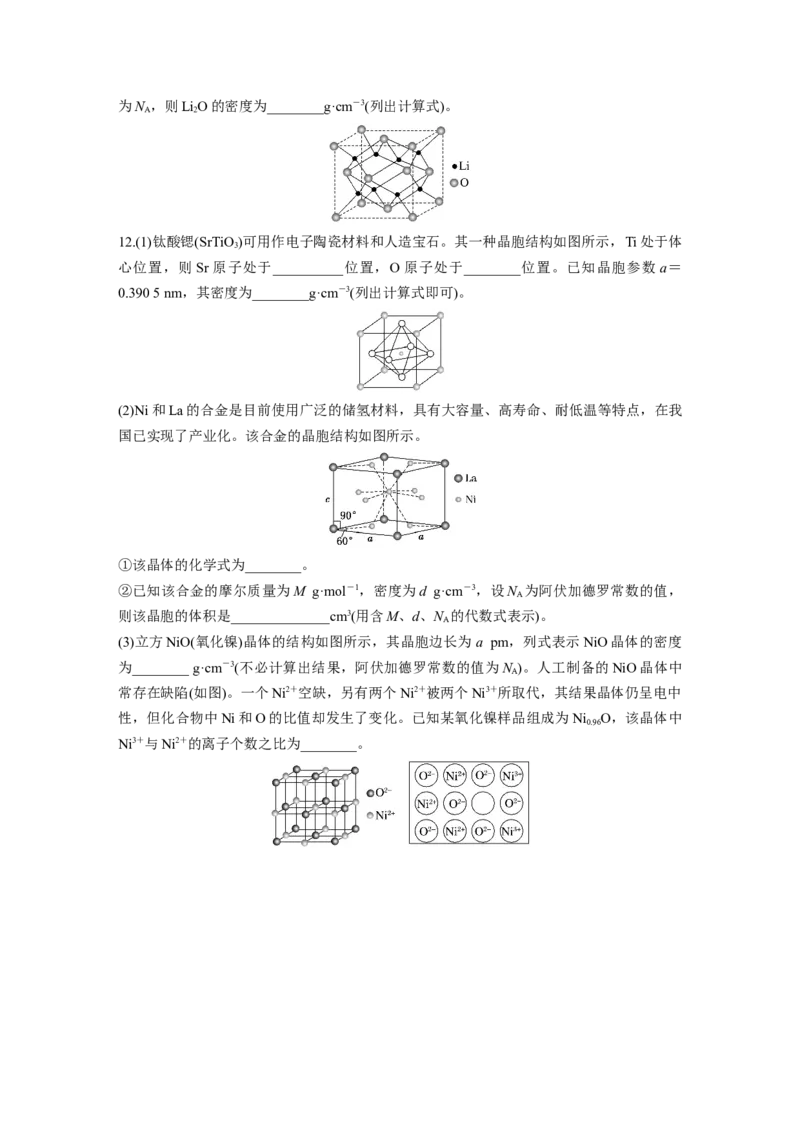
6.(2022·广州模拟)铁的氧化物有多种,科研工作者常使用FeO 来表示各种铁氧化物。如图
x y
为某种铁的氧化物样品的晶胞结构,其化学式为( )
A.FeO B.Fe O
2 3
C.Fe O D.Fe O
3 4 11 8
7.萤石(CaF )晶胞结构如图所示,晶胞边长为a pm,Ca2+和F-半径大小分别为r 和r。下列
2 1 2
说法正确的是( )
A.该晶胞中Ca2+的配位数为4
B.半径大小关系:r>r
1 2
C.该晶胞中含有的Ca2+数目为12
D.该晶胞中Ca2+和F-的最近距离为a pm
8.NaAlH 晶胞结构如图所示,它由两个正六面体叠加而成,已知正六面体的棱长为 a nm。
4
下列说法错误的是( )A.NaAlH 晶体中,与AlH紧邻且等距的Na+有8个
4
B.设阿伏加德罗常数的值为N ,则晶体的密度为 g·cm-3
A
C.制备NaAlH 的反应选择在乙醚(CHCHOCH CH)中进行,也可以在水中进行
4 3 2 2 3
D.AlH的空间结构为正四面体形
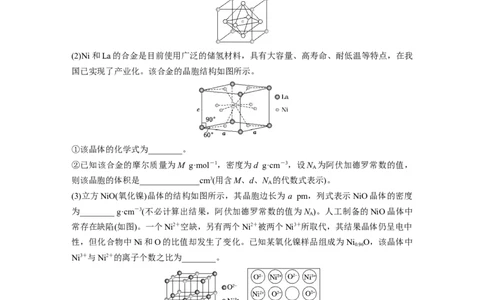
9.(1)铬是一种抗腐蚀性强的金属,常用于电镀和制造不锈钢。图1为铬的晶胞结构图,则
铬晶胞属于________堆积;该晶胞中原子的体积占晶胞体积的百分率为________。
(2)钴晶体的一种晶胞(如图2所示)的边长为a nm,密度为ρ g·cm-3,N 表示阿伏加德罗常
A
数的值,则钴原子半径为________nm,钴的相对原子质量可表示为______________。
10.(1)氮化铁晶体的晶胞结构如图1所示。该晶体中Fe、N的个数之比为________。
(2)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρ g·cm-3,N 代表阿伏
A
加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为________;Fe2+与O2-的
最短核间距为______________pm。
11.(1)金属锰有多种晶型,其中δ-Mn的结构为体心立方堆积,晶胞参数为a pm。δ-Mn中
锰的原子半径为________pm。已知阿伏加德罗常数的值为 N ,δ-Mn 的密度 ρ=
A
________________________________________________________________________
g·cm-3(列出计算式)。
(2)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验
测得MgO的晶胞参数为a=0.420 nm,则r(O2-)为________nm。MnO也属于NaCl型结构,
晶胞参数为a′=0.448 nm,则r(Mn2+)为________nm。
(3)Li O具有反萤石结构,晶胞如图所示。已知晶胞参数为0.466 5 nm,阿伏加德罗常数的值
2为N ,则LiO的密度为________g·cm-3(列出计算式)。
A 2
12.(1)钛酸锶(SrTiO )可用作电子陶瓷材料和人造宝石。其一种晶胞结构如图所示,Ti处于体
3
心位置,则Sr原子处于__________位置,O原子处于________位置。已知晶胞参数 a=
0.390 5 nm,其密度为________g·cm-3(列出计算式即可)。
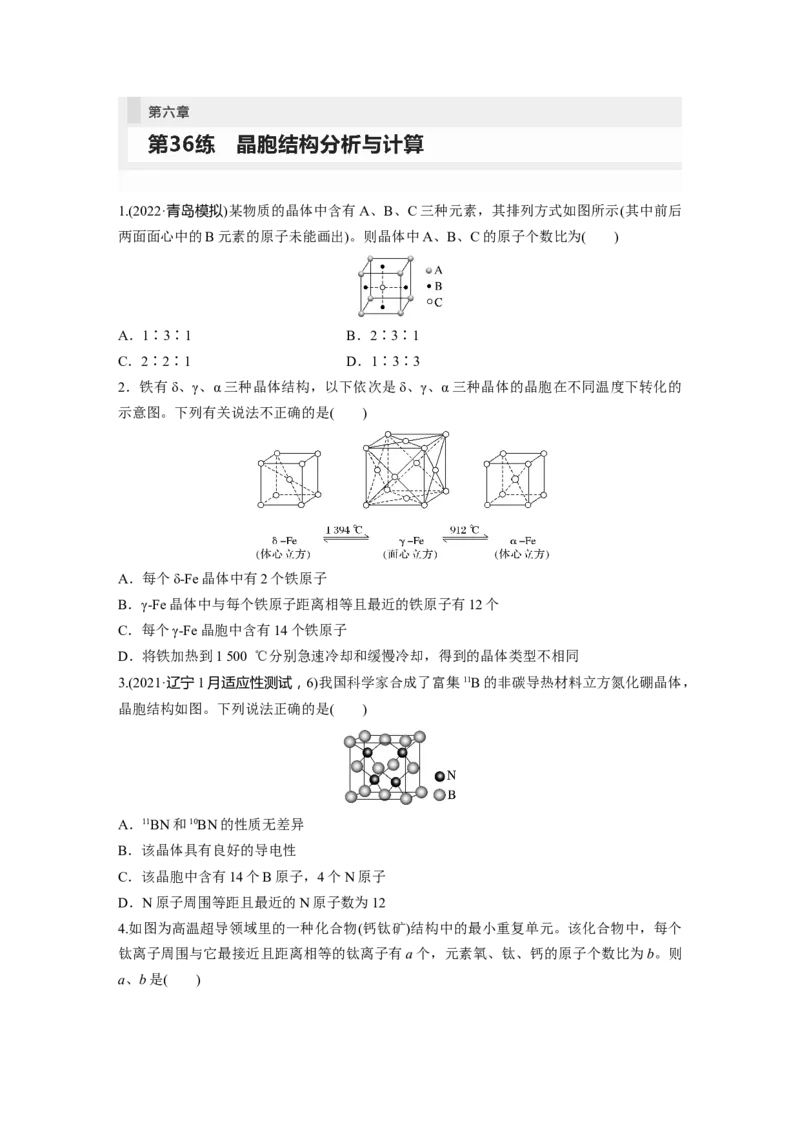
(2)Ni和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在我
国已实现了产业化。该合金的晶胞结构如图所示。
①该晶体的化学式为________。
②已知该合金的摩尔质量为M g·mol-1,密度为d g·cm-3,设N 为阿伏加德罗常数的值,
A
则该晶胞的体积是______________cm3(用含M、d、N 的代数式表示)。
A
(3)立方NiO(氧化镍)晶体的结构如图所示,其晶胞边长为 a pm,列式表示NiO晶体的密度
为________ g·cm-3(不必计算出结果,阿伏加德罗常数的值为N )。人工制备的NiO晶体中
A
常存在缺陷(如图)。一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代,其结果晶体仍呈电中
性,但化合物中Ni和O的比值却发生了变化。已知某氧化镍样品组成为Ni O,该晶体中
0.96
Ni3+与Ni2+的离子个数之比为________。