文档内容
第三章 金属及其化合物
测试卷
时间:75分钟 分值:100分
可能用到的相对原子质量:H 1 C 12 O16 Co 59
一、选择题(每小题只有一个正确选项,共15×3分)
1.(2024·重庆·模拟预测)下列实验操作产生的现象正确的是
A.将CO 通入苯酚钠溶液中,溶液出现浑浊
2
B.将少量Na放入CuSO 溶液中,出现红色沉淀
4
C.将蘸取NaCl溶液的铂丝在火焰上灼烧,火焰呈紫色
D.将葡萄糖溶液加入新制的Cu(OH) 悬浊液中,出现黑色沉淀
2
2.(2024·安徽·三模)化学与生活、生产密切相关。下列叙述不正确的是
A.裂化汽油、煤焦油、生物柴油的主要成分都是烷烃类
B.节日烟花呈现的是钠、钾、钡等金属元素的焰色试验,与电子跃迁有关
C. 在水处理过程中涉及:氧化还原反应、蛋白质变性、盐类水解、胶体聚沉
D.中国茶文化源远流长:治壶、投茶、出浴、淋壶、烫杯、酾茶、品茶……,泡茶过程涉及的操作有萃
取、过滤
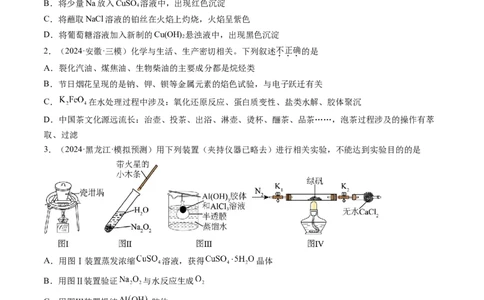
3.(2024·黑龙江·模拟预测)用下列装置(夹持仪器已略去)进行相关实验,不能达到实验目的的是
A.用图Ⅰ装置蒸发浓缩 溶液,获得 晶体
B.用图Ⅱ装置验证 与水反应生成
C.用图Ⅲ装置提纯 胶体
D.用图Ⅳ装置测定绿矾中结晶水的数目
4.(2024·陕西西安·二模)化学与生活、科技、环境密切相关,下列应用或事实不涉及氧化还原反应的是
A.植物油氢化制人造奶油
B.为减少污染,将煤气化或液化
C.常温下,用铁制容器盛装浓硝酸
D.用明矾作净水剂除去水中的悬浮杂质
5.(2024·海南·三模)物质的性质决定用途,下列前后对应关系正确的是A. 溶液显酸性,可除燃气中的
B. 溶液显碱性,可除废水中的
C.活性炭具有还原性,可吸附自来水中的悬浮物
D. 具有氧化性,可用于水的高效消毒杀菌
6.(2024·重庆涪陵·模拟预测)下列反应的离子方程式书写正确的是
A.将 固体投入 中:
B. 溶液中加入NaHS洛液:
C.向红色 溶液中加入过量铁粉至溶液红色褪去:
D.少量 通入苯酚钠溶液:2 2
7.(2024·黑龙江哈尔滨·三模)下列操作不能达到实验目的的是
A.用无水 检验甲苯中的少量水 B.用湿润的蓝色石蕊试纸检验
C.用 溶液检验水中是否含有苯酚 D.用 溶液检验 溶液是否变质
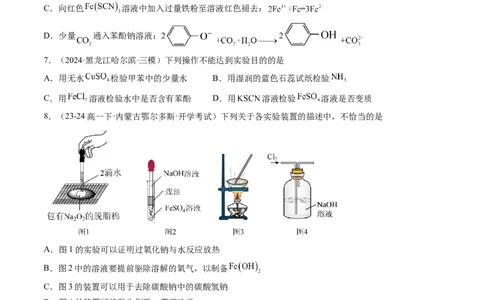
8.(23-24高一下·内蒙古鄂尔多斯·开学考试)下列关于各实验装置的描述中,不恰当的是
A.图1的实验可以证明过氧化钠与水反应放热
B.图2中的溶液要提前驱除溶解的氧气,以制备
C.图3的装置可以用于去除碳酸钠中的碳酸氢钠
D.图4的装置可能发生倒吸,需要改进
9.(2023·浙江绍兴·一模)硫酸铜是一种重要的盐,下列说法不正确的是
A.可用于泳池的消毒 B.可以用来检验酒精中是否含少量水
C.可以和石灰乳混合配制农药波尔多液 D.可以通过Cu与稀硫酸反应制备
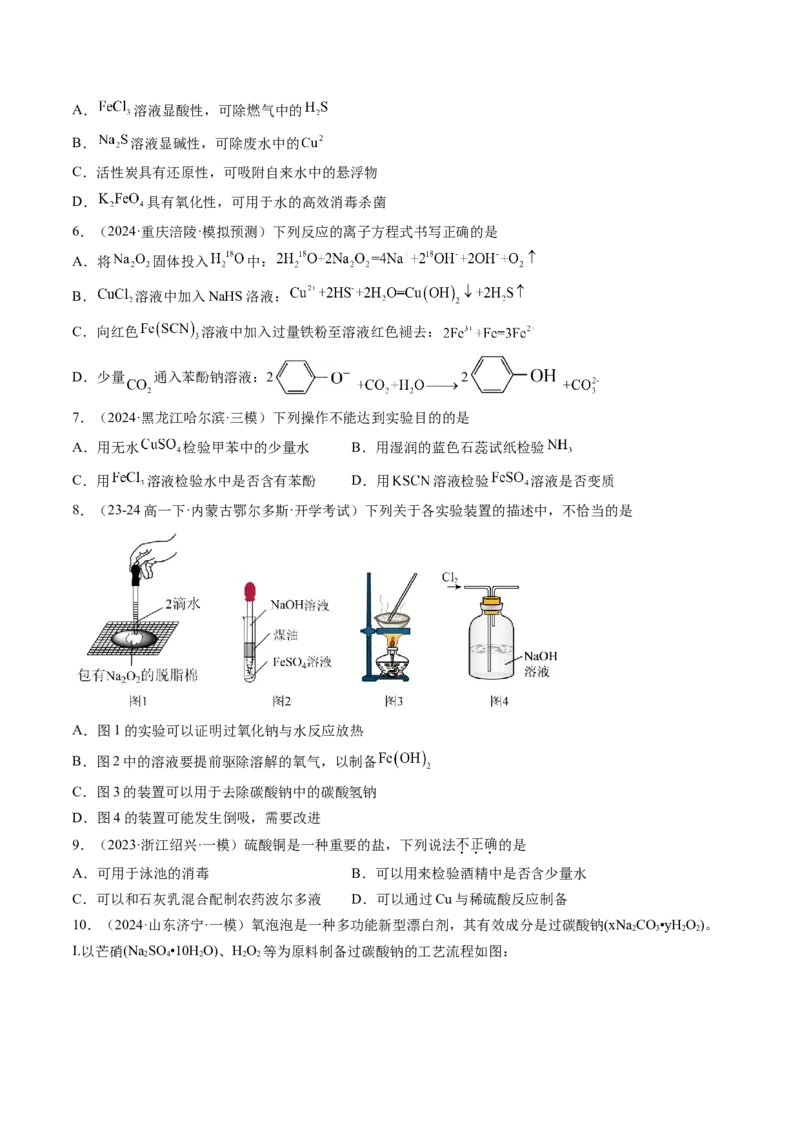
10.(2024·山东济宁·一模)氧泡泡是一种多功能新型漂白剂,其有效成分是过碳酸钠(xNa CO•yH O)。
2 3 2 2
I.以芒硝(Na SO •10H O)、HO 等为原料制备过碳酸钠的工艺流程如图:
2 4 2 2 2Ⅱ.测定过碳酸钠化学式的实验步骤如下(样品中杂质不参加反应):
①用电子天平称取两份质量均为mg的样品。
②将一份置于锥形瓶中,加水溶解,加催化剂使HO 充分快速分解(催化剂不参与其它反应),然后加酚酞
2 2
作指示剂,用0.0500mol•L-1HSO 溶液滴定至终点,消耗硫酸VmL。
2 4 1
③将另一份置于碘量瓶中,加入50mL蒸馏水,并立即加入6mL2.0mol•L-1HPO 溶液,再加入过量KI固
3 4
体,摇匀后于暗处放置10min,加入适量指示剂,用0.1000mol•L-1NaSO 标准溶液滴定至终点,消耗
2 2 3
NaSO 标准溶液VmL。(已知:2NaSO+I =Na SO+2NaI)
2 2 3 2 2 2 3 2 2 4 6
过碳酸钠制备的流程中,下列说法错误的是
A.步骤1中2mol芒硝参与反应时,消耗1molNa Cr O
2 2 7
B.滤渣的主要成分为CaSO
4
C.步骤2的方程式为2NaCrO+2CO +H O NaCr O+2NaHCO↓
2 4 2 2 2 2 7 3
D.稳定剂的作用是阻止微量杂质金属离子的催化作用,减少双氧水的分解
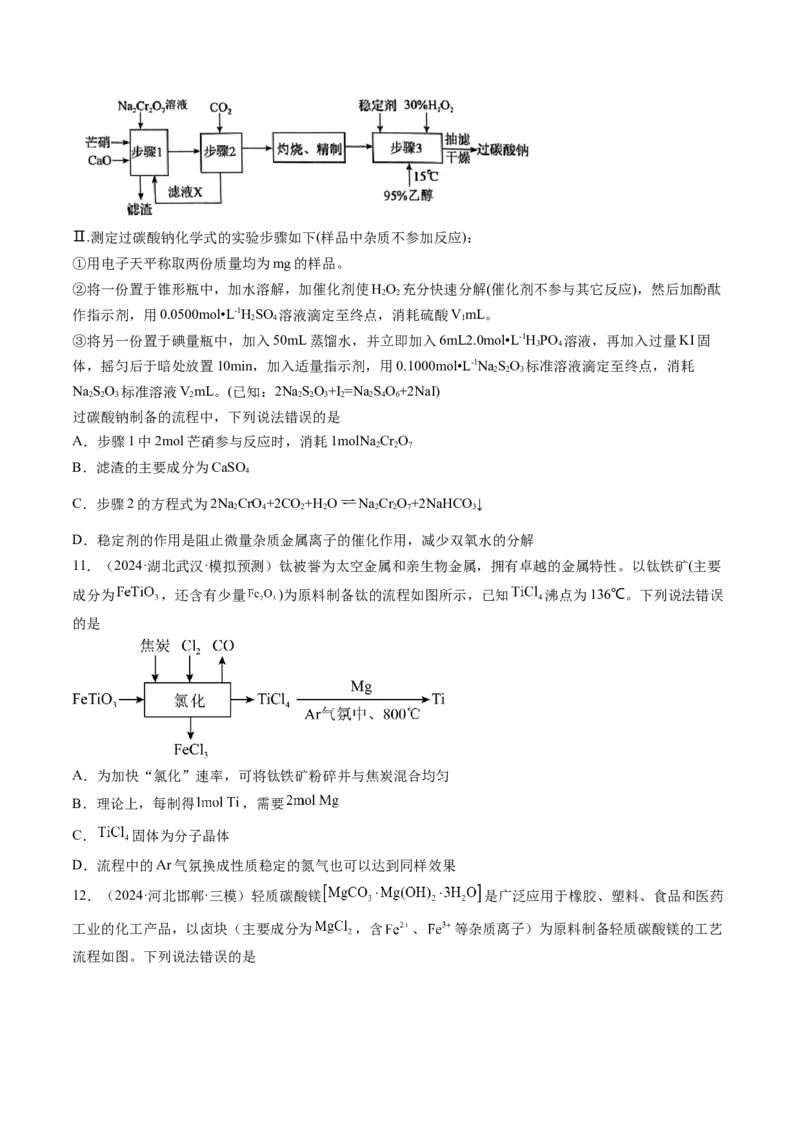
11.(2024·湖北武汉·模拟预测)钛被誉为太空金属和亲生物金属,拥有卓越的金属特性。以钛铁矿(主要
成分为 ,还含有少量 )为原料制备钛的流程如图所示,已知 沸点为136℃。下列说法错误
的是
A.为加快“氯化”速率,可将钛铁矿粉碎并与焦炭混合均匀
B.理论上,每制得 ,需要
C. 固体为分子晶体
D.流程中的Ar气氛换成性质稳定的氮气也可以达到同样效果
12.(2024·河北邯郸·三模)轻质碳酸镁 是广泛应用于橡胶、塑料、食品和医药
工业的化工产品,以卤块(主要成分为 ,含 、 等杂质离子)为原料制备轻质碳酸镁的工艺
流程如图。下列说法错误的是A.在实验室进行①操作所用的仪器为玻璃棒、烧杯
B.“氧化”工序中发生反应的离子方程式为
C.②和③工序名称均为“过滤”
D.“沉镁”工序控制合适的温度,产生的气体 主要为 和
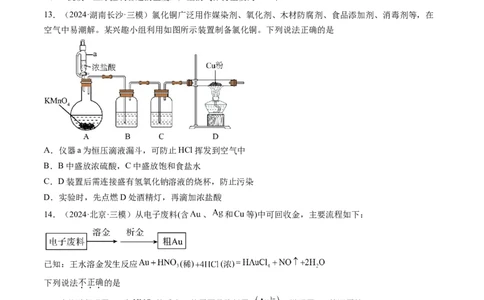
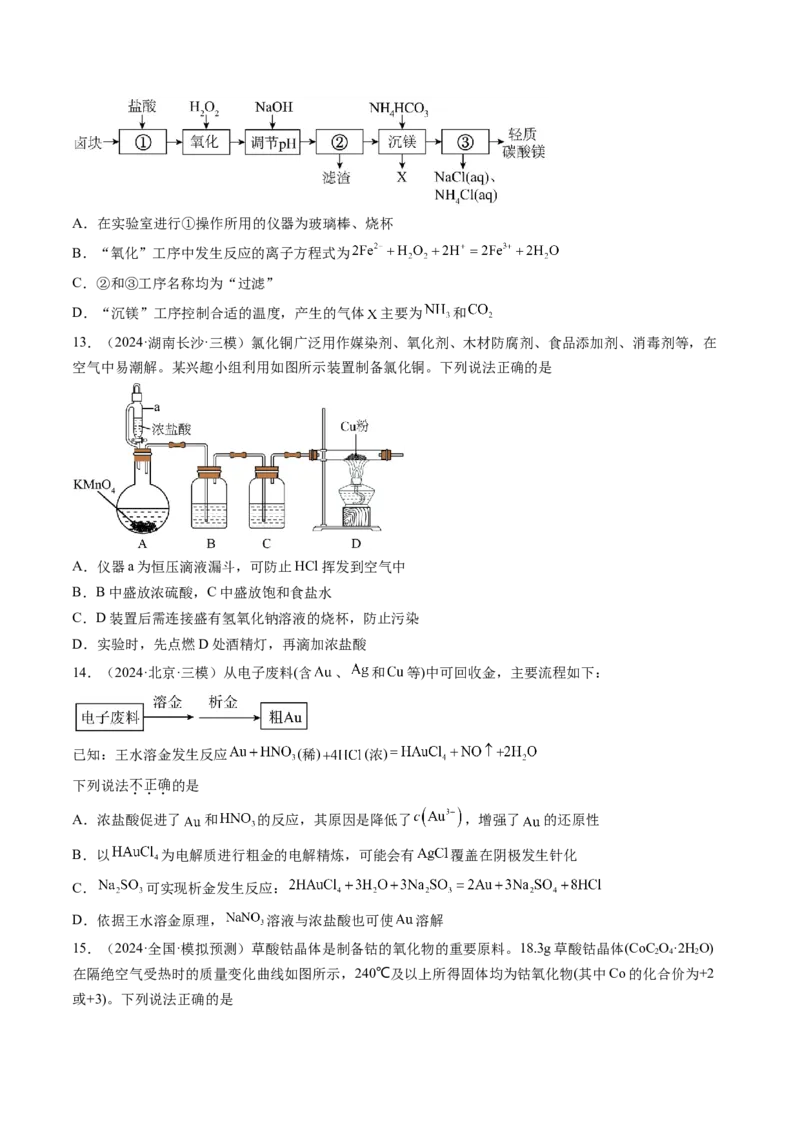
13.(2024·湖南长沙·三模)氯化铜广泛用作媒染剂、氧化剂、木材防腐剂、食品添加剂、消毒剂等,在
空气中易潮解。某兴趣小组利用如图所示装置制备氯化铜。下列说法正确的是
A.仪器a为恒压滴液漏斗,可防止HCl挥发到空气中
B.B中盛放浓硫酸,C中盛放饱和食盐水
C.D装置后需连接盛有氢氧化钠溶液的烧杯,防止污染
D.实验时,先点燃D处酒精灯,再滴加浓盐酸
14.(2024·北京·三模)从电子废料(含 、 和 等)中可回收金,主要流程如下:
已知:王水溶金发生反应 (稀) (浓)
下列说法不正确的是
A.浓盐酸促进了 和 的反应,其原因是降低了 ,增强了 的还原性
B.以 为电解质进行粗金的电解精炼,可能会有 覆盖在阴极发生针化
C. 可实现析金发生反应:
D.依据王水溶金原理, 溶液与浓盐酸也可使 溶解
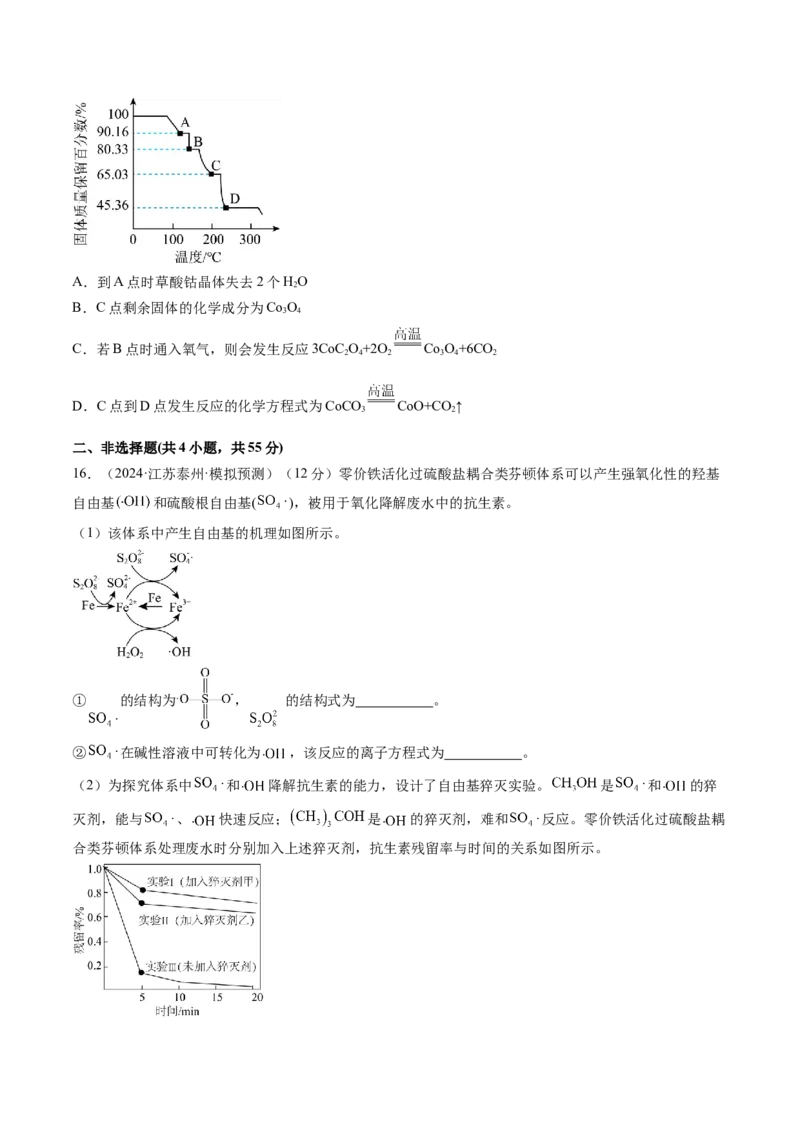
15.(2024·全国·模拟预测)草酸钴晶体是制备钴的氧化物的重要原料。18.3g草酸钴晶体(CoC O·2H O)
2 4 2
在隔绝空气受热时的质量变化曲线如图所示,240℃及以上所得固体均为钴氧化物(其中Co的化合价为+2
或+3)。下列说法正确的是A.到A点时草酸钴晶体失去2个HO
2
B.C点剩余固体的化学成分为Co O
3 4
C.若B点时通入氧气,则会发生反应3CoC O+2O Co O+6CO
2 4 2 3 4 2
D.C点到D点发生反应的化学方程式为CoCO CoO+CO↑
3 2
二、非选择题(共4小题,共55分)
16.(2024·江苏泰州·模拟预测)(12分)零价铁活化过硫酸盐耦合类芬顿体系可以产生强氧化性的羟基
自由基 和硫酸根自由基( ),被用于氧化降解废水中的抗生素。
(1)该体系中产生自由基的机理如图所示。
① 的结构为 , 的结构式为 。
② 在碱性溶液中可转化为 ,该反应的离子方程式为 。
(2)为探究体系中 和 降解抗生素的能力,设计了自由基猝灭实验。 是 和 的猝
灭剂,能与 、 快速反应; 是 的猝灭剂,难和 反应。零价铁活化过硫酸盐耦
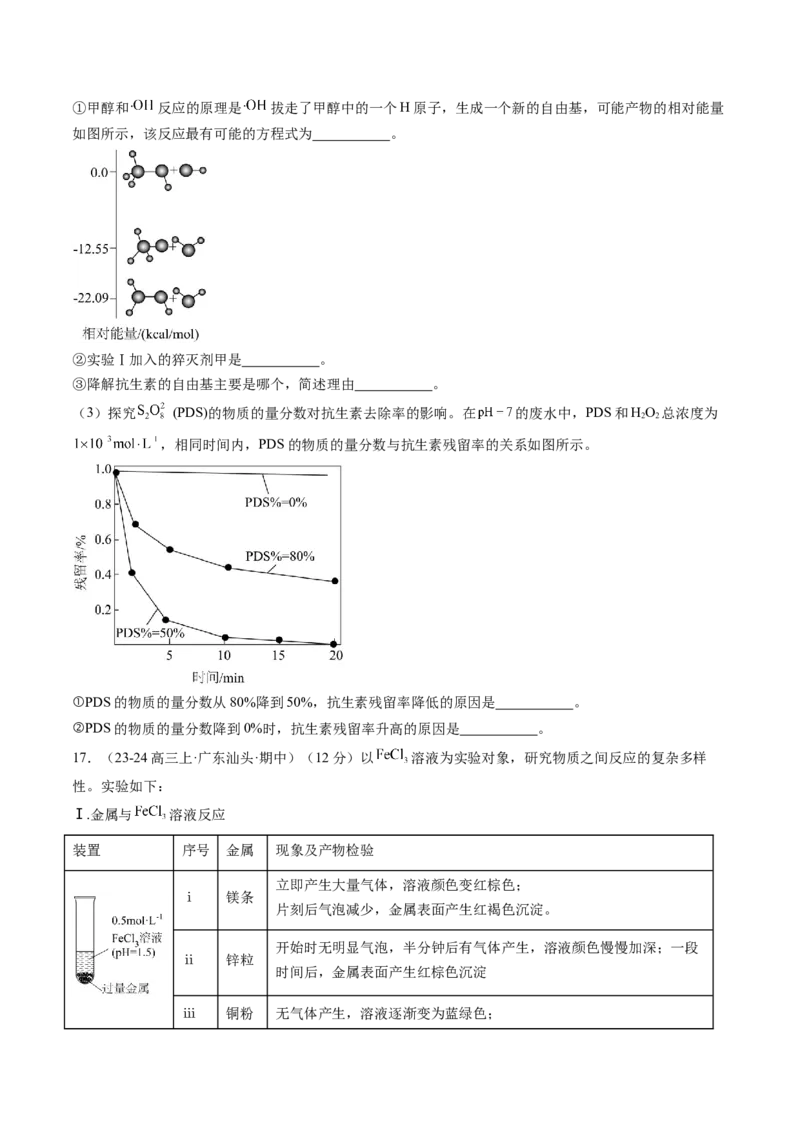
合类芬顿体系处理废水时分别加入上述猝灭剂,抗生素残留率与时间的关系如图所示。①甲醇和 反应的原理是 拔走了甲醇中的一个H原子,生成一个新的自由基,可能产物的相对能量
如图所示,该反应最有可能的方程式为 。
②实验Ⅰ加入的猝灭剂甲是 。
③降解抗生素的自由基主要是哪个,简述理由 。
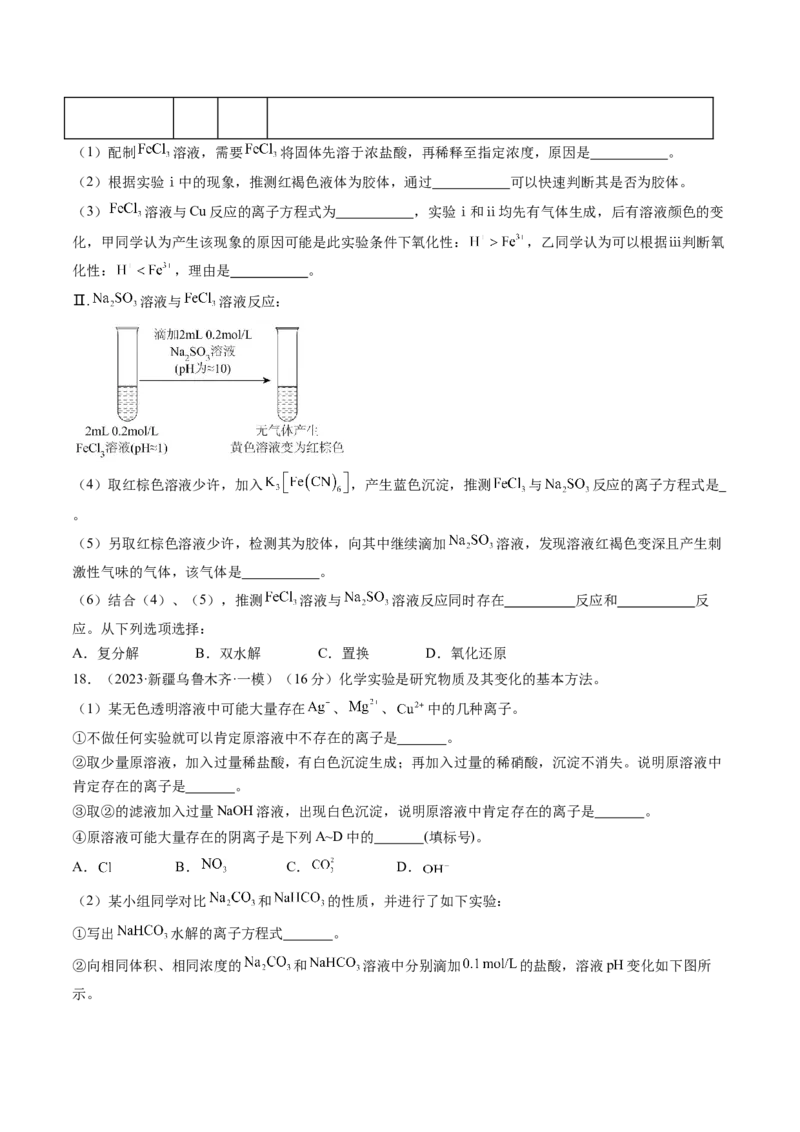
(3)探究 (PDS)的物质的量分数对抗生素去除率的影响。在 的废水中,PDS和HO 总浓度为
2 2
,相同时间内,PDS的物质的量分数与抗生素残留率的关系如图所示。
①PDS的物质的量分数从80%降到50%,抗生素残留率降低的原因是 。
②PDS的物质的量分数降到0%时,抗生素残留率升高的原因是 。
17.(23-24高三上·广东汕头·期中)(12分)以 溶液为实验对象,研究物质之间反应的复杂多样
性。实验如下:
Ⅰ.金属与 溶液反应
装置 序号 金属 现象及产物检验
立即产生大量气体,溶液颜色变红棕色;
ⅰ 镁条
片刻后气泡减少,金属表面产生红褐色沉淀。
开始时无明显气泡,半分钟后有气体产生,溶液颜色慢慢加深;一段
ⅱ 锌粒
时间后,金属表面产生红棕色沉淀
ⅲ 铜粉 无气体产生,溶液逐渐变为蓝绿色;(1)配制 溶液,需要 将固体先溶于浓盐酸,再稀释至指定浓度,原因是 。
(2)根据实验ⅰ中的现象,推测红褐色液体为胶体,通过 可以快速判断其是否为胶体。
(3) 溶液与Cu反应的离子方程式为 ,实验ⅰ和ⅱ均先有气体生成,后有溶液颜色的变
化,甲同学认为产生该现象的原因可能是此实验条件下氧化性: ,乙同学认为可以根据ⅲ判断氧
化性: ,理由是 。
Ⅱ. 溶液与 溶液反应:
(4)取红棕色溶液少许,加入 ,产生蓝色沉淀,推测 与 反应的离子方程式是
。
(5)另取红棕色溶液少许,检测其为胶体,向其中继续滴加 溶液,发现溶液红褐色变深且产生刺
激性气味的气体,该气体是 。
(6)结合(4)、(5),推测 溶液与 溶液反应同时存在 反应和 反
应。从下列选项选择:
A.复分解 B.双水解 C.置换 D.氧化还原
18.(2023·新疆乌鲁木齐·一模)(16分)化学实验是研究物质及其变化的基本方法。
(1)某无色透明溶液中可能大量存在 、 、 中的几种离子。
①不做任何实验就可以肯定原溶液中不存在的离子是 。
②取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中
肯定存在的离子是 。
③取②的滤液加入过量NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子是 。
④原溶液可能大量存在的阴离子是下列A~D中的 (填标号)。
A. B. C. D.
(2)某小组同学对比 和 的性质,并进行了如下实验:
①写出 水解的离子方程式 。
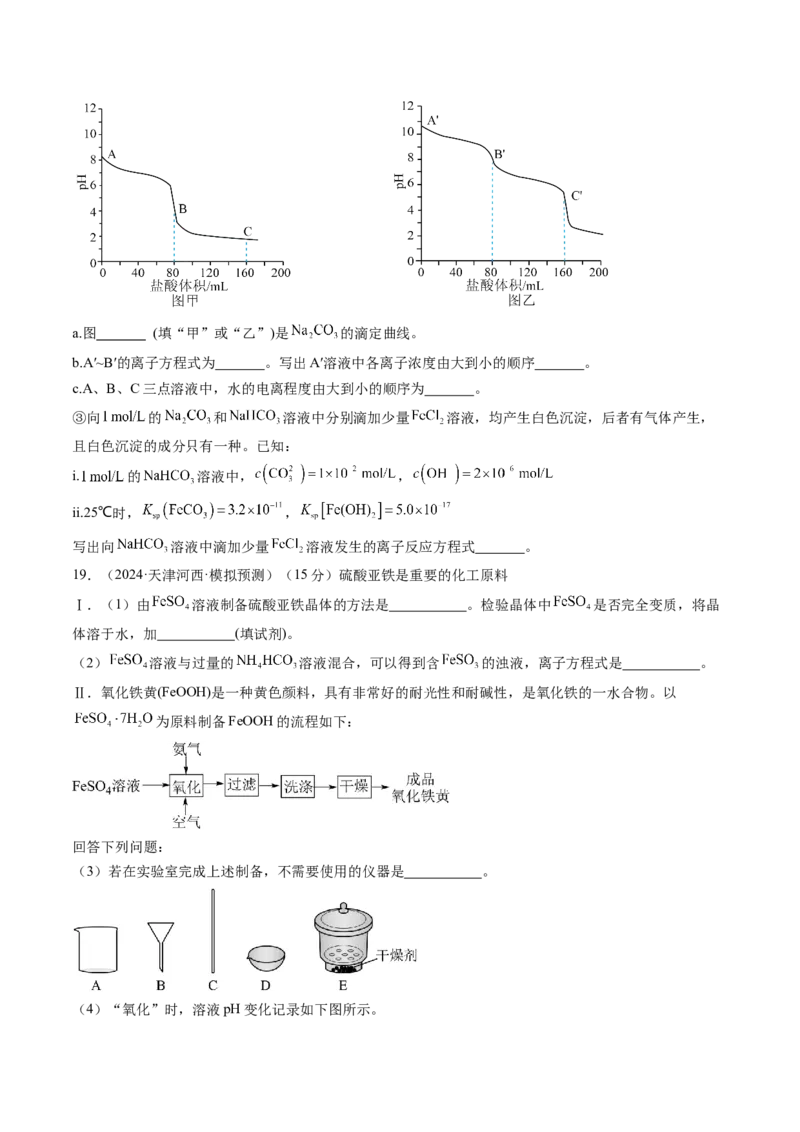
②向相同体积、相同浓度的 和 溶液中分别滴加 的盐酸,溶液pH变化如下图所
示。a.图 (填“甲”或“乙”)是 的滴定曲线。
b.A′~B′的离子方程式为 。写出A′溶液中各离子浓度由大到小的顺序 。
c.A、B、C三点溶液中,水的电离程度由大到小的顺序为 。
③向 的 和 溶液中分别滴加少量 溶液,均产生白色沉淀,后者有气体产生,
且白色沉淀的成分只有一种。已知:
i. 的 溶液中, ,
ii.25℃时, ,
写出向 溶液中滴加少量 溶液发生的离子反应方程式 。
19.(2024·天津河西·模拟预测)(15分)硫酸亚铁是重要的化工原料
Ⅰ.(1)由 溶液制备硫酸亚铁晶体的方法是 。检验晶体中 是否完全变质,将晶
体溶于水,加 (填试剂)。
(2) 溶液与过量的 溶液混合,可以得到含 的浊液,离子方程式是 。
Ⅱ.氧化铁黄(FeOOH)是一种黄色颜料,具有非常好的耐光性和耐碱性,是氧化铁的一水合物。以
为原料制备FeOOH的流程如下:
回答下列问题:
(3)若在实验室完成上述制备,不需要使用的仪器是 。
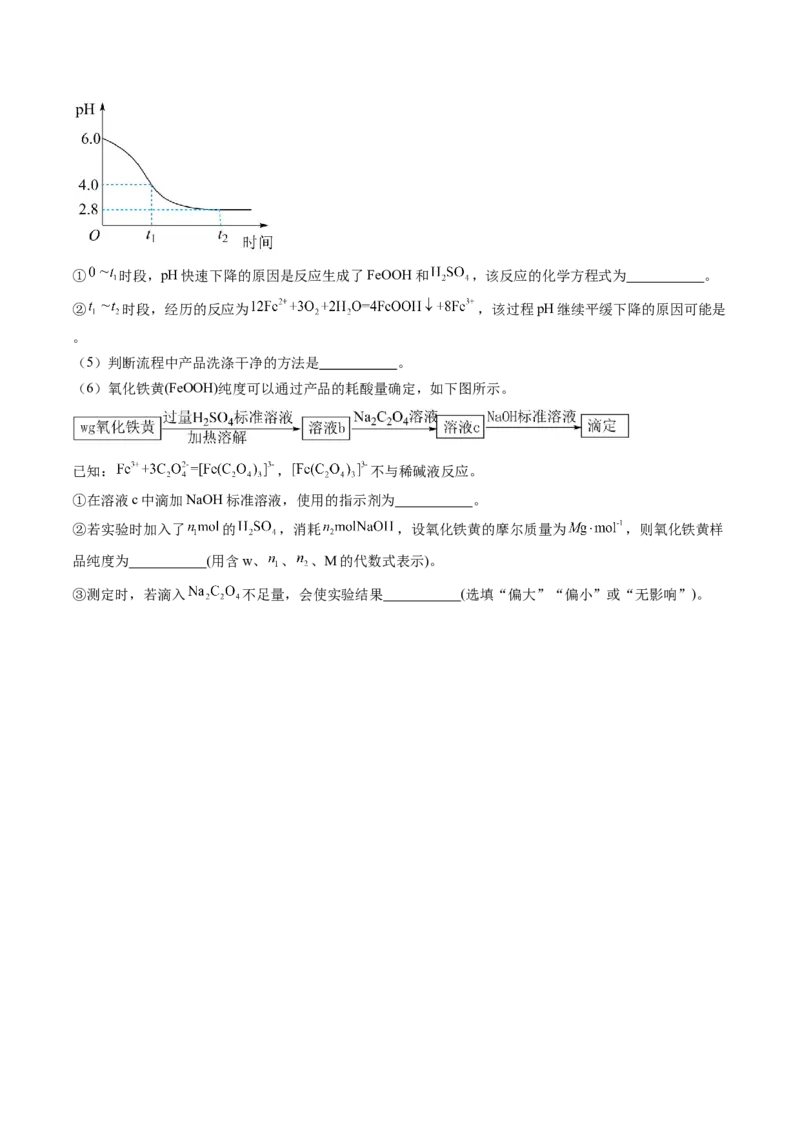
(4)“氧化”时,溶液pH变化记录如下图所示。① 时段,pH快速下降的原因是反应生成了FeOOH和 ,该反应的化学方程式为 。
② 时段,经历的反应为 ,该过程pH继续平缓下降的原因可能是
。
(5)判断流程中产品洗涤干净的方法是 。
(6)氧化铁黄(FeOOH)纯度可以通过产品的耗酸量确定,如下图所示。
已知: , 不与稀碱液反应。
①在溶液c中滴加NaOH标准溶液,使用的指示剂为 。
②若实验时加入了 的 ,消耗 ,设氧化铁黄的摩尔质量为 ,则氧化铁黄样
品纯度为 (用含w、 、 、M的代数式表示)。
③测定时,若滴入 不足量,会使实验结果 (选填“偏大”“偏小”或“无影响”)。