文档内容
考点 30 水的电离和溶液的酸碱性
目录
.............................................................................................................................................1
1.高考真题考点分布...................................................................................................................................1
2.命题规律及备考策略...............................................................................................................................1
.............................................................................................................................................2
考法01 水的电离与水的离子积常数.......................................................................................................2
考法02 溶液的酸碱性与pH......................................................................................................................4
考法03 酸碱中和滴定.............................................................................................................................10
...........................................................................................................................................12
1.高考真题考点分布
考点内容 考点分布
水的电离和溶液的 2024·安徽卷7题,3分;2024·安徽卷7题,3分;2024·山东卷10题,2分;2022·
酸碱性 浙江卷,2分;2022·浙江卷17题,2分
2023湖南卷12题,4分;2021辽宁卷15题,3分;2021湖北卷14题,3分;2021
酸碱中和滴定
海南卷14题,4分;
2.命题规律及备考策略
【命题规律】
高频考点从近几年全国高考试题来看,考查溶液的酸碱性判断、pH的计算,以及离子浓度的大小比较仍是
高考命题的热点。
【备考策略】
【命题预测】
预计2025年高考会以新的情境载体考查有关溶液的pH的计算、离子浓度的大小比较、酸碱滴定等知识,
题目难度一般较大。考法01 水的电离与水的离子积常数
1.水的电离
(1)水的电离方程式为 或HO H++OH-。
2
(2)25 ℃时,纯水中c(H+)=c(OH-)= 。任何水溶液中,由水电离出来的c(H+)与c(OH-)
都相等。
2.水的离子积常数
(1)水的离子积常数:K = 。
w
(2)影响因素:只与 有关,升高温度,K 。
w
(3)适用范围:K 不仅适用于纯水,也适用于酸、碱、盐的稀溶液。
w
(4)意义:K 揭示了在任何水溶液中均存在H+和OH-,只要 不变,K 不变。
w w
【易错提醒】
相同温度下,不论是纯水还是稀溶液,水的离子积常数不变。
3.影响水电离平衡的因素
(1)升高温度,水的电离程度 ,K 。
w
(2)加入酸或碱,水的电离程度均 ,K 。
w
(3)加入可水解的盐(如FeCl 、NaCO),水的电离程度 ,K 。
3 2 3 w
4.填写外界条件对HO H++OH- ΔH>0的具体影响
2
体系变化
移动方向 K 电离程度 c(OH-) c(H+)
W
条件
HCl
NaOH
可水解
的盐
温度
其他:如加入Na
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)温度一定时,水的电离常数与水的离子积常数相等( )
(2)100 ℃的纯水中c(H+)=1×10-6 mol·L-1,此时水呈酸性( )
(3)NaCl溶液和CHCOONH 溶液均显中性,两溶液中水的电离程度相同( )
3 4
(4)室温下,0.1 mol·L-1的HCl溶液与0.1 mol·L-1的NaOH溶液中水的电离程度相等( )
(5)任何水溶液中均存在H+和OH-,且水电离出的c(H+)和c(OH-)相等( )(6)在蒸馏水中滴加浓HSO ,K 不变。( )
2 4 W
(7)25 ℃与60 ℃时,水的pH相等。( )
(8)25 ℃时NH Cl溶液的K 小于100 ℃时NaCl溶液的K 。( )
4 W W
考向01 考查水的电离及其计算
【例1】(2024·福建泉州·一模)常温时,纯水中由水电离出的c(H+)=a mol·L-1,pH=1的盐酸中由水电
离出的c(H+)=b mol·L-1,0.1 mol·L-1的盐酸与0.1 mol·L-1的氨水等体积混合后,由水电离出的c(H+)=c
mol·L-1,则a、b、c的关系正确的是( )
A.a>b=c B.c>a>b
C.c>b>a D.b>c>a
【思维建模】
25 ℃时,由水电离出的c (H+)或c (OH-)的5种类型的计算方法
水 水
1.中性溶液:c (H+)=c (OH-)=1.0×10-7 mol/L
水 水
2.酸的溶液:H+来源于酸电离和水电离,而OH-只来源于水,故有c (OH-)=c (H+)=c (OH-)。
水 水 溶液
3.碱的溶液:OH-来源于碱电离和水电离,而H+只来源于水,故有c (H+)=c (OH-)=c (H+)。
水 水 溶液
4.水解呈酸性的盐溶液:c (H+)=c (H+)。
水 溶液
5.水解呈碱性的盐溶液:c (OH-)=c (OH-)。
水 溶液
考向02 考查水的电离影响因素
【例2】(2024·湖北荆门·一模)一定温度下,水存在HO H++OH- ΔH>0的平衡,下列叙述一定正
2
确的是( )
A.向水中滴入少量稀盐酸,平衡逆向移动,K 减小
W
B.将水加热,K 增大,pH减小
W
C.向水中加入少量固体CHCOONa,平衡逆向移动,c(H+) 降低
3
D.向水中加入少量固体硫酸钠,c(H+)=10-7 mol·L-1,K 不变
W
【思维建模】
(1)酸、碱抑制水的电离,酸溶液中求c(OH-),即c(H+)H O=c(OH-)H O=c(OH-),碱溶液中求c(H+),即
2 2
c(OH-)H O=c(H+)H O=c(H+)。
2 2
(2)水解的盐促进水的电离,故c(H+)H O等于显性离子的浓度。
2
(3)酸式盐溶液
酸式酸根以电离为主:c(H+)H O=c(OH-)H O=c(OH-)。
2 2
酸式酸根以水解为主:c(H+)H O=c(OH-)H O=c(OH-)。
2 2
考向03 考查水的电离平衡曲线
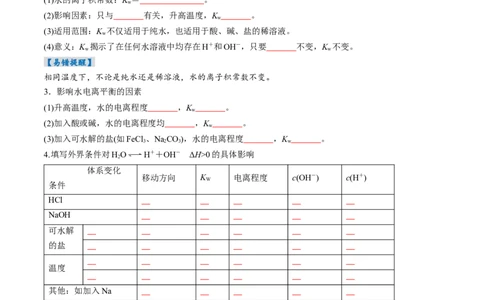
【例3】(2024·吉林四平·模拟)一定温度下,水溶液中H+和OH-的浓度变化曲线如图。下列说法正确的
是( )A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10-13
C.该温度下,加入FeCl 可能引起由b向a的变化
3
D.该温度下,稀释溶液可能引起由c向d的变化
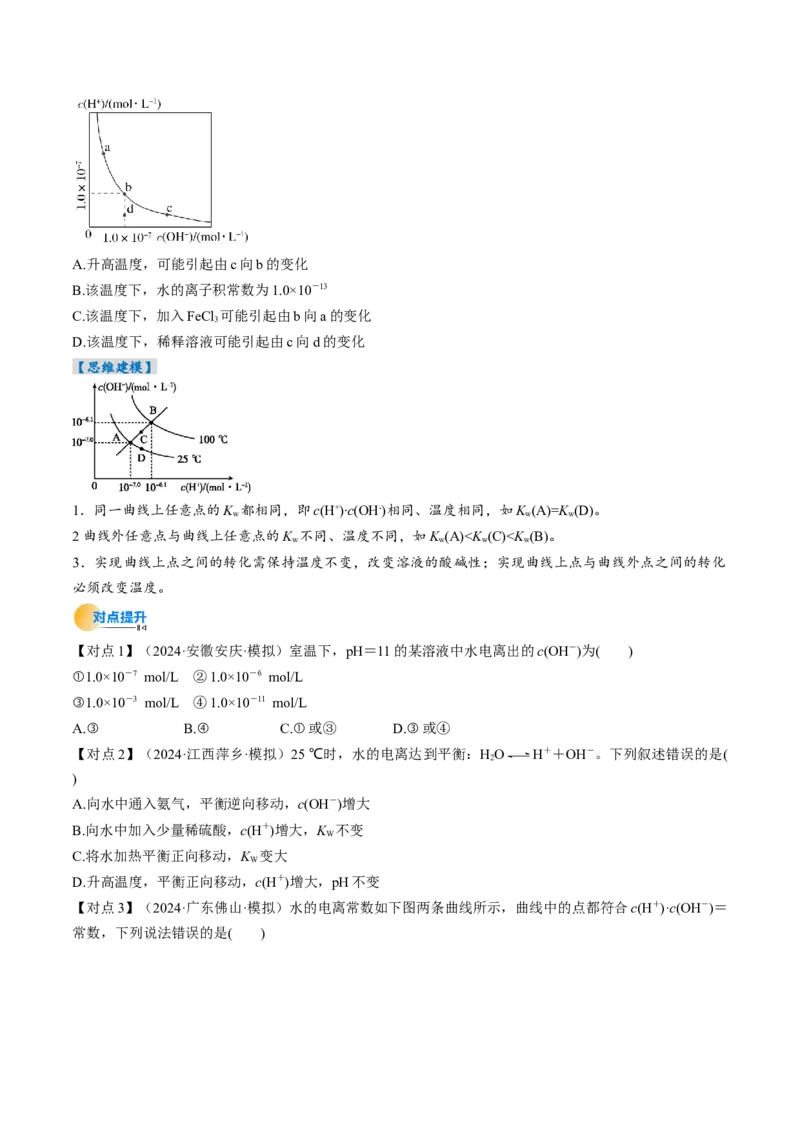
【思维建模】
1.同一曲线上任意点的K 都相同,即c(H+)·c(OH-)相同、温度相同,如K (A)=K (D)。
w w w
2曲线外任意点与曲线上任意点的K 不同、温度不同,如K (A)T
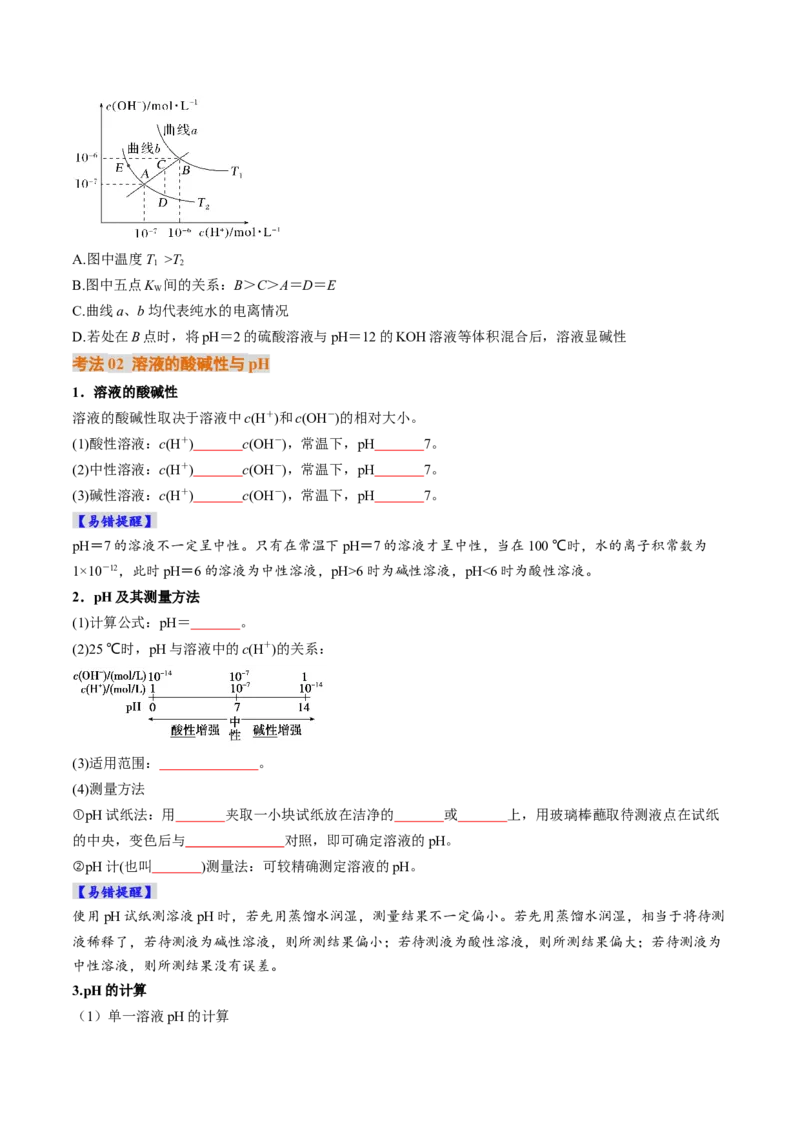
1 2
B.图中五点K 间的关系:B>C>A=D=E
W
C.曲线a、b均代表纯水的电离情况
D.若处在B点时,将pH=2的硫酸溶液与pH=12的KOH溶液等体积混合后,溶液显碱性
考法02 溶液的酸碱性与pH
1.溶液的酸碱性
溶液的酸碱性取决于溶液中c(H+)和c(OH-)的相对大小。
(1)酸性溶液:c(H+) c(OH-),常温下,pH 7。
(2)中性溶液:c(H+) c(OH-),常温下,pH 7。
(3)碱性溶液:c(H+) c(OH-),常温下,pH 7。
【易错提醒】
pH=7的溶液不一定呈中性。只有在常温下pH=7的溶液才呈中性,当在100 ℃时,水的离子积常数为
1×10-12,此时pH=6的溶液为中性溶液,pH>6时为碱性溶液,pH<6时为酸性溶液。
2.pH及其测量方法
(1)计算公式:pH= 。
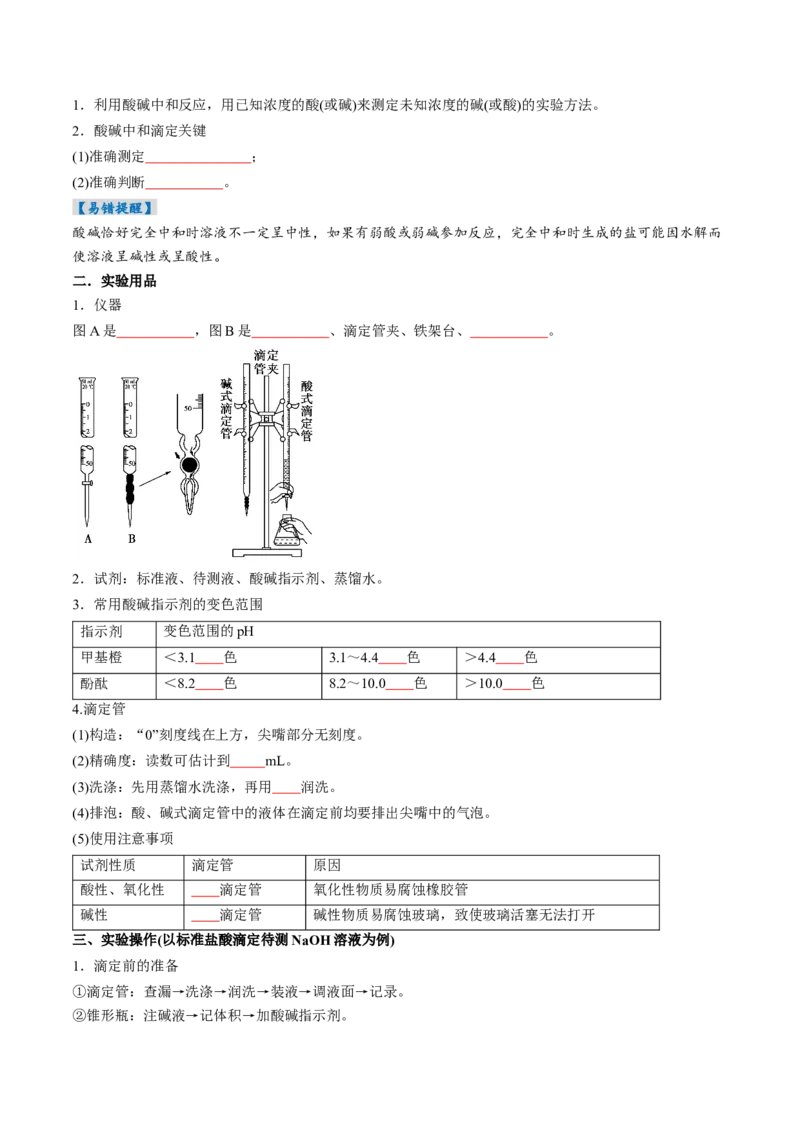
(2)25 ℃时,pH与溶液中的c(H+)的关系:
(3)适用范围: 。
(4)测量方法
①pH试纸法:用 夹取一小块试纸放在洁净的 或 上,用玻璃棒蘸取待测液点在试纸
的中央,变色后与 对照,即可确定溶液的pH。
②pH计(也叫 )测量法:可较精确测定溶液的pH。
【易错提醒】
使用pH试纸测溶液pH时,若先用蒸馏水润湿,测量结果不一定偏小。若先用蒸馏水润湿,相当于将待测
液稀释了,若待测液为碱性溶液,则所测结果偏小;若待测液为酸性溶液,则所测结果偏大;若待测液为
中性溶液,则所测结果没有误差。
3.pH的计算
(1)单一溶液pH的计算强酸溶液:如HA,设浓度为c mol·L-1,c(H+)=nc mol·L-1,pH=-lg c(H+)=-lg (nc)。
n
强碱溶液(25 ℃):如B(OH) ,设浓度为c mol·L-1,c(H+)= mol·L-1,pH=-lg c(H+)=14+lg (nc)。
n
(2)混合溶液pH的计算类型
两种强酸混合:直接求出c(H+) ,再据此求pH。c(H+) =。
混 混
两种强碱混合:先求出c(OH-) ,再根据K 求出c(H+) ,最后求pH。c(OH-) =。
混 w 混 混
强酸、强碱混合:先判断哪种物质过量,再由下式求出溶液中H+或OH-的浓度,最后求pH。c(H+) 或
混
c(OH-) =。
混
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)任何温度下,利用H+和OH-浓度的相对大小均可判断溶液的酸碱性( )
(2)某溶液的c(H+)>10-7mol·L-1,则该溶液呈酸性( )
(3)pH减小,溶液的酸性一定增强( )
(4)100 ℃时,K =1.0×10-12,0.01 mol·L-1盐酸的pH=2,0.01 mol·L-1的NaOH溶液的pH=10( )
w
(5)用蒸馏水润湿的pH试纸测溶液的pH,一定会使结果偏低( )
(6)用广泛pH试纸测得某溶液的pH为3.4( )
考向01 考查溶液的酸碱性与pH
【例1】(2024·山东淄博·一模)下列说法不正确的是( )
A.pH>7的溶液不一定呈碱性
B.中和pH和体积均相等的氨水、NaOH溶液,所需HCl的物质的量相同
C.相同温度下,pH相等的盐酸、CHCOOH溶液中,c(OH-)相等
3
D.氨水和盐酸反应后的溶液,若溶液呈中性,则c(Cl-)=c(NH)
考向02 考查溶液的稀释与pH
【例2】(2024·广东汕尾·模拟)常温下,关于溶液稀释的说法正确的是( )
A.将1 L 0.1 mol·L-1的Ba(OH) 溶液加水到体积为2 L,pH=13
2
B.pH=3的醋酸溶液加水稀释到原浓度的,pH=5
C.pH=4的HSO 溶液加水稀释到原浓度的,溶液中由水电离产生的c(H+)=1×10-6 mol·L-1
2 4
D.pH=8的NaOH溶液加水稀释到原浓度的,其pH=6
【思维建模】稀释酸、碱溶液时pH变化规律
酸(pH=a) 碱(pH=b)
弱酸 强酸 弱碱 强碱
稀释10n倍 <a+n a+n >b-n b-n
无限稀释 pH趋向于7
考向03 考查pH的计算
【例3】(2024·四川宜宾·模拟)在T ℃时,某NaOH稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-bmol·L-1,已知a+b=12。向该溶液中逐滴加入pH=c的盐酸(T ℃),测得混合溶液的部分pH如下表所示:
序号 NaOH溶液体积 盐酸体积 溶液pH
① 20.00 0.00 8
② 20.00 20.00 6
假设溶液混合前后的体积变化忽略不计,则c为( )
A.1 B.4 C.5 D.6
【思维建模】溶液pH计算的一般思维模型
【对点1】(2024·四川宜宾·模拟)下列溶液一定呈中性的是( )
A.c(H+)=c(OH-)=10-6mol·L-1的溶液
B.使石蕊试液呈紫色的溶液
C.pH=7的溶液
D.酸与碱恰好完全反应生成的溶液
【对点2】(2024·湖北咸宁·模拟)下列说法不正确的是( )
A.0.1 mol·L-1氨水的pH=a,将此溶液稀释1倍后,溶液pH=b,则a>b
B.常温下1 mL pH=13的NaOH溶液与100 mL盐酸混合后溶液pH=7,则盐酸的pH=3
C.纯水加热到100 ℃时,水的离子积变大、pH变小、呈中性
D.相同温度下,pH相同的NaCO 和NaSO 溶液中,水电离程度较大的是NaCO 溶液
2 3 2 3 2 3
【对点3】(2024·江苏南京·模拟)现有室温下四种溶液,有关叙述不正确的是( )
序号 ① ② ③ ④
pH 11 11 3 3
溶液 氨水 氢氧化钠溶液 醋酸 盐酸
A.③④中分别加入适量的醋酸钠晶体后,两溶液的pH均增大
B.②③两溶液等体积混合,所得溶液中c(H+)>c(OH-)
C.分别加水稀释10倍,四种溶液的pH:①>②>④>③
D.V L ④与V L ①混合,若混合后溶液pH=7,则V<V
1 2 1 2
考法03 酸碱中和滴定
一.实验原理1.利用酸碱中和反应,用已知浓度的酸(或碱)来测定未知浓度的碱(或酸)的实验方法。
2.酸碱中和滴定关键
(1)准确测定 ;
(2)准确判断 。
【易错提醒】
酸碱恰好完全中和时溶液不一定呈中性,如果有弱酸或弱碱参加反应,完全中和时生成的盐可能因水解而
使溶液呈碱性或呈酸性。
二.实验用品
1.仪器
图A是 ,图B是 、滴定管夹、铁架台、 。
2.试剂:标准液、待测液、酸碱指示剂、蒸馏水。
3.常用酸碱指示剂的变色范围
指示剂 变色范围的pH
甲基橙 <3.1 色 3.1~4.4 色 >4.4 色
酚酞 <8.2 色 8.2~10.0 色 >10.0 色
4.滴定管
(1)构造:“0”刻度线在上方,尖嘴部分无刻度。
(2)精确度:读数可估计到 mL。
(3)洗涤:先用蒸馏水洗涤,再用 润洗。
(4)排泡:酸、碱式滴定管中的液体在滴定前均要排出尖嘴中的气泡。
(5)使用注意事项
试剂性质 滴定管 原因
酸性、氧化性 滴定管 氧化性物质易腐蚀橡胶管
碱性 滴定管 碱性物质易腐蚀玻璃,致使玻璃活塞无法打开
三、实验操作(以标准盐酸滴定待测NaOH溶液为例)
1.滴定前的准备
①滴定管:查漏→洗涤→润洗→装液→调液面→记录。
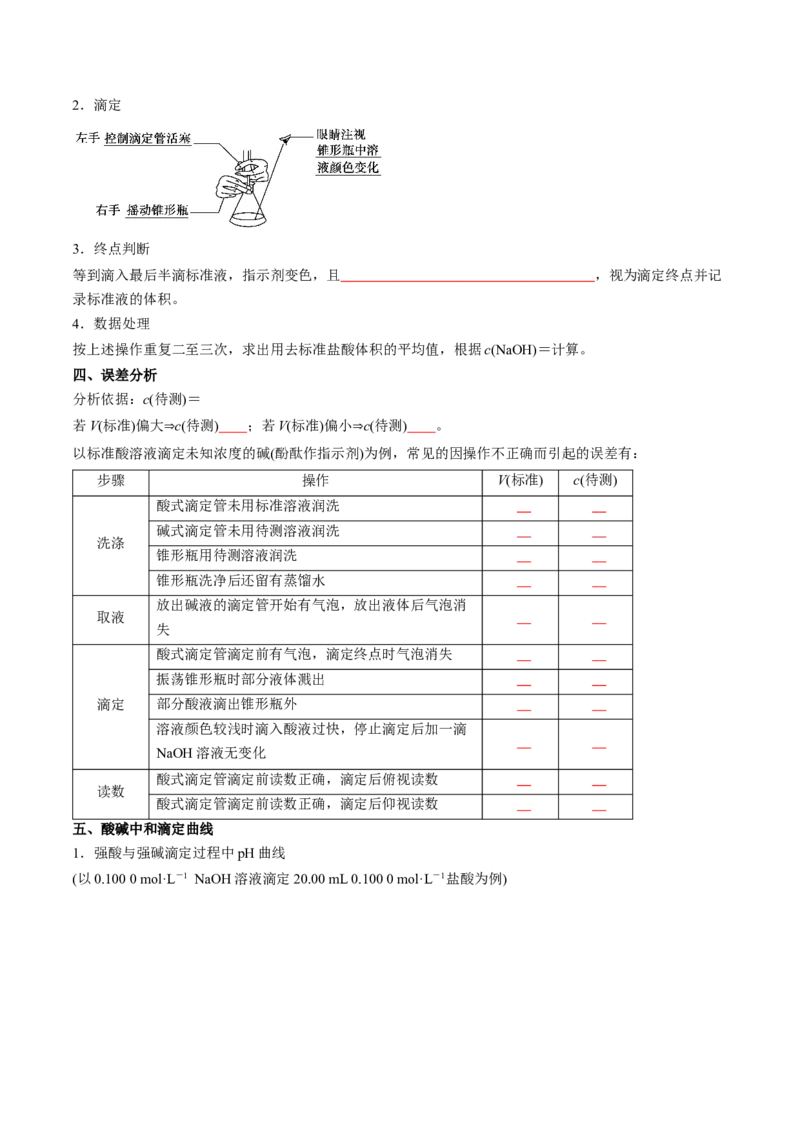
②锥形瓶:注碱液→记体积→加酸碱指示剂。2.滴定
3.终点判断
等到滴入最后半滴标准液,指示剂变色,且 ,视为滴定终点并记
录标准液的体积。
4.数据处理
按上述操作重复二至三次,求出用去标准盐酸体积的平均值,根据c(NaOH)=计算。
四、误差分析
分析依据:c(待测)=
若V(标准)偏大⇒c(待测) ;若V(标准)偏小⇒c(待测) 。
以标准酸溶液滴定未知浓度的碱(酚酞作指示剂)为例,常见的因操作不正确而引起的误差有:
步骤 操作 V(标准) c(待测)
酸式滴定管未用标准溶液润洗
碱式滴定管未用待测溶液润洗
洗涤
锥形瓶用待测溶液润洗
锥形瓶洗净后还留有蒸馏水
放出碱液的滴定管开始有气泡,放出液体后气泡消
取液
失
酸式滴定管滴定前有气泡,滴定终点时气泡消失
振荡锥形瓶时部分液体溅出
滴定 部分酸液滴出锥形瓶外
溶液颜色较浅时滴入酸液过快,停止滴定后加一滴
NaOH溶液无变化
酸式滴定管滴定前读数正确,滴定后俯视读数
读数
酸式滴定管滴定前读数正确,滴定后仰视读数
五、酸碱中和滴定曲线
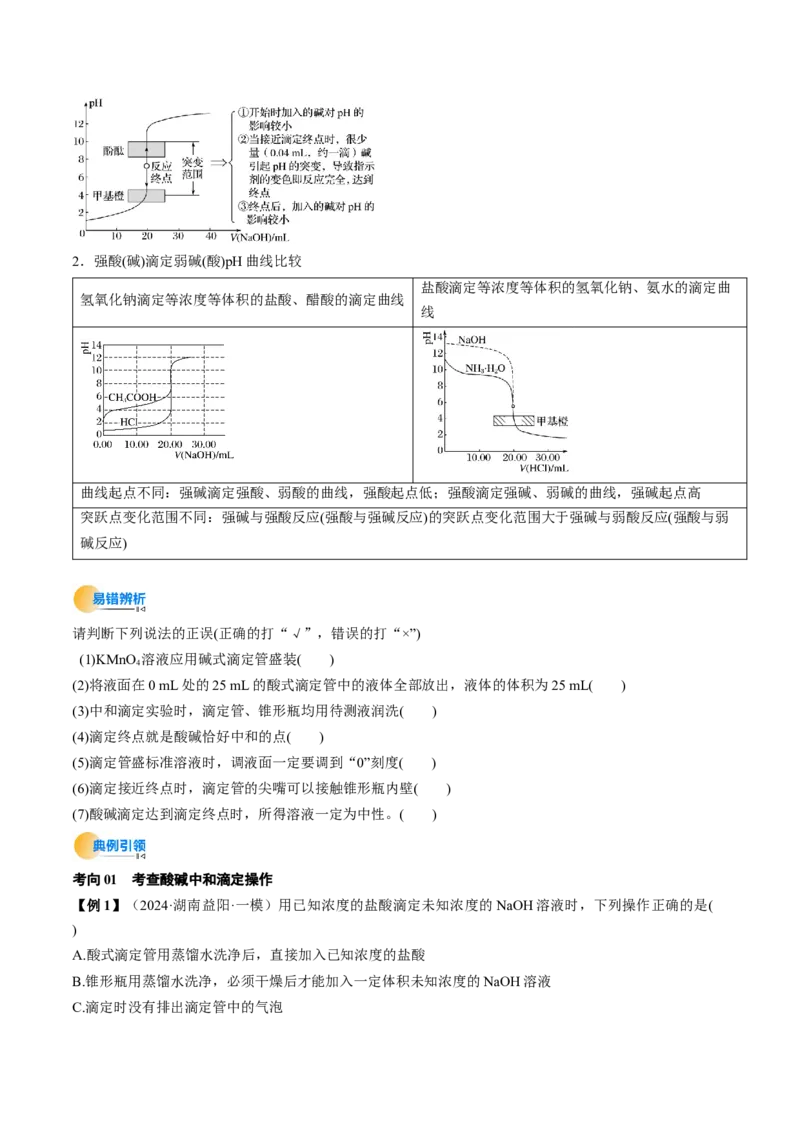
1.强酸与强碱滴定过程中pH曲线
(以0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1盐酸为例)2.强酸(碱)滴定弱碱(酸)pH曲线比较
盐酸滴定等浓度等体积的氢氧化钠、氨水的滴定曲
氢氧化钠滴定等浓度等体积的盐酸、醋酸的滴定曲线
线
曲线起点不同:强碱滴定强酸、弱酸的曲线,强酸起点低;强酸滴定强碱、弱碱的曲线,强碱起点高
突跃点变化范围不同:强碱与强酸反应(强酸与强碱反应)的突跃点变化范围大于强碱与弱酸反应(强酸与弱
碱反应)
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)KMnO 溶液应用碱式滴定管盛装( )
4
(2)将液面在0 mL处的25 mL的酸式滴定管中的液体全部放出,液体的体积为25 mL( )
(3)中和滴定实验时,滴定管、锥形瓶均用待测液润洗( )
(4)滴定终点就是酸碱恰好中和的点( )
(5)滴定管盛标准溶液时,调液面一定要调到“0”刻度( )
(6)滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁( )
(7)酸碱滴定达到滴定终点时,所得溶液一定为中性。( )
考向01 考查酸碱中和滴定操作
【例1】(2024·湖南益阳·一模)用已知浓度的盐酸滴定未知浓度的NaOH溶液时,下列操作正确的是(
)
A.酸式滴定管用蒸馏水洗净后,直接加入已知浓度的盐酸
B.锥形瓶用蒸馏水洗净,必须干燥后才能加入一定体积未知浓度的NaOH溶液
C.滴定时没有排出滴定管中的气泡D.读数时视线与滴定管内液体凹液面保持水平
考向02 考查酸碱中和滴定图像
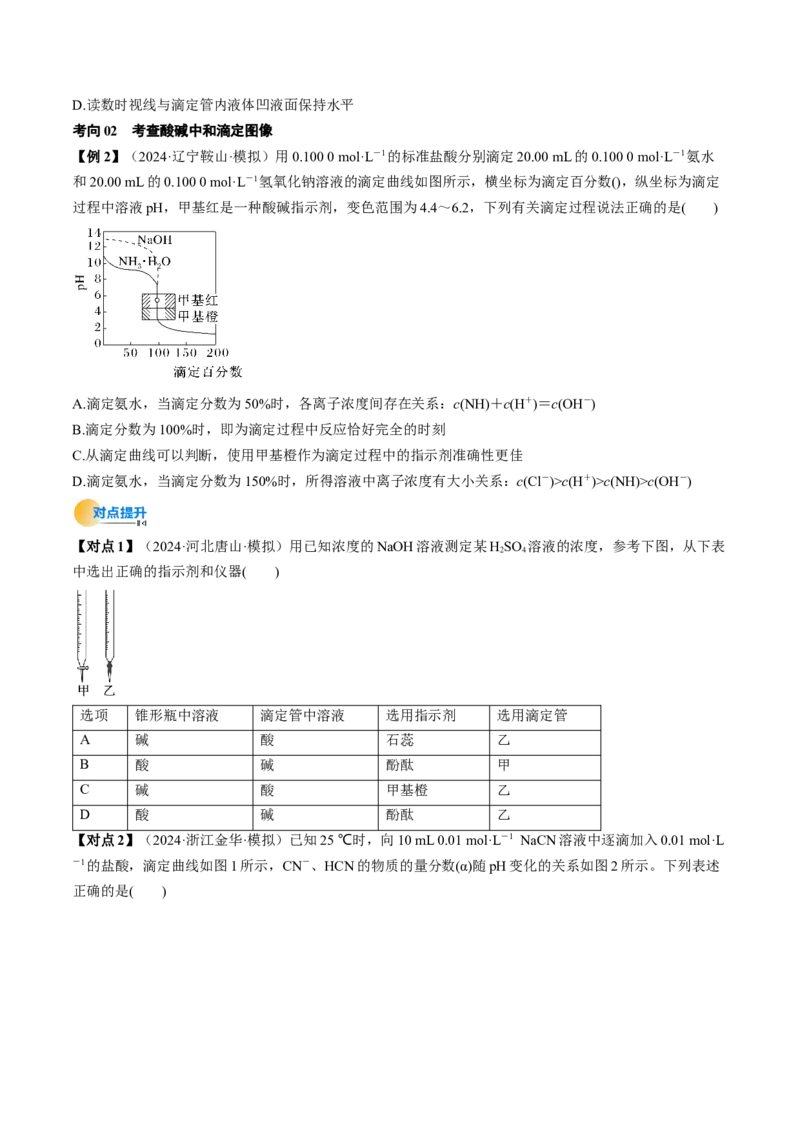
【例2】(2024·辽宁鞍山·模拟)用0.100 0 mol·L-1的标准盐酸分别滴定20.00 mL的0.100 0 mol·L-1氨水
和20.00 mL的0.100 0 mol·L-1氢氧化钠溶液的滴定曲线如图所示,横坐标为滴定百分数(),纵坐标为滴定
过程中溶液pH,甲基红是一种酸碱指示剂,变色范围为4.4~6.2,下列有关滴定过程说法正确的是( )
A.滴定氨水,当滴定分数为50%时,各离子浓度间存在关系:c(NH)+c(H+)=c(OH-)
B.滴定分数为100%时,即为滴定过程中反应恰好完全的时刻
C.从滴定曲线可以判断,使用甲基橙作为滴定过程中的指示剂准确性更佳
D.滴定氨水,当滴定分数为150%时,所得溶液中离子浓度有大小关系:c(Cl-)>c(H+)>c(NH)>c(OH-)
【对点1】(2024·河北唐山·模拟)用已知浓度的NaOH溶液测定某HSO 溶液的浓度,参考下图,从下表
2 4
中选出正确的指示剂和仪器( )
选项 锥形瓶中溶液 滴定管中溶液 选用指示剂 选用滴定管
A 碱 酸 石蕊 乙
B 酸 碱 酚酞 甲
C 碱 酸 甲基橙 乙
D 酸 碱 酚酞 乙
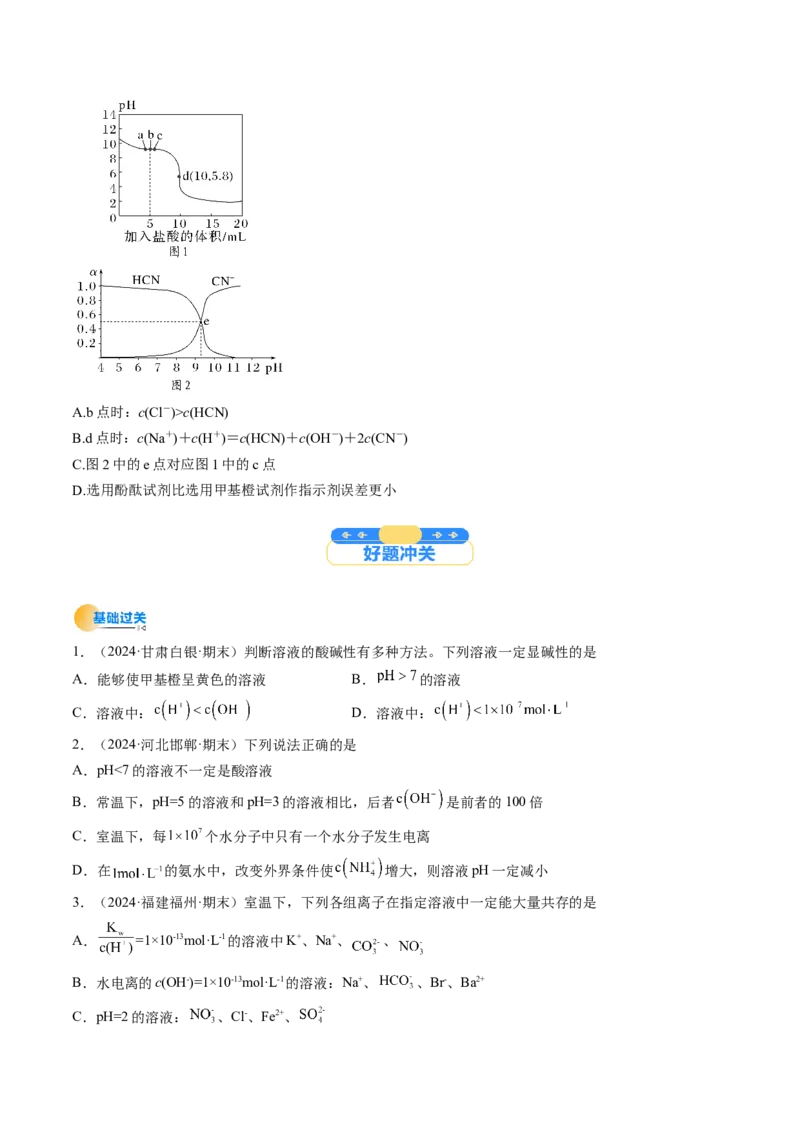
【对点2】(2024·浙江金华·模拟)已知25 ℃时,向10 mL 0.01 mol·L-1 NaCN溶液中逐滴加入0.01 mol·L
-1的盐酸,滴定曲线如图1所示,CN-、HCN的物质的量分数(α)随pH变化的关系如图2所示。下列表述
正确的是( )A.b点时:c(Cl-)>c(HCN)
B.d点时:c(Na+)+c(H+)=c(HCN)+c(OH-)+2c(CN-)
C.图2中的e点对应图1中的c点
D.选用酚酞试剂比选用甲基橙试剂作指示剂误差更小
1.(2024·甘肃白银·期末)判断溶液的酸碱性有多种方法。下列溶液一定显碱性的是
A.能够使甲基橙呈黄色的溶液 B. 的溶液
C.溶液中: D.溶液中:
2.(2024·河北邯郸·期末)下列说法正确的是
A.pH<7的溶液不一定是酸溶液
B.常温下,pH=5的溶液和pH=3的溶液相比,后者 是前者的100倍
C.室温下,每 个水分子中只有一个水分子发生电离
D.在 的氨水中,改变外界条件使 增大,则溶液pH一定减小
3.(2024·福建福州·期末)室温下,下列各组离子在指定溶液中一定能大量共存的是
A. =1×10-13mol·L-1的溶液中K+、Na+、 、
B.水电离的c(OH-)=1×10-13mol·L-1的溶液:Na+、 、Br-、Ba2+
C.pH=2的溶液: 、Cl-、Fe2+、D. =1012的溶液:Fe2+、Al3+、 、I-
4.(2024·江苏徐州·期中)常温下,下列各组离子在指定溶液中一定能大量共存的是
A.水电离出的c(H+)=1.0×10-13mol/L的溶液中:Na+、 、Cl-、
B.与Al反应放出H 的溶液:Mg2+、Cu2+、 、
2
C.加入少量KSCN后变为红色的溶液中:K+、Mg2+、I-、
D.无色透明的溶液中:CHCOO-、 、K+、Na+
3
5.(2024·广东湛江·期中)下列叙述正确的是
A.95℃纯水的 ,说明加热可导致水呈酸性
B. 的醋酸溶液,稀释至10倍后
C. 的醋酸溶液与 的氢氧化钠溶液等体积混合后
D. 的盐酸与等体积水混合后
6.(2024·山西晋城·期末)用已知浓度盐酸滴定未知浓度NaOH溶液的操作过程中,导致所测NaOH溶液
浓度偏低的操作是
A.滴定管装入盐酸前未用盐酸标准液润洗 B.锥形瓶未用未知浓度的NaOH溶液润洗
C.摇动锥形瓶时,因用力过猛,使少量溶液溅出 D.滴定前读数正确,滴定结束后仰视读数
7.(2024·广东东莞·期中)常温下,几种弱酸的电离平衡常数如下表所示,下列说法正确的是
化学式 HCOOH HCO HCN
2 3
电离平衡常数 K=1.8×10-4 K=4.3×10-7 K=5.6×10-11 K=4.9×10-10
1 2
A.酸性强弱顺序是:HCOOH > HCN > H CO
2 3
B.物质的量浓度均为0.1 mol·L-1的HCOONa溶液和NaCN溶液,pH大小顺序:HCOONa > NaCN
C.常温下,物质的量浓度为0.1mol/L的HCN溶液中c(OH-)浓度约为1.4×10-8mol/L
D.HCO 溶液和NaCN溶液反应的离子方程式为HCO +CN-=HCN + HCO
2 3 2 3
8.(2024·浙江杭州·期中)液氨与纯水类似,也存在微弱的电离: ,T℃时,液
氨的离子积常数 ,若用定义 的方式来规定 ,则下列叙述正
确的是
A.其他条件不变,增加液氨的量,电离平衡正向移动
B.液氨达到电离平衡时
C.T℃时的液氨中,
D.一定温度下,向液氨中加入氯化铵固体,电离平衡逆向移动,K值减小
9.(2024·四川成都·期末)常温下,下列有关叙述正确的是
A.水的离子积 只与温度有关,但水的电离程度一定会受外加酸、碱、盐的影响B.若HA的 ,BOH的 ,则HA溶液中的 与BOH中的 相等
C.将0.2mol/LHA溶液和0.1mol/LNaOH溶液等体积混合,则反应后的混合液中:
D. 能溶于 浓溶液的主要原因是 结合 使沉淀溶解平衡发生正向移动
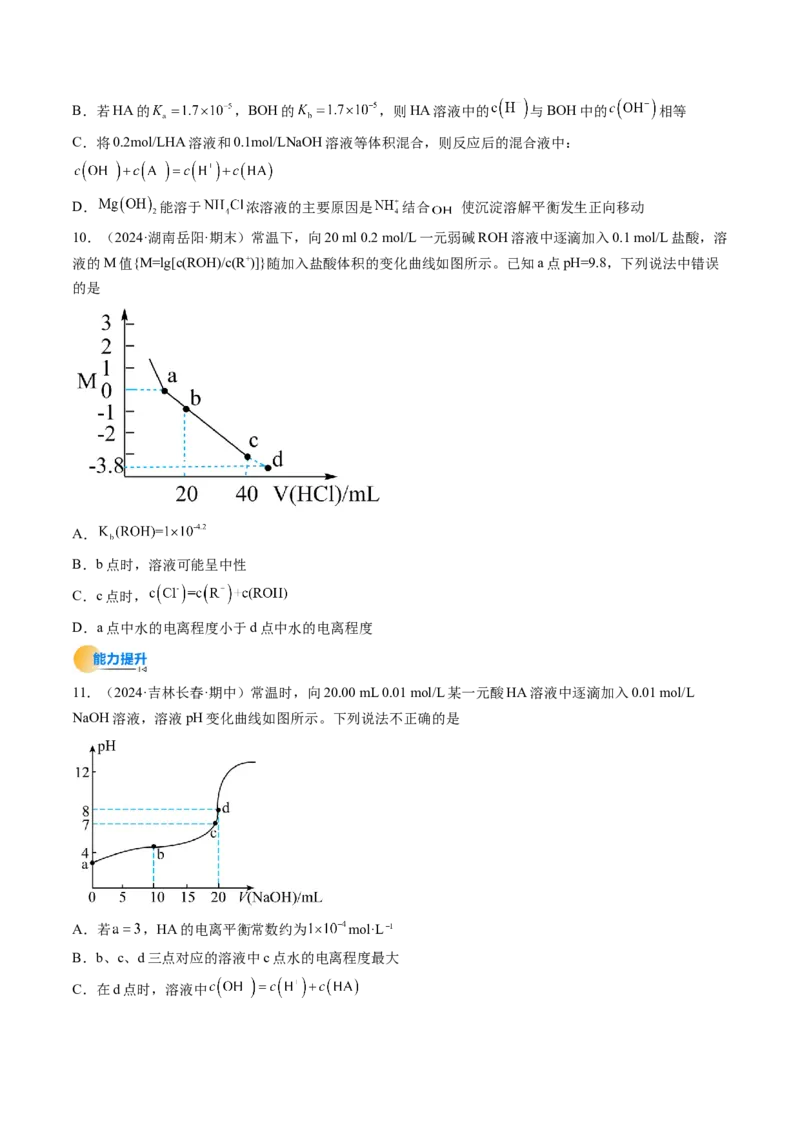
10.(2024·湖南岳阳·期末)常温下,向20 ml 0.2 mol/L一元弱碱ROH溶液中逐滴加入0.1 mol/L盐酸,溶
液的M值{M=lg[c(ROH)/c(R+)]}随加入盐酸体积的变化曲线如图所示。已知a点pH=9.8,下列说法中错误
的是
A.
B.b点时,溶液可能呈中性
C.c点时,
D.a点中水的电离程度小于d点中水的电离程度
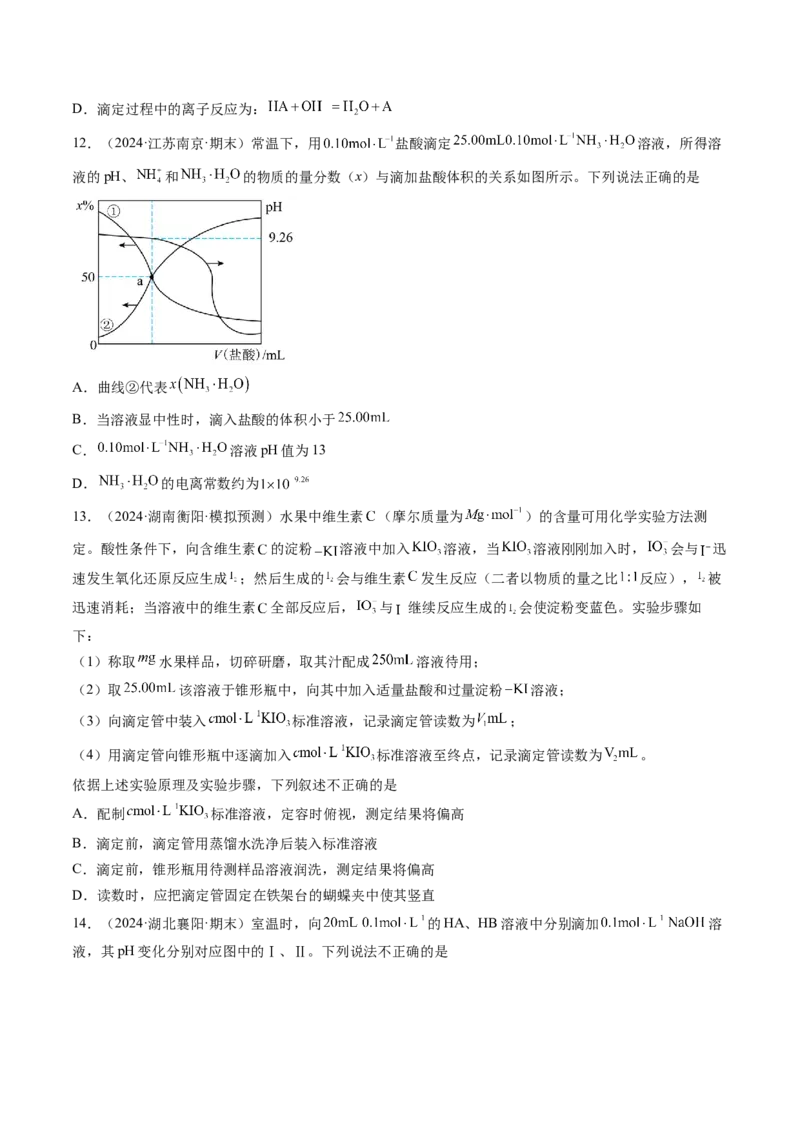
11.(2024·吉林长春·期中)常温时,向20.00 mL 0.01 mol/L某一元酸HA溶液中逐滴加入0.01 mol/L
NaOH溶液,溶液pH变化曲线如图所示。下列说法不正确的是
A.若 ,HA的电离平衡常数约为 mol·L
B.b、c、d三点对应的溶液中c点水的电离程度最大
C.在d点时,溶液中D.滴定过程中的离子反应为:
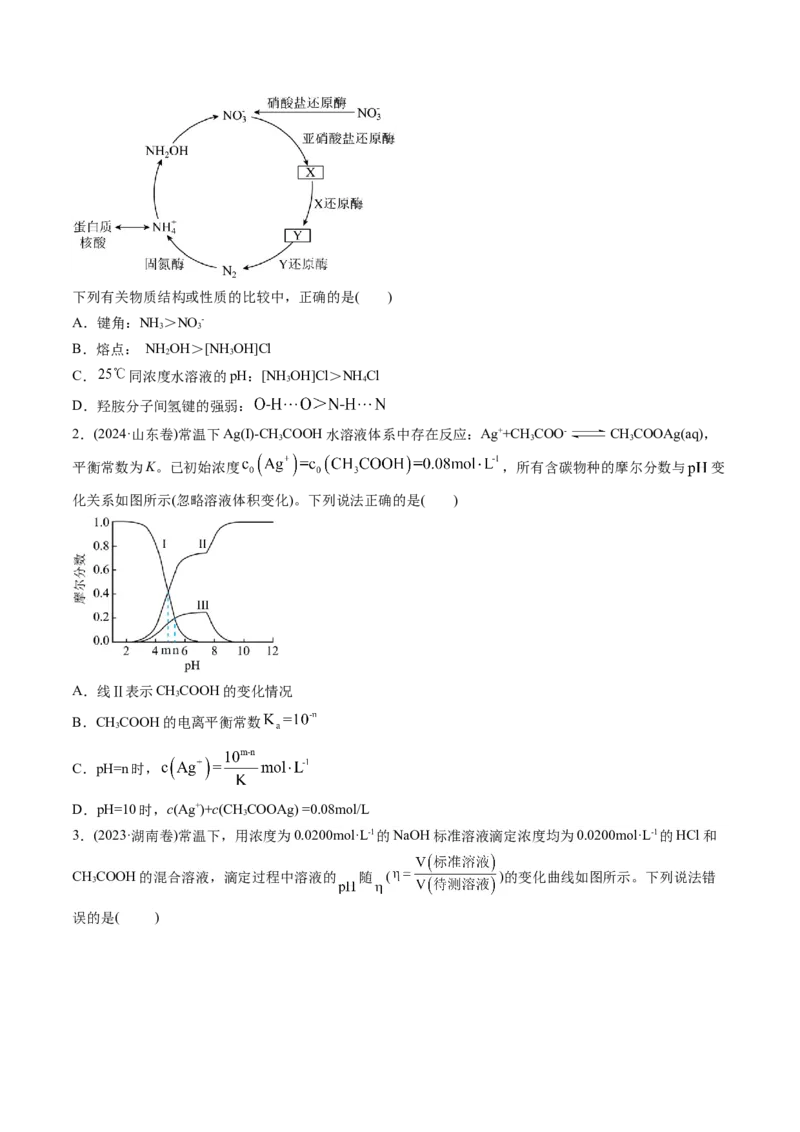
12.(2024·江苏南京·期末)常温下,用 盐酸滴定 溶液,所得溶
液的pH、 和 的物质的量分数(x)与滴加盐酸体积的关系如图所示。下列说法正确的是
A.曲线②代表
B.当溶液显中性时,滴入盐酸的体积小于
C. 溶液pH值为13
D. 的电离常数约为
13.(2024·湖南衡阳·模拟预测)水果中维生素 (摩尔质量为 )的含量可用化学实验方法测
定。酸性条件下,向含维生素 的淀粉 溶液中加入 溶液,当 溶液刚刚加入时, 会与 迅
速发生氧化还原反应生成 ;然后生成的 会与维生素 发生反应(二者以物质的量之比 反应), 被
迅速消耗;当溶液中的维生素 全部反应后, 与 继续反应生成的 会使淀粉变蓝色。实验步骤如
下:
(1)称取 水果样品,切碎研磨,取其汁配成 溶液待用;
(2)取 该溶液于锥形瓶中,向其中加入适量盐酸和过量淀粉 溶液;
(3)向滴定管中装入 标准溶液,记录滴定管读数为 ;
(4)用滴定管向锥形瓶中逐滴加入 标准溶液至终点,记录滴定管读数为 。
依据上述实验原理及实验步骤,下列叙述不正确的是
A.配制 标准溶液,定容时俯视,测定结果将偏高
B.滴定前,滴定管用蒸馏水洗净后装入标准溶液
C.滴定前,锥形瓶用待测样品溶液润洗,测定结果将偏高
D.读数时,应把滴定管固定在铁架台的蝴蝶夹中使其竖直
14.(2024·湖北襄阳·期末)室温时,向 的HA、HB溶液中分别滴加 溶
液,其pH变化分别对应图中的Ⅰ、Ⅱ。下列说法不正确的是A.向 溶液中滴加HA溶液可产生HB
B.
C.滴加 溶液至 时,两种溶液中
D.滴加 溶液时,Ⅱ中 的电离程度大于Ⅰ中
15.(2024·山东青岛·模拟预测)水果中维生素 (摩尔质量为 )的含量可用化学实验方法测
定。酸性条件下,向含维生素 的淀粉 溶液中加入 溶液,当 溶液刚刚加入时, 会与 迅
速发生氧化还原反应生成 ;然后生成的 会与维生素 发生反应(二者以物质的量之比 反应), 被
迅速消耗;当溶液中的维生素 全部反应后, 与 继续反应生成的 会使淀粉变蓝色。实验步骤如
下:
(1)称取 水果样品,切碎研磨,取其汁配成 溶液待用;
(2)取 该溶液于锥形瓶中,向其中加入适量盐酸和过量淀粉 溶液;
(3)向滴定管中装入 标准溶液,记录滴定管读数为 ;
(4)用滴定管向锥形瓶中逐滴加入 标准溶液至终点,记录滴定管读数为 。
水果样品中维生素 的含量为
A. B.
C. D.
1.(2024·安徽卷)地球上的生物氮循环涉及多种含氮物质,转化关系之一如下图所示(X、Y均为氮氧化
物),羟胺(NH OH)以中间产物的形式参与循环。常温常压下,羟胺易潮解,水溶液呈碱性,与盐酸反应的
2
产物盐酸羟胺([NH OH]Cl)广泛用子药品、香料等的合成。
3
已知25℃时,K(HNO)=7.2×10-4,K(NH ·H O)=1.8×10-5 ,K(NH OH)=8.7×10-9。
a 2 b 3 2 b 2下列有关物质结构或性质的比较中,正确的是( )
A.键角:NH >NO -
3 3
B.熔点: NH OH>[NH OH]Cl
2 3
C. 同浓度水溶液的pH:[NH OH]Cl>NH Cl
3 4
D.羟胺分子间氢键的强弱:
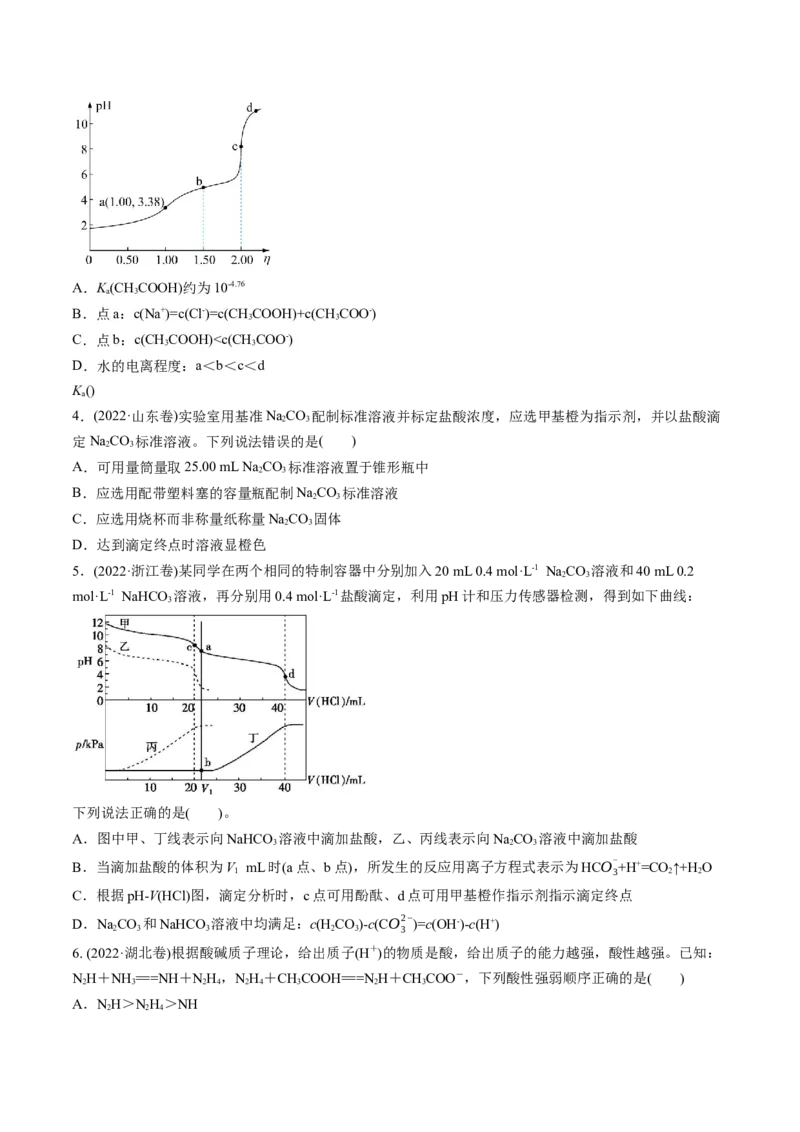
2.(2024·山东卷)常温下Ag(I)-CH COOH水溶液体系中存在反应:Ag++CH COO- CHCOOAg(aq),
3 3 3
平衡常数为K。已初始浓度 ,所有含碳物种的摩尔分数与 变
化关系如图所示(忽略溶液体积变化)。下列说法正确的是( )
A.线Ⅱ表示CHCOOH的变化情况
3
B.CHCOOH的电离平衡常数
3
C.pH=n时,
D.pH=10时,c(Ag+)+c(CHCOOAg) =0.08mol/L
3
3.(2023·湖南卷)常温下,用浓度为0.0200mol·L-1的NaOH标准溶液滴定浓度均为0.0200mol·L-1的HCl和
CHCOOH的混合溶液,滴定过程中溶液的 随 ( )的变化曲线如图所示。下列说法错
3
误的是( )A.K(CHCOOH)约为10-4.76
a 3
B.点a:c(Na+)=c(Cl-)=c(CH COOH)+c(CH COO-)
3 3
C.点b:c(CHCOOH)