文档内容
考点 36 烃的衍生物
目录
.............................................................................................................................................1
1.高考真题考点分布...................................................................................................................................1
2.命题规律及备考策略...............................................................................................................................2
.............................................................................................................................................2
考法01 卤代烃...........................................................................................................................................2
考法02 醇和酚...........................................................................................................................................6
考法03 醛和酮 酰胺.............................................................................................................................10
考法04 羧酸和酯.....................................................................................................................................14
...........................................................................................................................................16
1.高考真题考点分布
考点内
考点分布
容
卤代烃 2024·浙江卷,3分;2023浙江卷,3分;2022江苏卷,3分;2021湖南卷,3分;
2024·辽宁卷,3分;2024·湖北卷,3分;2024·山东卷,3分;2024·江苏卷,3分;
醇和酚 2024·甘肃卷,3分;2023年浙江卷,3分;2023湖北卷,3分;2023海南卷,3分;
2023江苏卷,3分;2022山东卷,3分;2022湖北卷,3分;2022福建卷,4分;
2024·河北卷,3分;2023北京卷,3分;2023山东卷,4分;2023湖北卷,3分;
醛和酮 2022山东卷,2分;2022重庆卷,3分;2022全国甲卷,6分;2022湖北卷,3分;
2022广东卷,3分;2022浙江卷,2分;
2024·新课标卷,3分;2024·江苏卷,3分;2024·甘肃卷,3分;2023新课标卷,6分;
羧酸、 2023全国乙卷,6分;2023全国甲卷,6分;2023广东卷,3分;2023山东卷,3分;
酯、 2023湖北卷,3分;2023北京卷,3分;2023辽宁卷,3分;2022全国乙卷,6分;
酰胺 2022河北卷,3分;2022湖南卷,3分;2022全国乙卷,6分;2022湖南卷,3分;
2022浙江卷,2分;2022北京卷,3分;2022湖南卷,3分;
2.命题规律及备考策略
【命题规律】
高频考点从近几年全国高考试题来看,卤代烃、醇、酚、醛和酮、酯、胺、酰胺结构与性质仍是高考命题的热点。
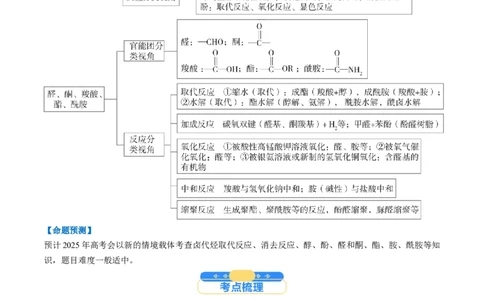
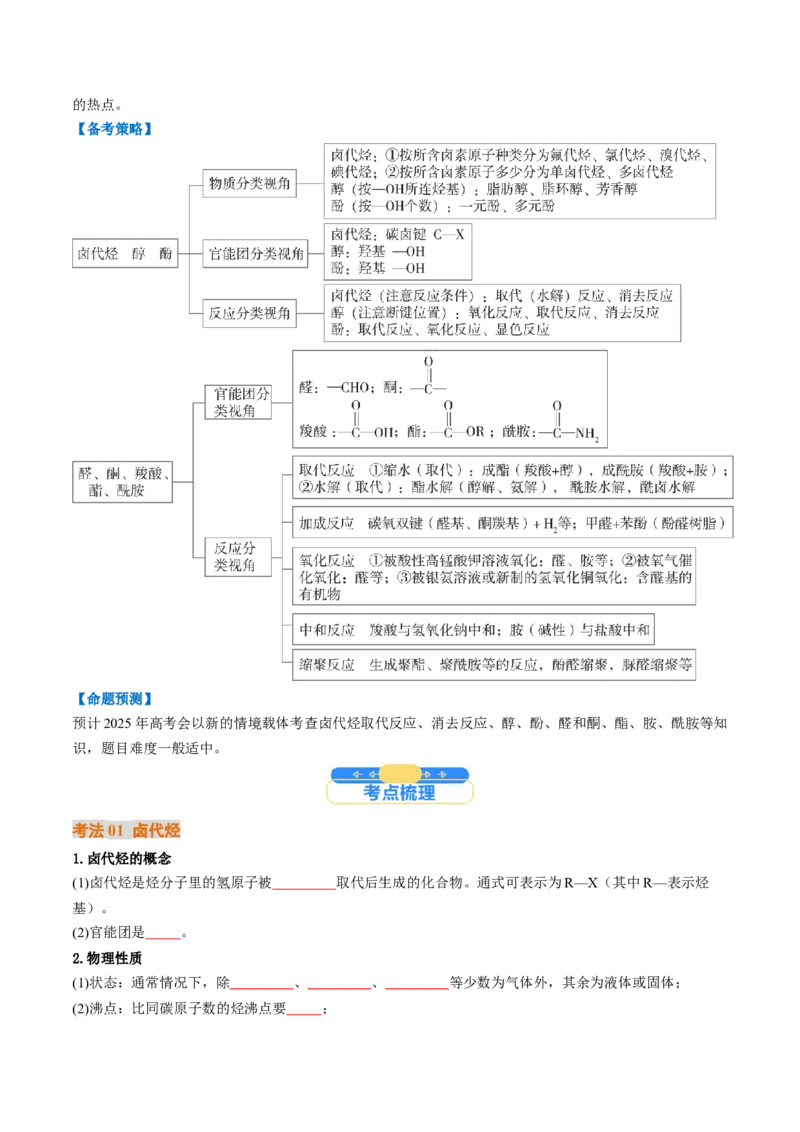
【备考策略】
【命题预测】
预计2025年高考会以新的情境载体考查卤代烃取代反应、消去反应、醇、酚、醛和酮、酯、胺、酰胺等知
识,题目难度一般适中。
考法01 卤代烃
1.卤代烃的概念
(1)卤代烃是烃分子里的氢原子被 取代后生成的化合物。通式可表示为R—X(其中R—表示烃
基)。
(2)官能团是 。
2.物理性质
(1)状态:通常情况下,除 、 、 等少数为气体外,其余为液体或固体;
(2)沸点:比同碳原子数的烃沸点要 ;(3)溶解性:水中 ,有机溶剂中 ;
(4)密度:一般一氟代烃、一氯代烃比水小,其余比水大。
3.化学性质
(1)水解反应
①反应条件: 。
②C HBr在碱性条件下水解的化学方程式为 。
2 5
③用R—CH—X表示卤代烃,碱性条件下水解的化学方程式为
2
。
(2)消去反应
①概念:有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如HO、HX等),而生成含不饱
2
和键的化合物的反应。
②卤代烃消去反应条件: 。
③溴乙烷发生消去反应的化学方程式为 。
④用R—CH—CH—X表示卤代烃,消去反应的化学方程式为 。
2 2
【特别提醒】卤代烃消去反应的规律
(1)两类卤代烃不能发生消去反应
结构特点 实例
与卤素原子相连的碳没有邻位碳原子 CHCl
3
与卤素原子相连的碳有邻位碳原子,但邻位碳原子上
无氢原子
(2)有两种或三种邻位碳原子,且碳原子上均带有氢原子时,发生消去反应可生成不同的产物。例如:
+NaOH――→NaCl+HO+CH===CH—CH—CH↑(或CH—CH===CH—CH↑)。
2 2 2 3 3 3
(3) 型卤代烃,发生消去反应可以生成R—C≡C—R。
例如:BrCHCHBr+2NaOH――→CH≡CH↑+2NaBr+2HO。
2 2 2
4.卤代烃(RX)中卤素原子的检验方法
(1)实验流程
(2)注意事项
①卤代烃不能电离出X-,必须转化成X-,酸化后方可用 溶液来检验。
②将卤代烃中的卤素原子转化为X-,可用卤代烃的水解反应,也可用消去反应(与卤素原子相连的碳原子
的邻位碳原子上有氢原子)。
5.卤代烃的制备(1)不饱和烃与卤素单质、卤代氢等能发生 ,如:
CH—CH===CH +Br ―→CHCHBrCH Br
3 2 2 3 2
CH—CH===CH +HBr――→
3 2
(2)取代反应
如:乙烷与Cl:
2
CHCHOH与HBr:
3 2
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)CH CHCl的沸点比CHCH 的沸点高( )
3 2 3 3
(2)溴乙烷与NaOH乙醇溶液共热生成乙烯( )
(3)在溴乙烷中加入AgNO 溶液,立即产生淡黄色沉淀( )
3
(4)取溴乙烷水解液,向其中加入AgNO 溶液,可观察到淡黄色沉淀
3
(5)所有卤代烃都能够发生水解反应和消去反应( )
考向01 考查卤代烃的性质
【例1】(2024·河北秦皇岛·一模)下列关于卤代烃的叙述中正确的是( )
A.所有卤代烃都是难溶于水,密度比水小的液体
B.所有卤代烃在适当条件下都能发生消去反应
C.所有卤代烃都含有卤原子
D.所有卤代烃都是通过取代反应制得的
【思维建模】卤代烃水解反应和消去反应的比较
反应类型 取代反应(水解反应) 消去反应
反应条件 强碱的水溶液、加热 强碱的醇溶液、加热
断键方式
卤代烃分子中—X被水中的—OH所
反应本质 相邻的两个碳原子间脱去小分子HX
取代,生成醇
引入—OH,生成含—OH的有机化 消去HX,生成含碳碳双键或碳碳三
产物特征
合物 键等不饱和键的有机化合物
考向02 考查卤代烃在有机转化中的作用
【例2】(2024·湖南湘潭·模拟)聚氯乙烯是生活中常用的塑料。工业生产聚氯乙烯的一种工艺路线如下:
――→――→――→
反应①的化学方程式为_____________________________________________________,
反应类型为________________;反应②的反应类型为________________。
【思维建模】(1)连接烃和烃的衍生物的桥梁
烃通过与卤素发生取代反应或加成反应转化为卤代烃,卤代烃在碱性条件下可水解转化为醇或酚,进一步
可转化为醛、酮、羧酸和酯等;醇在加热条件下与氢卤酸反应转化为卤代烃,卤代烃通过消去反应可转化
为烯烃或炔烃。
如: ―→醛或羧酸
(2)改变官能团的个数
如CHCHBr――→CH===CH ――→CHBrCHBr。
3 2 2 2 2 2
(3)改变官能团的位置
如CHBrCHCHCH――→CH===CHCHCH――→ 。
2 2 2 3 2 2 3
(4)进行官能团的保护
如在氧化CH===CHCHOH的羟基时,碳碳双键易被氧化,常采用下列方法保护:
2 2
CH===CHCHOH――→ ――→ CH===CH—COOH。
2 2 ――→ 2
【对点1】(2024·辽宁丹东·模拟)为了测定某卤代烃分子中所含有的卤素原子种类,可按下列步骤进行实
验: ①量取该卤代烃液体;②冷却后加入稀硝酸酸化;③加入AgNO 溶液至沉淀完全;④加入适量
3
NaOH溶液,煮沸至液体不分层;
正确操作顺序为( )
A.④③②① B.①④②③
C.③①④② D.①④③②
【对点2】(2024·江苏无锡·模拟)根据下面的反应路线及所给信息填空。
(1)A的结构简式是 ,名称是 。
(2)①的反应类型是 ;③的反应类型是 。
(3)反应④的化学方程式是__________________________________________________。
考法02 醇和酚
1.概念: 与烃基或苯环侧链上的饱和碳原子相连的化合物称为醇。
2.饱和一元醇的分子通式: (n≥1)。
3.分类4.物理性质的变化规律
(1)水溶性:低级脂肪醇 于水,饱和一元醇的溶解度随着分子中碳原子数的递增而 。
(2)密度:一元脂肪醇的密度一般小于1 g·cm-3。
(3)沸点
①直链饱和一元醇的沸点随着分子中碳原子数的递增而逐渐 。
②醇分子间存在 ,所以相对分子质量相近的醇和烷烃相比,醇的沸点远远 烷烃。
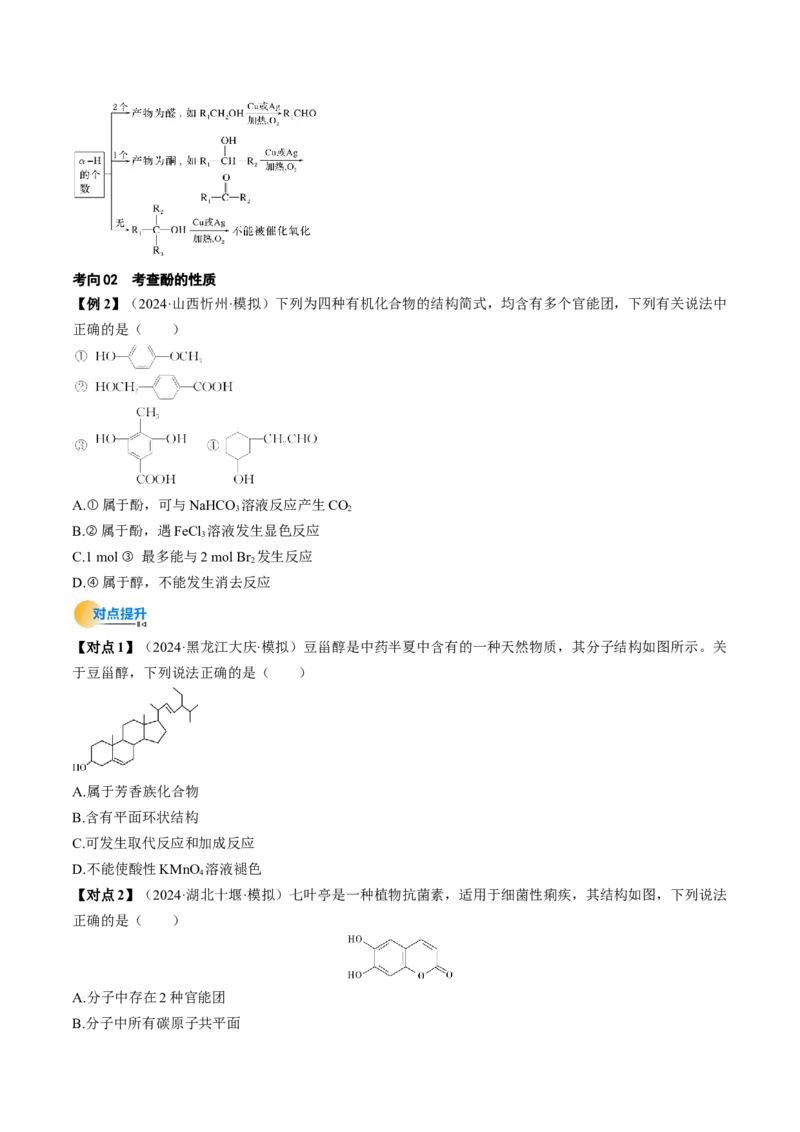
5.由断键方式理解醇的化学性质
如果将醇分子中的化学键进行标号如图所示,那么醇发生化学反应时化学键的断裂情况如图所示:
以1丙醇为例,完成下列条件下的化学方程式,并指明断键部位。
(1)与Na反应: ,①。
(2)催化氧化: ,①③。
(3)与HBr的取代: ,②。
(4)消去反应: ,②⑤。
(5)与乙酸的酯化反应: ,①。
6.常见几种醇的性质及应用
名称 甲醇 乙二醇 丙三醇
俗称 木精、木醇 甘油
结构简式 CHOH
3
状态
溶解性
重要的化工原料,可 用作汽车发动机的抗冻剂, 作护肤剂,制造烈性炸药硝化甘
应用
用于制造燃料电池 重要的化工原料 油,重要的化工原料
二、酚
1.概念: 与苯环 相连而形成的化合物,最简单的酚为 。
2.物理性质(1)纯净的苯酚是 晶体,有特殊气味,易被空气氧化呈 色。
(2)苯酚常温下在水中的溶解度 ,当温度高于 时,能与水 ,苯酚 于乙醇等有机溶剂。
(3)苯酚有毒,对皮肤有强烈的腐蚀作用,如果不慎沾到皮肤上,应立即用 洗涤,再用水冲洗。
3.苯酚的化学性质
(1)羟基中氢原子的反应
a.弱酸性:苯酚的电离方程式为 ,俗称 ,但酸性很弱,
不能使紫色石蕊溶液变红;
b.与活泼金属反应:与Na反应的化学方程式为 ;
c.与碱反应:苯酚的浑浊液――→变 ――→溶液又变 。
该过程中发生反应的化学方程式分别为 ,
。
(2)苯环上氢原子的取代反应
苯酚与饱和溴水反应的化学方程式为 ,反应产生 沉淀,此
反应常用于苯酚的定性检验和定量测定。
(3)显色反应:苯酚与FeCl 溶液作用显紫色,利用这一反应可以检验酚类物质的存在。
3
(4)加成反应:与H 反应的化学方程式为 。
2
(5)氧化反应
苯酚易被空气中的氧气氧化而显粉红色;易被酸性KMnO 溶液氧化;易燃烧。
4
4.苯酚的用途和对环境的影响
苯酚是重要的医用消毒剂和化工原料,广泛用于制造酚醛树脂、染料、医药、农药等。酚类化合物均有
毒,是重点控制的水污染物之一。
【易错提醒】脂肪醇、芳香醇、酚的比较
类别 脂肪醇 芳香醇 酚
实例 CHCHOH C HCHOH C HOH
3 2 6 5 2 6 5
官能团 —OH —OH —OH
—OH与芳香烃侧
结构特点 —OH与链烃基相连 —OH与苯环直接相连
链上的碳原子相连
(1)弱酸性;(2)取代反应;
(1)与钠反应;(2)取代反应;(3)消去反应;
主要化学性质 (3)显色反应;(4)氧化反应;
(4)氧化反应;(5)酯化反应
(5)加成反应
将红热的铜丝插入醇中有刺激性气味物质
特性 遇FeCl 溶液显紫色
3
产生(生成醛或酮)
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)CH OH和 都属于醇类,且二者互为同系物( )
3(2)CH OH、CHCHOH、 的沸点逐渐升高( )
3 3 2
(3)钠与乙醇反应时因断裂C—O失去—OH官能团( )
(4)所有的醇都能发生催化氧化反应和消去反应( )
(5)由于醇分子中含有—OH,醇类都易溶于水( )
(6)苯酚的水溶液呈酸性,说明酚羟基的活泼性大于水中羟基的活泼性( )
(7) 和 互为同系物( )
(8)除去苯中的苯酚,加入浓溴水再过滤( )
(9) 和 含有的官能团相同,二者的化学性质相似( )
(10)鉴别苯酚溶液与乙醇溶液可滴加FeCl 溶液( )
3
考向01 考查醇的消去反应和氧化反应
【例1】(2024·河南平顶山·一模)下列醇类物质中既能发生消去反应,又能发生催化氧化反应生成醛类的
物质是( )
【思维建模】 醇的消去反应和氧化反应
1.醇的消去规律
(1)结构条件
①醇分子中连有羟基(—OH)的碳原子必须有相邻的碳原子;
②该相邻的碳原子上必须连有氢原子。
(2)断键方式
2.醇的催化氧化规律
醇能否发生催化氧化及氧化产物类型取决于醇分子中是否有α-H及其个数:考向02 考查酚的性质
【例2】(2024·山西忻州·模拟)下列为四种有机化合物的结构简式,均含有多个官能团,下列有关说法中
正确的是( )
A.①属于酚,可与NaHCO 溶液反应产生CO
3 2
B.②属于酚,遇FeCl 溶液发生显色反应
3
C.1 mol ③ 最多能与2 mol Br 发生反应
2
D.④属于醇,不能发生消去反应
【对点1】(2024·黑龙江大庆·模拟)豆甾醇是中药半夏中含有的一种天然物质,其分子结构如图所示。关
于豆甾醇,下列说法正确的是( )
A.属于芳香族化合物
B.含有平面环状结构
C.可发生取代反应和加成反应
D.不能使酸性KMnO 溶液褪色
4
【对点2】(2024·湖北十堰·模拟)七叶亭是一种植物抗菌素,适用于细菌性痢疾,其结构如图,下列说法
正确的是( )
A.分子中存在2种官能团
B.分子中所有碳原子共平面C.1 mol该物质与足量溴水反应,最多可消耗2 mol Br
2
D.1 mol该物质与足量NaOH溶液反应,最多可消耗3 mol NaOH
考法03 醛和酮 酰胺
一、醛和酮
1.醛、酮的概述
(1)醛、酮的概念
物质 概念 表示方法
醛 由 与 相连的化合物 RCHO
酮 与两个 相连的化合物
(2)醛的分类
醛
饱和一元醛的通式: ,饱和一元酮的通式: 。
2.常见的醛、酮及物理性质
名称 结构简式 状态 气味 溶解性
甲醛(蚁醛) 易溶于水
乙醛 与水以任意比互溶
丙酮 液体 特殊气味 与水以任意比互溶
3.醛的化学性质
(1)请写出乙醛主要反应的化学方程式。
①银镜反应: 。
②与新制Cu(OH) 反应: 。
2
③催化氧化反应: 。
④还原(加成)反应: 。
(2)具有极性键共价分子与醛、酮的酮羰基发生加成反应:
。
4.醛的应用和对环境、健康产生的影响
(1)醛是重要的化工原料,广泛应用于合成纤维、医药、染料等行业。
(2)35%~40%的甲醛水溶液俗称 :具有杀菌(用于种子杀菌)和 性能(用于浸制生物标本)。
(3)劣质的装饰材料中挥发出的 是室内主要污染物之一。
二、酰胺
1.胺
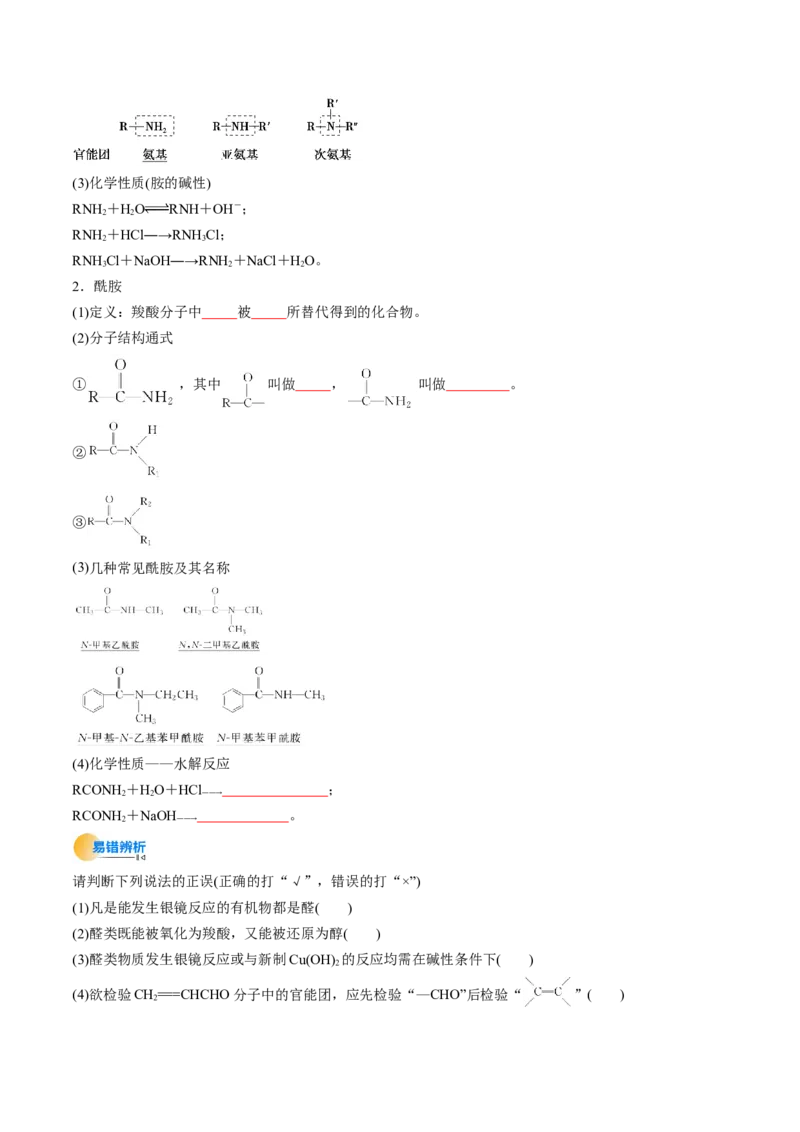
(1)定义: 取代 中的氢原子而形成的化合物。
(2)三种分子结构通式(3)化学性质(胺的碱性)
RNH +HO RNH+OH-;
2 2
RNH +HCl―→RNH Cl;
2 3
RNH Cl+NaOH―→RNH +NaCl+HO。
3 2 2
2.酰胺
(1)定义:羧酸分子中 被 所替代得到的化合物。
(2)分子结构通式
① ,其中 叫做 , 叫做 。
②
③
(3)几种常见酰胺及其名称
(4)化学性质——水解反应
RCONH +HO+HCl ;
2 2 ――→
RCONH +NaOH 。
2 ――→
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)凡是能发生银镜反应的有机物都是醛( )
(2)醛类既能被氧化为羧酸,又能被还原为醇( )
(3)醛类物质发生银镜反应或与新制Cu(OH) 的反应均需在碱性条件下( )
2
(4)欲检验CH===CHCHO分子中的官能团,应先检验“—CHO”后检验“ ”( )
2(5)1 mol HCHO与足量银氨溶液在水浴加热条件下充分反应,最多生成2 mol Ag( )
(6)苯胺盐酸盐可溶于水( )
(7)胺是指含有—NH 、—NHR或者—NR (R为烃基)的一系列有机化合物( )
2 2
(8) 中含有两种官能团( )
(9)CO(NH) 可以看作酰胺( )
2 2
(10)氯胺(NH Cl)的水解产物为NH OH和HCl( )
2 2
考向01 考查醛的性质
【例1】(2024·浙江温州·一模)有机物A是合成二氢荆芥内酯的重要原料,其结构简式为 ,
下列检验A中官能团的试剂和顺序正确的是( )
A.先加酸性高锰酸钾溶液,后加银氨溶液,微热
B.先加溴水,后加酸性高锰酸钾溶液
C.先加新制氢氧化铜悬浊液,微热,再加入溴水
D.先加入银氨溶液,微热,酸化后再加溴水
【思维建模】 醛基特征反应实验的注意事项
(1)银镜反应:
a.试管内壁必须洁净;
b.银氨溶液随用随配,不可久置;
c.水浴加热,不可用酒精灯直接加热;
d.醛用量不宜太多,一般加3滴;
e.银镜可用稀HNO 洗涤。
3
(2)与新制的Cu(OH) 反应:
2
a.Cu(OH) 要随用随配,不可久置;
2
b.配制Cu(OH) 时,所用NaOH必须过量;
2
c.反应液用酒精灯直接加热。
考向02 考查酰胺的性质
【例2】(2024·黑龙江七台河·模拟)丙烯酰胺是一种重要的有机合成的中间体,其结构简式为 。
下列有关丙烯酰胺的说法错误的是( )
A.丙烯酰胺分子中所有原子不可能在同一平面内
B.丙烯酰胺属于羧酸衍生物
C.丙烯酰胺在任何条件下都不能水解
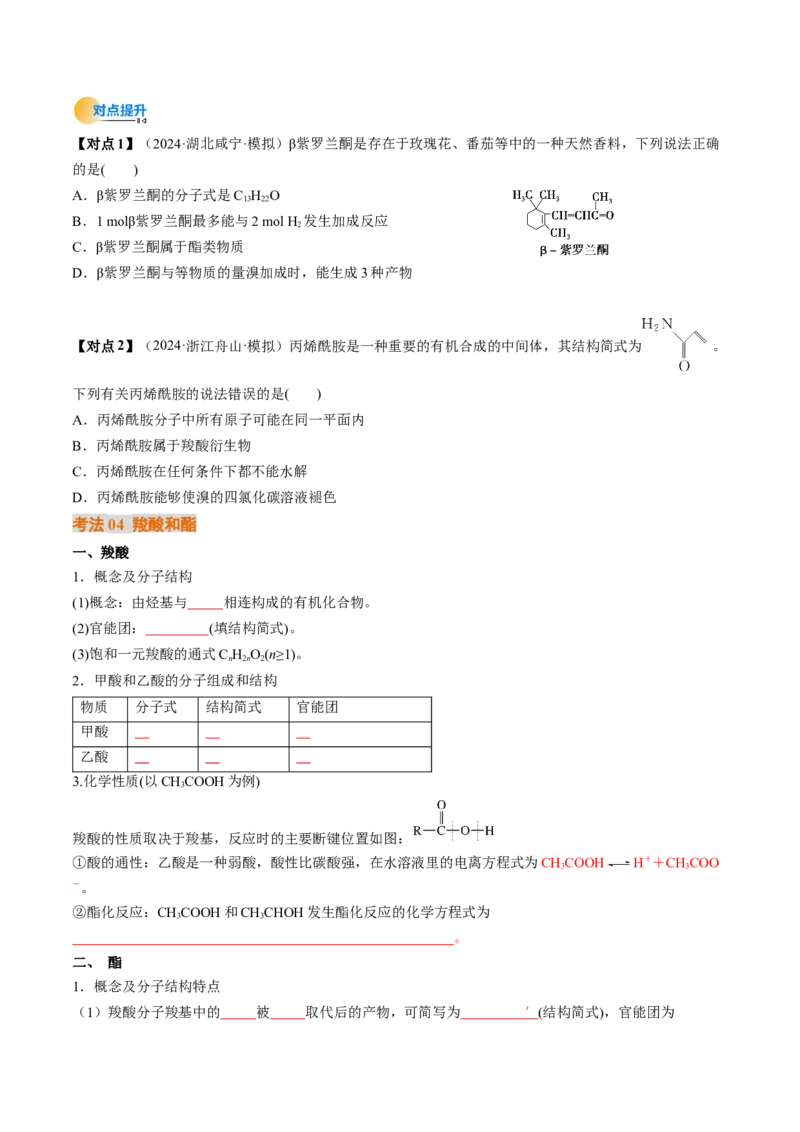
D.丙烯酰胺能够使溴的四氯化碳溶液褪色【对点1】(2024·湖北咸宁·模拟)β紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,下列说法正确
的是( )
A.β紫罗兰酮的分子式是C H O
13 22
B.1 molβ紫罗兰酮最多能与2 mol H 发生加成反应
2
C.β紫罗兰酮属于酯类物质
D.β紫罗兰酮与等物质的量溴加成时,能生成3种产物
【对点2】(2024·浙江舟山·模拟)丙烯酰胺是一种重要的有机合成的中间体,其结构简式为 。
下列有关丙烯酰胺的说法错误的是( )
A.丙烯酰胺分子中所有原子可能在同一平面内
B.丙烯酰胺属于羧酸衍生物
C.丙烯酰胺在任何条件下都不能水解
D.丙烯酰胺能够使溴的四氯化碳溶液褪色
考法04 羧酸和酯
一、羧酸
1.概念及分子结构
(1)概念:由烃基与 相连构成的有机化合物。
(2)官能团: (填结构简式)。
(3)饱和一元羧酸的通式C H O(n≥1)。
n 2n 2
2.甲酸和乙酸的分子组成和结构
物质 分子式 结构简式 官能团
甲酸
乙酸
3.化学性质(以CHCOOH为例)
3
羧酸的性质取决于羧基,反应时的主要断键位置如图:
①酸的通性:乙酸是一种弱酸,酸性比碳酸强,在水溶液里的电离方程式为CHCOOH H++CHCOO
3 3
-。
②酯化反应:CHCOOH和CHCHOH发生酯化反应的化学方程式为
3 3
。
二、 酯
1.概念及分子结构特点
(1)羧酸分子羧基中的 被 取代后的产物,可简写为 ′ (结构简式),官能团为。
(2)低级酯的物理性质:具有芳香气味的 体,密度一般比水 , 于有机溶剂。
(3)化学性质(以CHCOOC H 为例)
3 2 5
在酸或碱存在的条件下,酯可以发生水解反应生成相应的羧酸和醇,酯的水解反应是 的逆反
应。在酸性条件下的水解是可逆反应,但在碱性条件下的水解是不可逆的。
条件 化学方程式
稀HSO
2 4
NaOH溶液
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)羧基和酯基中的CO均能与H 加成( )
2
(2)可以用NaOH溶液来除去乙酸乙酯中的乙酸( )
(3)甲酸既能与新制的氢氧化铜发生中和反应,又能发生氧化反应( )
(4)羧酸都易溶于水( )
(5)甲酸乙酯、乙酸甲酯、丙酸互为同分异构体( )
考向01 考查羧酸的结构与性质
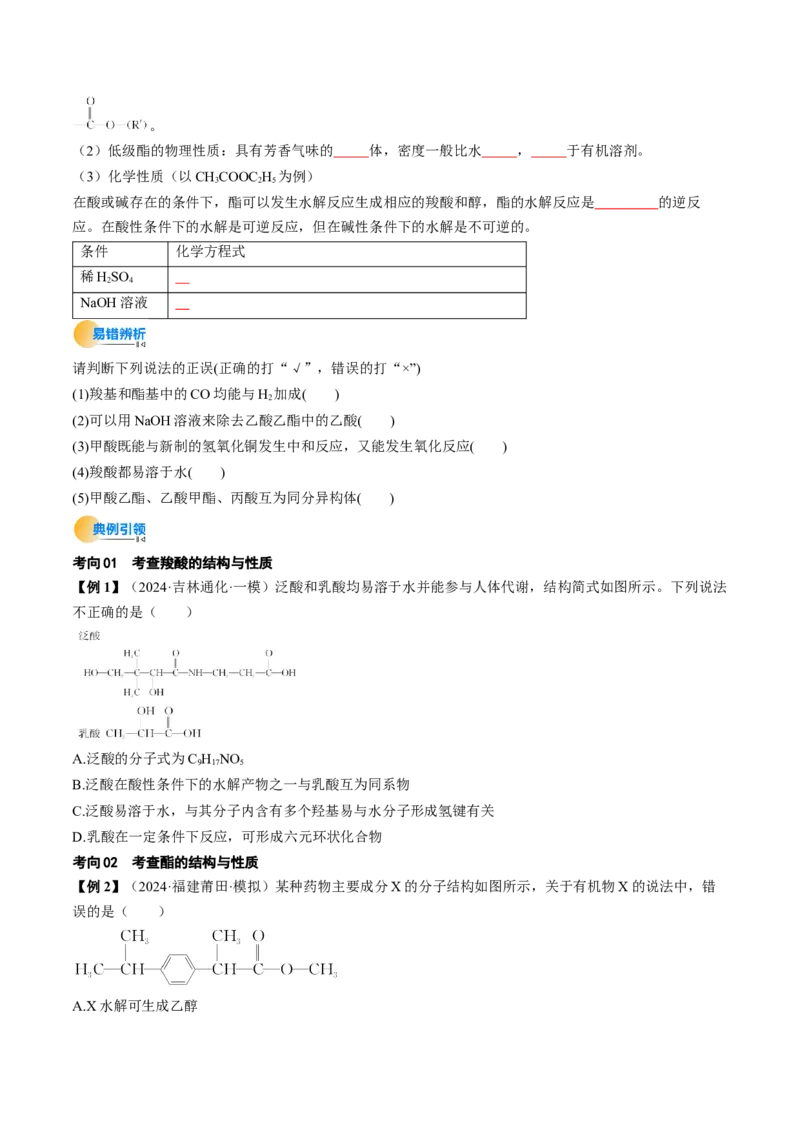
【例1】(2024·吉林通化·一模)泛酸和乳酸均易溶于水并能参与人体代谢,结构简式如图所示。下列说法
不正确的是( )
A.泛酸的分子式为C H NO
9 17 5
B.泛酸在酸性条件下的水解产物之一与乳酸互为同系物
C.泛酸易溶于水,与其分子内含有多个羟基易与水分子形成氢键有关
D.乳酸在一定条件下反应,可形成六元环状化合物
考向02 考查酯的结构与性质
【例2】(2024·福建莆田·模拟)某种药物主要成分X的分子结构如图所示,关于有机物X的说法中,错
误的是( )
A.X水解可生成乙醇B.X不能跟溴水反应
C.X能发生加成反应
D.X难溶于水,易溶于有机溶剂
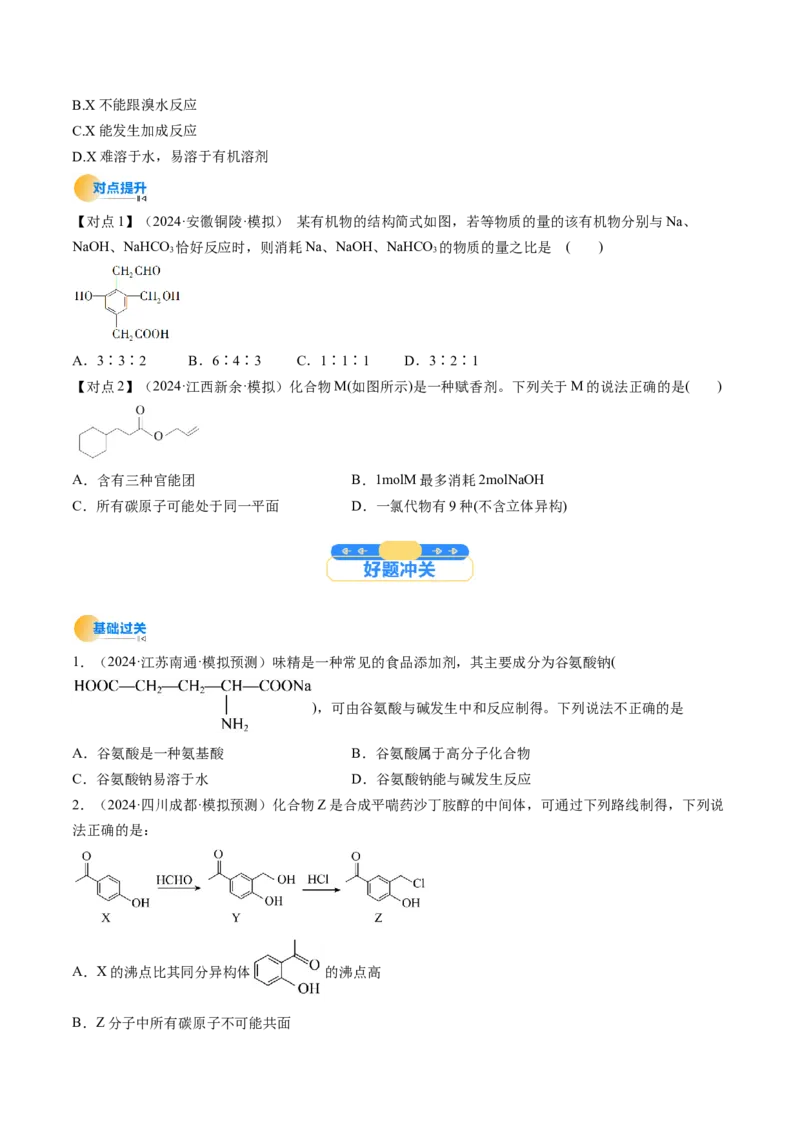
【对点1】(2024·安徽铜陵·模拟) 某有机物的结构简式如图,若等物质的量的该有机物分别与Na、
NaOH、NaHCO 恰好反应时,则消耗Na、NaOH、NaHCO 的物质的量之比是 ( )
3 3
A.3∶3∶2 B.6∶4∶3 C.1∶1∶1 D.3∶2∶1
【对点2】(2024·江西新余·模拟)化合物M(如图所示)是一种赋香剂。下列关于M的说法正确的是( )
A.含有三种官能团 B.1molM最多消耗2molNaOH
C.所有碳原子可能处于同一平面 D.一氯代物有9种(不含立体异构)
1.(2024·江苏南通·模拟预测)味精是一种常见的食品添加剂,其主要成分为谷氨酸钠(
),可由谷氨酸与碱发生中和反应制得。下列说法不正确的是
A.谷氨酸是一种氨基酸 B.谷氨酸属于高分子化合物
C.谷氨酸钠易溶于水 D.谷氨酸钠能与碱发生反应
2.(2024·四川成都·模拟预测)化合物Z是合成平喘药沙丁胺醇的中间体,可通过下列路线制得,下列说
法正确的是:
A.X的沸点比其同分异构体 的沸点高
B.Z分子中所有碳原子不可能共面C.1molY最多消耗2mol NaOH
D.X→Y的反应类型为取代反应
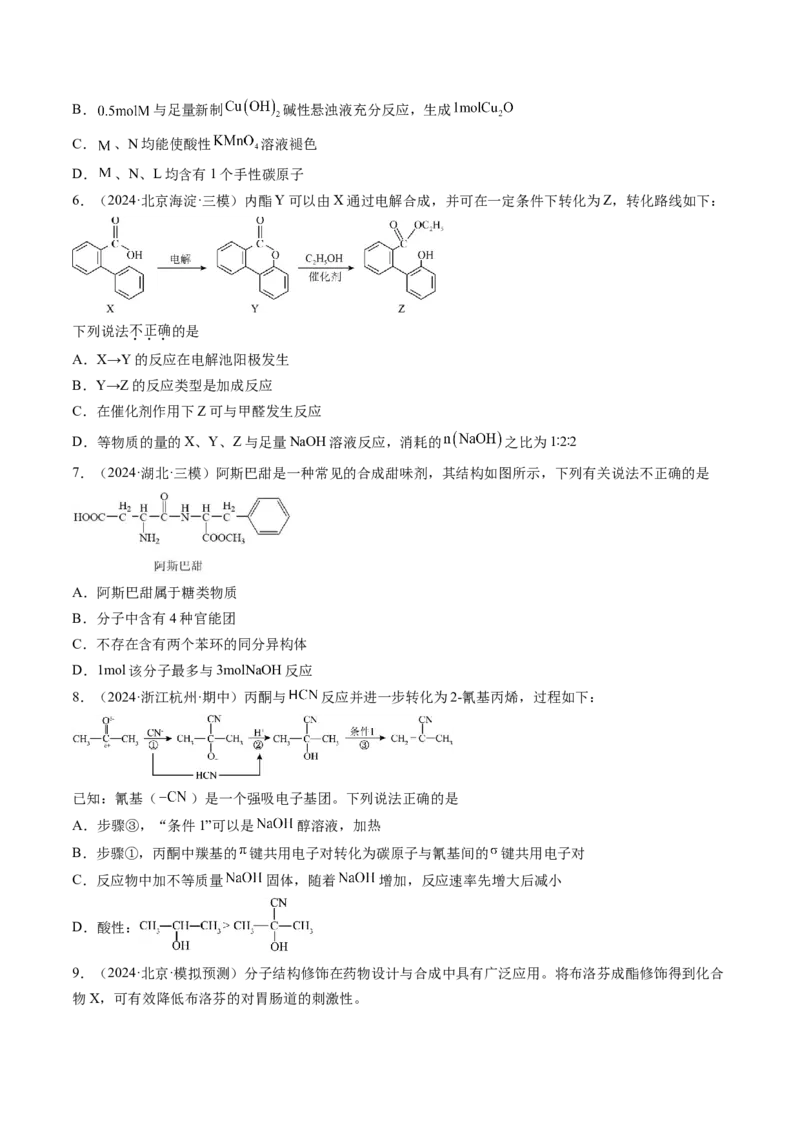
3.(2024·黑龙江佳木斯·一模)苯甲酸乙酯(无色液体,难溶于水,沸点213℃)天然存在于桃、菠萝、红
茶中,稍有水果气味,常用于配制香精和人造精油,也可用作食品添加剂。在环己烷中通过反应
制备,实验室中的反应装置如图所示:
已知:环己烷沸点为80.8℃,可与乙醇和水形成共沸物,其混合物沸点为62.1℃。下列说法错误的是
A.实验时应依次向圆底烧瓶中加入碎瓷片、浓硫酸、苯甲酸、无水乙醇、环己烷
B.实验时最好采用水浴加热,且冷却水应从b口流出
C.当分水器内下层液体高度不再发生变化时,实验结束,即可停止加热
D.依次通过碱洗分液,水洗分液的方法将粗产品从圆底烧瓶的反应液中分离出来
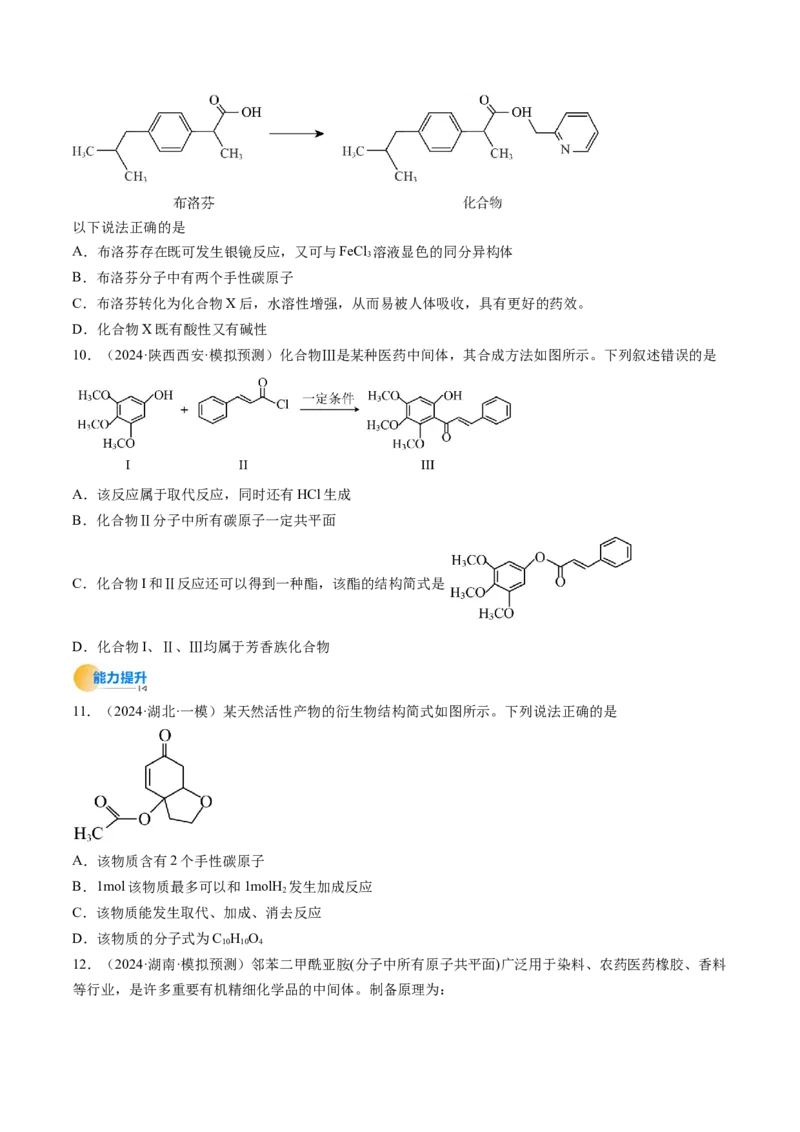
4.(2024·黑龙江大庆·模拟预测)高分子材料PPDO具有优良的生物降解性、相容性和吸收性,是一种优
良的医用缝合线,可通过如下反应来制备:
下列有关说法错误的是
A.K发生开环聚合反应生成M
B.K分子中含有醚键和酯基两种官能团
C.PPDO在人体内最终会降解代谢成 和
D.1mol M与足量NaOH溶液反应,消耗1mol NaOH
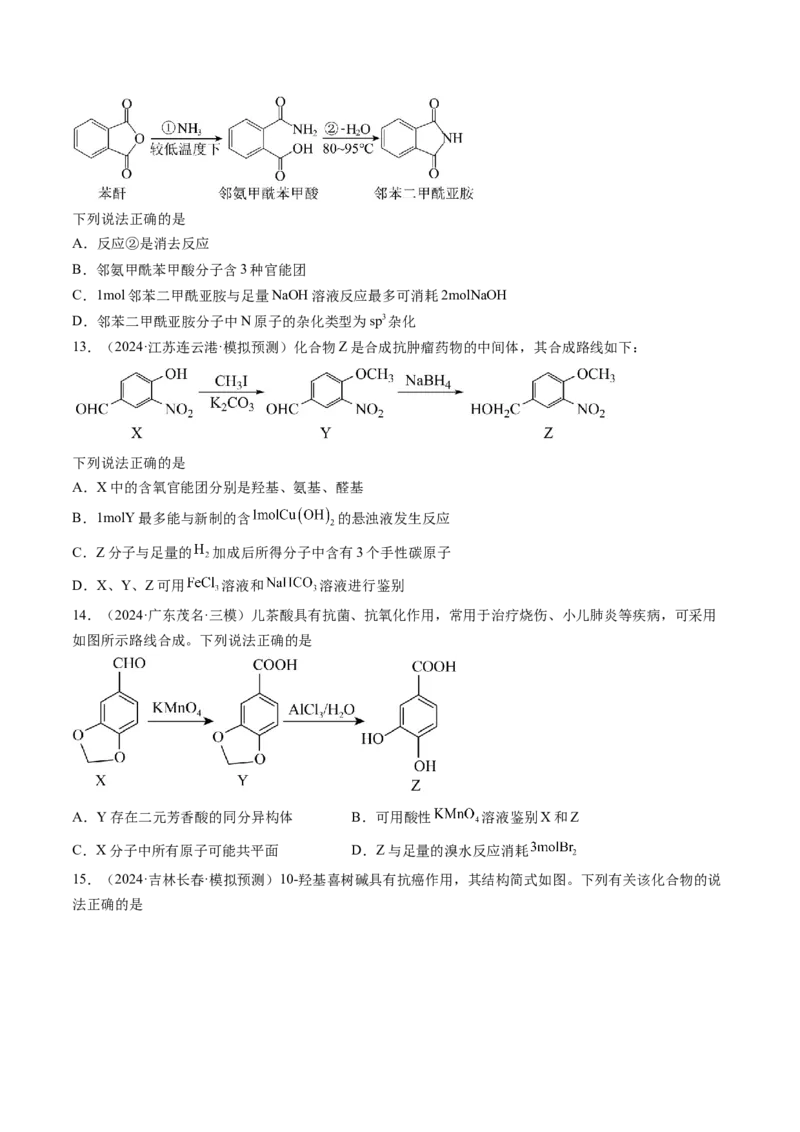
5.(2024·山东德州·三模)化合物 能发生如下转化,下列说法错误的是
A.过程Ⅰ中包含氧化反应与还原反应,过程Ⅱ发生酯化反应B. 与足量新制 碱性悬浊液充分反应,生成
C. 、N均能使酸性 溶液褪色
D. 、N、L均含有1个手性碳原子
6.(2024·北京海淀·三模)内酯Y可以由X通过电解合成,并可在一定条件下转化为Z,转化路线如下:
下列说法不正确的是
A.X→Y的反应在电解池阳极发生
B.Y→Z的反应类型是加成反应
C.在催化剂作用下Z可与甲醛发生反应
D.等物质的量的X、Y、Z与足量NaOH溶液反应,消耗的 之比为1∶2∶2
7.(2024·湖北·三模)阿斯巴甜是一种常见的合成甜味剂,其结构如图所示,下列有关说法不正确的是
A.阿斯巴甜属于糖类物质
B.分子中含有4种官能团
C.不存在含有两个苯环的同分异构体
D.1mol该分子最多与3molNaOH反应
8.(2024·浙江杭州·期中)丙酮与 反应并进一步转化为2-氰基丙烯,过程如下:
已知:氰基( )是一个强吸电子基团。下列说法正确的是
A.步骤③,“条件1”可以是 醇溶液,加热
B.步骤①,丙酮中羰基的 键共用电子对转化为碳原子与氰基间的 键共用电子对
C.反应物中加不等质量 固体,随着 增加,反应速率先增大后减小
D.酸性:
9.(2024·北京·模拟预测)分子结构修饰在药物设计与合成中具有广泛应用。将布洛芬成酯修饰得到化合
物X,可有效降低布洛芬的对胃肠道的刺激性。以下说法正确的是
A.布洛芬存在既可发生银镜反应,又可与FeCl 溶液显色的同分异构体
3
B.布洛芬分子中有两个手性碳原子
C.布洛芬转化为化合物X后,水溶性增强,从而易被人体吸收,具有更好的药效。
D.化合物X既有酸性又有碱性
10.(2024·陕西西安·模拟预测)化合物Ⅲ是某种医药中间体,其合成方法如图所示。下列叙述错误的是
A.该反应属于取代反应,同时还有HCl生成
B.化合物Ⅱ分子中所有碳原子一定共平面
C.化合物I和Ⅱ反应还可以得到一种酯,该酯的结构简式是
D.化合物I、Ⅱ、Ⅲ均属于芳香族化合物
11.(2024·湖北·一模)某天然活性产物的衍生物结构简式如图所示。下列说法正确的是
A.该物质含有2个手性碳原子
B.1mol该物质最多可以和1molH 发生加成反应
2
C.该物质能发生取代、加成、消去反应
D.该物质的分子式为C H O
10 10 4
12.(2024·湖南·模拟预测)邻苯二甲酰亚胺(分子中所有原子共平面)广泛用于染料、农药医药橡胶、香料
等行业,是许多重要有机精细化学品的中间体。制备原理为:下列说法正确的是
A.反应②是消去反应
B.邻氨甲酰苯甲酸分子含3种官能团
C.1mol邻苯二甲酰亚胺与足量NaOH溶液反应最多可消耗2molNaOH
D.邻苯二甲酰亚胺分子中N原子的杂化类型为sp3杂化
13.(2024·江苏连云港·模拟预测)化合物Z是合成抗肿瘤药物的中间体,其合成路线如下:
下列说法正确的是
A.X中的含氧官能团分别是羟基、氨基、醛基
B.1molY最多能与新制的含 的悬浊液发生反应
C.Z分子与足量的 加成后所得分子中含有3个手性碳原子
D.X、Y、Z可用 溶液和 溶液进行鉴别
14.(2024·广东茂名·三模)儿茶酸具有抗菌、抗氧化作用,常用于治疗烧伤、小儿肺炎等疾病,可采用
如图所示路线合成。下列说法正确的是
A.Y存在二元芳香酸的同分异构体 B.可用酸性 溶液鉴别X和Z
C.X分子中所有原子可能共平面 D.Z与足量的溴水反应消耗
15.(2024·吉林长春·模拟预测)10-羟基喜树碱具有抗癌作用,其结构简式如图。下列有关该化合物的说
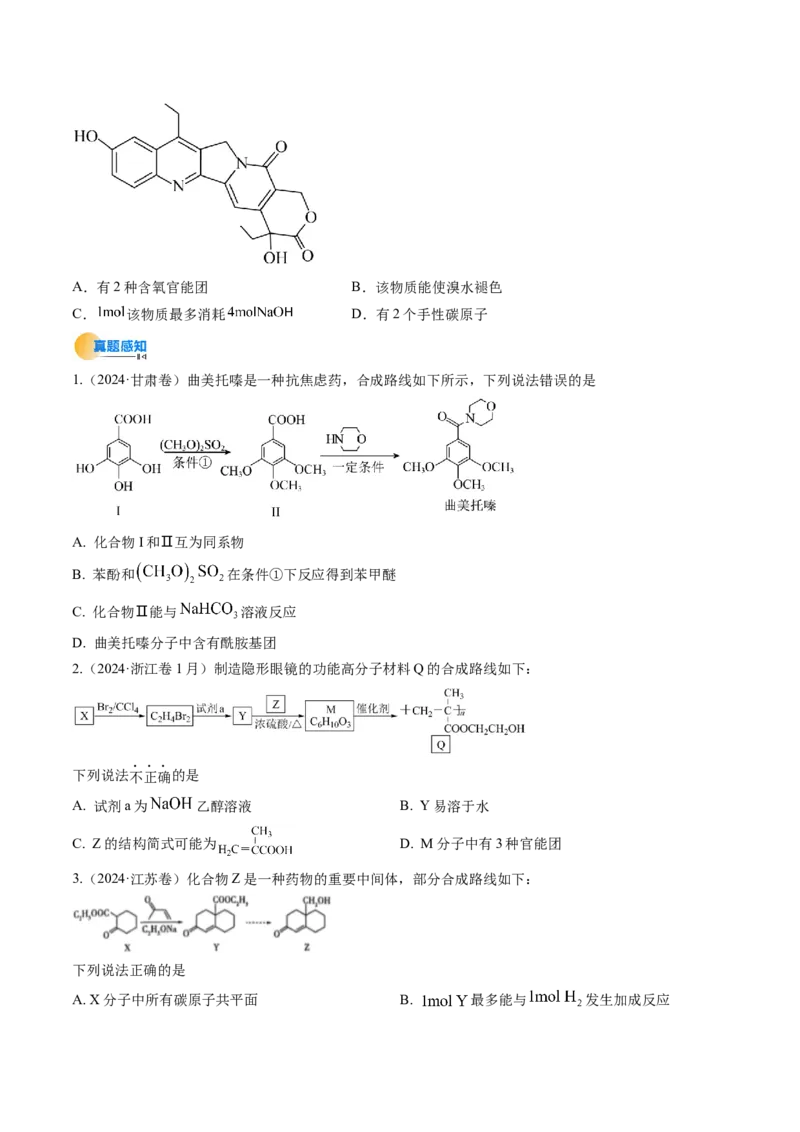
法正确的是A.有2种含氧官能团 B.该物质能使溴水褪色
C. 该物质最多消耗 D.有2个手性碳原子
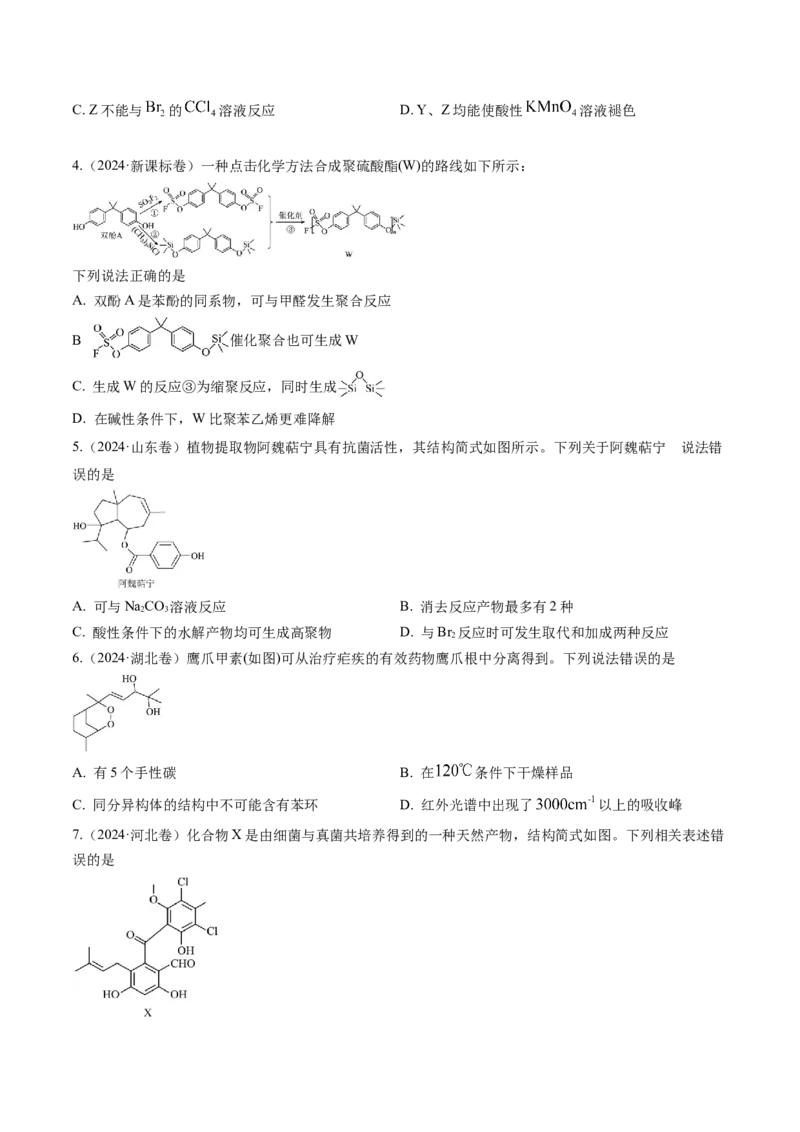
1.(2024·甘肃卷)曲美托嗪是一种抗焦虑药,合成路线如下所示,下列说法错误的是
A. 化合物I和Ⅱ互为同系物
B. 苯酚和 在条件①下反应得到苯甲醚
C. 化合物Ⅱ能与 溶液反应
D. 曲美托嗪分子中含有酰胺基团
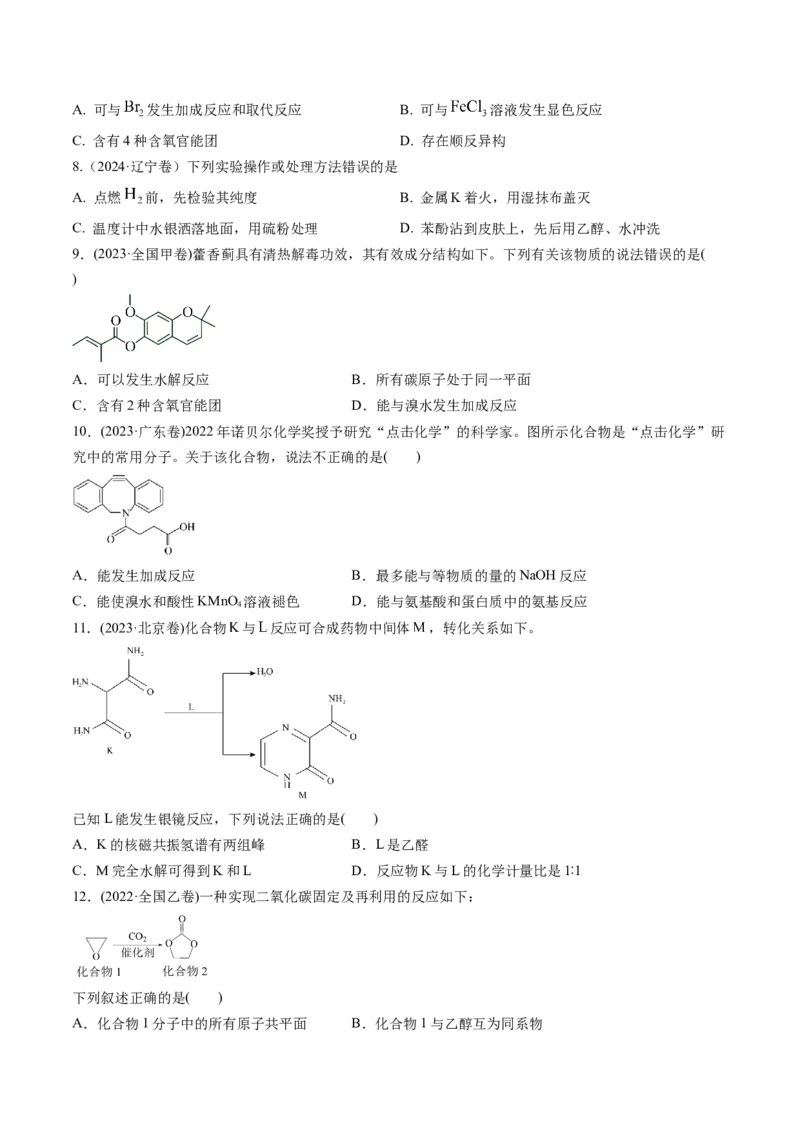
2.(2024·浙江卷1月)制造隐形眼镜的功能高分子材料Q的合成路线如下:
下列说法不正确的是
A. 试剂a为 乙醇溶液 B. Y易溶于水
C. Z的结构简式可能为 D. M分子中有3种官能团
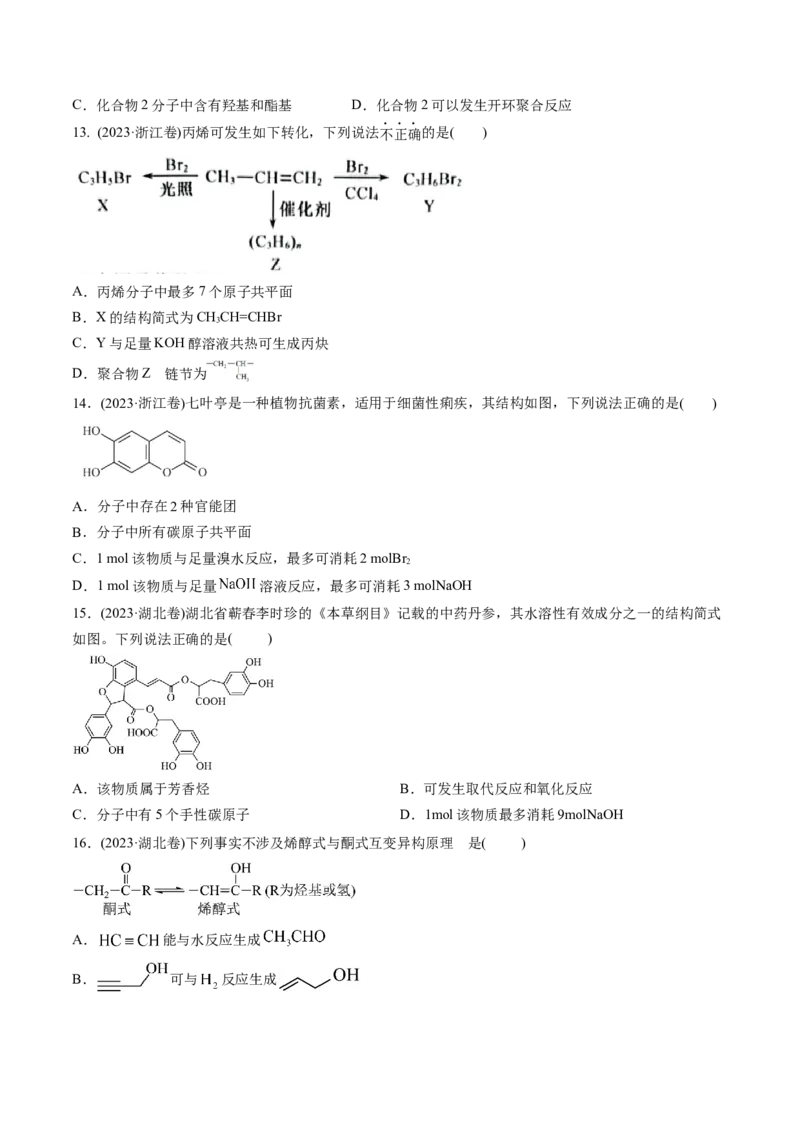
3.(2024·江苏卷)化合物Z是一种药物的重要中间体,部分合成路线如下:
下列说法正确的是
A. X分子中所有碳原子共平面 B. 最多能与 发生加成反应C. Z不能与 的 溶液反应 D. Y、Z均能使酸性 溶液褪色
4.(2024·新课标卷)一种点击化学方法合成聚硫酸酯(W)的路线如下所示:
下列说法正确的是
A. 双酚A是苯酚的同系物,可与甲醛发生聚合反应
.
B 催化聚合也可生成W
C. 生成W的反应③为缩聚反应,同时生成
D. 在碱性条件下,W比聚苯乙烯更难降解
5.(2024·山东卷)植物提取物阿魏萜宁具有抗菌活性,其结构简式如图所示。下列关于阿魏萜宁 说的法错
误的是
A. 可与NaCO 溶液反应 B. 消去反应产物最多有2种
2 3
C. 酸性条件下的水解产物均可生成高聚物 D. 与Br 反应时可发生取代和加成两种反应
2
6.(2024·湖北卷)鹰爪甲素(如图)可从治疗疟疾的有效药物鹰爪根中分离得到。下列说法错误的是
A. 有5个手性碳 B. 在 条件下干燥样品
C. 同分异构体的结构中不可能含有苯环 D. 红外光谱中出现了 以上的吸收峰
7.(2024·河北卷)化合物X是由细菌与真菌共培养得到的一种天然产物,结构简式如图。下列相关表述错
误的是A. 可与 发生加成反应和取代反应 B. 可与 溶液发生显色反应
C. 含有4种含氧官能团 D. 存在顺反异构
8.(2024·辽宁卷)下列实验操作或处理方法错误的是
A. 点燃 前,先检验其纯度 B. 金属K着火,用湿抹布盖灭
C. 温度计中水银洒落地面,用硫粉处理 D. 苯酚沾到皮肤上,先后用乙醇、水冲洗
9.(2023·全国甲卷)藿香蓟具有清热解毒功效,其有效成分结构如下。下列有关该物质的说法错误的是(
)
A.可以发生水解反应 B.所有碳原子处于同一平面
C.含有2种含氧官能团 D.能与溴水发生加成反应
10.(2023·广东卷)2022年诺贝尔化学奖授予研究“点击化学”的科学家。图所示化合物是“点击化学”研
究中的常用分子。关于该化合物,说法不正确的是( )
A.能发生加成反应 B.最多能与等物质的量的NaOH反应
C.能使溴水和酸性KMnO 溶液褪色 D.能与氨基酸和蛋白质中的氨基反应
4
11.(2023·北京卷)化合物 与 反应可合成药物中间体 ,转化关系如下。
已知L能发生银镜反应,下列说法正确的是( )
A.K的核磁共振氢谱有两组峰 B.L是乙醛
C.M完全水解可得到K和L D.反应物K与L的化学计量比是1∶1
12.(2022·全国乙卷)一种实现二氧化碳固定及再利用的反应如下:
下列叙述正确的是( )
A.化合物1分子中的所有原子共平面 B.化合物1与乙醇互为同系物C.化合物2分子中含有羟基和酯基 D.化合物2可以发生开环聚合反应
13. (2023·浙江卷)丙烯可发生如下转化,下列说法不正确的是( )
A.丙烯分子中最多7个原子共平面
B.X的结构简式为CHCH=CHBr
3
C.Y与足量KOH醇溶液共热可生成丙炔
D.聚合物Z 的链节为
14.(2023·浙江卷)七叶亭是一种植物抗菌素,适用于细菌性痢疾,其结构如图,下列说法正确的是( )
A.分子中存在2种官能团
B.分子中所有碳原子共平面
C.1 mol该物质与足量溴水反应,最多可消耗2 molBr
2
D.1 mol该物质与足量 溶液反应,最多可消耗3 molNaOH
15.(2023·湖北卷)湖北省蕲春李时珍的《本草纲目》记载的中药丹参,其水溶性有效成分之一的结构简式
如图。下列说法正确的是( )
A.该物质属于芳香烃 B.可发生取代反应和氧化反应
C.分子中有5个手性碳原子 D.1mol该物质最多消耗9molNaOH
16.(2023·湖北卷)下列事实不涉及烯醇式与酮式互变异构原理 是的( )
A. 能与水反应生成
B. 可与 反应生成C. 水解生成
D. 中存在具有分子内氢键的异构体
17.(2023·山东卷)有机物 的异构化反应如图所示,下列说法错误的是( )
A.依据红外光谱可确证X、Y存在不同的官能团
B.除氢原子外,X中其他原子可能共平面
C.含醛基和碳碳双键且有手性碳原子的Y的同分异构体有4种(不考虑立体异构)
D.类比上述反应, 的异构化产物可发生银镜反应和加聚反应
18.(2023·辽宁卷)冠醚因分子结构形如皇冠而得名,某冠醚分子c可识别 ,其合成方法如下。下列说
法错误的是( )
A.该反应为取代反应 B.a、b均可与 溶液反应
C.c核磁共振氢谱有3组峰 D.c可增加 在苯中 的溶解度
19.(2022·浙江省1月选考,6)下列说法不正确的是( )
A.液化石油气是纯净物 B.工业酒精中往往含有甲醇
C.福尔马林是甲醛的水溶液 D.许多水果和花卉有芳香气味是因为含有酯
20.(2022·江苏卷)精细化学品Z是X与HBr反应的主产物,X→Z的反应机理如下:
下列说法不正确的是( )
A.X与 互为顺反异构体
B.X能使溴的CCl 溶液褪色
4C.X与HBr 反应有副产物生成
D.Z分子中含有2个手性碳原子
21.(2022·湖北卷)莲藕含多酚类物质,其典型结构简式如图所示。下列有关该类物质的说法错误的是
( )
A.不能与溴水反应 B.可用作抗氧化剂
C.有特征红外吸收峰 D.能与 发生显色反应
22.(2022·山东卷) 崖柏素具天然活性,有酚的通性,结构如图。关于 崖柏素的说法错误的是( )
A.可与溴水发生取代反应
B.可与NaHCO 溶液反应
3
C.分子中的碳原子不可能全部共平面
D.与足量H 加成后,产物分子中含手性碳原子
2
23.(2022·浙江卷)染料木黄酮的结构如图,下列说法正确的是( )
A.分子中存在3种官能团
B.可与HBr反应
C.1 mol该物质与足量溴水反应,最多可消耗4 mol Br
2
D.1 mol该物质与足量NaOH溶液反应,最多可消耗2 mol NaOH
24.(2022·福建卷)络塞维是中药玫瑰红景天中含有的一种天然产物,分子结构见下图。关于该化合物下列
说法正确的是( )
A.不能发生消去反应 B.能与醋酸发生酯化反应
C.所有原子都处于同一平面 D.1mol络塞维最多能与3 molH 反应
225.(2022·重庆卷)关于M的说法正确的是( )
A.分子式为C H O B.含三个手性碳原子
12 16 6
C.所有氧原子共平面 D.与(CH)C=O互为同系物
3 2
26.(2022·全国甲卷)辅酶Q 具有预防动脉硬化的功效,其结构简式如下。下列有关辅酶Q 的说法正确的
10 10
是( )
A.分子式为C H O B.分子中含有14个甲基
60 90 4
C.分子中的四个氧原子不在同一平面 D.可发生加成反应,不能发生取代反应