文档内容
考点巩固卷 05 物质结构与性质 元素周期律(一)
——原子结构与性质 元素周期表、元素周期律
考点01原子结构与性质 考法01原子结构 同位素
(限时:15 min) 考法02核外电子排布与运动状态
考法01元素周期表的结构与分区
考法02原子结构与元素周期表的关系
考点02 元素周期表、元素周期律 考法03元素周期律及元素的性质
(限时:25min) 考法04电离能、电负性的比较与应用
考法05 元素周期律(表)的应用
考法06元素推断的综合考查
考点01 原子结构与性质
考法01 原子结构 同位素
1.(2024·湖南长沙期中)金属钛有“生物金属”之称。下列有关 和 的说法正确的是( )
❑
48Ti
❑
50Ti
22 22
A. 和 中均含有22个中子
❑
48Ti
❑
50Ti
22 22
B. 和 互为同位素,在元素周期表中的位置相同
❑
48Ti
❑
50Ti
22 22
C. 和 的化学性质不同
❑
48Ti
❑
50Ti
22 22
D. 和 为同一核素
❑
48Ti
❑
50Ti
22 22
2.人工合成 的过程可表示为 ,下列叙述中正确的是( )
Cn ❑ 70Zn+❑ 208Pb→ 277Cn+❑ 1n
30 82 112 0
1
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司A. ❑
277Cn的原子核内中子数比质子数多53
112
B. Cn元素的相对原子质量为277
C. ❑
208Pb的中子数比❑ 70Zn的中子数多138
82 30
D. Cn元素位于元素周期表的第六周期,是副族元素
3.某元素(X)构成的双原子单质分子有三种,其相对分子质量分别为158、160、162,在天然单质中,这
三种单质的物质的量之比为1∶1∶1,由此推断以下结论正确的是( )
A.此元素有3种不同的同位素
B.其中一种同位素质量数为80
C.其同位素79X占原子总数的
D.单质X 的平均相对分子质量为162
2
4.医学界通过用14C标记的C 发现了一种C 的羧酸衍生物,这种羧酸衍生物在特定条件下可以通过断裂
60 60
DNA抑制艾滋病毒的繁殖。下列有关14C的叙述正确的是( )
A.与12C 的碳原子化学性质不同
60
B.与14N含的中子数相同
C.14C 是12C 的同素异形体
60 60
D.与12C互为同位素
5.X、Y、Z和R分别代表4种元素。如果❑ Xm+ 、❑ Yn+ 、❑ Zn−、❑ Rm−4种离子的电子层结构相同
a b c d
(a、b、c、d为元素的原子序数),则下列关系正确的是( )
A. a−c=m−n B. a−b=n−m C. c−d=m+n D. b−d=n+m
考法02 核外电子排布与运动状态
6.(2024·安徽阜阳月考)下列几种表示电子排布的方法中正确的是( )
A. 基态❑ Ge原子的核外电子排布式:4s24 p2
32
B. 基态❑ Cr原子的价层电子排布式:
24
1s22s22p63s23p63d44s2
O
C. 原子的电子排布图:
D. 基态F−的电子排布式:1s22s23p6
7.下列原子的电子跃迁能释放光能形成发射光谱的是( )
A.1s22s22p63s2―→1s22s22p63p2
B.1s22s22p33s1―→1s22s22p4
2
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司C.1s22s2―→1s22s12p1
D.1s22s22p―→1s22s22p
8.下列有关电子排布图的表述正确的是( )
A. 可表示单核10电子粒子基态时电子排布
B. 违背了泡利原理
C. 表示基态N原子的价电子排布
D. 表示处于激发态的B的电子排布图
9.下列各组表述中,两个原子不属于同种元素原子的是( )
A.3p能级有一个空轨道的基态原子和核外电子的排布式为1s22s22p63s23p2的原子
B.2p能级无空轨道,且有一个未成对电子的基态原子和原子的最外层电子排布式为2s22p5的原子
C.M层全充满而N层为4s2的原子和核外电子排布式为1s22s22p63s23p64s2的原子
D.最外层电子数是核外电子总数的原子和最外层电子排布式为4s24p5的原子
10.(2023·石家庄模拟)下列有关电子排布式或排布图的结论错误的是( )
考点02 元素周期表、元素周期律
考法01 元素周期表的结构与分区
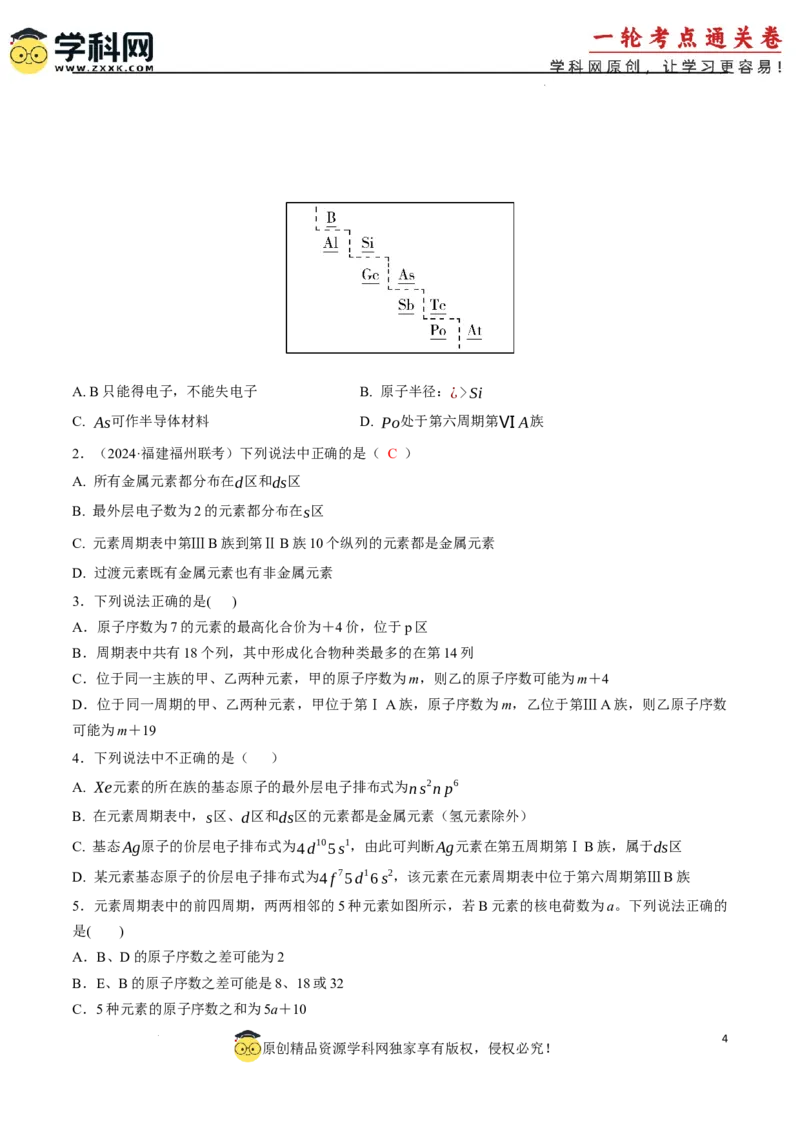
1.部分元素在周期表中的分布如图所示(虚线为金属元素与非金属元素的分界线),下列说法中不正确
的是( )
3
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司A. B只能得电子,不能失电子 B. 原子半径:¿>Si
C. As可作半导体材料 D. Po处于第六周期第ⅥA族
2.(2024·福建福州联考)下列说法中正确的是( C )
A. 所有金属元素都分布在d区和ds区
B. 最外层电子数为2的元素都分布在s区
C. 元素周期表中第ⅢB族到第ⅡB族10个纵列的元素都是金属元素
D. 过渡元素既有金属元素也有非金属元素
3.下列说法正确的是( )
A.原子序数为7的元素的最高化合价为+4价,位于p区
B.周期表中共有18个列,其中形成化合物种类最多的在第14列
C.位于同一主族的甲、乙两种元素,甲的原子序数为m,则乙的原子序数可能为m+4
D.位于同一周期的甲、乙两种元素,甲位于第ⅠA族,原子序数为m,乙位于第ⅢA族,则乙原子序数
可能为m+19
4.下列说法中不正确的是( )
A. Xe元素的所在族的基态原子的最外层电子排布式为ns2np6
B. 在元素周期表中,s区、d区和ds区的元素都是金属元素(氢元素除外)
C. 基态Ag原子的价层电子排布式为4d105s1,由此可判断Ag元素在第五周期第ⅠB族,属于ds区
D. 某元素基态原子的价层电子排布式为4f75d16s2,该元素在元素周期表中位于第六周期第ⅢB族
5.元素周期表中的前四周期,两两相邻的5种元素如图所示,若B元素的核电荷数为a。下列说法正确的
是( )
A.B、D的原子序数之差可能为2
B.E、B的原子序数之差可能是8、18或32
C.5种元素的原子序数之和为5a+10
4
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司D.A、E的原子序数之差可能是7
考法02 原子结构与元素周期表的关系
6.第114号和第116号元素的名称缩写为Fl、Lv。下列有关这两种元素的说法错误的是( )
A.两种元素位于同一周期,均属于p区
B.116号元素价层电子排布式为7s27p4
C.两种元素都是活泼的非金属元素
D.114号元素的原子半径比116号元素的原子半径大
7.元素周期表完美地将元素的结构、位置与性质结合在一起,根据元素的原子序数就能推断出该元素在
周期表中的位置,进而推断出该元素原子的结构和性质。下列关于33号元素的说法正确的是( )
A.该元素位于d区
B.该元素为金属元素
C.该元素位于第四周期第ⅢA族
D.该元素基态原子的电子排布式为1s22s22p63s23p63d104s24p3
8.(2024·福建三明一中月考)下列关于原子核外电子排布与元素在周期表中位置关系的表述正确的是( )
A.原子的价层电子排布式为ns2np6的元素一定是主族元素
B.基态原子的p能级上有5个电子的元素一定是第ⅦA族元素
C.原子的价层电子排布式为3d3~74s2的元素一定位于第ⅢB~ⅦB族
D.基态原子的N层上只有1个电子的元素一定是主族元素
9.周期表中27号元素钴的方格中注明“3d74s2”,由此可以推断( )
A.它位于周期表的第四周期ⅡA族
B.它的基态核外电子排布式可简写为[Ar]4s2
C.Co2+的核外价层电子排布式为3d54s2
D.Co位于周期表中第9列,属于d区
10.现有部分元素的原子结构特点如表:
X L层电子数是K层电子数的3倍
Y 核外电子层数等于原子序数
Z L层电子数是K层和M层电子数之和
W 共用三对电子形成双原子分子,常温下为气体单质
下列叙述中正确的是( )
5
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司W
A. 原子的结构示意图为
B. X和Y只能形成原子个数之比为1:2的化合物
C. X的非金属性比Z强
D. X、Y、Z、W四种元素不能形成离子化合物
考法03 元素周期律及元素的性质
11.下列各组粒子中按半径由大到小排列的是( )
A.O、Cl、S、P
B.Al3+、Mg2+、Ca2+、Ba2+
C.K+、Mg2+、Al3+、H+
D.Li、Na、K、Cs
12.根据下表(部分短周期元素的原子半径及主要化合价)信息,下列叙述正确的是 ( )
元素代号 A B C D E
原子半径/nm 0.186 0.143 0.089 0.104 0.074
主要化合价 +1 +3 +2 +6、-2 -2
A.E2-与B3+的核外电子数不可能相等
B.离子半径:B3+<A+<D2-
C.最高价氧化物对应水化物的碱性:A<C
D.氢化物的稳定性:D>E
13.下列关于金属性、非金属性强弱判断不正确的是( )
A.2C+SiO=====2CO↑+Si,说明非金属性:C>Si
2
B.同浓度下碱性:KOH>Mg(OH) ,说明金属性:K>Mg
2
C.氟气与氢气在暗处相遇就会爆炸,氯气与氢气混合在光照或点燃时发生爆炸,说明非金属性:F>Cl
D.氧化性:Cu2+>Na+,说明金属性:Na>Cu
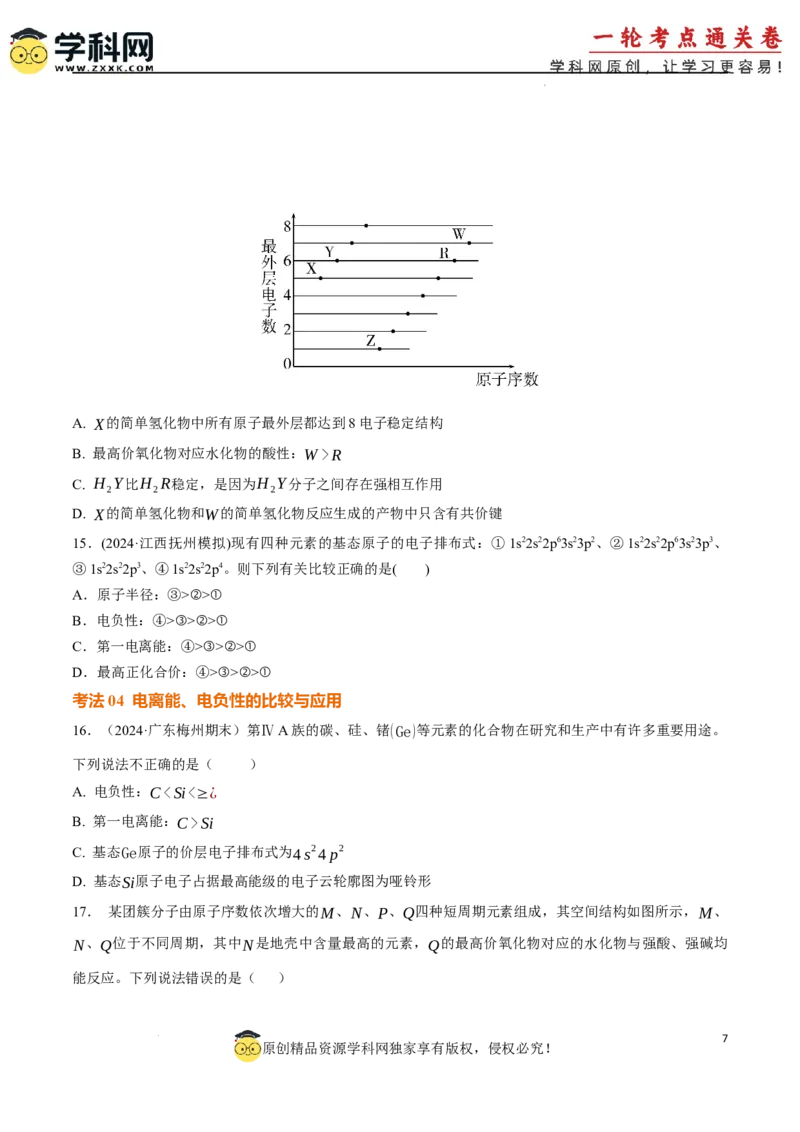
14.(2024·福建厦门期中)部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系如图所
示。下列说法中正确的是( )
6
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司A. X的简单氢化物中所有原子最外层都达到8电子稳定结构
B. 最高价氧化物对应水化物的酸性:W>R
C. H Y比H R稳定,是因为H Y分子之间存在强相互作用
2 2 2
D. X的简单氢化物和W的简单氢化物反应生成的产物中只含有共价键
15.(2024·江西抚州模拟)现有四种元素的基态原子的电子排布式:①1s22s22p63s23p2、②1s22s22p63s23p3、
③1s22s22p3、④1s22s22p4。则下列有关比较正确的是( )
A.原子半径:③>②>①
B.电负性:④>③>②>①
C.第一电离能:④>③>②>①
D.最高正化合价:④>③>②>①
考法04 电离能、电负性的比较与应用
16.(2024·广东梅州期末)第ⅣA族的碳、硅、锗(Ge)等元素的化合物在研究和生产中有许多重要用途。
下列说法不正确的是( )
A. 电负性:CSi
C. 基态Ge原子的价层电子排布式为4s24 p2
D. 基态Si原子电子占据最高能级的电子云轮廓图为哑铃形
17. 某团簇分子由原子序数依次增大的M、N、P、Q四种短周期元素组成,其空间结构如图所示,M、
N、Q位于不同周期,其中N是地壳中含量最高的元素,Q的最高价氧化物对应的水化物与强酸、强碱均
能反应。下列说法错误的是( )
7
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司A. 通常情况下M N比M N 更稳定
2 2 2
B. M、N、P组成的化合物中含离子键和共价键
C. P和Q能形成密度小、硬度大的合金材料
D. 元素的第一电离能:P
Si,则 SiHCl 充分水解的化学方程式为 3 ____________________________。 (2)氮杂氟硼二吡咯具有作为光动力学治疗(PDT)光敏剂的潜能,结构如图所示,该分子中所有元素的电负 性由大到小的顺序为____________________(用元素符号表示)。 20. (2024·湖南邵阳模拟)(1)Fe和Cu的部分电离能数据如下: 元素 Fe Cu 第一电离能I/( kJ·mol-1) 759 756 1 第二电离能I/( kJ·mol-1) 1561 1958 2 I(Cu)大于I(Fe)的主要原因是__________________________________________。 2 2 (2)Al 、 Si 、 P 和 S 的 第 一 电 离 能 由 小 到 大 的 顺 序 为 ____________ , 判 断 的 依 据 是 __________________________________________。 (3)Ga、As、Se三种元素的第一电离能由大到小的顺序为__________________。 (4)现有铜、锌元素的相应状态如下: ①锌:[Ar]3d104s2 ②锌:[Ar]3d104s1 8 原创精品资源学科网独家享有版权,侵权必究! 学科网(北京)股份有限公司③铜:[Ar]3d104s1 ④铜:[Ar]3d10 失去1个电子需要的能量由大到小排序是____________。 A.④②①③ B.④②③① C.①②④③ D.①④③② 考法05 元素周期律(表)的应用 21.Rb是第五周期第ⅠA族元素,下列关于 Rb的说法不正确的是( ) 37 A.中子数为50的Rb的核素:Rb B.元素的金属性:Rb>K C.与同周期元素 I的原子半径:ISi 2 3 C.硅、锗都位于金属元素与非金属元素的交界处,都可用作半导体材料 D.Be与Al在周期表中处于对角线位置,可推出:Be(OH) +2OH-===BeO+2HO 2 2 23.应用元素周期律可预测我们不知道的一些元素及其化合物的性质。下列预测正确的是( ) ①铍(Be)的氧化物对应的水化物可能具有两性 ②铊(Tl)能与稀盐酸和NaOH溶液反应,且均产生氢气 ③砹(At)单质为有色固体,AgAt不溶于水也不溶于稀硝酸 ④硫酸锶 可能是难溶于水的白色固体 (SrSO ) 4 ⑤硒化氢 无色,有毒,比 稳定 (H Se) H S 2 2 A. ①②③ B. ①③④ C. ①③⑤ D. ②④⑤ 24.[2023·福建莆田期中]四种短周期元素在周期表中的位置如图所示,X、Y的核外电子数之和等于W的 核外电子数。下列说法不正确的是( ) X Y Z W A. X、Y、Z三种元素的最高正价依次增大 B. Y、Z形成的简单氢化物,后者稳定性强 C. Y、Z形成的简单阴离子,后者半径小 9 原创精品资源学科网独家享有版权,侵权必究! 学科网(北京)股份有限公司D. 工业上用电解W和Z形成的化合物制备单质W 25. 由下列实验及相应事实推理所得的结论,不能用元素周期律解释的是( ) 选项 实验 事实 结论 将形状、大小相同的Na和 K与HO反应更剧 2 A 金属性:K>Na K分别投入冷水 烈 将足量硫酸与NaPO 溶液混 3 4 B 生成HPO 非金属性:S>P 3 4 合 分别加热HCl气体和HI气 C HI气体更易分解 稳定性:HCl>HI 体 SiO+2C=====Si 2 D 用焦炭还原石英砂制得粗硅 非金属性:C>Si +2CO↑ 考法06 元素推断的综合考查 26.(2024·山东聊城一模)短周期主族元素W、X、Y、Q的原子序数依次增大。W、X原子的最外层电 子数之和为6,且符合核反应: ; 原子中 电子与 电子的数目相同, 的 ❑ 9W+❑ 4He→ A X+❑ 1n Y s p Q Z 2 Z+2 0 原子序数等于X原子序数的2倍。下列说法正确的是( ) A. 电负性:Q>Y>X>W B. X的最高价氧化物对应的水化物属于强酸 C. 原子半径:W>X>Y>Q D. 单质Q与X的最高价氧化物可以发生反应 27. 一种用于合成治疗免疫疾病药物的结构如图所示,其中X、Y、Z、Q、W为1∼20号元素且原子序 数依次增大,Z与Q同主族,Q和W的简单离子具有相同的电子层结构。下列叙述正确的是( ) A. 第一电离能:Q>Z>W B. 电负性:X>Y>Z C. WZX与WXQ均是强电解质,在水溶液中可以发生反应 D. W Q Z 与X QZ 溶液反应生成黄色浑浊和无色气体的反应不属于氧化还原反应 2 2 3 2 4 28.(2024·湖北卷)主族元素W、X、Y、Z原子序数依次增大,X、Y的价电子数相等,Z的价电子所在 10 原创精品资源学科网独家享有版权,侵权必究! 学科网(北京)股份有限公司能层有16个轨道,4种元素形成的化合物如图。下列说法正确的是 A.电负性: B.酸性: C.基态原子的未成对电子数: D.氧化物溶于水所得溶液的 29.(2024·全国甲卷)W、X、Y、Z为原子序数依次增大的短周期元素。W和X原子序数之和等于 的 核外电子数,化合物 可用作化学电源的电解质。下列叙述正确的是 A.X和Z属于同一主族 B.非属性: C.气态氢化物的稳定性: D.原子半径: 30.(2023·广东卷)化合物XYZ ME 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅 4 4 有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为nsn−1,X与M同周期, E在地壳中含量最多。下列说法正确的是( ) A. 元素电负性:E>Y>Z B. 氢化物沸点:M>Y>E C. 第一电离能: D. 和 的空间结构均为三角锥形 X>E>Y YZ YE− 3 3 11 原创精品资源学科网独家享有版权,侵权必究! 学科网(北京)股份有限公司