文档内容
解密 11 非金属及其化合物
一、单选题
1.(2023春·青海西宁·高三统考开学考试)关于非金属元素及其化合物,下列说法正确的
是
A.氯原子最外层电子数为7,所以Cl 只具有氧化性
2
B.SO 、HClO的水溶液都具有漂白性,漂白原理也相同
2
C.制备酸性KMnO 溶液时,通常用硫酸酸化
4
D.将CO 或SO 通入Ba(NO ) 溶液中,均无沉淀生成
2 2 3 2
2.(2023·全国·高三专题练习)将KCl和KBr混合物13.4g溶于水配成500mL溶液,通入
过量Cl,反应后将溶液蒸干得固体11.175g,则原所配溶液中K+、Cl—、Br—的物质的量浓
2
度之比为
A.3:2:1 B.1:2:3 C.1:3:2 D.3:1:1
3.(2023·江苏·统考一模)氨、氮、硫的化合物应用广泛。ClO (分子空间填充模型为
2
)。NaClO等含氯消毒剂可用于杀菌消毒。人工固氮可将N 转化为NH ,再进一步制
2 3
备肼(N H)、硝酸、铵盐等化合物,肼和偏二甲肼(C HN)常用作火箭燃料,肼的燃烧热为
2 4 2 8 2
622.08 kJ·mol-1,H S可除去废水中Hg2+等重金属禹子,HS 水溶液在空气中会缓慢氧化生成
2 2
S而变诨浊。下列物质的性质与用途具有对应关系的是
A.HS具有还原性,可除去废水中的Hg2+
2
B.HNO 具有强氧化性,可用于制NH NO
3 4 3
C.NH Cl溶液呈酸性,可用于去除铁锈
4
D.NaClO 溶液呈碱性,可用于杀菌消毒
4.(2022秋·内蒙古兴安盟·高三乌兰浩特一中校考期中)下列有关氧化物的说法正确的是
A.ClO 具有氧化性,常用于饮用水的消毒杀菌
2
B.SO 会导致硫酸型酸雨,酸雨是pH<7的酸性降水
2
C.NO 与水反应生成HNO,NO 是酸性氧化物
2 3 2
D.SiO 与NaOH溶液反应,盛放NaOH溶液不能使用玻璃试剂瓶
2
5.(2022秋·江西赣州·高三校联考期中)在指定条件下,下列含氮化合物间的转化能一步
实现的是
A. B.
C.稀 D.
6.(2023·广东广州·统考二模)某小组同学用下图装置验证 的性质,培养皿中①、②、
③三个塑料瓶盖内盛有不同物质。向 固体上滴加适量稀 ,迅速用玻璃片将培养皿盖严,实验记录如下。下列说法不正确的是
瓶
实验装置 物质 实验现象
盖
① 酸性 溶液 紫色褪去
② 蘸有品红溶液的棉花 红色褪去
③ 蒸馏水 无明显变化
A.产生 的离子方程式:
B.瓶盖①中的实验现象证明 具有还原性
C.瓶盖②中的实验现象证明 具有漂白性
D.瓶盖③中的实验现象证明 和水不反应
7.(2023·全国·高三专题练习)硅是组成无机非金属材料的一种主要元素,下列有关硅的
化合物的叙述错误的是
A.氮化硅陶瓷是一种新型无机非金属材料,氮化硅的化学式为
B.碳化硅 的硬度大,熔点高,可用于制作高温结构陶瓷和轴承
C.光导纤维是一种新型无机非金属材料,其主要成分为
D.氮化硅、氧化铝、碳化硅和二氧化锆都可作为制高温结构陶瓷的材料
8.(2023·全国·高三专题练习)工业上以石英砂为原料制取单质硅,其工艺流程图如下:
流程一:
流程二:
有关反应分类说法不正确的是
A.①~⑥均属于氧化还原反应 B.只有①②③属于置换反应
C.⑥既属于氧化还原反应又属于分解反应 D.⑤中的两个化学反应均属于复分解反应
二、填空题
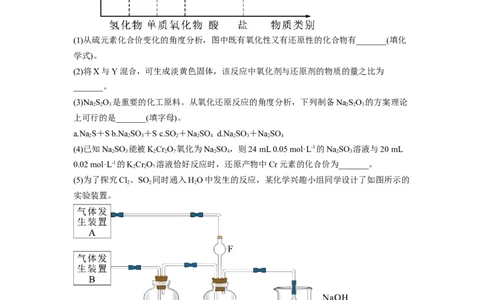
9.(2022秋·河北衡水·高三河北深州市中学校考阶段练习)利用元素的化合价推测物质的
性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有_______(填化
学式)。
(2)将X与Y混合,可生成淡黄色固体,该反应中氧化剂与还原剂的物质的量之比为
_______。
(3)Na SO 是重要的化工原料。从氧化还原反应的角度分析,下列制备NaSO 的方案理论
2 2 3 2 2 3
上可行的是_______(填字母)。
a.Na S+S b.Na SO +S c.SO +NaSO d.Na SO +NaSO
2 2 3 2 2 4 2 3 2 4
(4)已知NaSO 能被KCr O 氧化为NaSO ,则24 mL 0.05 mol·L-1的NaSO 溶液与20 mL
2 3 2 2 7 2 4 2 3
0.02 mol·L-1的KCr O 溶液恰好反应时,还原产物中Cr元素的化合价为_______。
2 2 7
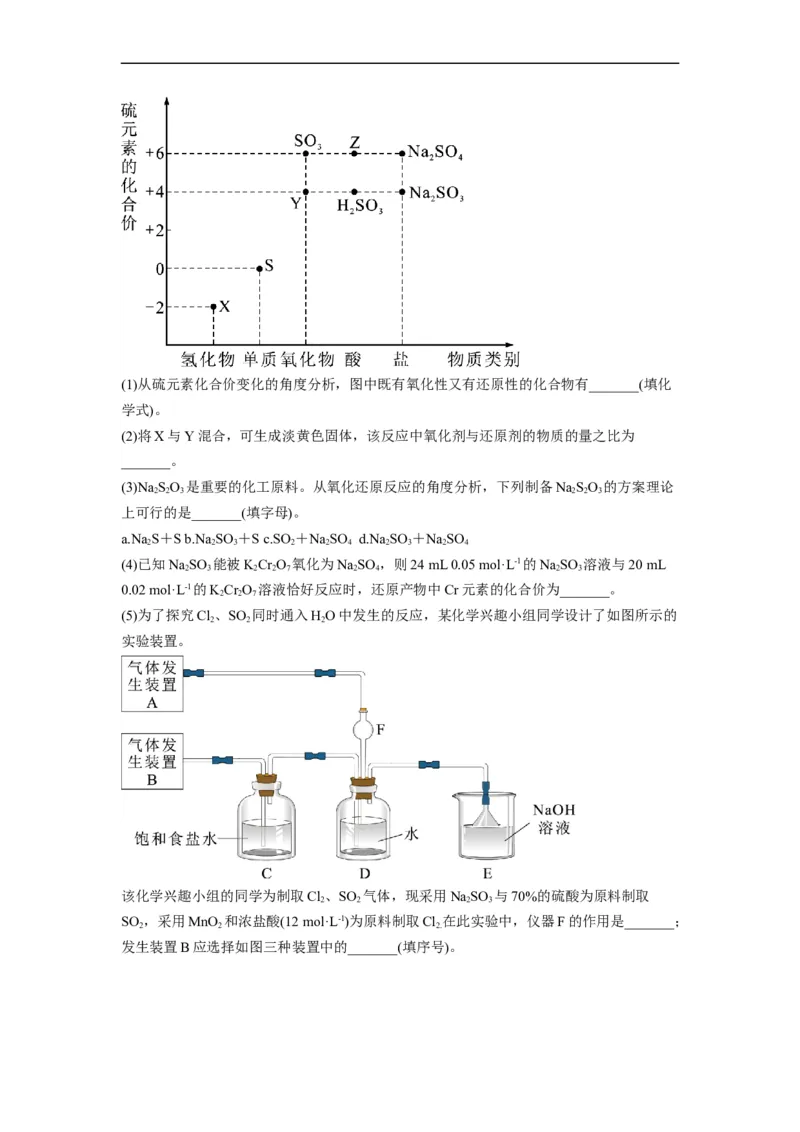
(5)为了探究Cl、SO 同时通入HO中发生的反应,某化学兴趣小组同学设计了如图所示的
2 2 2
实验装置。
该化学兴趣小组的同学为制取Cl、SO 气体,现采用NaSO 与70%的硫酸为原料制取
2 2 2 3
SO ,采用MnO 和浓盐酸(12 mol·L-1)为原料制取Cl 在此实验中,仪器F的作用是_______;
2 2 2.
发生装置B应选择如图三种装置中的_______(填序号)。10.(2022秋·河南信阳·高三统考阶段练习)氮、硫、氯是重要的非金属元素,根据所学
知识及题设信息按要求完成下列相关问题。
(1)偏二甲肼( )作为火箭的燃料,与 混合燃烧,放出巨大能量,从而把火箭送入
太空。已知反应产物全部是稳定的气态物质,反应中被氧化的氮原子和被还原的氮原子个
数比为_______。
(2)氨气作为极易溶于水的气体,在进行相关实验时,必须考虑防倒吸问题,下列可有效防
倒吸的是_______(填序号)。
A.导气管末端连接倒扣于烧杯的漏斗且漏斗下端不与水接触
B.烧杯中盛放水和苯,导气管口伸入到下层
C.向装置内通入氮气,使氮气和氨气的混合气经导管通入水中
(3) 的制备方法之一是将纯碱和水按一定比例搅拌均匀,待生成块状
时,放入反应器内,块与块之间保持一定的空隙,然后通入 ,反应完全即得。则该制
备反应的化学方程式为_______。
(4)向硫化钠溶液中通入足量的 充分反应后,溶液显酸性并有黄色浑浊,其反应离子方
程式为_______。
(5)卤素离子的检验方法有银盐沉淀法、氧化萃取法等。已知某溶液中的阴离子只有氯离子
和硫酸根离子,现需检验氯离子的存在,则需使用的试剂名称为_______。
(6)卤族元素主要从海洋中获取。海水提溴是常用的获取溴的方法,提溴过程中,浓缩后的
海水中通入足量的氧气后,再通入_______,将溴单质吹入盛有二氧化硫水溶液的吸收塔内
转化成氢溴酸,再向吸收塔内通入适量的氧气后,用四氧化碳萃取吸收塔中的溴单质。两
次通入氯气将溴离子氧化成溴单质操作的目的是_______。
一、单选题
1.(2023·浙江·统考高考真题)下列关于元素及其化合物的性质说法正确的是
A.预热的铁丝能在氯气中燃烧,生成棕褐色的烟雾B.工业上用 和 制备NaOH
C.硫酸工业中常用铁触媒做催化剂
D.工业上用浓氨水检验 管道是否泄漏
2.(2023秋·河北·高三统考期末)利用下图装置分别进行实验,对丙中实验现象描述错误
的是
试剂及现
象 甲 乙 丙 丙中实验现象
选项
饱和食盐 溴的四氯化碳溶
A 电石 溶液逐渐褪色
水 液
氢氧化 先生成蓝色沉淀,后沉淀消
B 浓氨水 硫酸铜溶液
钠 失
二氧化 酸化的KI淀粉溶
C 双氧水 溶液变蓝
锰 液
D 稀硫酸 碳酸钠 饱和碳酸钠溶液 先有沉淀生成,后沉淀消失
A.A B.B C.C D.D
3.(2022秋·黑龙江牡丹江·高三牡丹江市第三高级中学校考阶段练习)下列关于卤素(用
X表示)的叙述,错误的是
A. 的还原性依次为
B. 都极易溶于水,它们的热稳定性随X的核电荷数的增加而减小
C.卤素单质的颜色由 随相对分子质量增大而变深
D.卤素单质与水反应均可用 表示
4.(2023·江苏南通·统考一模) 易液化,能与多种物质发生反应,将金属钠投入液氨中有 产生, 能与 合生成 ,加热条件下 能将CuO还原成Cu。
下列说法正确的是
A. 分子中的H-N-H键角为120°
B. 与 反应生成的白烟成分为
C.金属钠与液氨反应体现了 的还原性
D. 易液化是由于 与 分子间形成氢键
5.(2023·安徽合肥·统考一模)下表中各组物质不能按照如图所示的转化关系一步实现的
是
选项 X Y Z
A
B Fe
C
D NO
A.A B.B C.C D.D
6.(2023·山东·日照一中校联考模拟预测) 都是大气污染物,下列说法正
确的是
A.都能使品红试液褪色,原理相同
B.将 、 同时通入水中,加入 有白色沉淀生成
C.等物质的量的 和 混合通入装有湿润的有色布条的试管中,漂白效果更好
D.都能与水反应,生成物都是电解质
7.(2023·湖南衡阳·高三衡阳市一中校考阶段练习)二氧化硫催化氧化生成三氧化硫的过
程是无机基础化工的重要催化过程,目前各国工业上用于 催化氧化的是钒系催化剂。
如图是实验室模拟制取三氧化硫的装置图:已知:二氧化硫催化氧化生成三氧化硫,可认为分成两步进行。
①
②……
总反应:
下列说法错误的是
A.浓硫酸的作用是与亚硫酸钠反应制取二氧化硫
B.若将烧杯中的NaOH溶液换成澄清石灰水也可以充分吸收尾气
C.冰盐浴的作用是冷凝三氧化硫
D.反应②为
8.(2023·安徽·统考一模)2022年11月30日,神舟十五号载人飞船入轨后,于11月30
日5时42分,成功对接于空间站“天和”核心舱前向端口。化学作为一门传统的理科,在
神舟飞船的研制过程中不可缺少。下列说法错误的是
A.火箭采用的高强度新型钛合金构件属于金属材料
B.使用的热控材料是新型保温材料——纳米气凝胶,纳米气凝胶具有丁达尔效应
C.“天和”核心舱其腔体使用的氮化硼陶瓷属于无机非金属材料
D.核心舱搭载的柔性太阳能电池,二氧化硅是太阳能电池板的核心材料
9.(2023春·广东广州·高三广州市第二中学校联考开学考试)证据推理是化学学科重要的
核心素养。下列实验操作、现象及相应结论都正确的是
实验操作 实验现象 实验结论
向2mL 0.1mol/L KI(aq)中加入1mL 0.1mol/L 四氯化碳层显紫
I-和Fe3+的反应存
A FeCl (aq),充分反应,用四氯化碳充分萃取后取 色,上层溶液试
3
在限度
上层溶液滴加KSCN(aq) 样变红
取适量火柴头的浸泡液于试管中,滴加AgNO 火柴头不含氯元
3
B 无白色沉淀
溶液和稀HNO 素
3
C 向CH 2 =CHCHO中滴加溴水 溴水褪色 CH 2 =CHCHO中含醛基
D 在某透明溶液中通入足量CO 产生白色沉淀
2 原溶液中含
A.A B.B C.C D.D
10.(2023·安徽·统考一模)下列化学反应的离子方程式正确的是
A.向硫酸铝溶液中滴加碳酸钠溶液:
B.用氨水吸收少量的二氧化硫:
C.Fe与稀硝酸反应,当 时:
D.向 溶液中逐滴加入 溶液至 恰好完全沉淀:
二、填空题
11.(2022·上海)硅是重要的半导体材料,构成现代电子工业的基础。硅及其化合物在工
业中应用广泛,在国防和航天工业中亦有许多用途。
(1)硅原子中最外层电子排布式为___,该层电子的电子云有___种不同的伸展方向。
(2)温石棉矿是一种硅酸盐类矿物,化学式写作氧化物形式为6MgO•4SiO•4H O,其中
2 2
原子半径最大的元素在周期表中的位置是___。SiO 存在与金刚石结构类似的晶体,其中硅
2
氧原子之间以___相结合。
a.离子键 b.极性键 c.非极性键 d.范德华力
(3)甲硅烷(SiH)是一种无色的液体,遇到空气能爆炸性自燃,生成二氧化硅固体和水。
4
在室温下,10gSiH 自燃放出热量446kJ,请写出其燃烧的热化学方程式:___;
4
(4)SiH 的热稳定性不如CH,其原因是___。
4 4
工业上硅铁可以用于冶镁。以煅白(CaO•MgO)为原料与硅铁(含硅75%的硅铁合金)混合,
置于密闭设备中于1200℃发生反应:2(CaO•MgO)(s)+Si(s) Ca SiO(l)+2Mg(g)
2 4
(5)常温下镁的还原性强于硅。上述方法能够获得镁的原因是:___。
(6)若上述反应在容积为aL的密闭容器中发生,一定能说明反应已达平衡的是___(选填
编号)。
a.反应物不再转化为生成物
b.炉内Ca SiO 与CaO•MgO的质量比保持不变
2 4
c.反应放出的总热量不再改变
d.单位时间内,n(CaO•MgO) :n(Ca SiO) =2:1
消耗 2 4 生成
若bg煅白经tmin反应后转化率达70%,该时段内Mg的生成速率是___。
12.(2022秋·湖南常德·高三湖南省桃源县第一中学校考阶段练习)Ⅰ. 和 都是大气
污染物。(1)利用氨水可以将 和 吸收,原理如下图所示:
被吸收的离子方程式是_________。
(2) ( 储存还原)工作原理: 的储存和还原在不同时段交替进行,如下图所示。
①通过 和 的相互转化实现 的储存和还原。储存 的物质是_________,
生成 的化学方程式是_________。
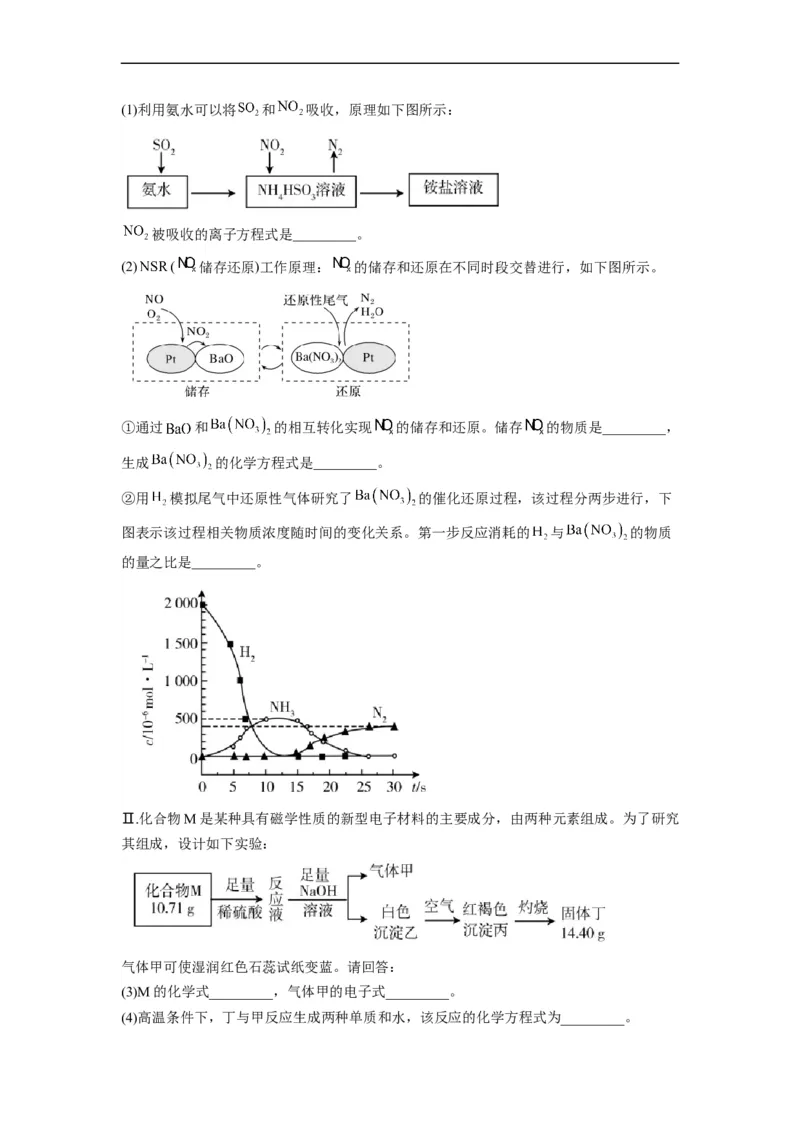
②用 模拟尾气中还原性气体研究了 的催化还原过程,该过程分两步进行,下
图表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的 与 的物质
的量之比是_________。
Ⅱ.化合物M是某种具有磁学性质的新型电子材料的主要成分,由两种元素组成。为了研究
其组成,设计如下实验:
气体甲可使湿润红色石蕊试纸变蓝。请回答:
(3)M的化学式_________,气体甲的电子式_________。
(4)高温条件下,丁与甲反应生成两种单质和水,该反应的化学方程式为_________。