文档内容
高频考点 9 氧化还原反应的综合应用
1.(2022·山东卷)实验室制备 过程为:①高温下在熔融强碱性介质中用 氧化 制备
;②水溶后冷却,调溶液 至弱碱性, 歧化生成 和 ;③减压过滤,将滤
液蒸发浓缩、冷却结晶,再减压过滤得 。下列说法正确的是( )
A.①中用瓷坩埚作反应器
B.①中用 作强碱性介质
C.②中 只体现氧化性
D. 转化为 的理论转化率约为66.7%
1.D A.①中高温下在熔融强碱性介质中用KClO 氧化 MnO 制备K MnO ,由于瓷坩埚易被强碱腐蚀,故
3 2 2 4
不能用瓷坩埚作反应器,A说法不正确;B.制备KMnO 时为为防止引入杂质离子,①中用KOH作强碱性
4
介质,不能用 ,B说法不正确;C.②中K MnO 歧化生成KMnO 和MnO ,故其既体现氧化性又体现
2 4 4 2
还原性,C说法不正确;D.根据化合价的变化分析,K MnO 歧化生成KMnO 和MnO 的物质的量之比为
2 4 4 2
2:1,根据Mn元素守恒可知,MnO 中的Mn元素只有 转化为KMnO ,因此,MnO 转化为KMnO 的理论
2 4 2 4
转化率约为66.7%,D说法正确;综上所述,本题选D。
2.(2021·北京卷)用电石(主要成分为CaC ,含CaS和Ca P 等)制取乙炔时,常用CuSO 溶液除去乙炔
2 3 2 4
中的杂质。反应为:
①CuSO +H S=CuS↓+H SO
4 2 2 4
②11PH +24CuSO +12H O=3H PO +24H SO +8Cu P↓
3 4 2 3 4 2 4 3
下列分析不正确的是( )
A.CaS、Ca P 发生水解反应的化学方程式:CaS+2H O=Ca(OH) +H S↑、Ca P +6H O=3Ca(OH) +2PH ↑
3 2 2 2 2 3 2 2 2 3
B.不能依据反应①比较硫酸与氢硫酸的酸性强弱
C.反应②中每24 mol CuSO 氧化11 mol PH
4 3
D.用酸性KMnO 溶液验证乙炔还原性时,H S、PH 有干扰
4 2 32.C A.水解过程中元素的化合价不变,根据水解原理结合乙炔中常混有H S、PH 可知CaS的水解方程式
2 3
为CaS+2H O=Ca(OH) +H S↑;Ca P 水解方程式为Ca P +6H O=3Ca(OH) +2PH ↑,A项正确;B.该反应能发
2 2 2 3 2 3 2 2 2 3
生是因为有不溶于水也不溶于酸的CuS生成,因此反应①不能说明H S的酸性强于H SO ,事实上硫酸的酸
2 2 4
性强于氢硫酸,B项正确;C.反应②中Cu元素化合价从+2价降低到+1价,得到1个电子,P元素化合价
从-3价升高到+5价,失去8个电子,则24molCuSO 完全反应时,可氧化PH 的物质的量是24mol÷8=
4 3
3mol,C项错误;D.H S、PH 均被KMnO 酸性溶液氧化,所以会干扰KMnO 酸性溶液对乙炔性质的检验,
2 3 4 4
D项正确;答案选C。
3.(2022·哈尔滨三中高三阶段练习)下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是(
)
物质(括号内为杂质) 除杂试剂
A FeCl 溶液(FeCl) Fe粉
2 3
B NaCl溶液(MgCl) NaOH溶液、稀HCl
2
C Cl(HCl) HO、浓HSO
2 2 2 4
D CuCl(FeCl) 氨水
2 3
A.A B.B C.C D.D
3.B A.FeCl 与Fe反应生成FeCl,2FeCl+Fe=3FeCl,此过程中Fe的化合价发生变化,涉及到了氧化
3 2 3 2
还原反应,故A不符合题意;B.MgCl 与NaOH溶液发生复分解反应MgCl+2NaOH=Mg(OH) +2NaCl,过量
2 2 2
的NaOH溶液可用HCl除去HCl+NaOH=NaCl+HO ,此过程中没有元素化合价发生变化,未涉及氧化还原反应,
2
故B符合题意;C.部分氯气与HO 发生反应生成氯化氢和次氯酸为氧化还原反应,应该用饱和食盐水除去
2
HCl,除杂方法不正确,故C不符合题意;D.氨水和氯化铜、氯化铁均生成沉淀,除杂方式不正确;反应
过程中化合价没有发生变化,不涉及到了氧化还原反应,故D不符合题意;故选B。
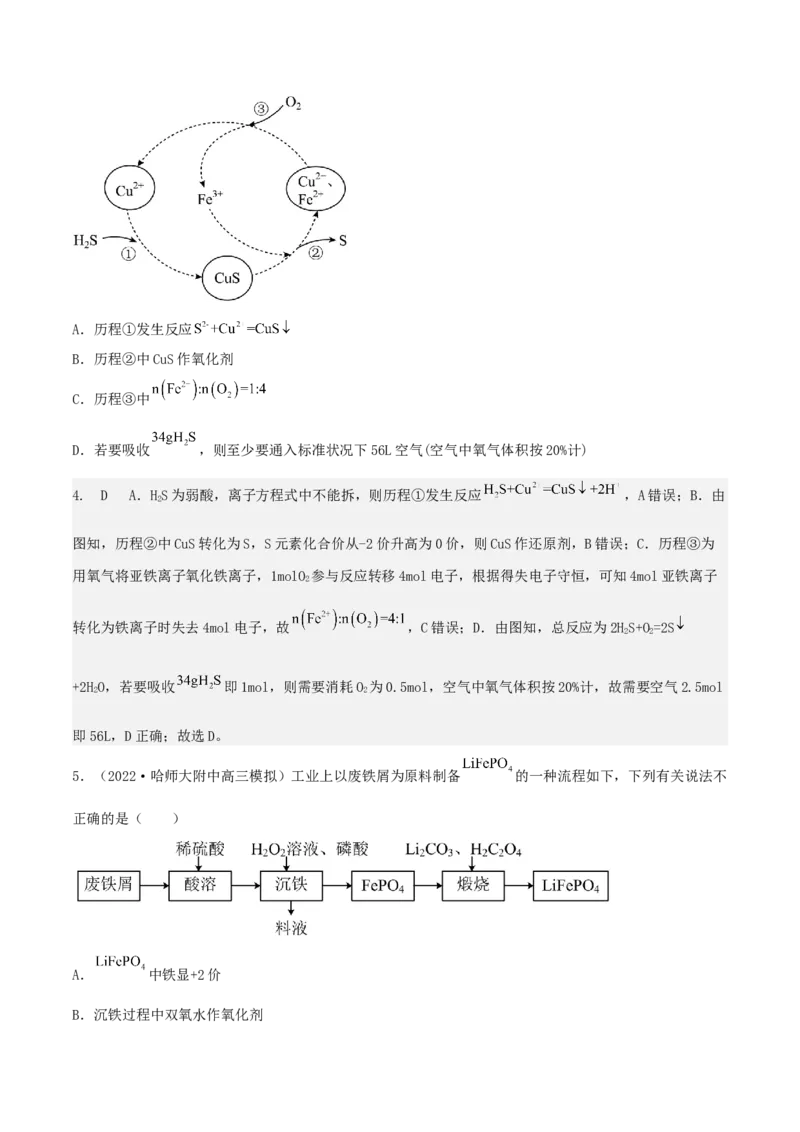
4.(2022·广东高三期末)硫化氢的转化是资源利用和环境保护的重要研究课题。将 和空气的混合气
体通入 和HCl的混合溶液中反应回收S,其物质转化历程如图所示。下列说法正确的是(
)A.历程①发生反应
B.历程②中CuS作氧化剂
C.历程③中
D.若要吸收 ,则至少要通入标准状况下56L空气(空气中氧气体积按20%计)
4. D A.HS为弱酸,离子方程式中不能拆,则历程①发生反应 ,A错误;B.由
2
图知,历程②中CuS转化为S,S元素化合价从-2价升高为0价,则CuS作还原剂,B错误;C.历程③为
用氧气将亚铁离子氧化铁离子,1molO 参与反应转移4mol电子,根据得失电子守恒,可知4mol亚铁离子
2
转化为铁离子时失去4mol电子,故 ,C错误;D.由图知,总反应为2HS+O=2S
2 2
+2HO,若要吸收 即1mol,则需要消耗O 为0.5mol,空气中氧气体积按20%计,故需要空气2.5mol
2 2
即56L,D正确;故选D。
5.(2022·哈师大附中高三模拟)工业上以废铁屑为原料制备 的一种流程如下,下列有关说法不
正确的是( )
A. 中铁显+2价
B.沉铁过程中双氧水作氧化剂C.沉铁中离子方程式为
D.实验室进行煅烧操作中需要使用泥三角、酒精灯、蒸发皿、玻璃棒等仪器
5.D A.根据化学式化合价代数和为0可知,LiFePO 中Fe显+2价,故A项正确;B.沉铁过程中加双氧水
4
的目的是将Fe2+氧化为Fe3+,双氧水作氧化剂,故B项正确;C.沉铁时,加入了双氧水、磷酸,发生反应
的离子方程式为: ,故C项正确;D.实验室进行煅烧操作中需
要使用坩埚、泥三角、酒精灯、玻璃棒等仪器,故D项错误;故答案选D。
6.(双选)(2022·石家庄二中实验学校高三开学考试)向重铬酸盐酸性溶液中加入乙醚和HO,水层发
2 2
生反应:CrO +4HO+2H+=2CrO+5HO(已知CrO 中Cr的化合价为+6价),乙醚层发生反应:CrO+
2 2 2 5 2 5 5
(CH)O=CrO•O(CH)(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色
2 5 2 5 2 5 2
(Cr3+),下列说法正确的是( )
A.由水层反应可知,氧化性:CrO >CrO
2 5
B.乙醚在检验过程中作稳定剂和萃取剂,不可用乙醇代替
C.CrO•O(CH) 中不存在非极性键
5 2 5 2
D.水相变为绿色的离子反应为4CrO+12H+=4Cr3++6HO+7O↑
5 2 2
6.BD A.水层反应中元素化合价不变,属于非氧化还原反应,故A错误;
B.乙醚在检验过程中作稳定剂和萃取剂,乙醇能溶于水且具有还原性,能被CrO 氧化,所以不可用乙
2
醇代替乙醚,故B正确;C.CrO 中Cr的化合价为+6价,则CrO 的结构式为 ,所以
5 5
CrO•O(CH) 中存在非极性键,故C错误;D.水相变为绿色说明CrO 生成Cr3+生成,根据得失电子守恒,
5 2 5 2 5
反应的离子反应为4CrO+12H+=4Cr3++6HO+7O↑。选BD。
5 2 2
7.(2022·商丘市第一高级中学高三检测)重铬酸钠(NaCrO)俗称红矾钠,工业上有着广泛的用途,五
2 2 7
氧化二钒广泛地用于冶金、印染、陶瓷及石油工业等方面。某化工厂用钒铬渣[主要成分为VO•xHO、
2 2
Cr(OH) 及少量的SiO]为原料生产上述两种物质的工艺流程如图所示:
3 2已知:①有关物质的溶解度(g/100gHO)如表所示:
2
温
20 40 60 80 100
度/℃
376.
NaCrO 183.6 215.1 269.2 415.0
2 2 7 4
NaSO 19.5 48.8 45.3 43.7 42.5
2 4
②当pH>4.1时,Cr3+开始沉淀。
回答下列问题:
(1)NaSO 名称为过二硫酸钠,存在一个过氧键,则该化合物中硫元素的化合价是____价;写出滤渣的一
2 2 8
种用途:____。
(2)“氧化1”过程中,钒元素由VO2+转化为VO ,相应反应的离子方程式为_____。
(3)“氧化2”过程中,铬元素由Cr3+转化为CrO ,当有3molCrO 生成时,理论上消耗____molHO;两
2 2
次氧化均需要加热,但“氧化2”中加热的温度应较低,原因是____。
(4)重结晶包括蒸发浓缩、趁热过滤、降温结晶、过滤、洗涤等步骤,则“趁热过滤”得到的晶体成分是
_____(填化学式);“降温结晶”时得到的物质是_____(填“纯净”或“混合”)物。
7. (1) +6 制作光导纤维、光学玻璃
(2)2VO2++SO +2HO=2VO +2SO +4H+
2 2
(3) 2VO +(x-1)HO+2OH-=VO•xHO 1×10-29.7
2 2 5 2
(4) 4.5 温度过高会导致HO 分解
2 2
(5) NaSO 混合
2 4
解析:(1) 中存在一个过氧键,即有2个氧显 价,其余的氧显-2价,根据化合物的化合价为
0,可得硫元素为 价;根据分析,滤渣成分是 ,可用于制作光导纤维、光学玻璃等。(2)反应过程中 表现氧化性,还原产物为 ,相应的离子方程式为
。
(3)“氧化2”中 ,Cr化合价由+3升高为+6,为还原剂,1mol还原剂失去3mol电子,
被还原为 ,1mol 得到2mol电子,由得失电子守恒可知,当有3mol 生成时,理论上
消耗 =4.5mol ;温度高会导致较多的 分解,故“氧化2”中加热的温度应较低。
(4)由 、 溶解度随着温度变化可知, 的溶解度随着温度的升高增大的较少,而
则增加很多,故蒸发浓缩过程中首先析出 ,趁热过滤后再降温结晶得到 ,因此
蒸发浓缩过程中析出 后剩余溶液中 仍是饱和的,故再降温结晶时得到的是 、
的混合物。