文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(山东专用)
黄金卷05
(考试时间:90分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mn 55
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.科技助力2022年北京冬奥会。下列说法错误的是
A.制比赛的雪橇所用碳纤维材料,属于有机高分子材料
B.制火炬接力火种灯所用可再生铝合金硬度大于纯铝
C.主体为钢结构的首钢滑雪大跳台,钢属于合金材料
D.首次使用氢能作火炬燃料,践行“绿色、低碳”理念
【答案】A
【解析】A.碳纤维属于无机非金属材料,A错误;B.合金的硬度一般大于成分金属,B正确;C.钢为
铁碳合金,属于合金材料,C正确;D.氢气燃料产物为水,环保无污染,D正确。故选A。
2.下列物质性质与用途具有对应关系的是
A. 呈淡黄色,可用作供氧剂 B.NaCl熔点较高,可用于制取NaOH
C. 溶液呈碱性,可用于除油污 D. 易分解,可用于治疗胃酸过多
【答案】C
【解析】A. 能与水和二氧化碳反应生成氧气,因此可做供氧剂,与颜色无关,故A错误;B.电
解饱和NaCl溶液生成NaOH,与NaCl熔点无关,故B错误;C. 溶液呈碱性,可使油污水解呈溶
水物质除去,故C正确;D. 能与胃酸中HCl反应生成二氧化碳,因此可以用于治疗胃酸过多,
与其不稳定性无关,故D错误;故选:C。
3.实验室制取FeSO 溶液和NaHCO 溶液,并利用两者反应制取FeCO,下列有关实验装置和操作不能达
4 3 3
到实验目的的是
A.用装置甲制取FeSO 溶液 B.用装置乙制取NaHCO 溶液
4 3
C.用装置丙制取FeCO D.用装置丁过滤所得的浊液
3
【答案】C【解析】A.稀硫酸与Fe反应生成硫酸亚铁,同时过量的铁屑可防止Fe2+被氧化成Fe3+,A正确;B.碳酸
钠溶液中通入二氧化碳,两者反应生成碳酸氢钠,B正确;C.碳酸氢钠和FeSO 反应生成FeCO 的同时还
4 3
会生成CO,不能关闭止水夹,C错误;D.装置丁可用于过滤所得到的浊液分离出FeCO,且过滤操作正
2 3
确,D正确;故答案选C。
4.已知: 可由 与过量的 溶液反应生成。类推是常用的思维方法,下列类推中正确
的是
A. 属于酸式盐, 也属于酸式盐
B. 是酸性氧化物, 也是酸性氧化物
C.15-冠-5(冠醚)能识别 ,则12-冠-4(冠醚)也能识别
D. 与水反应生成碱, 与水反应也生成碱
【答案】D
【解析】A. 属于酸式盐;由已知 可由 与过量的 溶液反应生成,说明
HPO 只能电离出一个氢离子,为一元酸,则 属于正盐,故A错误;B. 是酸性氧化物,CO
3 2
不和碱反应,不是酸性氧化物,故B错误;C.15-冠-5(冠醚)能识别 ,12-冠-4(冠醚)与锂离子络合而不
与钠、钾离子络合,故C错误;D. 与水反应生成Ca(OH) , 与水反应生成NaOH,故D正确;
2
故选D。
5.某化学兴趣小组探究 催化 分解制取氧气,小组成员闻到制得的氧气有轻微的刺激性气味。
下列有关分析推理不正确的是
A.反应后所得固体除 外,还可能含有KCl、
B. 催化 分解,降低了反应的活化能,加快分解速率
C.标准状况下制得22.4L氧气,反应中转移电子4mol
D.将制得的气体通入 溶液,可能会产生不溶于硝酸的白色沉淀
【答案】C
【解析】A.根据氧化还原反应规律,KClO 受热分解过程中还能发生副反应4KClO 3KClO+KCl,故反
3 3 4
应后所得固体除MnO 外,还可能含有KCl、KClO,A正确;
2 4
B.MnO 催化KClO 分解时,MnO 作催化剂,催化剂能够降低了反应的活化能,加快分解速率,B正确;
2 3 2
C.由于制得的氧气有轻微的刺激性气味,即混有少量的Cl,故不能光计算制备O 过程中的电子转移,不
2 2
知道Cl 的量,无法计算电子转移数目,C错误;D.由于制得的氧气有轻微的刺激性气味,即混有少量的
2
Cl,Cl+H O=HCl+HClO,则将制得的气体通入AgNO 溶液,可能会产生不溶于硝酸的白色沉淀AgCl,D
2 2 2 3
正确;故答案为:C。
6.已知反应:2[Co(H O) ]2++10NH+2NH +H O=2[Co(NH)]3++14H O,下列说法错误的是
2 6 3 2 2 3 6 2A.NH 和HO的中心原子的杂化类型相同
3 2
B.反应中HO 作氧化剂,发生还原反应,被还原
2 2
C.NH 和HO与Co3+的配位能力:NH >HO
3 2 3 2
D.1mol[Co(H O) ]2+配离子中,含有的σ键数目为6×6.02×1023
2 6
【答案】D
【详解】A.NH 中心N的孤对电子对数1,σ键电子对数3,价层电子对数4,为sp3杂化,HO中心O孤
3 2
对电子对数2,σ键电子对数2,价层电子对数4,为sp3杂化,A正确;
B.反应中HO 氧元素为-1价,反应后生成HO,氧元素化合价为-2价,化合价降低,作氧化剂,发生还
2 2 2
原反应,被还原,B正确;
C.根据反应方程式可知NH 和HO与Co3+的配位能力:NH >HO,原因是N的电负性小于O,即N对孤
3 2 3 2
对电子吸引小于O,故NH 更容易成为配体,C正确;
3
D.[Co(H O) ]2+配离子中每个HO含有2个H-O键,1个配位键,都是σ键,1mol[Co(H O) ]2+配离子中含
2 6 2 2 6
有的σ键数目为18×6.02×1023,D错误;
故答案为:D。
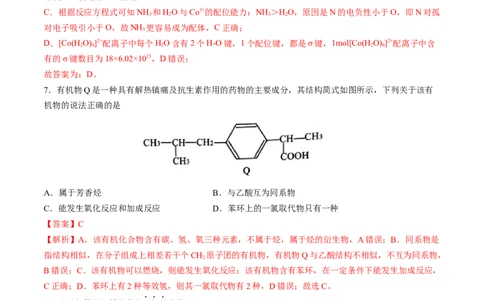
7.有机物Q是一种具有解热镇痛及抗生素作用的药物的主要成分,其结构简式如图所示,下列关于该有
机物的说法正确的是
A.属于芳香烃 B.与乙酸互为同系物
C.能发生氧化反应和加成反应 D.苯环上的一氯取代物只有一种
【答案】C
【解析】A.该有机化合物含有碳、氢、氧三种元素,不属于烃,属于烃的衍生物,A错误;B.同系物是
指结构相似,在分子组成上相差若干个CH 原子团的有机物,有机物Q与乙酸结构不相似,不互为同系物,
2
B错误;C.该有机物可以燃烧,则能发生氧化反应;该有机物含有苯环,在一定条件下能发生加成反应,
C正确;D.苯环上有2种等效氢,则其一氯取代物有2种,D错误;故选C。
8.下列方程式与所给事实不相符的是
A.用碳酸钠溶液处理锅炉水垢:
B. 通入水中制氯水:
C.氢氧化亚铁暴露于空气中变色:
D.常温下 氨水的pH约为11:
【答案】B
【解析】A.碳酸钙比硫酸钙更难溶,可用碳酸钠溶液处理锅炉水垢,反应的离子方程式为,A正确;B.HClO为弱酸,书写离子方程式保留化学式,
反应的离子方程式为 ,B错误;C.氢氧化亚铁暴露于空气中,反应的化学方
程式为 ,C正确;D.氨水电离使溶液显碱性,电离方程式为
,D正确; 故选B。
9.一定量的甲苯和 溶液发生反应得到混合物,按如下流程分离出苯甲酸、回收未反应的甲苯。下
列说法错误的是
A.苯甲酸可反应形成盐、酯、酰胺、酸酐等
B.操作Ⅰ和操作Ⅱ依次为蒸发浓缩、冷却结晶和蒸馏
C.甲苯、苯甲酸依次由①、②获得
D.苯甲酸100℃时迅速升华,故其粗品精制除采用重结晶方法外,还可用升华法
【答案】B
【解析】A.苯甲酸中含有羧基,能形成盐、酯、酰胺、酸酐等故A正确;B.滤液经过萃取分为有机相
和水相,有机相经过无水硫酸钠干燥,蒸馏后得到甲苯,水相经过蒸发浓缩和冷却过滤得到苯甲酸,故B
错误;C.据B分析可知,甲苯、苯甲酸依次由①、②,故C正确;D.苯甲酸在100℃左右开始升华。故
除了重结晶方法外,也可用升华方法精制苯甲酸,故D正确;故答案选B。
10.我国科学家合成了一种深紫外非线性光学晶体新材料 ,晶体中阴离子为 。元素
M、X、Y、Z均为短周期元素,M、Y与Z同周期,M的最外层电子数比次外层电子数多1,Z为电负性
最强的元素,Y是地壳中含量最高的元素,X的 轨道有3个电子。下列说法中不正确的是
A.电负性:
B.简单离子半径:
C.简单气态氢化物的稳定性:
D.M最高价氧化物对应水化物能与盐酸反应
【答案】D
【解析】元素M、X、Y、Z均为短周期元素,M的最外层电子数比次外层电子数多1,说明M是B;Z为
电负性最强的元素,说明Z是F;Y是地壳中含量最高的元素,说明Y是O;X的 轨道有3个电子,说
明X是P。A.电负性O>P,故Y>X,A正确;B.电子层数相同,核电核数越大,半径越小,故O2->
F-,即Y>Z,B正确;C.非金属性F>P,则简单气态氢化物的稳定性Z>X,C正确;D.M最高价氧化
物对应水化物为硼酸,硼酸不与盐酸反应,D错误;故选D。二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得
4分,选对但不全的得2分,有选错的得0分。
11.硫代碳酸钠 在农业上用作杀菌剂和杀线虫剂,在工业上用于处理废水中的重金属离子。其制
备原理为: 。下列说法不正确的是
A.该制备反应属于熵增反应
B. 与 性质相似,不能被氧化
C.制备 的反应属于非氧化还原反应
D. 与盐酸反应,生成NaCl、 和
【答案】B
【解析】A.根据方程式可判断反应前气体体积增加,所以该制备反应属于熵增反应,A正确;B.
与 性质相似,但由于硫元素是-2价,处于最低价态,因此能被氧化,B错误;C.制备
的反应中元素化合价均是不变的,所以属于非氧化还原反应,C正确;D.根据碳酸钠和盐酸的反
应可知 与盐酸反应,生成NaCl、 和 ,D正确;答案选B。
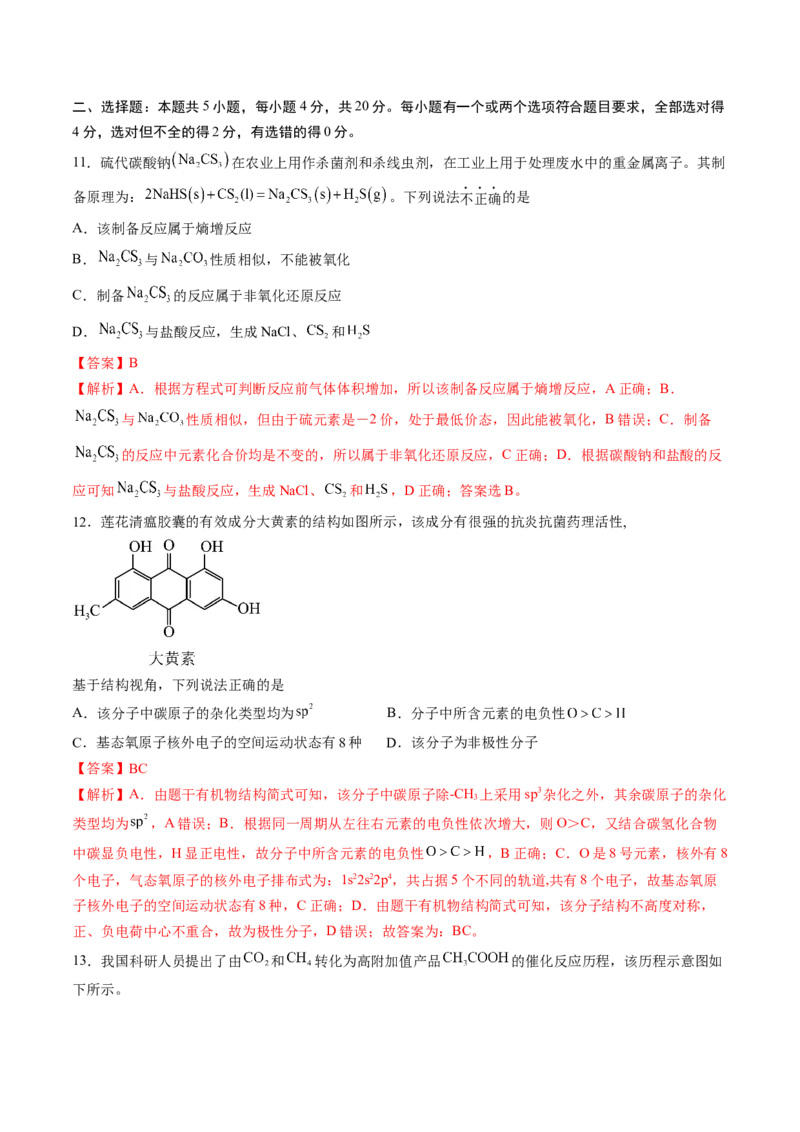
12.莲花清瘟胶囊的有效成分大黄素的结构如图所示,该成分有很强的抗炎抗菌药理活性,
基于结构视角,下列说法正确的是
A.该分子中碳原子的杂化类型均为 B.分子中所含元素的电负性
C.基态氧原子核外电子的空间运动状态有8种 D.该分子为非极性分子
【答案】BC
【解析】A.由题干有机物结构简式可知,该分子中碳原子除-CH 上采用sp3杂化之外,其余碳原子的杂化
3
类型均为 ,A错误;B.根据同一周期从左往右元素的电负性依次增大,则O>C,又结合碳氢化合物
中碳显负电性,H显正电性,故分子中所含元素的电负性 ,B正确;C.O是8号元素,核外有8
个电子,气态氧原子的核外电子排布式为:1s22s22p4,共占据5个不同的轨道,共有8个电子,故基态氧原
子核外电子的空间运动状态有8种,C正确;D.由题干有机物结构简式可知,该分子结构不高度对称,
正、负电荷中心不重合,故为极性分子,D错误;故答案为:BC。
13.我国科研人员提出了由 和 转化为高附加值产品 的催化反应历程,该历程示意图如
下所示。下列说法正确的是
A.E为该催化反应的活化能
B.生成 总反应的原子利用率为100%
C.①→②吸收能量并形成了 键
D.该催化剂可有效提高反应物的平衡转化率
【答案】B
【解析】A.E为①→②反应的活化能,故A错误;B.总反应为CO+CH →CHCOOH,总反应的原子利
2 4 3
用率为100%,故B正确;C.①→②是放热反应,放出能量并形成了 键,故C错误;D.催化剂不
能使平衡移动,催化剂不能提高反应物的平衡转化率,故D错误;选B。
14.我国科学家发现,将纳米级 嵌入电极材料,能大大提高可充电铝离子电池的容量。其中有机离子
导体主要含 ,隔膜仅允许含铝元素的微粒通过。工作原理如图所示:
下列说法正确的是
A.若 从电极表面脱落,则电池单位质量释放电量减少
B.为了提高电导效率,左极室采用酸性 水溶液
C.放电时, 离子可经过隔膜进入右极室中
D.充电时,电池的阳极反应为
【答案】AC
【解析】根据图中电子流动方向知铝电极为负极, 嵌入电极是正极,工作时,铝单质失去电子生成,再与 结合生成 ,电极反应式为 。A.“将纳米级 嵌入电
极材料,能大大提高可充电铝离子电池的容量”,若 从电极表面脱落,电池容量减小,则电池单位质
量释放电量减少,A正确;B.把左极室的有机离子导体改成水溶液后,会使左极室溶液中的离子总浓度
减小,导致电导效率下降,B错误;C.放电时,左边电极为正极,右边电极为负极,阴离子向负极移动,
结合分析可知右边负极需要消耗 ,故 离子经过隔膜进入右极室中,C正确;D.电池的阳极即
负极,充电时,为电解池装置,电池的负极与外接电源负极相连为阴极,电极反应为放电时负极反应的逆
过程,即反应为 ,D错误;故选AC。
15.按如图1装置,常温下分别向25mL0.3mol•L-1NaCO 溶液和25mL0.3mol•L-1NaHCO 溶液中逐滴滴加
2 3 3
0.3mol•L-1的稀盐酸,测得压强随盐酸体积的变化曲线如图2所示,已知:碳酸K =4.3×10-7;K =5.6×10-
a1 a2
11。下列说法正确的是
A.X为NaCO 溶液的反应曲线
2 3
B.a点溶液中c(H+)的数量级为10-12
C.a到c点之间的离子浓度大小关系:c(Na+)>c(HCO )>c(CO )>c(OH-)>c(H+)
D.水的电离程度:c<a<b
【答案】C
【解析】碳酸钠与盐酸反应先发生NaCO+HCl=NaHCO +NaCl,继续滴加盐酸,
2 3 3
NaHCO +HCl=NaCl+CO ↑+H O,碳酸氢钠与盐酸反应直接生成二氧化碳,因此碳酸氢钠与盐酸反应压强
3 2 2
逐渐增大,碳酸钠与盐酸反应开始时压强几乎不变,随着反应进行压强增大,因此图像中X曲线代表碳酸
氢钠与盐酸反应;A.根据上述分析,曲线X为碳酸氢钠溶液反应曲线,曲线Y为碳酸钠溶液反应的曲线,
故A错误;B.25mL0.3mol/L碳酸钠与12.5mL0.3mol/L盐酸反应,反应后溶液中的溶质有NaHCO 和
3
NaCO,且物质的量相等,推出c(CO )≈c(HCO ),利用电离平衡常数K =c(H+)≈5.6×10-11mol/L,a点溶
2 3 a2
液中c(H+)的数量级为10-11,故B错误;C.a点溶质为NaHCO 和NaCO,且物质的量相等,c点加入
3 2 3
25mL0.3mol/L盐酸,溶质为NaHCO ,溶液显碱性,因此a到c点之间的离子浓度大小顺序是c(Na+)>
3
c(HCO )>c(CO )>c(OH-)>c(H+),故C正确;D.a点溶质为NaHCO 和NaCO,c点溶质为NaHCO ,
3 2 3 3
b点溶质为NaCl,HCO 、CO 发生水解,促进水的电离,NaCl对水的电离无影响,b点水的电离程度最
小,故D错误;答案为C。
三、非选择题:本题共5小题,共60分。16.(12分)硒(Se)是人体必需微量元素之一,含硒化合物在材料和药物等领域具有重要应用。
(1)Se与S同族,基态硒原子价电子排布式为__________。
(2) 的沸点低于 ,其原因是__________。
(3)硒的两种含氧酸的酸性强弱为 __________ (填“>”或“<”)。 的空间结构为
__________。比较键角大小:气态 分子__________ 离子(填“>”“<”或“=”)。
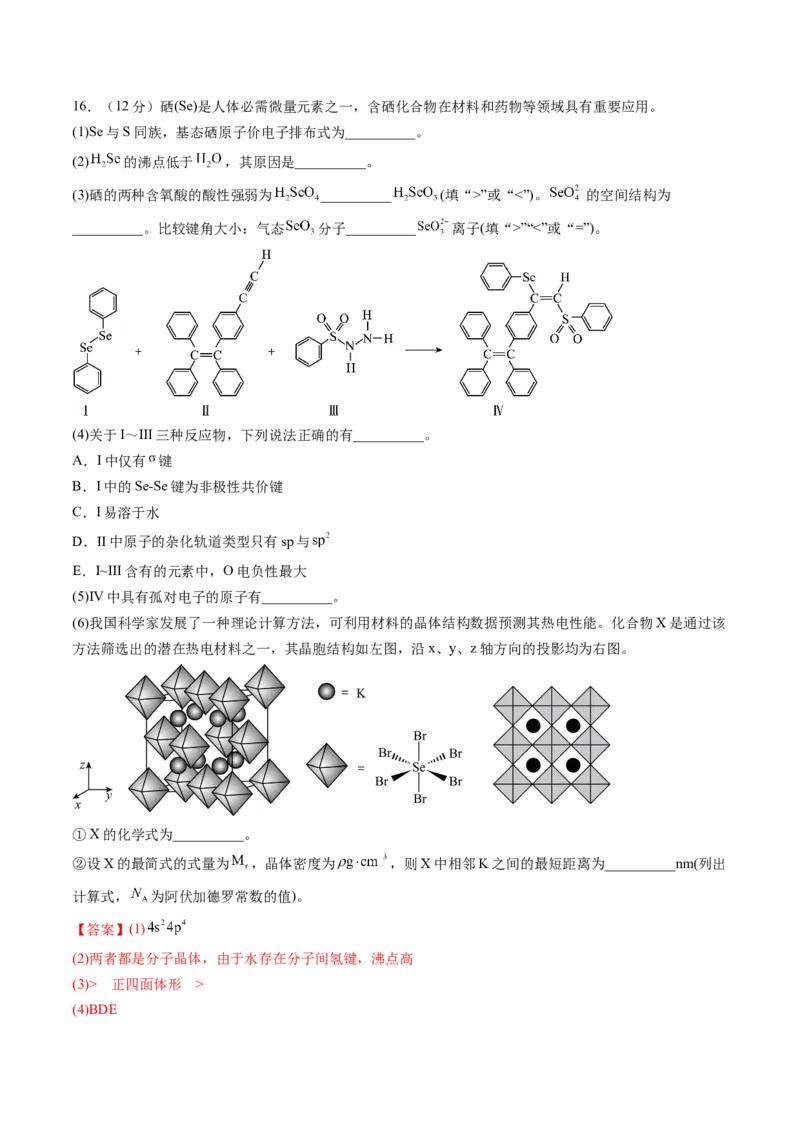
(4)关于I~III三种反应物,下列说法正确的有__________。
A.I中仅有 键
B.I中的Se-Se键为非极性共价键
C.I易溶于水
D.II中原子的杂化轨道类型只有sp与
E.I~III含有的元素中,O电负性最大
(5)IV中具有孤对电子的原子有__________。
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能。化合物X是通过该
方法筛选出的潜在热电材料之一,其晶胞结构如左图,沿x、y、z轴方向的投影均为右图。
①X的化学式为__________。
②设X的最简式的式量为 ,晶体密度为 ,则X中相邻K之间的最短距离为__________nm(列出
计算式, 为阿伏加德罗常数的值)。
【答案】(1)
(2)两者都是分子晶体,由于水存在分子间氢键,沸点高
(3)> 正四面体形 >
(4)BDE(5)O、Se
(6)
【解析】(1)Se与S同族,位于第4周期,ⅥA族,故基态硒原子价电子排布式为: ;
(2)两者都是分子晶体,但是水中含有氢键,分子间作用力较大,沸点较高,故答案为:两者都是分子
晶体,由于水存在分子间氢键,沸点高;
(3)在含氧酸中,非羟基氧越多,起酸性越强, 和 非羟基氧的个数分别为2和1,故酸性
> ; 中心原子的价层电子对数为4,则其空间结构为:正四面体形;SeO 中Se是sp2
3
杂化,平面三角形,键角120°; 中Se是sp3杂化,Se原子上有孤对电子,离子空间结构为三角锥形,
键角小于120°,故键角气态 分子> 离子;
(4)A.I中含有苯环,除了有σ键之外还有其它化学键,A错误;
B.I中的Se-Se键是相同原子形成的共价键,为非极性共价键,B正确;
C.I为相对分子较大的有机物,没有亲水基,一般不易溶于水,C错误
D.II的主要结构是苯环、碳碳双键和碳碳三键,其中原子的杂化轨道类型只有sp与sp2,D正确;
E.I~III含有的元素包括:H、C、N、O、S、Se,O电负性最大,E正确;
故选BDE;
(5)根据题中信息IV中O、Se都有孤对电子,碳、氢、硫都没有孤对电子;故答案为:O、Se;
(6)①根据晶胞结构得到K有8个, 有 ,则X的化学式为KSeBr ;故答案为:
2 6
KSeBr 。
2 6
②设X的最简式的式量为 ,晶体密度为 ,设晶胞参数为anm,得到
,解得 ,X中相邻K之间的最短距离为晶胞参数的一半
即 ;故答案为: 。
17.(12分)电解金属锰阳极渣(主要成分 ,杂质为 、 、 元素的化合物)和黄铁矿 为
原料可制备 ,其流程如图所示:
已知: 、 ,回答下列问题:(1)锰原子价层电子的轨道表示式为_______,它处于周期表的_______区, 中 的化合价为
_______。
(2)“酸浸”时,所用的稀酸X是_______。
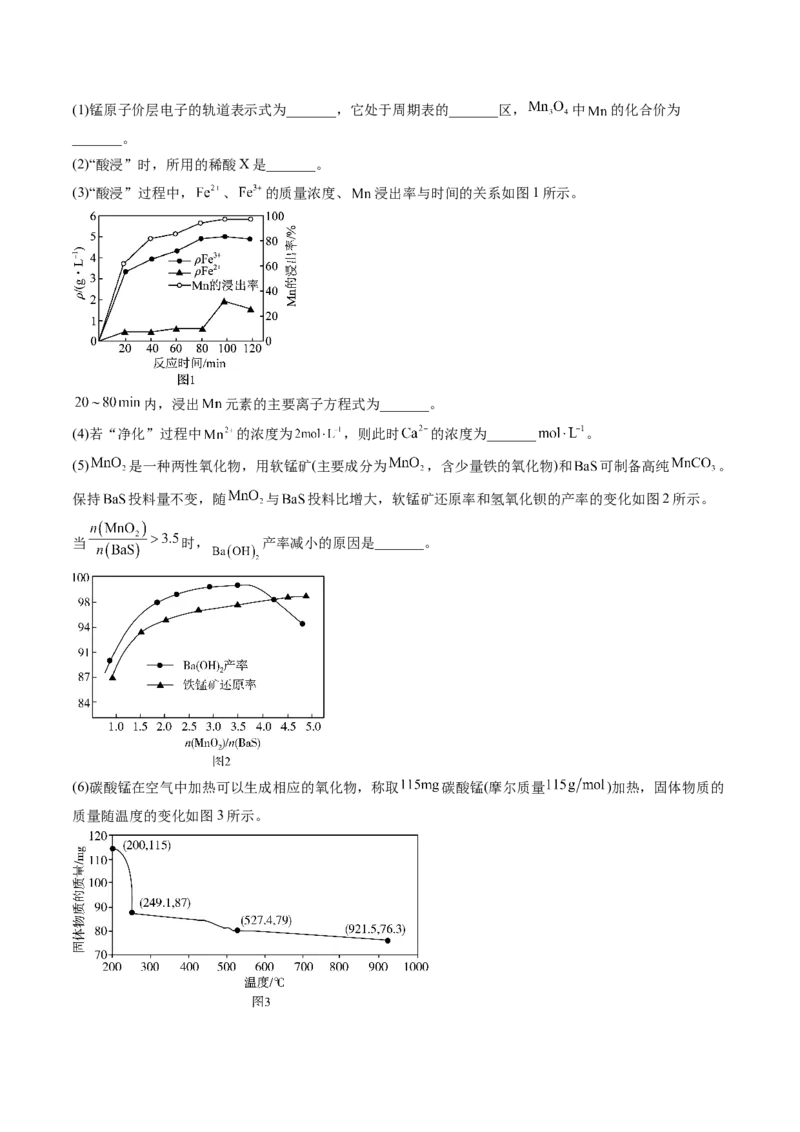
(3)“酸浸”过程中, 、 的质量浓度、 浸出率与时间的关系如图1所示。
内,浸出 元素的主要离子方程式为_______。
(4)若“净化”过程中 的浓度为 ,则此时 的浓度为_______ 。
(5) 是一种两性氧化物,用软锰矿(主要成分为 ,含少量铁的氧化物)和 可制备高纯 。
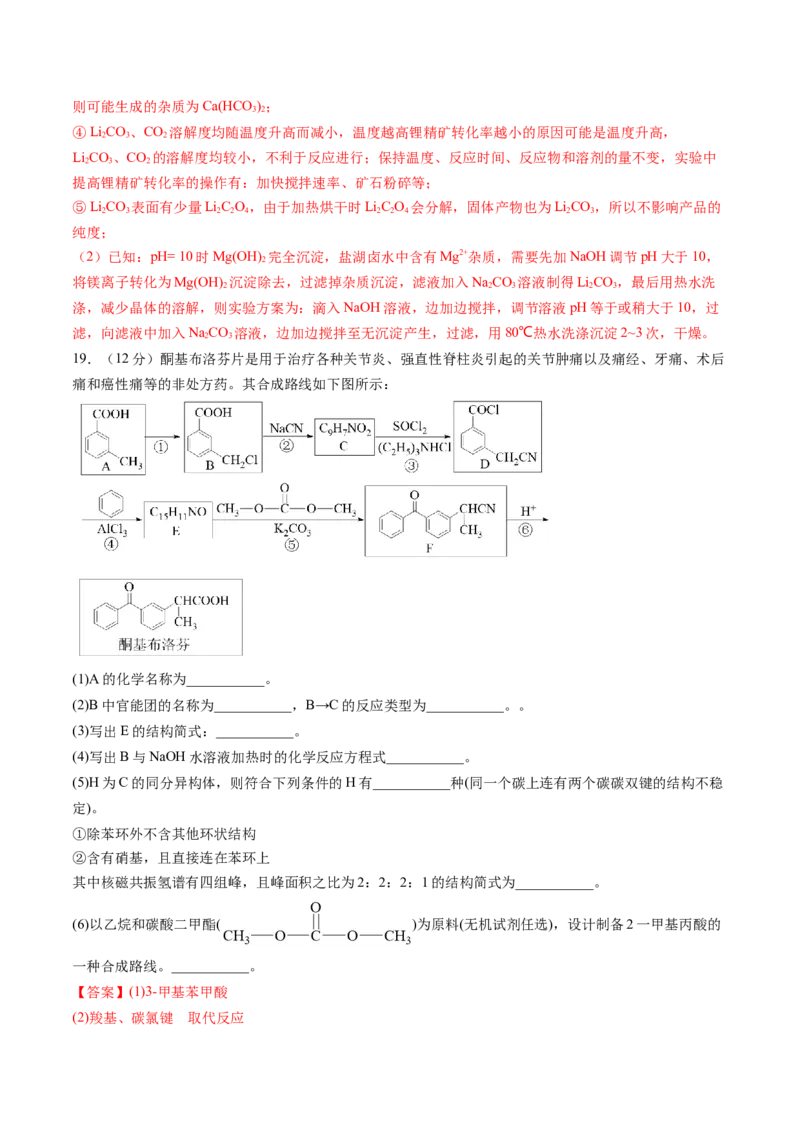
保持 投料量不变,随 与 投料比增大,软锰矿还原率和氢氧化钡的产率的变化如图2所示。
当 时, 产率减小的原因是_______。
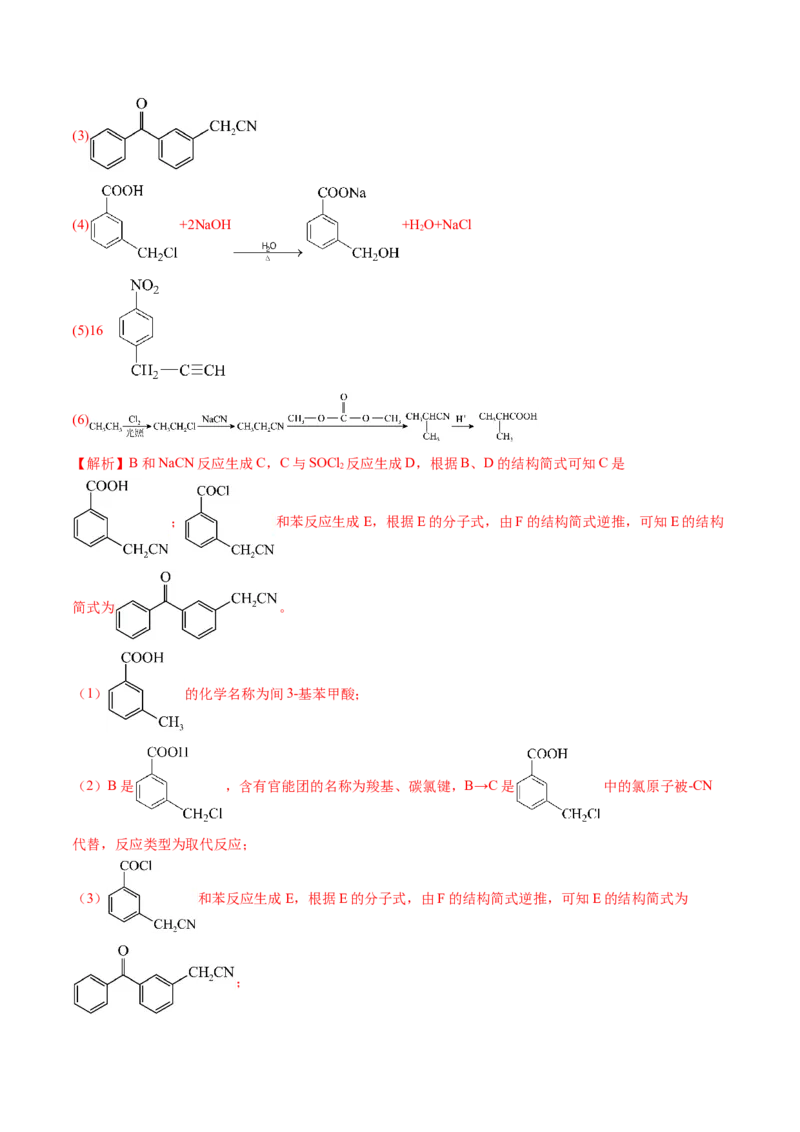
(6)碳酸锰在空气中加热可以生成相应的氧化物,称取 碳酸锰(摩尔质量 )加热,固体物质的
质量随温度的变化如图3所示。527.4℃时, 生成相应固体物质的化学方程式为_______。
【答案】(1) d +2、+3
(2)稀硫酸
(3)
(4)
(5)过量的 消耗了反应生成的Ba(OH)
2
(6)
【解析】MnO 在酸性条件下有强氧化性,FeS 有强还原性,二者在酸浸的时候会发生氧化还原反应,结
2 2
合题图中后续操作后得到的是MnSO 溶液,可知所用的稀酸X为稀硫酸。然后向滤液中加入HO 可以将
4 2 2
杂质离子为Fe2+氧化为Fe3+,再加入CaO调整溶液pH,使Fe3+ Cu2+形成Fe(OH) 、Cu(OH) 沉淀,但是用
、 3 2
CaO来调pH又会导致溶液中留下较多的Ca2+,净化阶段加入MnF 的目的就是使Ca2+转化为难溶物CaF 除
2 2
去,过滤得到的滤液含有MnSO ,然后经一系列处理得到MnO;
4 3 4
、(1)Mn原子序数为25,价电子排布图为 ,位于周期表中d区;
中O为-2价,结合化合物中各元素的代数和为可知, 中Mn的化合价既有+2价也有+3价,
故答案为: ;d;+2、+3;
(2)由分析知,稀酸X为稀硫酸,故答案为:稀硫酸;
(3)由图可知, 内,Mn元素浸出率提高, 含量明显增加,说明此时 与 反应生
成Mn2+、 、S等,对应的离子方程式为: ,故答案为:
;
(4)由 , 的浓度为 ,可得: ;
再由 ,可得 ,故答案
为: ;
(5)由题意可知,二氧化锰与硫化钡反应生成氢氧化钡,因反应物 是一种两性氧化物,当
时,二氧化锰过量,过量的二氧化锰与氢氧化钡反应消耗氢氧化钡,导致其产率降低,故
答案为:过量的 消耗了反应生成的Ba(OH) ;
2(6) ,则 , ;
527.4℃时, , ,可知:
,则此时产物为: ,反应方程式为:
,故答案为: 。
18.(12分)以盐湖锂精矿(主要成分为LiCO,还含有少量的CaCO )和盐湖卤水(含一定浓度的LiCl 和
2 3 3
MgCl )为原料均能制备高纯LiCO。回答下列问题:
2 2 3
(1)由锂精矿为原料制取碳酸锂的过程中,需要先“碳化溶解”使LiCO 转为LiHCO ,实验装置如图所示。
2 3 3
已知: I.20℃时LiOH的溶解度为12.8g。
II.LiCO 在不同温度下的溶解度:0℃ 1.54 g,20℃ 1.33 g,80℃ 0.85 g。
2 3
①装有盐酸的仪器的名称为_______。
②装置B中盛放的试剂为_______,其作用是_______。
③装置C中除了生成LiHCO ,还可能生成的杂质为_______(填化学式)。
3
④装置C中的反应需在常温下进行,温度越高锂精矿转化率越小的原因可能是_______。保持温度、反应
时间、反应物和溶剂的量不变,实验中提高锂精矿转化率的操作有_______。
⑤热解过滤获得的LiCO 表面有少量LiC O,不进行洗涤也不会影响最终LiCO 产品的纯度,其原因是
2 3 2 2 4 2 3
_______。
(2)设计由盐湖卤水制取高纯LiCO 的实验方案:向浓缩后的盐湖卤水中_______。(实验中必须使用的试剂:
2 3
NaOH溶液、NaCO 溶液;已知:pH= 10时Mg(OH) 完全沉淀)
2 3 2
【答案】(1)①恒压滴液漏斗②饱和NaHCO 溶液 吸收HCl③Ca(HCO ) ④温度升高,LiCO、CO 的溶
3 3 2 2 3 2
解度均较小 加快搅拌速率 ⑤加热烘干时LiC O 会分解,固体产物也为LiCO
2 2 4 2 3
(2)滴入NaOH溶液,边加边搅拌,调节溶液pH等于或稍大于10,过滤,向滤液中加入NaCO 溶液,边加
2 3
边搅拌至无沉淀产生,过滤,用80℃热水洗涤沉淀2~3次,干燥
【解析】装置A用大理石和盐酸反应产生了CO,在装置B中用饱和NaHCO 溶液除去HCl气体杂质,向
2 3
锂精矿中通入CO,将LiCO 转化为溶于水的LiHCO ,发生的反应为LiCO+H O+CO=2LiHCO ,加热分
2 2 3 3 2 3 2 2 3
解LiHCO 得到LiCO,由信息可知,温度越高,LiCO 的溶解度越小,所以蒸发结晶出LiCO 晶体。
3 2 3 2 3 2 3
(1)①装有盐酸的仪器可以起到平衡气压,使盐酸顺利滴下的作用,仪器名称为:恒压滴液漏斗;
②盐酸易挥发,A中产生的CO 混有HCl,所以装置B中应盛放饱和NaHCO 溶液,用来吸收HCl;
2 3
③锂精矿中除含有LiCO,还含有少量的CaCO ,通入CO,会发生反应CaCO +H O+CO= Ca(HCO ),
2 3 3 2 3 2 2 3 2则可能生成的杂质为Ca(HCO );
3 2
④LiCO、CO 溶解度均随温度升高而减小,温度越高锂精矿转化率越小的原因可能是温度升高,
2 3 2
LiCO、CO 的溶解度均较小,不利于反应进行;保持温度、反应时间、反应物和溶剂的量不变,实验中
2 3 2
提高锂精矿转化率的操作有:加快搅拌速率、矿石粉碎等;
⑤LiCO 表面有少量LiC O,由于加热烘干时LiC O 会分解,固体产物也为LiCO,所以不影响产品的
2 3 2 2 4 2 2 4 2 3
纯度;
(2)已知:pH= 10时Mg(OH) 完全沉淀,盐湖卤水中含有Mg2+杂质,需要先加NaOH调节pH大于10,
2
将镁离子转化为Mg(OH) 沉淀除去,过滤掉杂质沉淀,滤液加入NaCO 溶液制得LiCO,最后用热水洗
2 2 3 2 3
涤,减少晶体的溶解,则实验方案为:滴入NaOH溶液,边加边搅拌,调节溶液pH等于或稍大于10,过
滤,向滤液中加入NaCO 溶液,边加边搅拌至无沉淀产生,过滤,用80℃热水洗涤沉淀2~3次,干燥。
2 3
19.(12分)酮基布洛芬片是用于治疗各种关节炎、强直性脊柱炎引起的关节肿痛以及痛经、牙痛、术后
痛和癌性痛等的非处方药。其合成路线如下图所示:
(1)A的化学名称为___________。
(2)B中官能团的名称为___________,B→C的反应类型为___________。。
(3)写出E的结构简式:___________。
(4)写出B与NaOH水溶液加热时的化学反应方程式___________。
(5)H为C的同分异构体,则符合下列条件的H有___________种(同一个碳上连有两个碳碳双键的结构不稳
定)。
①除苯环外不含其他环状结构
②含有硝基,且直接连在苯环上
其中核磁共振氢谱有四组峰,且峰面积之比为2:2:2:1的结构简式为___________。
(6)以乙烷和碳酸二甲酯( )为原料(无机试剂任选),设计制备2一甲基丙酸的
一种合成路线。___________。
【答案】(1)3-甲基苯甲酸
(2)羧基、碳氯键 取代反应(3)
(4) +2NaOH +H O+NaCl
2
(5)16
(6)
【解析】B和NaCN反应生成C,C与SOCl 反应生成D,根据B、D的结构简式可知C是
2
; 和苯反应生成E,根据E的分子式,由F的结构简式逆推,可知E的结构
简式为 。
(1) 的化学名称为间3-基苯甲酸;
(2)B是 ,含有官能团的名称为羧基、碳氯键,B→C是 中的氯原子被-CN
代替,反应类型为取代反应;
(3) 和苯反应生成E,根据E的分子式,由F的结构简式逆推,可知E的结构简式为
;(4)B与NaOH水溶液加热时卤素原子发生水解,且羧基与NaOH反应生成羧酸钠,反应方程式:
+2NaOH +H O+NaCl;
2
(5)①除苯环外不含其他环状结构;②含有硝基,且直接连在苯环上;符合条件的 的同分
异构体,苯环上有2个取代基-NO 、-CH-C≡CH,有3种结构,或者2个取代基为-NO 、-C≡C-CH ,有3
2 2 2 3
种;或者有3个取代基-NO 、-C≡CH,-CH,有10种结构;所以同分异构体种数是6种;
2 3
其中核磁共振氢谱有四组峰,且峰面积之比为2:2:2:1的结构简式为 。
(6)乙烷和氯气在光照条件下发生取代反应生成氯乙烷,氯乙烷和NaCN发生取代反应生成CHCHCN;
3 2
CHCHCN和碳酸二甲酯发生取代反应生成 , 在酸性条件下生成 ,合
3 2
成路线为 。
20.(12分)短链烯烃是重要的有机化工原料,如丙烯(C H)和乙烯等。利用它们间的转化可有效强化节
3 6
能减排,达到“碳达峰”和“碳中和”的目的。请回答下列问题:
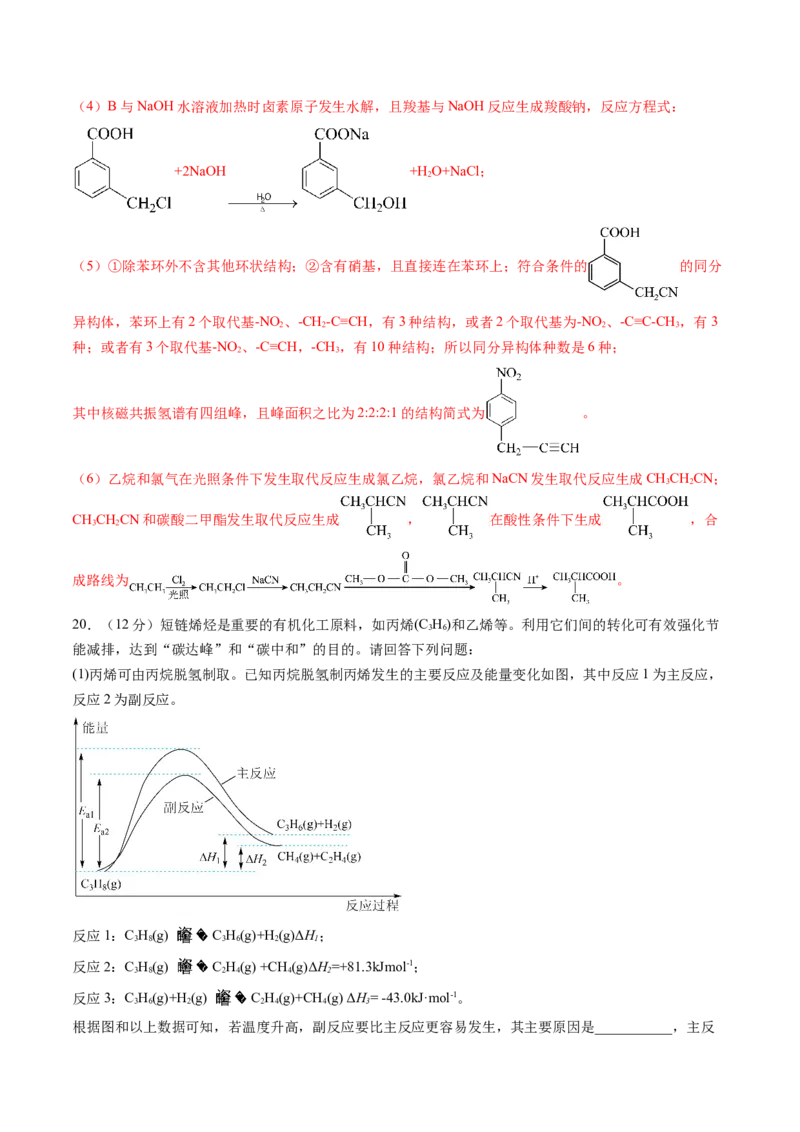
(1)丙烯可由丙烷脱氢制取。已知丙烷脱氢制丙烯发生的主要反应及能量变化如图,其中反应1为主反应,
反应2为副反应。
反应1:C H(g) C H(g)+H(g)ΔH;
3 8 3 6 2 1
反应2:C H(g) C H(g) +CH (g)ΔH=+81.3kJmol-1;
3 8 2 4 4 2
反应3:C H(g)+H(g) C H(g)+CH (g) ΔH= -43.0kJ·mol-1。
3 6 2 2 4 4 3
根据图和以上数据可知,若温度升高,副反应要比主反应更容易发生,其主要原因是___________,主反应的焓变ΔH=___________。
1
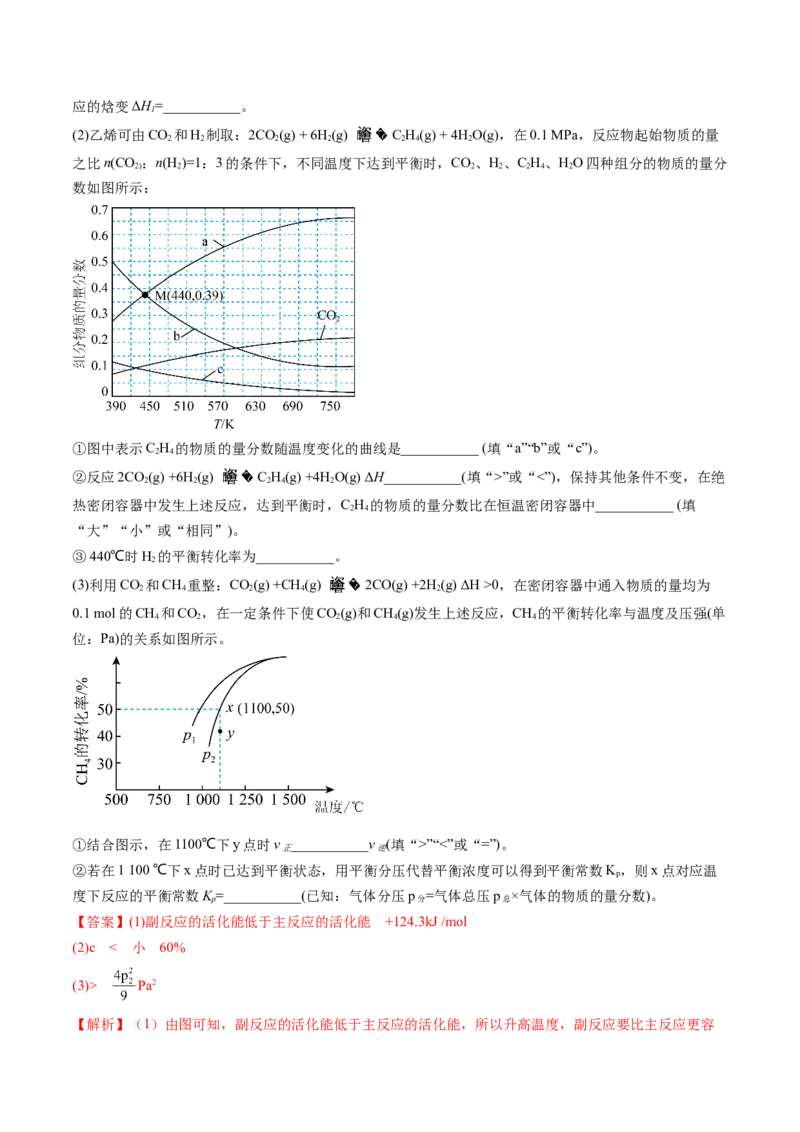
(2)乙烯可由CO 和H 制取:2CO(g) + 6H(g) C H(g) + 4HO(g),在0.1 MPa,反应物起始物质的量
2 2 2 2 2 4 2
之比n(CO :n(H )=1:3的条件下,不同温度下达到平衡时,CO、H、C H、HO四种组分的物质的量分
2) 2 2 2 2 4 2
数如图所示:
①图中表示C H 的物质的量分数随温度变化的曲线是___________ (填“a”“b”或“c”)。
2 4
②反应2CO(g) +6H (g) C H(g) +4H O(g) ΔH___________(填“>”或“<”),保持其他条件不变,在绝
2 2 2 4 2
热密闭容器中发生上述反应,达到平衡时,C H 的物质的量分数比在恒温密闭容器中___________ (填
2 4
“大”“小”或“相同”)。
③440℃时H 的平衡转化率为___________。
2
(3)利用CO 和CH 重整:CO(g) +CH (g) 2CO(g) +2H (g) ΔH >0,在密闭容器中通入物质的量均为
2 4 2 4 2
0.1 mol的CH 和CO,在一定条件下使CO(g)和CH(g)发生上述反应,CH 的平衡转化率与温度及压强(单
4 2 2 4 4
位:Pa)的关系如图所示。
①结合图示,在1100℃下y点时v ___________v (填“>”“<”或“=”)。
正 逆
②若在1 100 ℃下x点时已达到平衡状态,用平衡分压代替平衡浓度可以得到平衡常数K,则x点对应温
p
度下反应的平衡常数K =___________(已知:气体分压p =气体总压p ×气体的物质的量分数)。
p 分 总
【答案】(1)副反应的活化能低于主反应的活化能 +124.3kJ /mol
(2)c < 小 60%
(3)> Pa2
【解析】(1)由图可知,副反应的活化能低于主反应的活化能,所以升高温度,副反应要比主反应更容易发生;由盖斯定律可知,反应2—反应3得到反应1,则主反应的焓变ΔH=( +81.3)—(—43.0 kJ
1
/mol)=+124.3kJ /mol,故答案为:副反应的活化能低于主反应的活化能;+124.3kJ /mol;
(2)①由图中表示二氧化碳物质的量分数随温度变化的曲线可知,表示氢气的物质的量分数随温度变化
的曲线是a,由方程式可知,水蒸气的物质的量分数是乙烯物质的量分数的4倍,则表示水蒸气和乙烯的
物质的量分数随温度变化的曲线分别是b、c,故答案为:c;
②由图可知,升高温度,二氧化碳的物质的量分数增大,说明平衡向逆反应方向移动,该反应为放热反应,
反应的焓变ΔH小于0;保持其他条件不变,在绝热密闭容器中发生上述反应,反应放出的热量会使反应
温度升高,平衡向逆反应方向移动,所以乙烯的物质的量分数比在恒温密闭容器中小,达到平衡时,故答
案为:<;小;
③由图可知,440℃时氢气和水蒸气的物质的量分数都为0.39,设起始二氧化碳、氢气的物质的量为
1mol、3mol,平衡时生成乙烯的物质的量为amol,由方程式可得:3—6a=4a,解得a=0.3,则氢气的转化
率为 ×100%=60%,故答案为:60%;
(3)①由图可知,1100℃时y点反应未达到平衡,正反应速率大于逆反应速率,故答案为:>;
②由图可知,1100℃反应达到平衡时,甲烷的转化率为50%,由方程式可知,平衡时二氧化碳、甲烷、一
氧化碳、氢气的物质的量分别为0.1mol—0.1mol×50%=0.05mol、0.1mol—0.1mol×50%=0.05mol、
0.1mol×50%×2=0.1mol、0.1mol×50%×2=0.1mol,则反应的分压常数K =
p
= Pa2,故答案为: Pa2。