文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(河北专用)
黄金卷07
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64 Ce 140
第Ⅰ卷
一、单项选择题:共14题,每题3分,共42分。每题只有一个选项最符合题意。
1.我国自主设计建造的亚洲第一深水导管架“海基一号”在广东珠海建造完工,开创了我国深海油气资
源开发的新模式。下列有关说法正确的是
A.“海基一号”成功从深海开采石油和天然气水合物,天然气属于新能源
B.深海开采勘察船采用的新型钛合金材料硬度大、韧性好,具有良好的抗压性能
C.石油的分馏和裂解都是化学变化
D.导管架海水浸泡区可采用镶嵌铜块的方法从而保障钢材不易被腐蚀
【答案】B
【解析】A.天然气属于一次能源,被消耗后不可再生,在燃烧时会产生污染环境的气体,不属于新能
源,选项A错误;
B.合金比成分金属硬度更大、韧性更好,选项B正确;
C.石油的分馏属于物理变化,选项C错误;
D.铜没有铁活泼,不可失去电子牺牲阳极保障船体不易被腐蚀,选项D错误;
故选B。
2.下列化学用语或表述正确的是
A. 的电子式: B. 的VSEPR模型为
C.基态 原子价电子排布式: D.顺-2-丁烯的结构简式:
【答案】A
【解析】A.根据 的结构式,其电子式为 ,A正确;
B. 含有3个键对,1个孤对 分子VSEPR模型为三角锥型,B错误;C.Ni有28个电子,基态 原子价电子排布式: ,C错误;
D. 为反-2-丁烯的结构简式,D错误;
故选A。
3.N 为阿伏加德罗常数的值。下列说法正确的是
A
A.标准状况下,4gSO 中电子的数目为2N
3 A
B.常温常压下,2.24L氨气中共价键的数目为0.3N
A
C.46gNO 和NO 的混合气体中所含氮原子的数目为1.5N
2 2 4 A
D.常温下,1.0LpH=12的Ba(OH) 溶液中OH-的数目是0.02N
2 A
【答案】A
【解析】A.4gSO 的物质的量为: ,则其中含有的电子数为0.05×40=2 N ,A正确;
3 A
B.不是标准状况,无法计算其物质的量,B错误;
C.NO 与NO 的最简式均为NO ,46g该混合气体可看成只由NO 组成,所含N原子数为
2 2 4 2 2
,C错误;
D.25℃时, 为12的 溶液中,含有OH-的物质的量为1L×0.01mol/L=0.01mol,则含有OH-数
目为0.01 NA,D错误;
故选A。
4.下列过程中的化学反应,相应的离子方程式正确的是
A. 在碱性环境中被空气氧化:
B.氢氧化铁加入氢碘酸溶液中:
C.用铁作阳极电解氯化镁溶液:
D.碳酸钙加入乙酸溶液中:【答案】A
【解析】A. 被氧气氧化为 ,在碱性环境中生成 沉淀,A正确;
B.氢氧化铁加入氢碘酸溶液中,反应的离子方程式为 ,B错误;
C.阳极材料为铁时,铁失去电子,反应的离子方程式为 ,C错误;
D.碳酸钙加入乙酸溶液中,反应的离子方程式为
,D错误;
故选A。
5.下列实验能达到实验目的的是
A.制取 B.测定 溶液的浓度
C.验证相同温度下的溶解度: D.检验 溶液是否变质
【答案】A
【解析】A.实验室制备 ,可用NaSO 粉末和70%的硫酸反应,故A正确;
2 3
B.高锰酸钾溶液具有强氧化性,不能盛装在碱式滴定管中,会氧化橡胶管,故B错误;
C.图中NaOH溶液过量,一定会与FeCl 溶液反应生成氢氧化铁沉淀,无法证明溶解度:
3
,故C错误;
D.稀硝酸能将NaSO 氧化NaSO ,与BaCl 作用生成沉淀,无法检验是否变质,故D错误;
2 3 2 4 2
故选A。
6.下列实验设计、现象和结论都正确的是选
实验操作及现象 实验结论
项
取少量 样品溶于水,加入 溶液,再加入足量盐酸,
A 原样品已变质
产生白色沉淀
B 向某溶液中滴加浓盐酸,将产生气体通入石蕊试液,溶液先变红后褪色 溶液中含有 或
气体X不一定是氧化性
C 向溶有 的 溶液中通入气体X,出现白色沉淀
气体
该固体试样中不可能存
在某固体试样加水后的溶液中,滴加 溶液,没有产生使湿润红色
D
石蕊试纸变蓝的气体 在
【答案】C
【解析】A.若样品未变质,在溶液中亚硫酸氢根离子与硝酸根离子发生氧化还原反应,亚硫酸氢根离子
被硝酸根离子氧化为硫酸根离子,也会与钡离子反应产生白色沉淀,故结论无法得出,A不符合题意;
B.若溶液中含有 或 ,滴加稀盐酸产生二氧化硫气体,通入石蕊试液中石蕊会变红,但二氧化硫
无法漂白石蕊,故溶液不会褪色,B不符合题意;
C.气体X可以是氨气,与二氧化硫一起通入氯化钡溶液后,氨气与二氧化硫优先反应,生成亚硫酸铵,
后与氯化钡复分解生成亚硫酸钡白色沉淀,C符合题意;
D. 与氢氧根离子反应若不加热或者碱溶液浓度不够只能够生成一水合氨,不会产生氨气,故D不符
合题意;
故选C。
7.X、Y、Z、W是原子半径依次增大的短周期主族元素,X与其他元素不在同一周期,Y元素的电负性
仅次于氟元素,Z的基态原子中单电子与成对电子个数比为3∶4,W原子电子总数与Y原子的最外层电子
数相同。下列说法正确的是
A.第一电离能:Z>Y>W B.基态Z原子核外电子有7种空间运动状态
C.由四种元素组成的化合物仅含共价键 D.X、Y形成的化合物都是由极性键构成的极性分子
【答案】A
【分析】由题干信息可知,X、Y、Z、W是原子半径依次增大的短周期主族元素,X与其他元素不在同一
周期,Y元素的电负性仅次于氟元素,则Y为O,Z的基态原子成单电子与成对电子个数比为3:4,即电
子排布式为:1s22s22p3,则Z为N,W原子电子总数与Y原子的最外层电子数相同,则W为C,X为H,
据此分析解题。
【解析】A.由分析可知,Y为O,Z为N,W为C,根据同一周期第一电离能从左往右呈增大趋势,ⅡA、ⅤA比相邻元素都高,故第一电离能N>O>C即Z>Y>W,A正确;
B.由分析可知,Z为N,核外有7个电子,电子排布式为:1s22s22p3,故基态Z原子核外电子有5种空间
运动状态,B错误;
C.由四种元素组成的化合物即(NH )CO、NH HCO 等,既含有共价键又含有离子键,C错误;
4 2 3 4 3
D.由分析可知,X为H,Y为O,故X、Y形成的化合物HO由极性键构成的极性分子,但HO 是由极
2 2 2
性键和非极性键组成的极性分子,D错误;
故选A。
8.汞钡铜氧晶体的晶胞如图A所示,通过掺杂Ca2+获得的具有更高临界温度的超导材料如图B所示。下
列说法正确的是
A.掺杂后晶体密度增大是因为晶胞中增加了1个Ca2+
B.汞钡铜氧晶体中的Hg和Cu个数比为1∶2
C.图A晶胞中一个Ba的分数坐标为( , , ),则另一个( , , )
D.图B晶胞中Ca周围距离最近的Hg数目和Hg周围距离最近的Ca的数目不同
【答案】C
【解析】A.由图A可知,汞钡铜氧晶体的晶胞中含 个Hg,2个Ba, 个Cu,
个O,掺杂Ca2+后,晶胞中含 个Hg,2个Ba, 个Cu, 个
O,1个Ca2+,所以掺杂后晶体密度增大不是因为晶胞中增加了1个Ca2+,故A错误;
B.由汞钡铜氧晶体的晶胞可知,Hg位于晶胞的顶点,则一个晶胞中含 个Hg,Cu位于晶胞的棱上,则则一个晶胞中含 个Cu,汞钡铜氧晶体中的Hg和Cu个数比为1∶1,故B错误;
C.图A晶胞中两个Ba位于同一轴上,若一个Ba的分数坐标为( , , ),则另一个Ba的分数坐标
为( , , ),故C正确;
D.图B晶胞中Ca周围距离最近的Hg数目为8,Hg周围距离最近的Ca的数目也为8,则图B晶胞中Ca
周围距离最近的Hg数目和Hg周围距离最近的Ca的数目相同,故D错误;
故选C。
9.β﹣生育酚是天然维生素E的一种水解产物,具有较高的生物活性,其结构简式如图。下列有关β﹣生
育酚的说法正确的是
A.1个分子中含有47个氢原子 B.该分子中含有6个甲基
C.环上的一氯代物只有1种 D.能发生取代反应和加成反应
【答案】D
【解析】A.根据β﹣生育酚的结构简式可知,分子中含有48个氢原子,A错误;
B.根据β﹣生育酚的结构简式可知,含有7个甲基,B错误;
C.根据β﹣生育酚的结构简式可知,环上含有3种氢原子,则环上的一氯代物只有3种,C错误;
D.结构中具有苯环、酚羟基,苯环能发生加成反应和取代反应,D正确;
故选D。
10.钠硒电池是一类以单质硒或含硒化合物为正极、金属钠为负极的新型电池,具有能量密度大、导电率
高、成本低等优点。以 填充碳纳米管作为正极材料的一种钠硒电池工作原理如图所示,充放电过程
中正极材料立方晶胞内未标出因放电产生的0价Cu原子。下列说法正确的是A.每个 晶胞中 个数为
B.放电时,正极的电极反应式为
C.充电时外电路中转移1mol电子,两极质量变化差为23g
D.在 晶胞结构中,晶胞参数为a pm,则其密度为
【答案】B
【解析】A.由题意可知, 填充碳纳米管作为正极材料,钠较为活泼,钠为负极材料。根据“均摊
法”,每个 晶胞中含 个Se,则晶胞内铜离子、亚铜离子和为 个,设铜离
子、亚铜离子分别为a、b,则 ,由化合价代数和为零可知, ,解得 ,
,A错误;
B.放电时,正极 得到电子发生还原反应生成零价铜,电极反应式为
,B正确;
C.充电时外电路中转移1mol电子,阳极释放出1mol钠离子,质量减小23g,阴极生成1mol钠,质量增
加23g,两极质量变化差为46g,C错误;D.晶胞中 有8个, 有4个,故在计算个数时要乘4,正确故选 ,D错误;
故选B。
11.X、Y、Z、W为原子序数依次增大的四种短周期主族元素,A、B、C、D、E为上述四种元素中的一
种或几种所组成的物质。已知Y元素最外层电子数是内层的3倍,Z与Y同主族,A中含有18个电子,D
有漂白性,五种物质间的转化关系如图所示,下列说法正确的是
A.简单气态氢化物的稳定性:W>Y>Z B.离子半径:W>Z>Y
C.A与C可以反应生成B D.X和Y组成的二元化合物中不含有非极性键
【答案】C
【分析】X、Y、Z、W为原子序数依次增大的四种短周期主族元素,A、B、C、D、E为上述四种元素中
的一种或几种所组成的物质,已知Y元素最外层电子数是内层的3倍,则Y为O元素;Z与Y同主族,则
Z为S元素、W为Cl元素;E、B分别为Y、Z元素对应的单质,A中含有18个电子,D有漂白性,结合
图中转化可知,A为HS、D为HClO、B为S、E为O、C为SO ,则X为H元素。
2 2 2
【解析】A.元素的非金属性越强,简单气态氢化物的稳定性越强,元素的非金属性强弱顺序为O>Cl>S,
则简单气态氢化物的稳定性强弱顺序为O>Cl>S,故A错误;
B.电子层结构相同的离子,核电荷数越大,离子的离子半径越小,则硫离子的离子半径大于氯离子,故
B错误;
C.硫化氢与二氧化硫发生氧化还原反应生成硫和水,故C正确;
D.过氧化氢分子是含有极性键和非极性键的共价化合物,故D错误;
故选C。
12.钛酸钡 是一种压电材料,主要用于电子陶瓷、PTC热敏电阻、电容器等多种电子元器件的配
制。某工厂以重晶石 为原料,生产 的工业流程如下图,下列说法不正确的是资料:“焙烧”后固体产物有 、易溶于水的BaS和微溶于水的CaS
A.“焙烧”步骤中碳粉的主要作用是做还原剂,将 还原
B.“酸化”中的酸为硫酸
C.“沉淀”步骤中生成 的化学方程式为:
D.“热分解”生成粉状钛酸钡,产生的
【答案】B
【分析】重晶石 、炭粉、氯化钙焙烧生成 、BaS、 CaS和CO,浸取、过滤,滤渣为CaS,滤
液中含有 、BaS;加盐酸酸化,把BaS转化为 ,浓缩结晶得 固体,用水溶液 ,加
TiCl 、草酸铵生成 沉淀, 加热分解生成 ;
4
【解析】A.“焙烧”步骤中碳粉的主要作用是做还原剂,将 还原为BaS,故A正确;
B. 与硫酸反应生成硫酸钡沉淀,“酸化”中的酸不能为硫酸,应该为盐酸,故B错误;
C.“沉淀”步骤中 、TiCl 、草酸铵反应生成 沉淀,反应的化学方程式为:
4
,故C正确;
D.“热分解”时, 分解生成粉状钛酸钡,根据元素守恒,产生的 ,故
D正确;故选B。
13.中石化的《丁烯双键异构化的方法》获得第二十届中国专利优秀奖。在100kPa和298K下,丁烯双键
异构化反应的机理如图所示。下列说法不正确的是
A.上述两种烯烃均能发生加成反应、氧化反应
B.CH=CH﹣CH﹣CH 比CH﹣CH=CH﹣CH 的稳定性差
2 2 3 3 3
C.丁烯的同分异构体只有上述2种结构
D.以上两种丁烯分子,每个分子中最多都有8个原子在同一平面上
【答案】C
【解析】A.烯烃均含有碳碳双键,故能发生加成反应和氧化反应,A正确;
B.能量越低越稳定CH=CH﹣CH﹣CH 能量高更不稳定,故CH=CH﹣CH﹣CH 比CH﹣CH=CH﹣CH
2 2 3 2 2 2 3 3
的稳定性差,B正确;
C.丁烯的同分异构体有2﹣丁烯、2﹣甲基丙烯、甲基环丙烷,C错误;
D.乙烯中所有原子共平面、2﹣丁烯相当于乙烯分子中的两个氢原子被两个甲基取代,甲基中的3个氢原
子通过旋转最多有1个氢原子与之共面,所以以上两种丁烯分子,,每个分子中最多都有8个原子在同一
平面上,D正确;
故选C。
14.两份 溶液中,分别滴加未知浓度的 溶液和 溶液,两溶液中的
和 随所加入溶液体积的变化如图所示,下列有关说法不正确的是(已知:
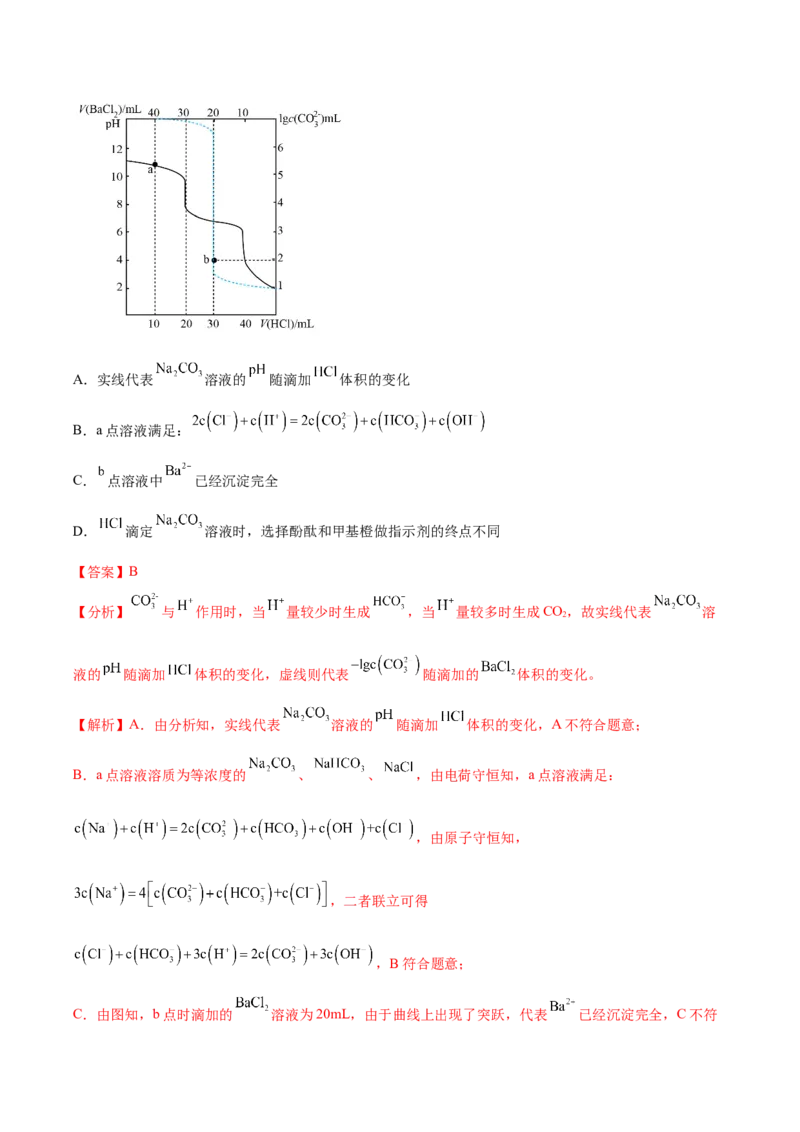
)A.实线代表 溶液的 随滴加 体积的变化
B.a点溶液满足:
C. 点溶液中 已经沉淀完全
D. 滴定 溶液时,选择酚酞和甲基橙做指示剂的终点不同
【答案】B
【分析】 与 作用时,当 量较少时生成 ,当 量较多时生成CO,故实线代表 溶
2
液的 随滴加 体积的变化,虚线则代表 随滴加的 体积的变化。
【解析】A.由分析知,实线代表 溶液的 随滴加 体积的变化,A不符合题意;
B.a点溶液溶质为等浓度的 、 、 ,由电荷守恒知,a点溶液满足:
,由原子守恒知,
,二者联立可得
,B符合题意;
C.由图知,b点时滴加的 溶液为20mL,由于曲线上出现了突跃,代表 已经沉淀完全,C不符合题意;
D.用酚酞作指示剂时滴定的总反应为:NaCO+HCl=NaHCO +NaCl,用甲基橙作指示剂时滴定的总反应
2 3 3
为:NaCO+2HCl=2NaCl+CO ↑+H O,故二者滴定终点不同,D不符合题意;
2 3 2 2
故选B。
第Ⅱ卷
二、非选择题:共4题,共58分。
15.(14分)己二酸( )是一种重要的化工原料和合成中间体。某实验小组以钨磷酸为催化
剂,开展己二酸的合成及性质探究实验。
Ⅰ.催化剂钨磷酸晶体(H PW O )的制备
3 12 40
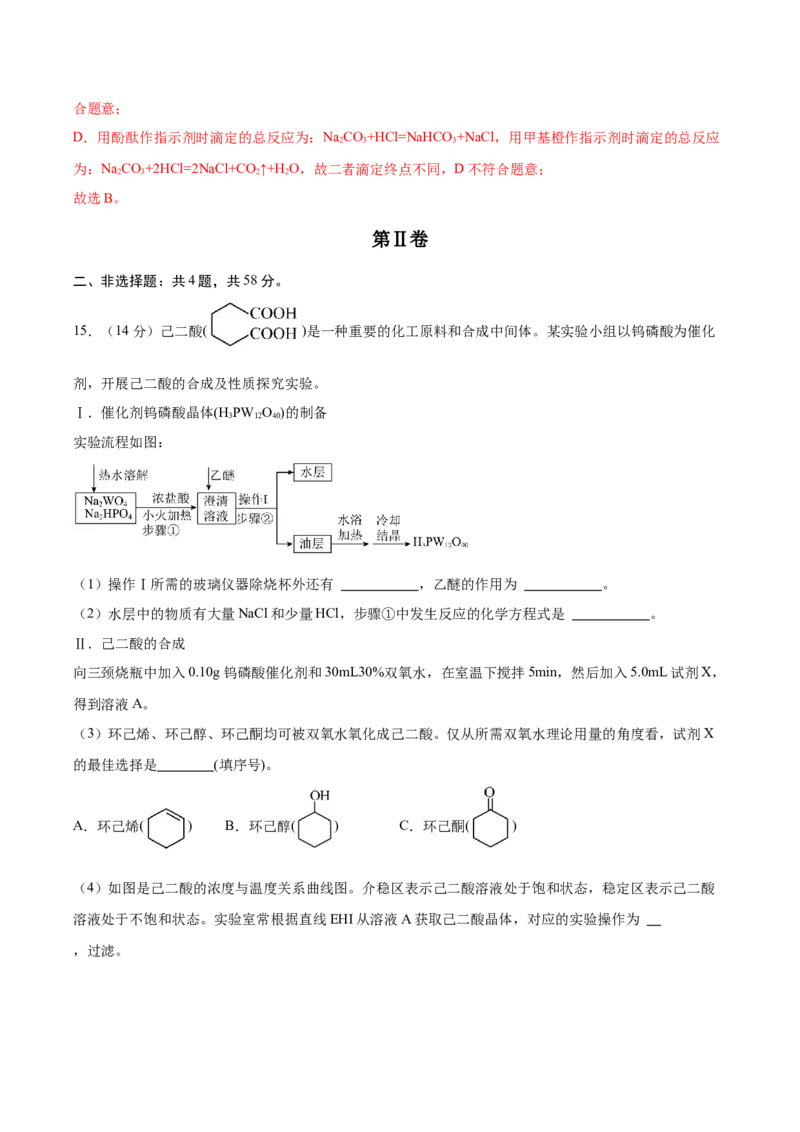
实验流程如图:
(1)操作Ⅰ所需的玻璃仪器除烧杯外还有 ,乙醚的作用为 。
(2)水层中的物质有大量NaCl和少量HCl,步骤①中发生反应的化学方程式是 。
Ⅱ.己二酸的合成
向三颈烧瓶中加入0.10g钨磷酸催化剂和30mL30%双氧水,在室温下搅拌5min,然后加入5.0mL试剂X,
得到溶液A。
(3)环己烯、环己醇、环己酮均可被双氧水氧化成己二酸。仅从所需双氧水理论用量的角度看,试剂X
的最佳选择是 (填序号)。
A.环己烯( ) B.环己醇( ) C.环己酮( )
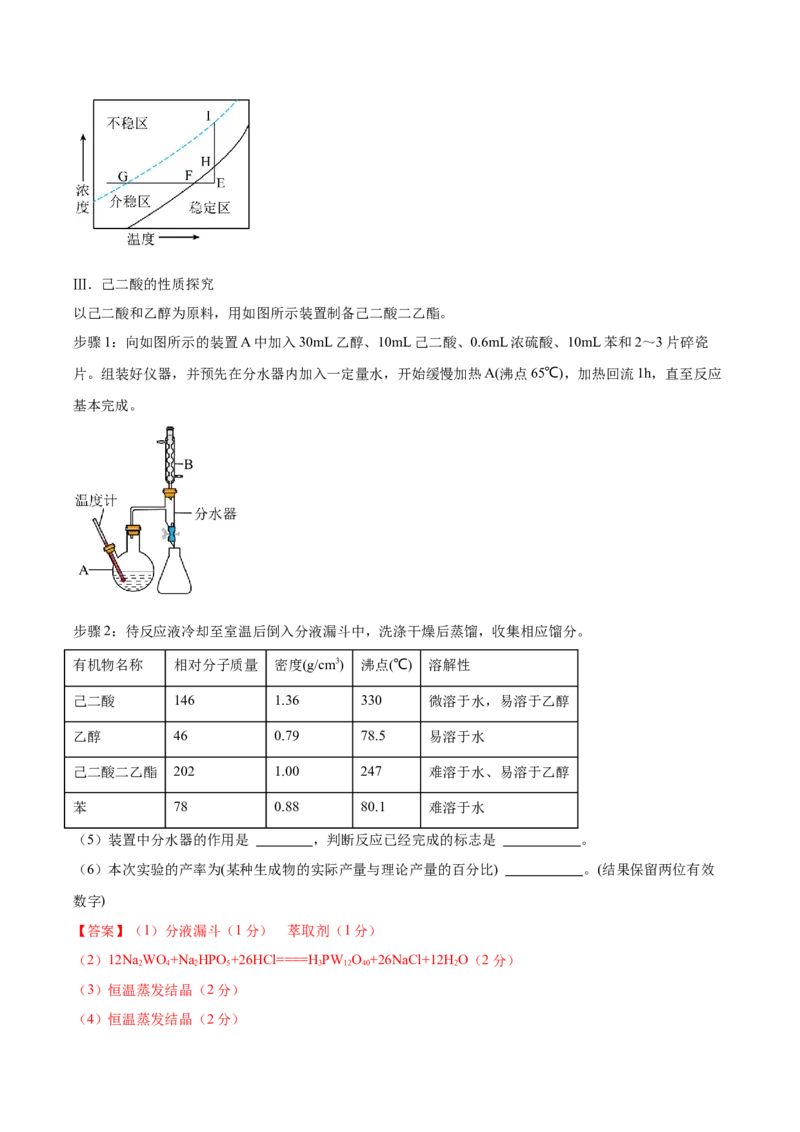
(4)如图是己二酸的浓度与温度关系曲线图。介稳区表示己二酸溶液处于饱和状态,稳定区表示己二酸
溶液处于不饱和状态。实验室常根据直线EHI从溶液A获取己二酸晶体,对应的实验操作为
,过滤。Ⅲ.己二酸的性质探究
以己二酸和乙醇为原料,用如图所示装置制备己二酸二乙酯。
步骤1:向如图所示的装置A中加入30mL乙醇、10mL己二酸、0.6mL浓硫酸、10mL苯和2~3片碎瓷
片。组装好仪器,并预先在分水器内加入一定量水,开始缓慢加热A(沸点65℃),加热回流1h,直至反应
基本完成。
步骤2:待反应液冷却至室温后倒入分液漏斗中,洗涤干燥后蒸馏,收集相应馏分。
有机物名称 相对分子质量 密度(g/cm3) 沸点(℃) 溶解性
己二酸 146 1.36 330 微溶于水,易溶于乙醇
乙醇 46 0.79 78.5 易溶于水
己二酸二乙酯 202 1.00 247 难溶于水、易溶于乙醇
苯 78 0.88 80.1 难溶于水
(5)装置中分水器的作用是 ,判断反应已经完成的标志是 。
(6)本次实验的产率为(某种生成物的实际产量与理论产量的百分比) 。(结果保留两位有效
数字)
【答案】(1)分液漏斗(1分) 萃取剂(1分)
(2)12NaWO+Na HPO +26HCl====HPW O +26NaCl+12HO(2分)
2 4 2 5 3 12 40 2
(3)恒温蒸发结晶(2分)
(4)恒温蒸发结晶(2分)(5)使反应向正反应方向移动,提高原料转化率(2分) 分水器中不再有水生成或分水器中水的液面不
变时(2分)
(6)51%(2分)
【分析】Ⅰ.Na WO 和NaHPO 热水溶解,加入浓盐酸并小火加热,加入乙醚萃取HPW O ,然后分液,
2 4 2 4 3 12 40
水层中的物质有大量NaCl和少量HCl,则步骤①中发生反应的化学方程式为
12NaWO+Na HPO +26HCl====HPW O +26NaCl+12HO,油层中含有HPW O ,油层水浴加热然后冷
2 4 2 4 3 12 40 2 3 12 40
却结晶得到晶体HPW O ;
3 12 40
Ⅱ.(3)A. 环己烯( )中C元素平均化合价为 , 中C元素的平均化合价为 ;
B. 环己醇( )中C元素平均化合价为 , 中C元素的平均化合价为 ;
C. 环己酮( )中C元素平均化合价为 , 中C元素的平均化合价为 ;
得到相同物质的量的己二酸时选项中转移电子越少,则消耗双氧水的量越少;
(4)根据图知,稳定相同时,溶液浓度越大,其稳定性越差;浓度相同时,稳定越高其稳定性越好;实
验室常根据直线EHI从溶液A获取己二酸晶体,该操作过程中溶液温度不变,溶液浓度增大;
Ⅲ.(5)反应生成水,通过分水器不断分离出水可以使反应向正反应方向移动;浓硫酸作用是催化剂和吸
水剂;由于反应生成水,分水器水层液面不断上升,待分水器中水层不再增加时,表示反应已基本完成;
(6)根据反应过程,乙醇过量,根据己二酸计算产率。
【解析】(1)操作I为萃取,操作Ⅰ所需的玻璃仪器除烧杯外还有分液漏斗,HPW O 易溶于有机溶
3 12 40
剂,NaCl,所以用乙醚萃取HPW O ,则乙醚的作用为作萃取剂,将钨磷酸转移到乙醚中;
3 12 40
(2)通过以上分析知,步骤①中发生反应的化学方程式为
12NaWO+Na HPO +26HCl====HPW O +26NaCl+12HO;
4 4 2 7 3 12 40 2
(3)由分子式可知,1mol环己烯和1mol环己醇转化为己二酸时8mol电子,1mol环己酮转化为己二酸时
失去6mol电子,由得失电子数目守恒可知,生成等量的己二酸,环己酮消耗过氧化氢的物质的量最少,
则试剂X为环己酮,故选C;
(4)据图知,温度一定时,介稳区表示己二酸溶液处于饱和状态;实验室常根据直线EHI从溶液A获取己二酸晶体,溶液浓度增大,对应的实验操作为恒温蒸发结晶;
(5)由于反应生成水,通过分水器不断分离出水可以使反应向正反应方向移动;由于反应生成水,待分
水器中水层不再增加时,故分水器中不再有水生成或分水器中水的液面不变时;
(6)30mL乙醇物质的量为 ≈0.6mol, ≈6.09mol ~
2CH3CH OH~己二酸二乙酯,乙醇过量,产率为 ×100%≈51%。
7
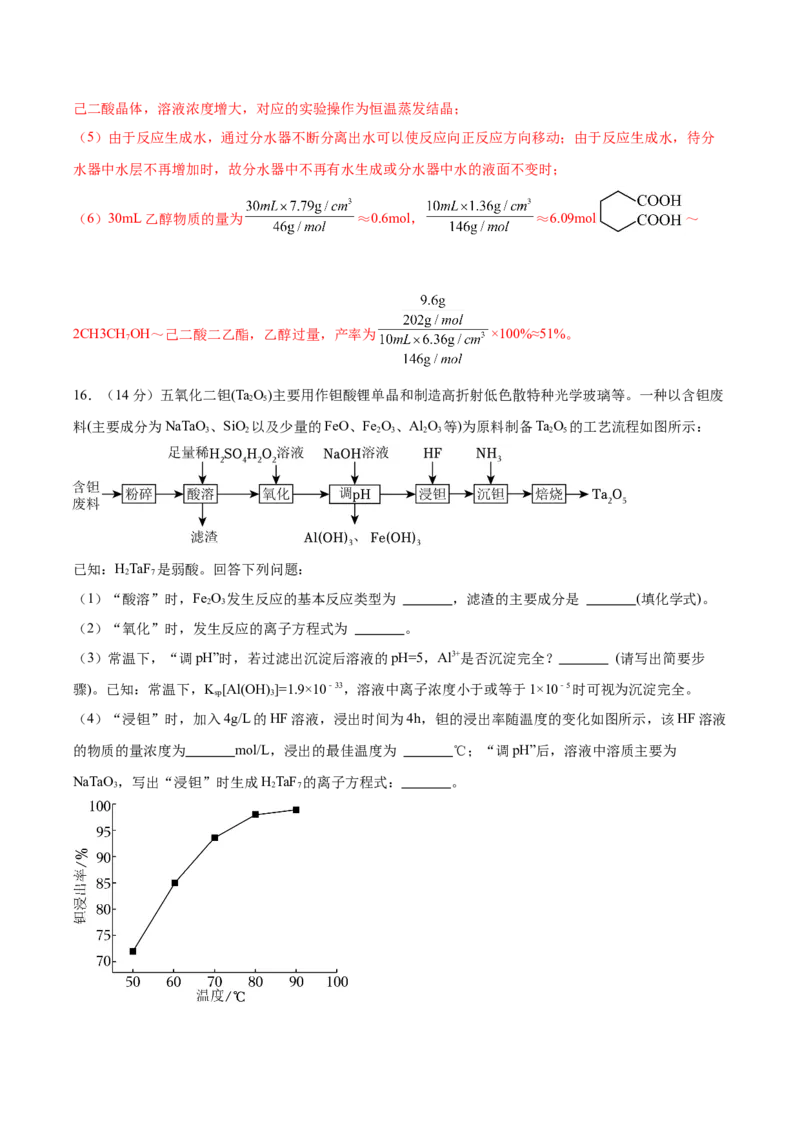
16.(14分)五氧化二钽(TaO)主要用作钽酸锂单晶和制造高折射低色散特种光学玻璃等。一种以含钽废
2 5
料(主要成分为NaTaO 、SiO 以及少量的FeO、Fe O、Al O 等)为原料制备TaO 的工艺流程如图所示:
3 2 2 3 2 3 2 5
已知:HTaF 是弱酸。回答下列问题:
2 7
(1)“酸溶”时,Fe O 发生反应的基本反应类型为 ,滤渣的主要成分是 (填化学式)。
2 3
(2)“氧化”时,发生反应的离子方程式为 。
(3)常温下,“调pH”时,若过滤出沉淀后溶液的pH=5,Al3+是否沉淀完全? (请写出简要步
骤)。已知:常温下,K [Al(OH) ]=1.9×10﹣33,溶液中离子浓度小于或等于1×10﹣5时可视为沉淀完全。
sp 3
(4)“浸钽”时,加入4g/L的HF溶液,浸出时间为4h,钽的浸出率随温度的变化如图所示,该HF溶液
的物质的量浓度为 mol/L,浸出的最佳温度为 ℃;“调pH”后,溶液中溶质主要为
NaTaO ,写出“浸钽”时生成HTaF 的离子方程式: 。
3 2 7(5)“沉钽”时,生成Ta(OH),反应化学方程式为 。
5
【答案】(1)复分解反应(1分) SiO(2分)
2
(2)2H++2Fe2++H O=2H O+2Fe3+(2分)
2 2 2
(3)沉淀完全(1分)
(4)0.2(2分) 80(2分) 7HF+TaO +H+= H TaF +3H O(2分)
2 7 2
(5)HTaF +7NH•H O=Ta(OH) +7NHF+2HO(2分)
2 7 3 2 5 4 2
【分析】以含钽废料(主要成分为NaTaO 、SiO 以及少量的FeO、Fe O、Al O 等)为原料制备TaO,含钽
3 2 2 3 2 3 2 5
废料先粉碎,然后加入稀硫酸酸溶,SiO 不溶于硫酸,FeO、Fe O、Al O 等溶解生成Fe2+、Fe3+、Al3+,加
2 2 3 2 3
双氧水将Fe2+氧化成Fe3+,然后加入氢氧化钠溶液调节pH生成氢氧化铁、氢氧化铝沉淀,过滤得到对应沉
淀,“调pH”后,溶液中溶质主要为NaTaO ,“浸钽”时生成HTaF 和水,“沉钽”时,HTaF 与
3 2 7 2 7
NH •H O反应生成Ta(OH),焙烧得TaO。
3 2 5 2 5
【解析】(1)“酸溶”时,Fe O 发生Fe O+3H SO =Fe (SO )+3H O反应,属于复分解反应,SiO 不溶于
2 3 2 3 2 4 2 4 3 8 2
硫酸,滤渣的主要成分是SiO,故选复分解反应;SiO;
2 6
(2)加双氧水将Fe2+氧化成Fe3+,发生反应的离子方程式为2H++2Fe2++H O=2H O+2Fe3+;
2 2 2
(3)常温下,“调pH=5”时,此时溶液中c(OH﹣)=1×10﹣9mol/L,可得c(Al3+)=
,Al7+沉淀完全;
(4)HF溶液的物质的量浓度c(HF)= = =2.2mol/L,由图可知,浸出的最佳温度为80℃,温度过
低,浸出率低,温度过高,Ta浸出率变化不大,但耗能增大;“调pH”后,溶液中溶质主要为NaTaO ,
3
“浸钽”时生成HTaF 和水,离子方程式:7HF+TaO +H+= H TaF +3H O,
2 7 2 7 2
故选0.2;80;7HF+TaO +H+= H TaF +3H O;
2 7 2
(5)“沉钽”时通入氨气,生成了一水合氨,HTaF 与NH •H O反应生成Ta(OH),反应化学方程式为
2 7 3 2 5
HTaF +7NH•H O=Ta(OH) +7NHF+2HO。
2 7 3 2 5 4 2
17.(15分)氨是重要的基础化工原料,可以制备亚硝酸(HNO)、连二次硝酸(H NO)、尿素[CO(NH)]
2 2 2 2 2 2
等多种含氮的化工产品。
(1)NH 极易溶于水且溶液显碱性,请用化学方程式解释原因: 。
3(2)25℃时,亚硝酸和连二次硝酸的电离常数如下表所示:
化学式 HNO HNO
2 2 2 2
电离常数 K=5.1×10-4 K =6.17×10-8、K =2.88×10-12
a a1 a2
①物质的量浓度相同的NaNO 和NaHN O 溶液的pH(NaHNO) pH(NaNO)(填“>”、“<”或
2 2 2 2 2 2
“=”)。
②25℃时NaHN O 溶液中存在水解平衡,其水解常数K= (保留三位有效数字)。
2 2 h
③0.1mol/LNa NO 溶液中离子浓度由大到小的顺序为 。
2 2 2
(3)以NH 与CO 为原料可以合成尿素[CO(NH)],涉及的化学反应如下:
3 2 2 2
反应Ⅰ:2NH (g)+CO (g) NH CONH (s) ΔH=﹣159.5kJ•mol-1;
3 2 2 2 4 1
反应Ⅱ:NH CONH (s) CO(NH)(s)+HO(g) ΔH=+116.5kJ•mol-1;
2 2 4 2 2 2 2
反应Ⅲ:HO(l)=HO(g) ΔH=+44.0kJ•mol-1。
2 2 3
则反应Ⅳ:NH 与CO 合成尿素同时生成液态水的热化学方程式为 。
3 2
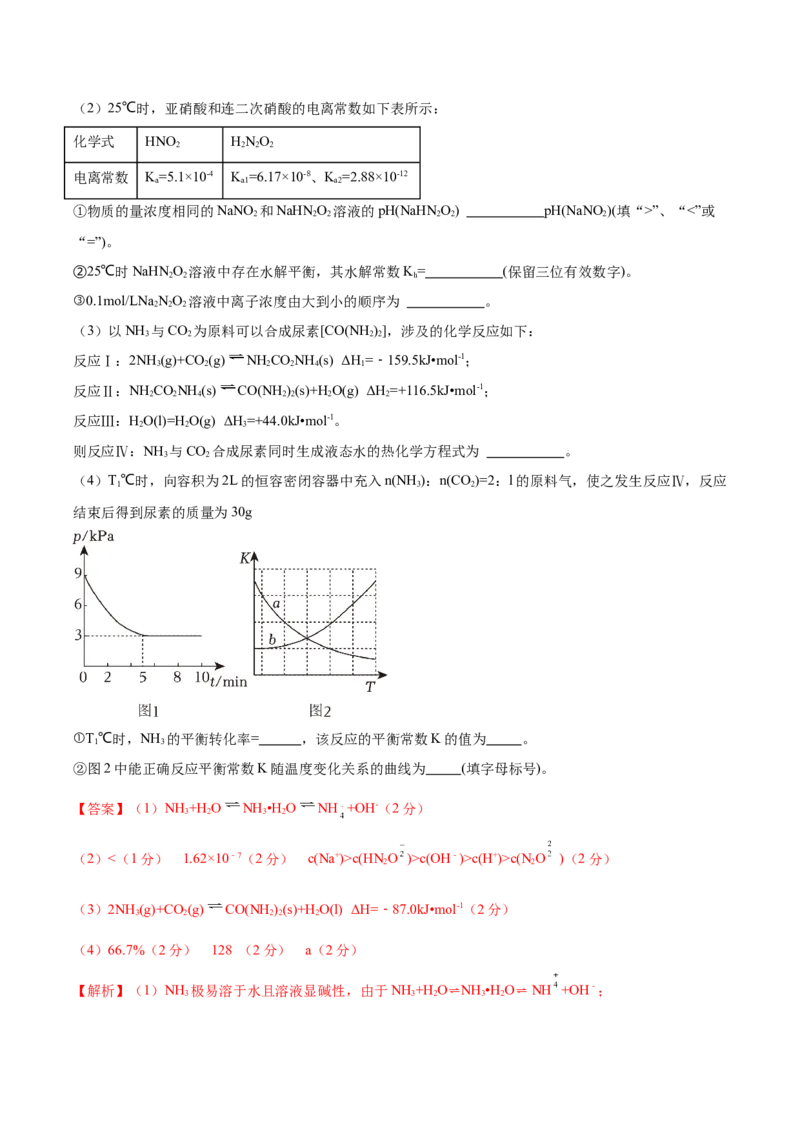
(4)T℃时,向容积为2L的恒容密闭容器中充入n(NH ):n(CO)=2:l的原料气,使之发生反应Ⅳ,反应
1 3 2
结束后得到尿素的质量为30g
①T℃时,NH 的平衡转化率= ,该反应的平衡常数K的值为 。
1 3
②图2中能正确反应平衡常数K随温度变化关系的曲线为 (填字母标号)。
【答案】(1)NH +H O NH •H O NH +OH-(2分)
3 2 3 2
(2)<(1分) 1.62×10﹣7(2分) c(Na+)>c(HNO )>c(OH﹣)>c(H+)>c(N O )(2分)
2 2
(3)2NH (g)+CO (g) CO(NH)(s)+HO(l) ΔH=﹣87.0kJ•mol-1(2分)
3 2 2 2 2
(4)66.7%(2分) 128 (2分) a(2分)
【解析】(1)NH
3
极易溶于水且溶液显碱性,由于NH
3
+H
2
O⇌NH
3
•H
2
O⇌ NH +OH﹣;(2)①根据电离平衡常数判断HNO、HNO 的酸性强弱顺序为:HNO>H NO,所以物质的量浓度相同
2 2 2 2 2 2 2 2
的弱酸强碱盐NaNO 和NaHN O 溶液中 水解程度大于NaNO 溶液中NO ,即物质的量浓度相同的
2 2 2 2
NaNO 和NaHN O 溶液中,NaHN O 溶液的碱性强、pH大;
2 2 2 2 2
②NaHN O 溶液中, 水解常数K 与第一级电离常数K 关系为K ×K =Kw,所以25℃时,K=
2 2 h a1 a1 h h
;
③由于NaHN O 的K>K ,即NaHN O 溶液中的 电离程度小于水解程度,所以NaHN O 溶液呈碱
2 2 h a2 2 2 2 2
性,但NaHN O 的水解和电离均微弱,结合水的微弱电离,故NaHN O 溶液中粒子浓度由大到小为
2 2 2 2
c(Na+)>c( )>c(OH﹣)>c(H NO)>c(H+)>c( );
2 2 2
(3)NH
3
与CO
2
合成尿素同时生成液态水的化学方程式为2NH
3
(g)+CO
2
(g)⇌CO(NH
2
)
2
(s)+H
2
O(l),根据盖
斯定律I+Ⅱ﹣Ⅲ有:2NH
3
(g)+CO
2
(g)⇌CO(NH
2
)
2
(s)+H
2
O(l)ΔH=﹣159.5kJ•mol﹣1+(+116.5kJ•mol﹣1)﹣
(+44.4kJ•mol﹣1)=﹣87.0 kJ•mol﹣1;
(4)①设起始n(CO)=x,则n(NH )=2x,平衡时生成尿素的物质的量为 ,反应Ⅳ的三段
2 3
式为:
根据恒温恒容条件下,气体的物质的量之比等于压强之比有3x:(2x-1+x-0.5)=9:3,解得:x=0.75;NH 的
3
平衡转化率= ×100%=66.7%,该反应的平衡常数K= =128;
②2NH
3
(g)+CO
2
(g)⇌CO(NH
2
)
2
(s)+H
2
O(l)ΔH=﹣87.0 kJ•mol﹣1,该反应正向放热,所以升高温度,K减小,
故选a。
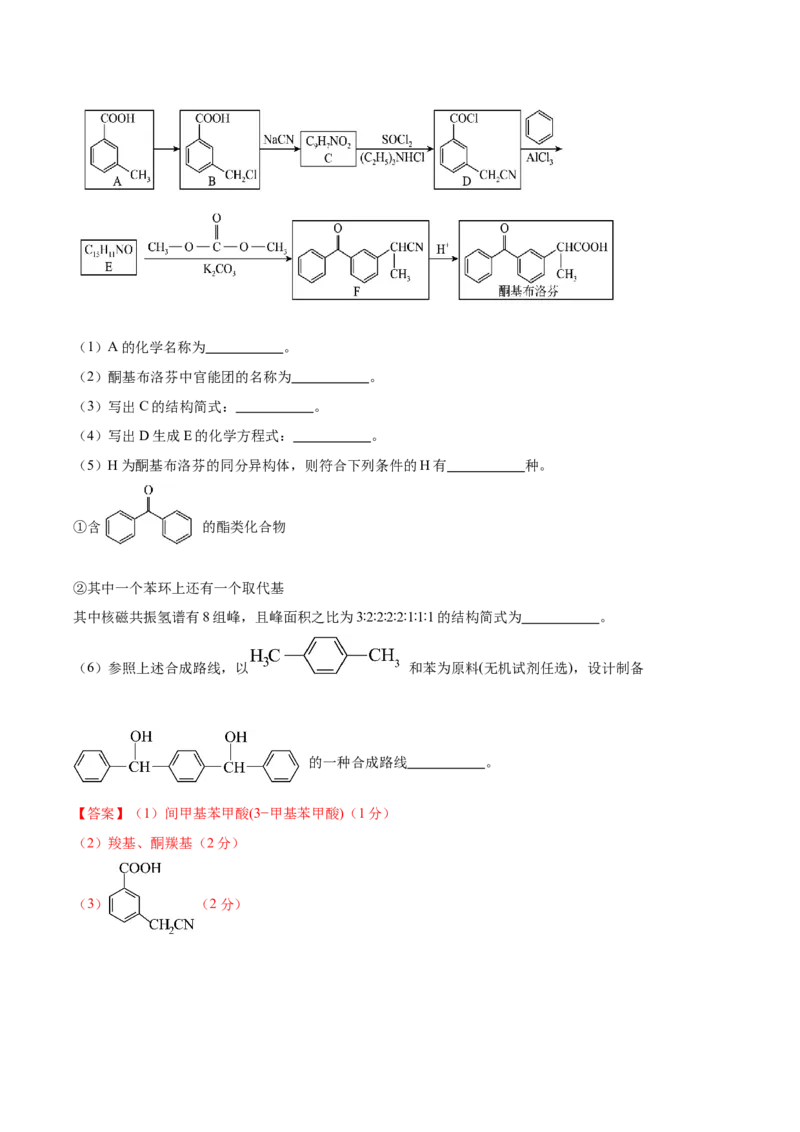
18.(15分)酮基布洛芬片是用于治疗各种关节肿痛以及牙痛、术后痛等的非处方药。其合成路线如图所
示:(1)A的化学名称为 。
(2)酮基布洛芬中官能团的名称为 。
(3)写出C的结构简式: 。
(4)写出D生成E的化学方程式: 。
(5)H为酮基布洛芬的同分异构体,则符合下列条件的H有 种。
①含 的酯类化合物
②其中一个苯环上还有一个取代基
其中核磁共振氢谱有8组峰,且峰面积之比为3∶2∶2∶2∶2∶1∶1∶1的结构简式为 。
(6)参照上述合成路线,以 和苯为原料(无机试剂任选),设计制备
的一种合成路线 。
【答案】(1)间甲基苯甲酸(3−甲基苯甲酸)(1分)
(2)羧基、酮羰基(2分)
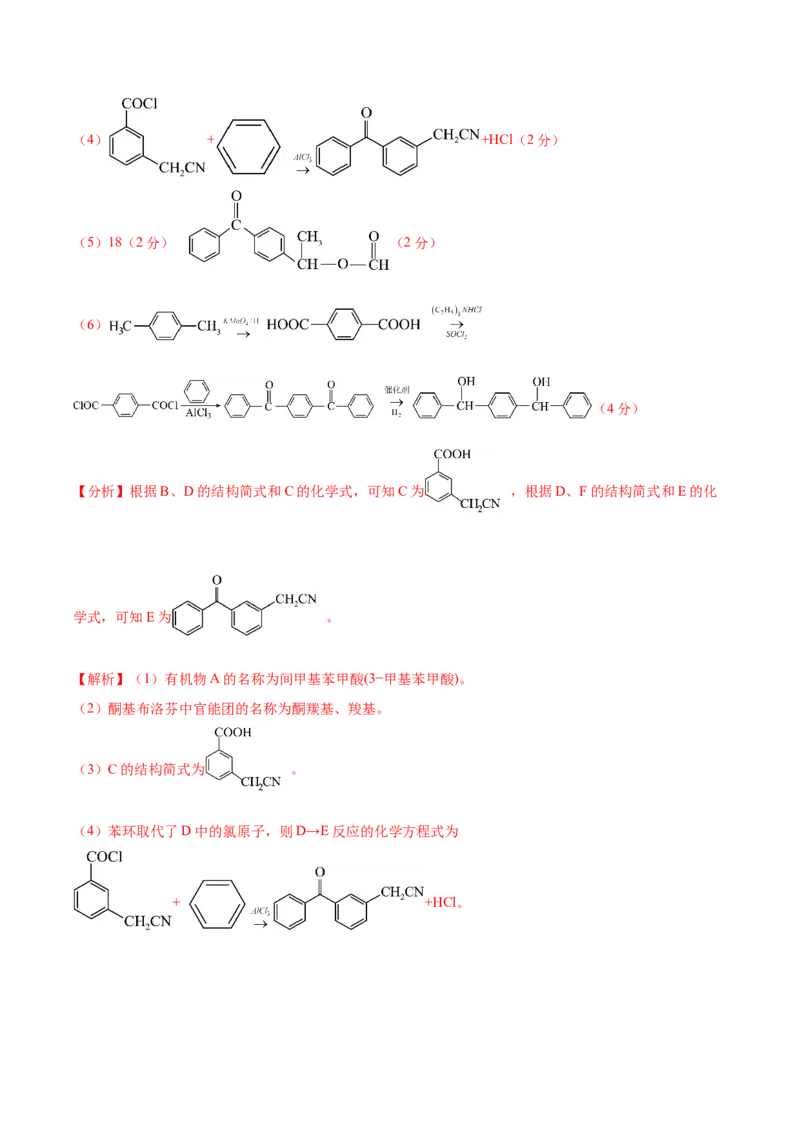
(3) (2分)(4) + +HCl(2分)
(5)18(2分) (2分)
(6)
(4分)
【分析】根据B、D的结构简式和C的化学式,可知C为 ,根据D、F的结构简式和E的化
学式,可知E为 。
【解析】(1)有机物A的名称为间甲基苯甲酸(3−甲基苯甲酸)。
(2)酮基布洛芬中官能团的名称为酮羰基、羧基。
(3)C的结构简式为 。
(4)苯环取代了D中的氯原子,则D→E反应的化学方程式为
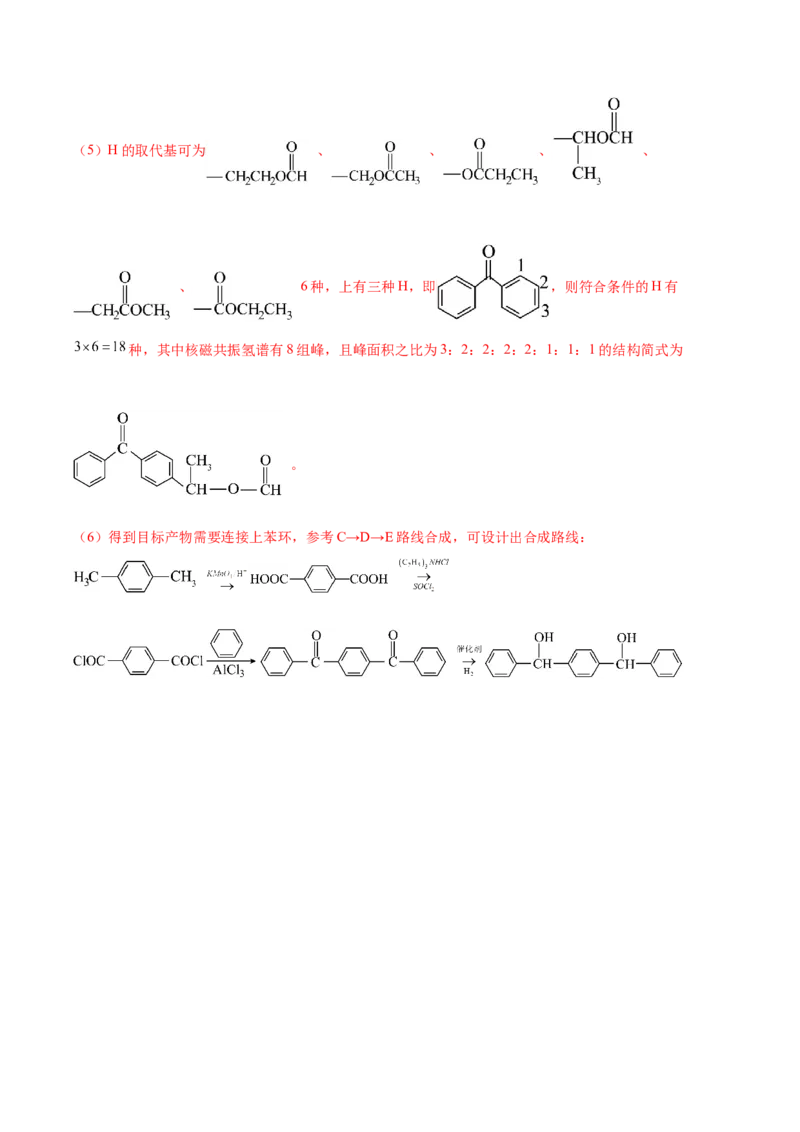
+ +HCl。(5)H的取代基可为 、 、 、 、
、 6种,上有三种H,即 ,则符合条件的H有
种,其中核磁共振氢谱有8组峰,且峰面积之比为3:2:2:2:2:1:1:1的结构简式为
。
(6)得到目标产物需要连接上苯环,参考C→D→E路线合成,可设计出合成路线: