文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(河北专用)
黄金卷07
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64 Ce 140
第Ⅰ卷
一、单项选择题:共14题,每题3分,共42分。每题只有一个选项最符合题意。
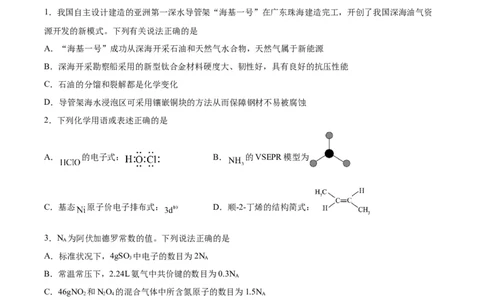
1.我国自主设计建造的亚洲第一深水导管架“海基一号”在广东珠海建造完工,开创了我国深海油气资
源开发的新模式。下列有关说法正确的是
A.“海基一号”成功从深海开采石油和天然气水合物,天然气属于新能源
B.深海开采勘察船采用的新型钛合金材料硬度大、韧性好,具有良好的抗压性能
C.石油的分馏和裂解都是化学变化
D.导管架海水浸泡区可采用镶嵌铜块的方法从而保障钢材不易被腐蚀
2.下列化学用语或表述正确的是
A. 的电子式: B. 的VSEPR模型为
C.基态 原子价电子排布式: D.顺-2-丁烯的结构简式:
3.N 为阿伏加德罗常数的值。下列说法正确的是
A
A.标准状况下,4gSO 中电子的数目为2N
3 A
B.常温常压下,2.24L氨气中共价键的数目为0.3N
A
C.46gNO 和NO 的混合气体中所含氮原子的数目为1.5N
2 2 4 A
D.常温下,1.0LpH=12的Ba(OH) 溶液中OH-的数目是0.02N
2 A
4.下列过程中的化学反应,相应的离子方程式正确的是
A. 在碱性环境中被空气氧化:
B.氢氧化铁加入氢碘酸溶液中:C.用铁作阳极电解氯化镁溶液:
D.碳酸钙加入乙酸溶液中:
5.下列实验能达到实验目的的是
A.制取 B.测定 溶液的浓度
C.验证相同温度下的溶解度: D.检验 溶液是否变质
6.下列实验设计、现象和结论都正确的是
选
实验操作及现象 实验结论
项
取少量 样品溶于水,加入 溶液,再加入足量盐酸,
A 原样品已变质
产生白色沉淀
B 向某溶液中滴加浓盐酸,将产生气体通入石蕊试液,溶液先变红后褪色 溶液中含有 或
气体X不一定是氧化性
C 向溶有 的 溶液中通入气体X,出现白色沉淀
气体
该固体试样中不可能存
在某固体试样加水后的溶液中,滴加 溶液,没有产生使湿润红色
D
石蕊试纸变蓝的气体 在
7.X、Y、Z、W是原子半径依次增大的短周期主族元素,X与其他元素不在同一周期,Y元素的电负性
仅次于氟元素,Z的基态原子中单电子与成对电子个数比为3∶4,W原子电子总数与Y原子的最外层电子
数相同。下列说法正确的是
A.第一电离能:Z>Y>W B.基态Z原子核外电子有7种空间运动状态
C.由四种元素组成的化合物仅含共价键 D.X、Y形成的化合物都是由极性键构成的极性分子
8.汞钡铜氧晶体的晶胞如图A所示,通过掺杂Ca2+获得的具有更高临界温度的超导材料如图B所示。下列说法正确的是
A.掺杂后晶体密度增大是因为晶胞中增加了1个Ca2+
B.汞钡铜氧晶体中的Hg和Cu个数比为1∶2
C.图A晶胞中一个Ba的分数坐标为( , , ),则另一个( , , )
D.图B晶胞中Ca周围距离最近的Hg数目和Hg周围距离最近的Ca的数目不同
9.β﹣生育酚是天然维生素E的一种水解产物,具有较高的生物活性,其结构简式如图。下列有关β﹣生
育酚的说法正确的是
A.1个分子中含有47个氢原子 B.该分子中含有6个甲基
C.环上的一氯代物只有1种 D.能发生取代反应和加成反应
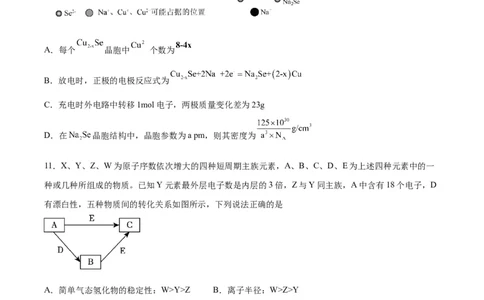
10.钠硒电池是一类以单质硒或含硒化合物为正极、金属钠为负极的新型电池,具有能量密度大、导电率
高、成本低等优点。以 填充碳纳米管作为正极材料的一种钠硒电池工作原理如图所示,充放电过程
中正极材料立方晶胞内未标出因放电产生的0价Cu原子。下列说法正确的是A.每个 晶胞中 个数为
B.放电时,正极的电极反应式为
C.充电时外电路中转移1mol电子,两极质量变化差为23g
D.在 晶胞结构中,晶胞参数为a pm,则其密度为
11.X、Y、Z、W为原子序数依次增大的四种短周期主族元素,A、B、C、D、E为上述四种元素中的一
种或几种所组成的物质。已知Y元素最外层电子数是内层的3倍,Z与Y同主族,A中含有18个电子,D
有漂白性,五种物质间的转化关系如图所示,下列说法正确的是
A.简单气态氢化物的稳定性:W>Y>Z B.离子半径:W>Z>Y
C.A与C可以反应生成B D.X和Y组成的二元化合物中不含有非极性键
12.钛酸钡 是一种压电材料,主要用于电子陶瓷、PTC热敏电阻、电容器等多种电子元器件的配
制。某工厂以重晶石 为原料,生产 的工业流程如下图,下列说法不正确的是资料:“焙烧”后固体产物有 、易溶于水的BaS和微溶于水的CaS
A.“焙烧”步骤中碳粉的主要作用是做还原剂,将 还原
B.“酸化”中的酸为硫酸
C.“沉淀”步骤中生成 的化学方程式为:
D.“热分解”生成粉状钛酸钡,产生的
13.中石化的《丁烯双键异构化的方法》获得第二十届中国专利优秀奖。在100kPa和298K下,丁烯双键
异构化反应的机理如图所示。下列说法不正确的是
A.上述两种烯烃均能发生加成反应、氧化反应
B.CH=CH﹣CH﹣CH 比CH﹣CH=CH﹣CH 的稳定性差
2 2 3 3 3
C.丁烯的同分异构体只有上述2种结构
D.以上两种丁烯分子,每个分子中最多都有8个原子在同一平面上
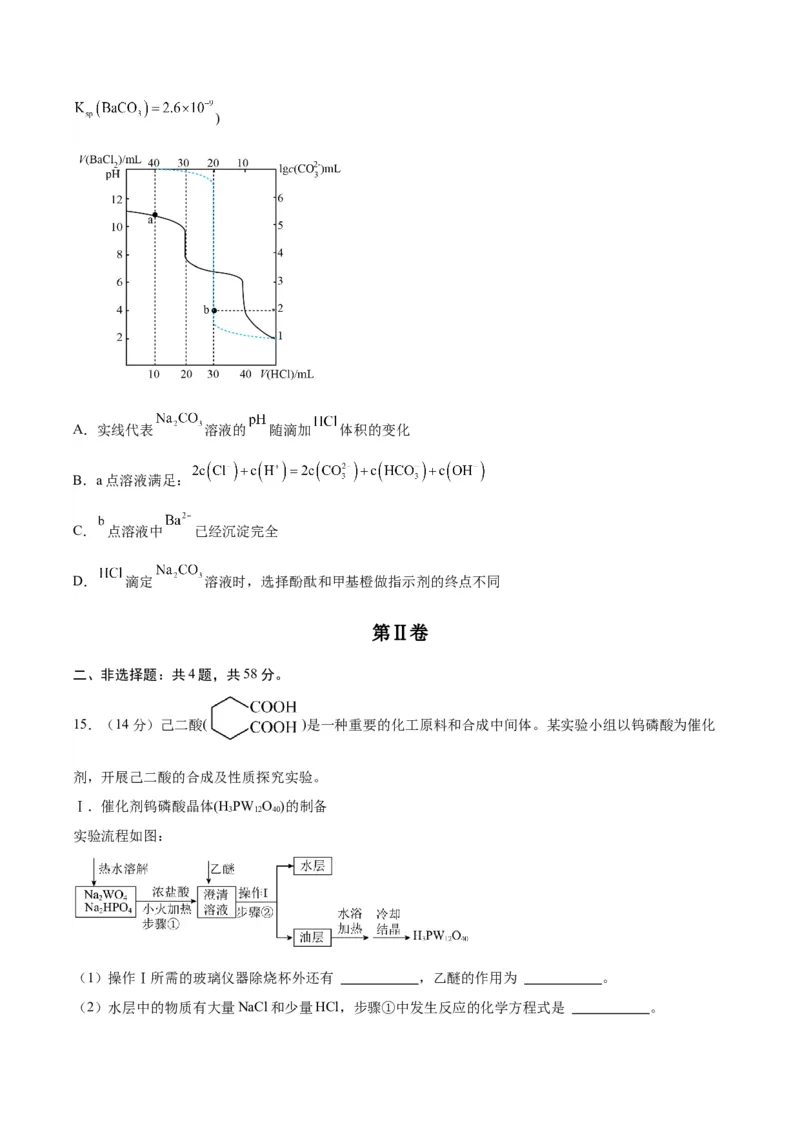
14.两份 溶液中,分别滴加未知浓度的 溶液和 溶液,两溶液中的
和 随所加入溶液体积的变化如图所示,下列有关说法不正确的是(已知:)
A.实线代表 溶液的 随滴加 体积的变化
B.a点溶液满足:
C. 点溶液中 已经沉淀完全
D. 滴定 溶液时,选择酚酞和甲基橙做指示剂的终点不同
第Ⅱ卷
二、非选择题:共4题,共58分。
15.(14分)己二酸( )是一种重要的化工原料和合成中间体。某实验小组以钨磷酸为催化
剂,开展己二酸的合成及性质探究实验。
Ⅰ.催化剂钨磷酸晶体(H PW O )的制备
3 12 40
实验流程如图:
(1)操作Ⅰ所需的玻璃仪器除烧杯外还有 ,乙醚的作用为 。
(2)水层中的物质有大量NaCl和少量HCl,步骤①中发生反应的化学方程式是 。Ⅱ.己二酸的合成
向三颈烧瓶中加入0.10g钨磷酸催化剂和30mL30%双氧水,在室温下搅拌5min,然后加入5.0mL试剂X,
得到溶液A。
(3)环己烯、环己醇、环己酮均可被双氧水氧化成己二酸。仅从所需双氧水理论用量的角度看,试剂X
的最佳选择是 (填序号)。
A.环己烯( ) B.环己醇( ) C.环己酮( )
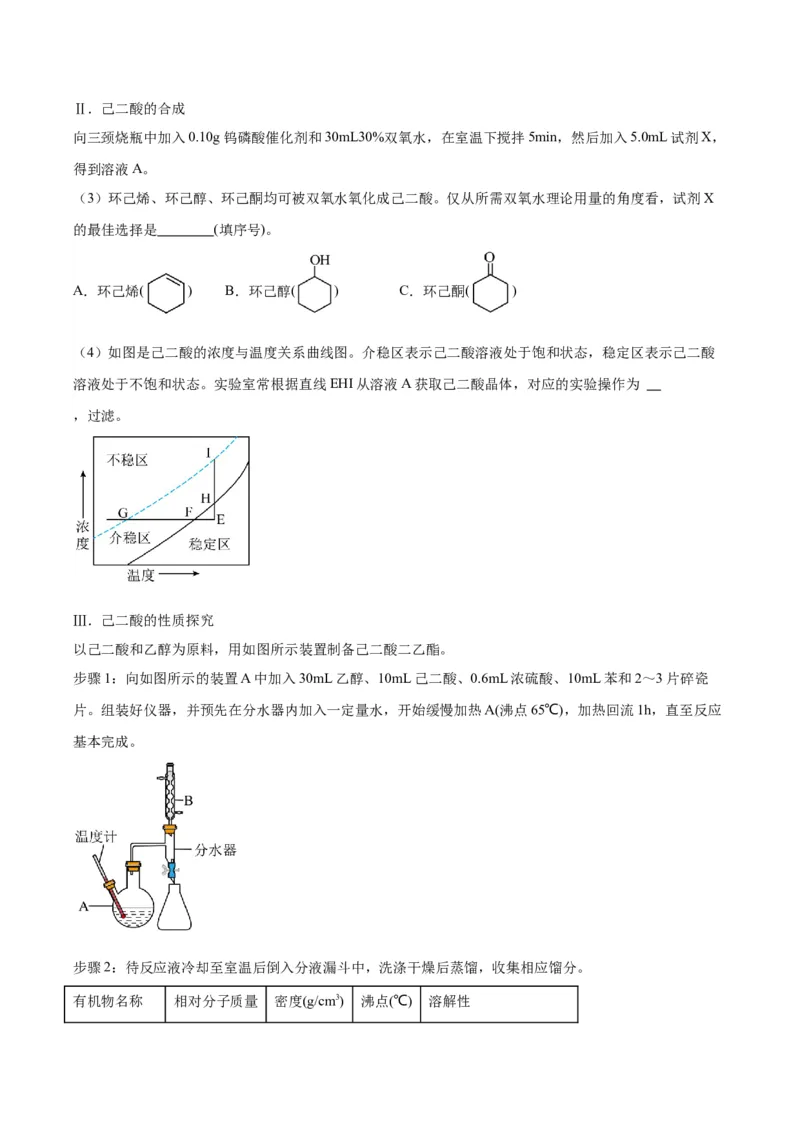
(4)如图是己二酸的浓度与温度关系曲线图。介稳区表示己二酸溶液处于饱和状态,稳定区表示己二酸
溶液处于不饱和状态。实验室常根据直线EHI从溶液A获取己二酸晶体,对应的实验操作为
,过滤。
Ⅲ.己二酸的性质探究
以己二酸和乙醇为原料,用如图所示装置制备己二酸二乙酯。
步骤1:向如图所示的装置A中加入30mL乙醇、10mL己二酸、0.6mL浓硫酸、10mL苯和2~3片碎瓷
片。组装好仪器,并预先在分水器内加入一定量水,开始缓慢加热A(沸点65℃),加热回流1h,直至反应
基本完成。
步骤2:待反应液冷却至室温后倒入分液漏斗中,洗涤干燥后蒸馏,收集相应馏分。
有机物名称 相对分子质量 密度(g/cm3) 沸点(℃) 溶解性己二酸 146 1.36 330 微溶于水,易溶于乙醇
乙醇 46 0.79 78.5 易溶于水
己二酸二乙酯 202 1.00 247 难溶于水、易溶于乙醇
苯 78 0.88 80.1 难溶于水
(5)装置中分水器的作用是 ,判断反应已经完成的标志是 。
(6)本次实验的产率为(某种生成物的实际产量与理论产量的百分比) 。(结果保留两位有效
数字)
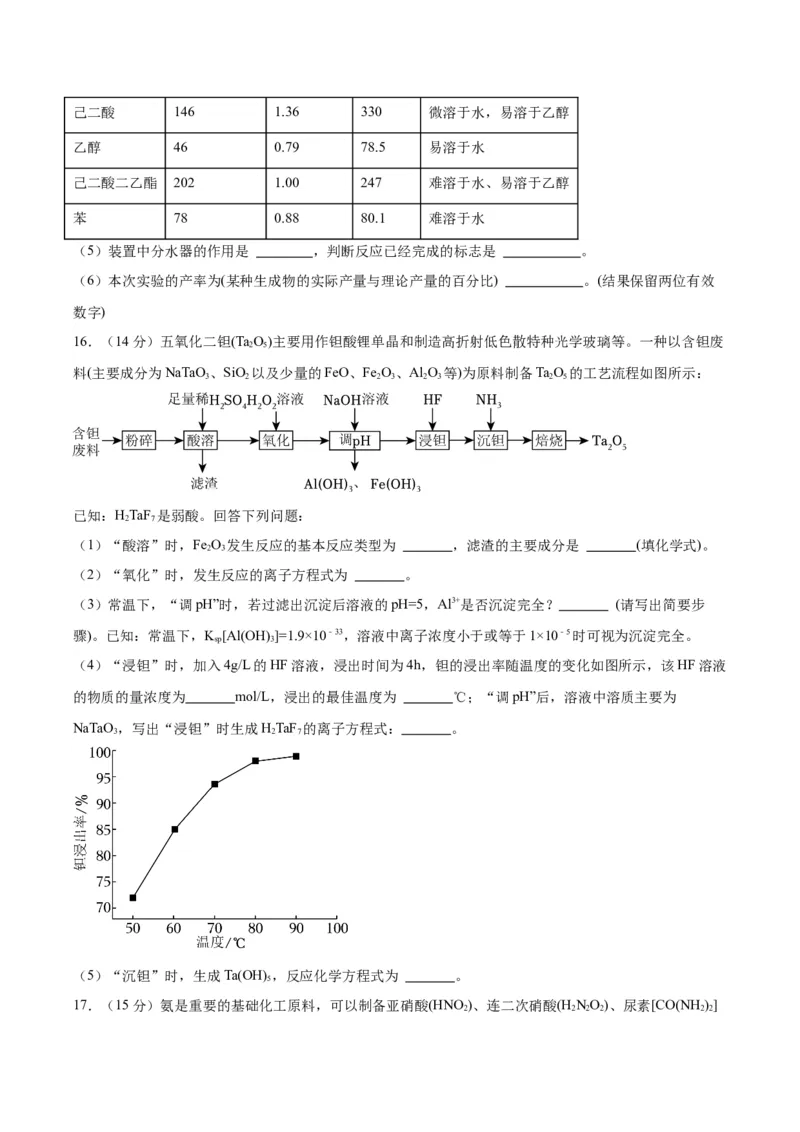
16.(14分)五氧化二钽(TaO)主要用作钽酸锂单晶和制造高折射低色散特种光学玻璃等。一种以含钽废
2 5
料(主要成分为NaTaO 、SiO 以及少量的FeO、Fe O、Al O 等)为原料制备TaO 的工艺流程如图所示:
3 2 2 3 2 3 2 5
已知:HTaF 是弱酸。回答下列问题:
2 7
(1)“酸溶”时,Fe O 发生反应的基本反应类型为 ,滤渣的主要成分是 (填化学式)。
2 3
(2)“氧化”时,发生反应的离子方程式为 。
(3)常温下,“调pH”时,若过滤出沉淀后溶液的pH=5,Al3+是否沉淀完全? (请写出简要步
骤)。已知:常温下,K [Al(OH) ]=1.9×10﹣33,溶液中离子浓度小于或等于1×10﹣5时可视为沉淀完全。
sp 3
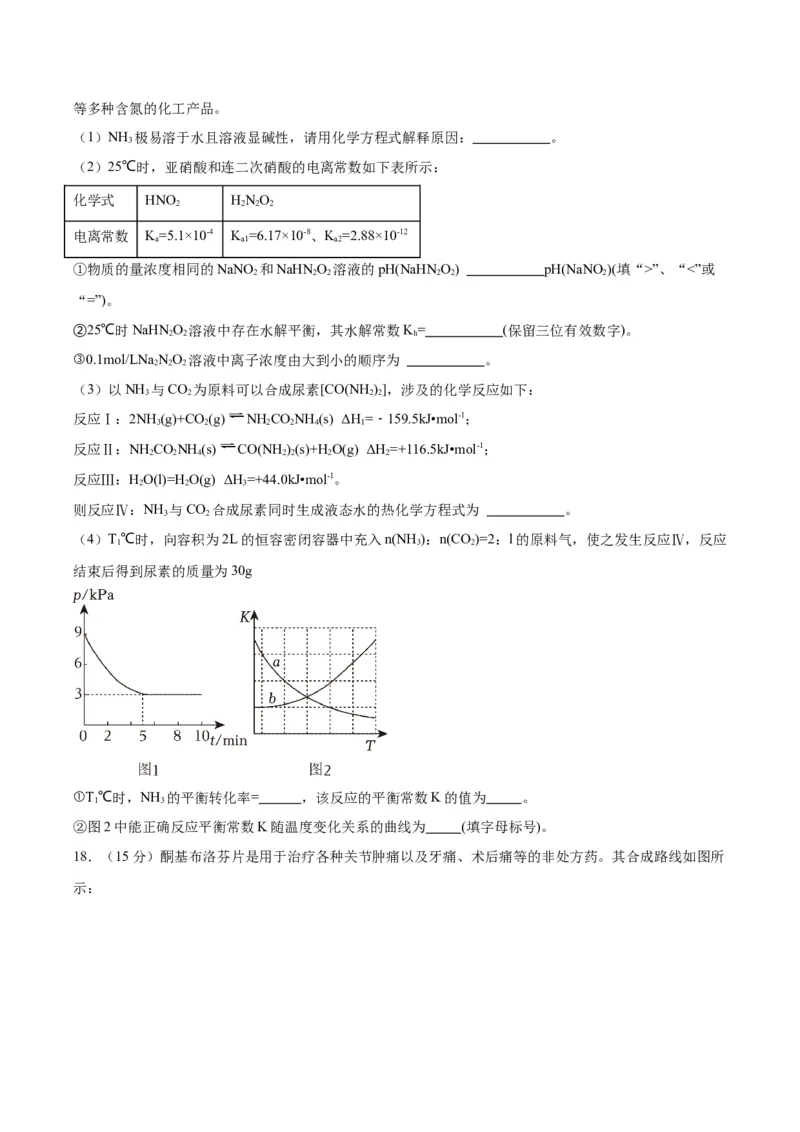
(4)“浸钽”时,加入4g/L的HF溶液,浸出时间为4h,钽的浸出率随温度的变化如图所示,该HF溶液
的物质的量浓度为 mol/L,浸出的最佳温度为 ℃;“调pH”后,溶液中溶质主要为
NaTaO ,写出“浸钽”时生成HTaF 的离子方程式: 。
3 2 7
(5)“沉钽”时,生成Ta(OH),反应化学方程式为 。
5
17.(15分)氨是重要的基础化工原料,可以制备亚硝酸(HNO)、连二次硝酸(H NO)、尿素[CO(NH)]
2 2 2 2 2 2等多种含氮的化工产品。
(1)NH 极易溶于水且溶液显碱性,请用化学方程式解释原因: 。
3
(2)25℃时,亚硝酸和连二次硝酸的电离常数如下表所示:
化学式 HNO HNO
2 2 2 2
电离常数 K=5.1×10-4 K =6.17×10-8、K =2.88×10-12
a a1 a2
①物质的量浓度相同的NaNO 和NaHN O 溶液的pH(NaHNO) pH(NaNO)(填“>”、“<”或
2 2 2 2 2 2
“=”)。
②25℃时NaHN O 溶液中存在水解平衡,其水解常数K= (保留三位有效数字)。
2 2 h
③0.1mol/LNa NO 溶液中离子浓度由大到小的顺序为 。
2 2 2
(3)以NH 与CO 为原料可以合成尿素[CO(NH)],涉及的化学反应如下:
3 2 2 2
反应Ⅰ:2NH (g)+CO (g) NH CONH (s) ΔH=﹣159.5kJ•mol-1;
3 2 2 2 4 1
反应Ⅱ:NH CONH (s) CO(NH)(s)+HO(g) ΔH=+116.5kJ•mol-1;
2 2 4 2 2 2 2
反应Ⅲ:HO(l)=HO(g) ΔH=+44.0kJ•mol-1。
2 2 3
则反应Ⅳ:NH 与CO 合成尿素同时生成液态水的热化学方程式为 。
3 2
(4)T℃时,向容积为2L的恒容密闭容器中充入n(NH ):n(CO)=2:l的原料气,使之发生反应Ⅳ,反应
1 3 2
结束后得到尿素的质量为30g
①T℃时,NH 的平衡转化率= ,该反应的平衡常数K的值为 。
1 3
②图2中能正确反应平衡常数K随温度变化关系的曲线为 (填字母标号)。
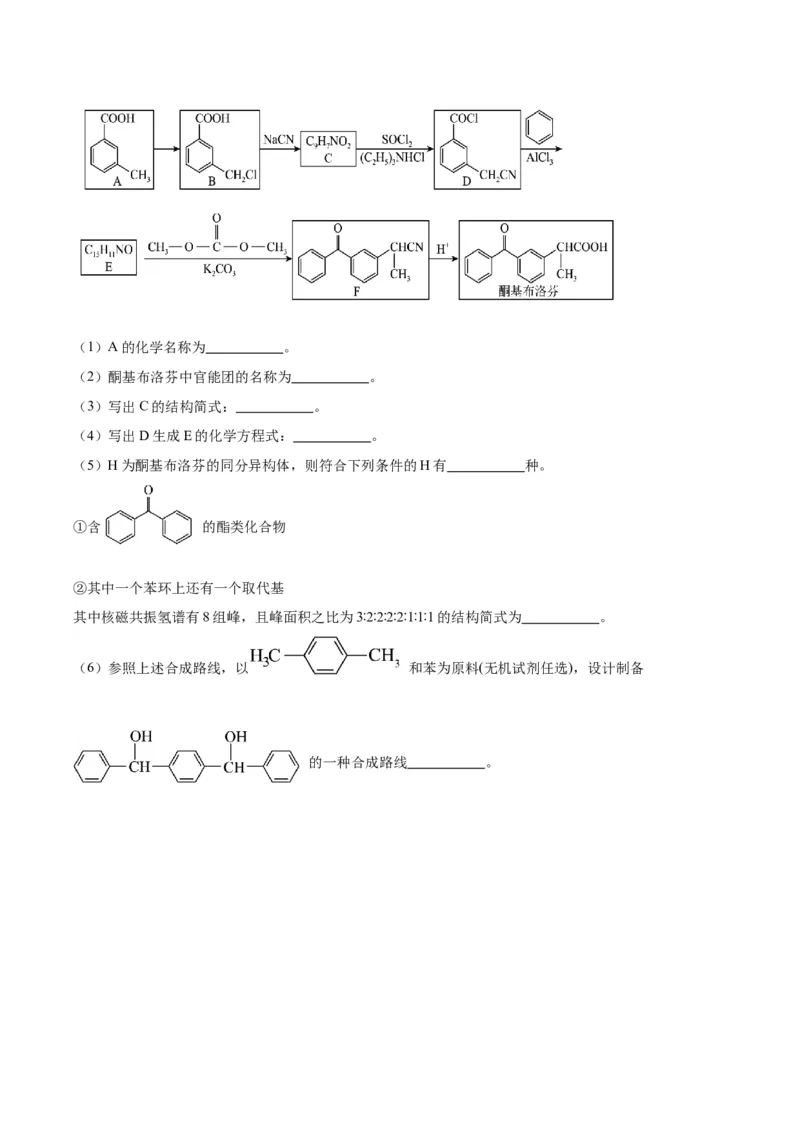
18.(15分)酮基布洛芬片是用于治疗各种关节肿痛以及牙痛、术后痛等的非处方药。其合成路线如图所
示:(1)A的化学名称为 。
(2)酮基布洛芬中官能团的名称为 。
(3)写出C的结构简式: 。
(4)写出D生成E的化学方程式: 。
(5)H为酮基布洛芬的同分异构体,则符合下列条件的H有 种。
①含 的酯类化合物
②其中一个苯环上还有一个取代基
其中核磁共振氢谱有8组峰,且峰面积之比为3∶2∶2∶2∶2∶1∶1∶1的结构简式为 。
(6)参照上述合成路线,以 和苯为原料(无机试剂任选),设计制备
的一种合成路线 。