文档内容
化学反应速率和限度(1)同步练习
(答题时间:25分钟)
一、选择题:
1. 下列关于化学反应速率的说法不正确的是( )
A. 化学反应速率是衡量化学反应进行快慢程度的物理量
B. 化学反应速率通常用单位时间内生成或消耗某物质的质量的多少来表示
C. 在同一个反应中,各物质的反应速率之比等于反应方程式中对应物质的化学计量数
之比
D. 化学反应速率的常用单位有 mol·L-1·s-1和 mol·L-1·min-1
2. 把下列选项中四种X溶液分别加入四个盛有相同温度的10 mL 2 mol·L-1盐酸的烧杯
中,均加水稀释到100 mL。此时,X与盐酸缓缓地进行反应,其中反应速率最大的是(
)
A. 10 ℃ 20 mL 3 mol·L-1的X溶液
B. 20 ℃ 30 mL 2 mol·L-1的X溶液
C. 20 ℃ 10 mL 4 mol·L-1的X溶液
D. 10 ℃ 20 mL 2 mol·L-1的X溶液
3. 在2 L密闭容器中,发生以下反应:2A(g)+B(g) 2C(g)+D(g)。
若最初加入的A和B都是4 mol,在前10 s A的平均反应速率为0. 12 mol·L-1·s-1,则10 s
时,容器中B的物质的量是( )
A. 1. 6 mol B. 2. 8 mol
C. 2. 4 mol D. 1. 2 mol
4. 在一密闭容器中充入1 mol H (g)和1 mol I (g),压强为p(Pa),并在一定温度
2 2
下使其发生反应H
2
(g)+I
2
(g) ⇄2HI(g)。下列说法正确的是( )
A. 保持容器容积不变,向其中加入1 mol I (g),化学反应速率不变
2
B. 保持容器容积不变,向其中加入1 mol He,化学反应速率加快
C. 保持容器内气体压强不变,向其中加入1 mol H (g)和1 mol I (g),化学反应速
2 2
率不变
D. 保持容器内气体压强不变,向其中加入1 mol He,化学反应速率不变
5. 一定能使化学反应速率加快的因素是( )
①扩大容器容积 ②使用正催化剂 ③增大反应物的物质的量 ④升高温度 ⑤缩小
容器容积 ⑥增大压强
A. ②③ B. ②③④⑥
C. ②③④⑤ D. ②④
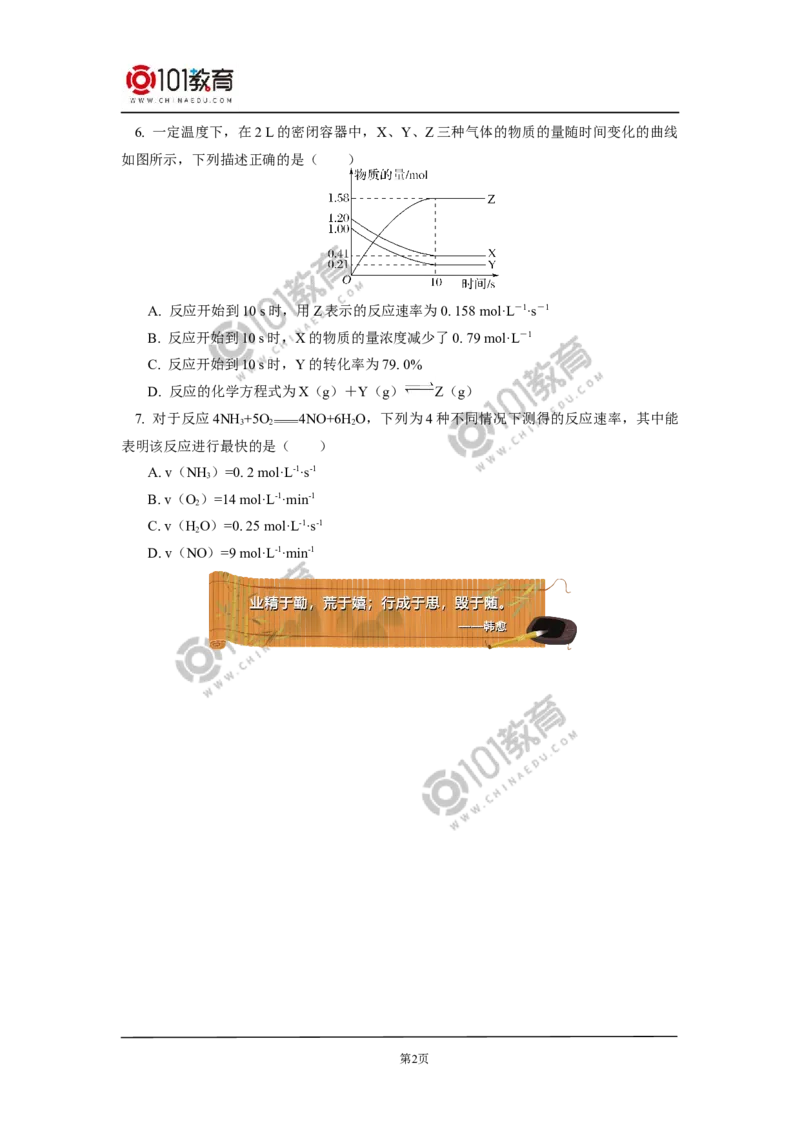
第1页6. 一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线
如图所示,下列描述正确的是( )
A. 反应开始到10 s时,用Z表示的反应速率为0. 158 mol·L-1·s-1
B. 反应开始到10 s时,X的物质的量浓度减少了0. 79 mol·L-1
C. 反应开始到10 s时,Y的转化率为79. 0%
D. 反应的化学方程式为X(g)+Y(g) Z(g)
7. 对于反应4NH +5O 4NO+6H O,下列为4种不同情况下测得的反应速率,其中能
3 2 2
表明该反应进行最快的是( )
A. v(NH )=0. 2 mol·L-1·s-1
3
B. v(O)=14 mol·L-1·min-1
2
C. v(HO)=0. 25 mol·L-1·s-1
2
D. v(NO)=9 mol·L-1·min-1
第2页化学反应速率和限度(1)同步练习参考答案
1.【答案】B
【解析】化学反应速率通常用单位时间内反应物浓度的减少量或生成物浓度的增加量
来表示,B项错误。
2.【答案】B
【解析】温度越高,反应速率越大;浓度越大,反应速率越大。由于溶液体积均为
100 mL,则X物质的量越大,浓度越大。
3.【答案】B
【解析】根据化学反应速率之比等于对应物质的化学计量数之比,可得 v(B)=0. 5v
(A)=0. 5×0. 12 mol·L-1·s-1=0. 06 mol·L-1·s-1,则Δc(B)=0. 06 mol·L-1·s-1×10 s=0.
6 mol·L-1,Δn(B)=0. 6 mol·L-1×2 L=1. 2 mol,故10 s时容器中B的物质的量为4 mol
-1. 2 mol=2. 8 mol。
4.【答案】C
【解析】保持容器容积不变,向其中加入1 mol I (g),反应物浓度增大,反应速率
2
加快,A错误;保持容器容积不变,向其中加入1 mol He,参加反应的物质的浓度不变,
则反应速率不变,B错误;保持容器内气体压强不变,向其中加入1 mol H (g)和1 mol I
2 2
(g),因物质的量增大1倍,体积也增大1倍,则浓度不变,反应速率不变,C正确;保
持容器内气体压强不变,向其中加入1 mol He,体积增大,参加反应的物质的浓度减小,
则反应速率减慢,D错误。
5.【答案】D
【解析】①对于有气体参加的反应,扩大容器容积,会使物质的浓度降低,反应速率
减慢,但对无气体参加的反应没有影响,错误;②使用正催化剂,一定能使化学反应速率
加快,正确;③若反应物是固体或纯液体物质,则增大反应物的物质的量,化学反应速率
不变,错误;④升高温度一定能使化学反应速率加快,正确;⑤对于有气体参加的反应,
缩小容器容积,会导致气体的浓度增大,化学反应速率加快,但对无气体参加的反应没有
影响,错误;⑥若反应无气体参加,则增大压强,化学反应速率不变,错误。综上所述,
符合题意的为②④,D正确。
6.【答案】C
1.58mol
2L
【解析】反应开始到10 s时,用Z表示的反应速率为
10s
=0. 079 mol·L-1·s-1,
1.2mol−0.41mol
2L
故A错误;反应开始到 10 s时,X的物质的量浓度减少了 =0. 395
1.00mol−0.21mol
1.00mol
mol·L-1,故B错误;反应开始到10 s时,Y的转化率为 ×100%=79.
第3页0%。故C正确;由图像可以看出,反应中X、Y的物质的量减少,应为反应物,Z的物质
的量增多,应为生成物,当反应进行到 10 s时. Δn(X)=0. 79 mol,Δn(Y)=0. 79
mol,Δn(Z)=1. 58 mol,则Δn(X)∶Δn(Y)∶Δn(Z)=1∶1∶2,参加反应的物质
的物质的量之比等于化学计量数之比,则反应的化学方程式为 X(g)+Y(g)2Z
(g),故D错误。
7.【答案】A
【解析】首先,统一单位,A项v(NH )=0. 2 mol·L-1·s-1=12 mol·L-1·min-1,C 项v
3
(HO)=0. 25 mol·L-1·s-1=15 mol·L-1·min-1;其次,物质的化学反应速率与其化学计量数之
2
比越大,则该物质表示的化学反应速率就越大,A、B、C、D四个选项中该比值分别是
12÷4=3,14÷5=2. 8,15÷6=2. 5,9÷4=2. 25,故选A。
第4页