文档内容
难溶电解质的沉淀溶解平衡同步练习
(答题时间:40分钟)
一、选择题
1. 下列有关溶度积常数K 的说法正确的是( )
sp
A. 常温下,向BaCO 饱和溶液中加入NaCO 固体,BaCO 的K 减小
3 2 3 3 sp
B. 溶度积常数K 只受温度影响,温度升高K 减小
sp sp
C. 溶度积常数K 只受温度影响,温度升高K 增大
sp sp
D. 常温下,向Mg(OH) 饱和溶液中加入NaOH固体,Mg(OH) 的K 不变
2 2 sp
2. 在一定温度下,当Mg(OH) 固体在水溶液中达到下列平衡时:Mg(OH) (s)
2 2
Mg2+(aq)+2OH-(aq),要使Mg(OH) 固体减少而c(Mg2+)不变,可采取的
2
措施是( )
A. 加MgSO 固体 B. 加HCl溶液
4
C. 加NaOH固体 D. 加少量水
3. 已知:K (AgCl)=1.8×10-10,K (AgI)=1.5×10-16,K (Ag CrO )=2.0×10-
sp sp sp 2 4
12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是( )
A. AgCl>AgI>Ag CrO
2 4
B. AgCl>Ag CrO>AgI
2 4
C. Ag CrO>AgCl>AgI
2 4
D. Ag CrO>AgI>AgCl
2 4
*4. 在t ℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知t ℃时AgCl的K =4×10-
sp
10,下列说法不正确的是( )
A. 在t ℃时,AgBr的K 为4.9×l0-13
sp
B. 在AgBr饱和溶液中加入NaBr固体,可使溶液由c点到b点
C. 图中a点对应的是t ℃ AgBr的不饱和溶液
D. 在t ℃时,AgCl(s)+Br-(aq) ⇌AgBr(s)+Cl- (aq)的平衡常数K≈816
*5. 已知几种难溶电解质的溶度积常数K (25 ℃)见下表:
sp
难溶电解质 AgCl AgBr AgI Ag SO Ag CrO
2 4 2 4
K 1.8×10-10 5.4×10-13 8.5×10-17 1.4×10-5 1.12×10-12
sp
下列叙述不正确的是 ( )
第1页A. 由溶度积常数可判断在相同条件下一些物质的溶解性大小
B. 将等体积的4×10-3 mol·L-1的AgNO 溶液和4×10-3 mol·L-1的KCrO 溶液混合,
3 2 4
有Ag CrO 沉淀产生
2 4
C. 向AgCl的悬浊液中滴加饱和NaBr溶液可以得到黄色AgBr悬浊液
D. 向100 mL 0.1 mol·L-1的NaSO 溶液中加入1 mL 0.1 mol·L-1的AgNO 溶液,有白
2 4 3
色沉淀生成
6. 在饱和Ca(OH)
2
溶液中存在溶解平衡:Ca(OH)
2
(s) ⇌Ca2+(aq)+2OH-
(aq),加入以下溶液,可使pH减小的是( )
A. Na S溶液 B. AlCl 溶液
2 3
C. NaOH溶液 D. Na CO
2 3
二、非选择题
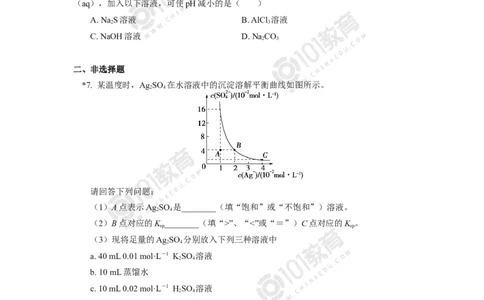
*7. 某温度时,Ag SO 在水溶液中的沉淀溶解平衡曲线如图所示。
2 4
请回答下列问题:
(1)A点表示Ag SO 是________(填“饱和”或“不饱和”)溶液。
2 4
(2)B点对应的K ________(填“>”、“<”或“=”)C点对应的K 。
sp sp
(3)现将足量的Ag SO 分别放入下列三种溶液中
2 4
a. 40 mL 0.01 mol·L-1 KSO 溶液
2 4
b. 10 mL蒸馏水
c. 10 mL 0.02 mol·L-1 HSO 溶液
2 4
则Ag SO 的溶解程度由大到小的排列顺序为________________(填字母)。
2 4
第2页难溶电解质的沉淀溶解平衡同步练习参考答案
1.【答案】D
【解析】温度不变,溶度积常数不变,A项不正确;大多数难溶物温度升高,K 增大,
sp
但也有少数物质相反,故B、C均不正确。
2.【答案】D
【解析】Mg(OH) (s) Mg2+(aq)+2OH-(aq),加MgSO 固体使该溶解
2 4
平衡左移,Mg(OH) 固体增多,c(Mg2+)变大;加HCl溶液使该溶解平衡右移,Mg
2
(OH) 固体减少,c(Mg2+)变大;加NaOH固体使该溶解平衡左移,Mg(OH) 固体
2 2
增多,c(Mg2+)变小。
3.【答案】C
【解析】因为AgCl和AgI的结构相似,由K 可知AgCl的c(Ag+)大于AgI的;
sp
2−
AgCl中的c2(Ag+)=K
sp
=1.8×10-10,Ag
2
CrO
4
(s) ⇌2Ag+(aq)+CrO4 (aq)的K
sp
=c2
1
2−
2
(Ag+)·c(CrO4 )= c3(Ag+)=2.0×10-12,所以Ag CrO 中c(Ag+)大于AgCl中
2 4
的c(Ag+)。
4.【答案】B
【解析】根据溶度积的定义,K =c(Ag+)×c(Br-)=7×10-7×7×10-7=4.9×10-13,
sp
故说法A正确;AgBr(s) ⇌Ag+(aq)+Br-(aq),加入溴化钠溶液中,c(Br-)增大,
促使平衡向逆反应方向进行,c(Ag+)减小,故说法B错误;此时的离子积a>c
【解析】(1)A点没有达到平衡状态。
(2)K 只与温度有关。
sp
2−
(3)c(SO4 )越大,难溶电解质的溶解平衡逆向移动程度越大,Ag SO 的溶解程度
2 4
第3页越小。
第4页沉淀溶解平衡的应用同步练习
(答题时间:40分钟)
一、选择题
1. 25 ℃时,K [Mg(OH) ]=5.61×10-12,K [MgF ]=7.42×10-11。下列说法正确的是(
sp 2 sp 2
)
A. 25 ℃时,饱和Mg(OH) 溶液与饱和MgF 溶液相比,前者的c(Mg2+)大
2 2
B. 25 ℃时,在Mg(OH) 的悬浊液中加入少量的NH Cl固体,c(Mg2+)增大
2 4
C. 25 ℃时,Mg(OH) 固体在20 mL 0.01 mol·L-1氨水中的K 比在20 mL 0.01 mol·L-1
2 sp
NH Cl溶液中的K 小
4 sp
D. 25 ℃时,在Mg(OH) 的悬浊液加入NaF溶液后,Mg(OH) 不可能转化成为
2 2
MgF
2
2. 25 ℃时,已知下列三种金属硫化物的溶度积常数(K )分别为K (FeS)=6.3×10-
sp sp
18;K (CuS)=1.3×10-36;K (ZnS)=1.6×10-24。下列关于常温时的有关叙述正确的是
sp sp
( )
A. 硫化锌、硫化铜、硫化亚铁的溶解度依次增大
B. 将足量的ZnSO 晶体加入到0.1 mol·L-1的NaS溶液中,Zn2+的浓度最大只能达到
4 2
1.6×10-23 mol·L-1
C. 除去工业废水中含有的Cu2+,可采用FeS固体作为沉淀剂
D. 向饱和的FeS溶液中加入FeSO 溶液后,混合液中c(Fe2+)变大、c(S2-)变小,
4
但K (FeS)变大
sp
3. 实验:①向盛有1 mL 0.1 mol·L-1 MgCl 溶液试管中加1 mL 0.2 mol·L-1 NaOH溶液,
2
得到浊液a,过滤得到滤液b和白色沉淀c。②向沉淀c中滴加0.1 mol·L-1 FeCl 溶液,沉
3
淀变为红褐色。下列分析不正确的是( )
A. 浊液a中存在沉淀溶解平衡:Mg(OH)
2
(s) ⇌Mg2+(aq)+2OH-(aq)
B. 滤液b中不含有Mg2+
C. ②中颜色变化说明Mg(OH) 转化为Fe(OH)
2 3
D. 实验可以证明Fe(OH) 比Mg(OH) 更难溶
3 2
*4. 下列说法正确的是( )
A. 根据K (AgCl)=1.77×10-10,K (Ag CrO )=2.0×10-12,可以推知AgCl的溶
sp sp 2 4
解度比Ag CrO 的溶解度大
2 4
B. 0.1 mol·L-1的ZnCl 溶液中通入足量硫化氢气体最终得不到ZnS沉淀是因为溶液中c
2
(Zn2+)·c(S2-)>K (ZnS)
sp
C. 向碳酸钡沉淀中加入稀硫酸,沉淀发生转化,可推知硫酸钡的K 比碳酸钡的大
sp
第5页D. AgCl在10 mL 0.01 mol·L-1的KCl溶液中比在10 mL 0.05 mol·L-1的AgNO 溶液中
3
溶解的质量多
5. 锅炉水垢是一种安全隐患,除去水垢中的CaSO,可先用NaCO 溶液处理,使之转化
4 2 3
为易溶于酸的CaCO ,而后用酸除去。下列说法不正确的是( )
3
A. CaCO 的溶解度小于CaSO 的
3 4
B. 沉淀转化的实质是沉淀溶解平衡的移动
C. 沉淀转化的难易与溶解度差别的大小无关
D. CaSO 到CaCO 的沉淀转化中并存着两个沉淀溶解平衡
4 3
*6. 实验:①0.1 mol·L-1 AgNO 溶液和0.1 mol·L-1NaCl溶液等体积混合得到浊液a,过
3
滤得到滤液b和白色沉淀c;
②向滤液b中滴加0.1 mol·L-1 KI溶液,出现浑浊;
③向沉淀 c 中滴加 0.1 mol·L-1 KI 溶液,沉淀变为黄色。下列分析不正确的是
( )
A. 浊液a中存在沉淀溶解平衡:AgCl(s) ⇌Ag+(aq)+Cl-(aq)
B. 滤液b中不含有Ag+
C. ③中颜色变化说明AgCl转化为AgI
D. 实验可以证明AgI比AgCl更难溶
7. 下列事实不能用平衡移动原理解释的是( )
A. Mg(OH) 不溶于水,但能溶于浓NH Cl溶液中
2 4
B. 水垢中含有的 CaSO ,先用 NaCO 溶液处理,使之转化为疏松、易溶于酸的
4 2 3
CaCO ,再用酸除去
3
C. 洗涤BaSO 沉淀时,用稀硫酸洗涤BaSO 沉淀比用蒸馏水洗涤损失少
4 4
D. FeCl 溶液中混有FeCl ,常加入少量的HO,使Fe2+氧化为Fe3+
3 2 2 2
二、非选择题
*8. 高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫
化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
相关金属离子[c(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
0
金属离子 Mn2+ Fe2+ Fe3+ Al3+ Mg2+ Zn2+ Ni2+
开始沉淀的pH 8.1 6.3 1.5 3.4 8.9 6.2 6.9
第6页沉淀完全的pH 10.1 8.3 2.8 4.7 10.9 8.2 8.9
(1)“滤渣1”含有S和 ;写出“溶浸”中二氧化锰与硫化锰反应
的化学方程式 。
(2)“氧化”中添加适量的MnO 的作用是 。
2
(3)“调pH”除铁和铝,溶液的pH范围应调节为 ~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是 。
(5)“除杂2”的目的是生成MgF 沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,
2
原因是 。
(6)写出“沉锰”的离子方程式 。
第7页沉淀溶解平衡的应用同步练习参考答案
1.【答案】B
【解析】由于Mg(OH) 的溶度积小,所以其电离出的Mg2+浓度要小一些,A项错
2
+
误;由于NH4可以直接结合Mg(OH) 电离出的OH-,从而促使Mg(OH) 的电离平衡
2 2
正向移动,c(Mg2+)增大,B项正确;由于K 仅与温度有关,与溶液中离子浓度的大小、
sp
难溶电解质量的多少等无关,C项错误;因为K [Mg(OH) ]和K (MgF )相差不大,
sp 2 sp 2
在Mg(OH) 悬浊液中加入NaF,若溶液中c(Mg2+)·
2
c2(F-)>7.42×10-11时,也可以生成MgF 沉淀,即由Mg(OH) 转化为MgF ,D项
2 2 2
错误。
2.【答案】C
【解析】化学式所表示的组成中阴、阳离子个数比相同时,K 数值越大的难溶电解质
sp
在水中的溶解能力越强,由K 可知,常温下,CuS的溶解度最小,故A错;将足量的
sp
ZnSO 晶体加入到0.1 mol·L-1的NaS溶液中,c(S2-)将减至非常小,而Zn2+的浓度远远
4 2
大于1.6×10-23 mol·L-1;因CuS比FeS更难溶,FeS沉淀可转化为CuS沉淀;温度不变,
K (FeS)不变。
sp
3.【答案】B
【解析】绝对不溶的物质是不存在的,B选项错误。
4.【答案】D
√1.77
【解析】A 项,c(Ag+)= ×10-5mol·L-1,1 L 水中溶解的 AgCl 的质量为
√1.77 2−
×10-5×143.5 g,由Ag
2
CrO
4
(s) ⇌2Ag+(aq)+CrO4 (aq),可知,
2− 2− 2− √ 3 0.5
c2(Ag+)·c(CrO4 )=4c3(CrO4 ),所以c(CrO4 )= ×10-4 mol·L-1,1 L
√ 3 0.5
水中溶解的Ag CrO 的质量为 ×10-4×332 g,A错误。
2 4
5.【答案】C
【解析】沉淀转化的方向是难溶物向更难溶的方向转化,所以沉淀的溶解度差别越大,
越易转化,C选项错误。
6.【答案】B
【解析】注意“0.1 mol·L-1 AgNO 溶液和0.1 mol·L-1 NaCl溶液等体积混合”,即二
3
者恰好完全反应,是分析、解答本题的关键。
A. 向二者恰好反应后的滤液b中滴加0.1 mol·L-1 KI溶液出现碘化银沉淀,则说明浊
液a中存在沉淀溶解平衡,A正确。B.向滤液b中加入0.1 mol·L-1 KI溶液,出现浑浊,则
说明b中含有Ag+,B错误。C.③中颜色变化是沉淀进行了转化,即AgCl转化为AgI,C
正确。D.因AgCl沉淀能转化为AgI沉淀,所以K (AgI)