文档内容
深度揭秘原电池同步练习
(答题时间:40分钟)
一、选择题
1. 有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
实验装置
a极质量减小;b b极有气体产 d极溶解;c极 电流从a极流向
部分实验现象
极质量增加 生;c极无变化 有气体产生 d极
由此可判断这四种金属的活动性顺序是( )
A. a>b>c>d B. b>c>d>a
C. d>a>b>c D. a>b>d>c
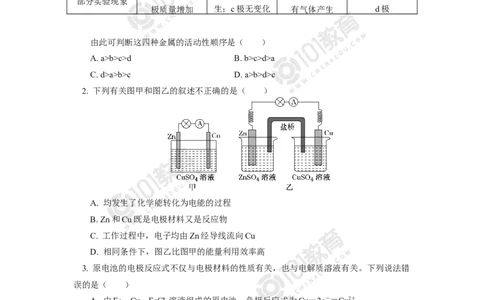
2. 下列有关图甲和图乙的叙述不正确的是( )
A. 均发生了化学能转化为电能的过程
B. Zn和Cu既是电极材料又是反应物
C. 工作过程中,电子均由Zn经导线流向Cu
D. 相同条件下,图乙比图甲的能量利用效率高
3. 原电池的电极反应式不仅与电极材料的性质有关,也与电解质溶液有关。下列说法错
误的是( )
A. 由Fe、Cu、FeCl 溶液组成的原电池,负极反应式为Cu-2e-=Cu2+
3
B. 由Al、Cu、稀硫酸组成的原电池,负极反应式为Al-3e-=Al3+
−
C. 由Al、Mg、NaOH溶液组成的原电池,负极反应式为 Al+4OH--3e-=AlO2 +
2HO
2
D. 由Al、Cu、浓硝酸组成的原电池,负极反应式为Cu-2e-=Cu2+
*4. 工业上利用氢气在氯气中燃烧,所得产物再溶于水的方法制得盐酸,流程复杂且造
成能量浪费。有人设想利用原电池原理直接制盐酸的同时获取电能,假设这种想法可行,
下列说法肯定错误的是( )
第1页A. 通入氢气的电极为原电池的正极
B. 两极材料都用石墨,用稀盐酸作电解质溶液
C. 电解质溶液中的阳离子向通入氯气的电极移动
D. 通入氯气的电极反应式为Cl+2e-=2Cl-
2
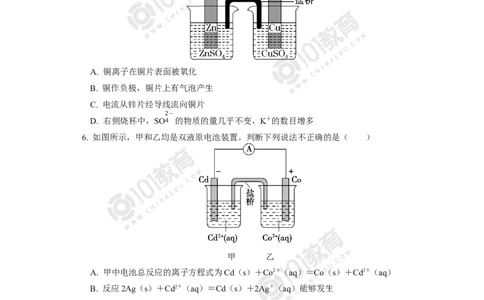
*5. 关于下图所示装置(盐桥含KCl)的叙述,正确的是( )
A. 铜离子在铜片表面被氧化
B. 铜作负极,铜片上有气泡产生
C. 电流从锌片经导线流向铜片
2−
D. 右侧烧杯中,SO4 的物质的量几乎不变,K+的数目增多
6. 如图所示,甲和乙均是双液原电池装置。判断下列说法不正确的是( )
甲 乙
A. 甲中电池总反应的离子方程式为Cd(s)+Co2+(aq)=Co(s)+Cd2+(aq)
B. 反应2Ag(s)+Cd2+(aq)=Cd(s)+2Ag+(aq)能够发生
C. 盐桥的作用是形成闭合回路,并使两边溶液保持电中性
D. 乙电池中有1 mol电子通过外电路时,正极有108 g Ag析出
*7. 已知某原电池的电极反应是Fe-2e-=Fe2+,Cu2++2e-=Cu,据此设计该原电池,
并回答问题。
第2页图1 图2
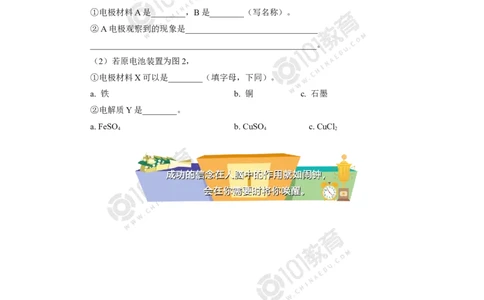
(1)若原电池装置为图1,
①电极材料A是________,B是________(写名称)。
②A电极观察到的现象是_______________________________
_____________________________________________________。
(2)若原电池装置为图2,
①电极材料X可以是________(填字母,下同)。
a. 铁 b. 铜 c. 石墨
②电解质Y是________。
a. FeSO b. CuSO c. CuCl
4 4 2
第3页深度揭秘原电池同步练习参考答案
1. 【答案】C
【解析】由第一个装置a极溶解,可知a极是负极,金属活动性a>b,对于第二个装置,
依据还原性规律知,金属活动性b>c,第三个装置的金属活动性d>c,由第四个装置电流从
a→d,则电子从d→a,故金属活动性d>a。
2. 【答案】B
【解析】两个装置都为原电池装置,均发生化学能转化成电能的过程,故 A正确;根
据原电池的工作原理,锌比铜活泼,锌作负极,铜作正极,铜本身不是反应物,故 B错误;
锌作负极,电子从负极经外电路流向正极,故 C正确;图乙中装置产生的电流在一段时间
内变化不大,但图甲装置产生的电流在较短时间内就会衰减,故D正确。
3. 【答案】A
【解析】铁比铜活泼,铁作负极,负极反应式为Fe-2e-=Fe2+,故A错误;铝比铜
活泼,铝作负极,负极反应式为Al-3e-=Al3+,故B正确;虽然镁比铝活泼,但镁不与
−
氢氧化钠溶液反应,因此铝作负极,负极反应式为Al+4OH--3e-=AlO2 +2HO,故C
2
正确;Al遇浓硫酸发生钝化反应,则铜作负极,负极反应式为Cu-2e-=Cu2+,故D正确。
4. 【答案】A
【解析】根据燃料电池工作原理,利用原电池原理直接制盐酸的方程式为H +Cl =
2 2
2HCl。氢气发生氧化反应,故通入氢气的电极为原电池的负极,故 A错误;两极材料可以
都用石墨,一极通入氢气,一极通入氯气,可以用稀盐酸作电解质溶液,故 B正确;在原
电池中,电解质溶液中的阳离子向正极移动,氯气发生还原反应,通入氯气的电极为正极
故C正确;氯气在正极发生得电子的还原反应,电极反应式为Cl+2e-=2Cl-,故D正确。
2
5. 【答案】D
【解析】铜离子在铜片表面被还原,A不正确;铜作正极,铜片上有铜析出,无气泡
产生,B不正确;电子从锌片经导线流向铜片,而电流方向与电子的定向移动方向相反,C
不正确;盐桥中阳离子移向正极,右侧烧杯中K+的数目增多,D正确。
6. 【答案】B
【解析】根据甲、乙装置分析可知A项正确,且可推知Cd的活泼性强于Ag,故Ag
不能置换出Cd,B项错误。
7. 【答案】(1)①铜(或其他合理答案) 铁 ②有红色物质析出
(2)①bc ②bc
第4页新型化学电源同步练习
(答题时间:40分钟)
一、选择题
1. 下列说法中正确的是( )
A. 碱性锌锰电池是二次电池
B. 铅蓄电池是一次电池
C. 二次电池又叫蓄电池,它放电后可以再充电使活性物质获得再生
D. 燃料电池的活性物质储存在电池内
2. 新型LiFePO 可充电锂离子动力电池以其独特的优势成为绿色能源的新宠。已知该电
4
池放电时的电极反应式为:正极:FePO +Li++e-=LiFePO ,负极:Li-e-=Li+。下列
4 4
说法中正确的是( )
A. 充电时动力电池上标注“+”的电极应与外接电源的正极相连
B. 充电时电池反应为FePO +Li++e-=LiFePO
4 4
C. 放电时电池内部Li+向负极移动
D. 放电时,在正极上Li+得电子被还原
*3. 美国海军海底战事中心与麻省理工大学共同研制成功了用于潜航器的镁—过氧化氢
燃料电池系统。其工作原理如图所示。以下说法中错误的是( )
A. 电池的负极反应为:Mg-2e-=Mg2+
B. 电池工作时,H+向负极移动
C. 电池工作一段时间后,溶液的pH增大
D. 电池总反应式是:Mg+HO+2H+=Mg2++2HO
2 2 2
*4. 科技工作者制造了一种甲烷燃料电池,一个电极通入空气,另一个电极通入甲烷,
电解质是掺杂了YO 的ZrO 晶体,它在高温下能传导O2-。以下判断错误的是( )
2 3 2
A. 电池正极发生的反应:O+4e-=2O2-
2
B. 电池负极发生的反应:CH+4O2--8e-=CO+2HO
4 2 2
C. 固体电解质里的O2-的移动方向:由正极移向负极
D. 向外电路释放电子的电极:正极(即电子由正极流向负极)
5. 铅蓄电池是化学电源,其电极材料分别是Pb和PbO ,电解质为稀硫酸,工作时该电
2
第5页池的总反应式为Pb+PbO +2HSO =2PbSO +2HO。试根据上述情况判断:
2 2 4 4 2
(1)蓄电池的负极材料是________。
(2)工作时,正极反应为________________________________。
(3)工作时,电解质溶液的pH________(填“增大”“减小”或“不变”)。
(4)工作时,电解质溶液中阴离子移向________极。
(5)电流方向从________极流向________极。
(6)充电时,铅蓄电池的负极与电源的________极相连接。
*6. 请仔细观察下列四种装置的构造示意图,完成下列问题。
(1)碱性锌锰电池的总反应式:Zn+2MnO +2HO=2MnOOH+Zn(OH) ,则负
2 2 2
极的电极反应式:__________________________________。
(2)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。试从影响反应速
率的因素分析其原因是____________________________________________。
(3)铅-硫酸蓄电池放电过程中,HSO 浓度________(填“变大”“变小”或“不
2 4
变”),放电时负极的电极反应式为____________________。
(4)锌银纽扣电池在工作过程中________(填物质名称)被还原。
第6页新型化学电源同步练习参考答案
1.【答案】C
【解析】碱性锌锰电池是一次电池,铅蓄电池是二次电池;燃料电池的活性物质没有
储存在电池内而是从外界不断输入电池。
2.【答案】A
【解析】A项,充电时动力电池上标注“+”的电极应与外接电源的正极相连,发生
氧化反应:LiFePO -e-=FePO +Li+,故A正确;B项,放电时电池反应为FePO +Li=
4 4 4
LiFePO ,则充电时电池反应为LiFePO =FePO +Li,故B错误;C项,放电时电池内部
4 4 4
Li+向正极移动,故C错误;D项,放电时,在正极上FePO 得电子被还原,故D错误。
4
3.【答案】B
【解析】Mg为负极,则负极反应为Mg-2e-=Mg2+,A正确;电池工作时,H+向正
极移动,B错误;电池总反应式是Mg+HO +2H+=Mg2++2HO,消耗H+,则电池工作
2 2 2
一段时间后,溶液pH增大,C正确,D正确。
4.【答案】D
【解析】因为放电时,电池正极发生还原反应(元素化合价降低),负极发生氧化反
应(元素化合价升高)。所以正极反应式是O +4e-=2O2-,负极反应式是CH +4O2--
2 4
8e-=CO+2HO。 由上述电池的正、负极反应式可以看出:正极反应“源源不断”地产
2 2
生O2-,负极反应要持续进行,则需要“持续不断”地消耗O2-,故电池内O2-的移动方向
是由正极移向负极。电池的负极发生氧化反应,失去电子,故外电路电子从负极流出,所
以D错误。
2−
5.【答案】(1)Pb (2)PbO +4H++SO4 +2e-=PbSO +2HO (3)增大 (4)
2 4 2
负 (5)正 负 (6)负
6.【答案】(1)Zn+2OH--2e-=Zn(OH)
2
(2)碱性锌锰电池用锌粉替代了原锌锰电池的锌壳,增大了反应物的接触面积,加快
了反应速率,故放电电流大(合理答案均可)
2−
(3)变小 Pb-2e-+SO4 =PbSO (4)氧化银
4
【解析】(1)原电池的负极发生氧化反应,根据元素化合价变化知锌失电子,负极的
电极反应式为Zn+2OH--2e-=Zn(OH)
2
第7页