文档内容
3.3.1 金属晶体与离子晶体(导学案)
1.知道金属晶体的结构特点,能辨识常见的金属晶体,能用金属键理论解释金属的一些物
理性质。
2.能借助金属晶体模型说明金属晶体中的粒子及粒子间的相互作用。
3.借助NaCl、CsCl的晶胞模型认识离子晶体的结构特点,能辨识常见的离子晶体。
4.能说明离子键的形成,并能从微观角度理解离子键对离子晶体性质的影响,从宏观角度
解释离子晶体性质的差异,促进“宏观辨识与微观探析”化学核心素养的发展。
重点:金属晶体与离子晶体的结构与性质。
难点:金属晶体与离子晶体的结构与性质。
1.金属键
(1)概念:金属阳离子和自由电子之间存在的强烈的相互作用称为金属键。
(2)本质:金属原子脱落下来的 形成遍布整块晶体的“ ”,被所有原
子共用,从而把所有的 维系在一起,形成一种“巨分子”。
(3)描述金属键本质的最简单理论是“ ”。
2.金属晶体
(1)通过金属阳离子与 之间的较强作用形成的晶体,叫做金属晶体,包括纯金
属和合金。
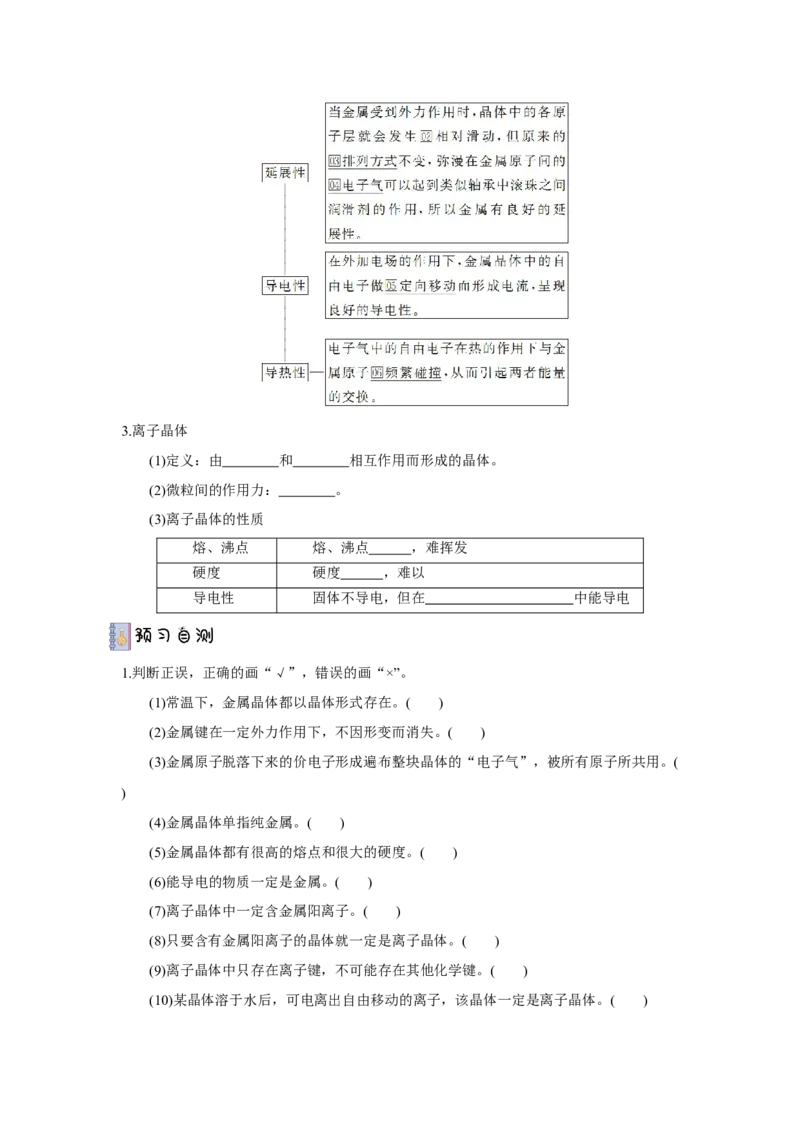
(2)用电子气理论解释金属的物理性质3.离子晶体
(1)定义:由 和 相互作用而形成的晶体。
(2)微粒间的作用力: 。
(3)离子晶体的性质
熔、沸点 熔、沸点 ,难挥发
硬度 硬度 ,难以
导电性 固体不导电,但在 中能导电
1.判断正误,正确的画“√”,错误的画“×”。
(1)常温下,金属晶体都以晶体形式存在。( )
(2)金属键在一定外力作用下,不因形变而消失。( )
(3)金属原子脱落下来的价电子形成遍布整块晶体的“电子气”,被所有原子所共用。(
)
(4)金属晶体单指纯金属。( )
(5)金属晶体都有很高的熔点和很大的硬度。( )
(6)能导电的物质一定是金属。( )
(7)离子晶体中一定含金属阳离子。( )
(8)只要含有金属阳离子的晶体就一定是离子晶体。( )
(9)离子晶体中只存在离子键,不可能存在其他化学键。( )
(10)某晶体溶于水后,可电离出自由移动的离子,该晶体一定是离子晶体。( )(11)可通过某一晶体的离子键成分来判断该晶体属于离子晶体还是共价晶体。(
2.下列有关叙述正确的是( )
A.金属晶体中含有阳离子和阴离子
B.金属键越强,则该金属的金属性越强
C.金属钨的熔点高于金属钠的熔点,是因为钨的金属键比钠的金属键强
D.金属导电的过程实质上就是金属键被破坏的过程,不能用“电子气理论”来解释
3.下图是金属晶体内部的电子气理论示意图。电子气理论可以用来解释金属的性质,其中
正确的是( )
A.金属能导电是因为金属阳离子在外加电场作用下定向移动
B.金属能导热是因为自由电子在热的作用下相互碰撞,从而发生热的传导
C.金属具有延展性是因为在外力的作用下,金属各原子层间会出现相对滑动,但自
由电子可以起到润滑的作用,使金属不会断裂
D.合金与纯金属相比,由于增加了不同的金属或非金属,使电子数目增多,所以合
金的延展性比纯金属强,硬度比纯金属小
4.某新型“防盗玻璃”为多层结构,每层中间嵌有极细的金属线。当玻璃被击碎时,与金
属线相连的警报系统就会立即报警。“防盗玻璃”能报警是利用了金属的( )
A.延展性 B.导电性
C.弹性 D.导热性
考点1金属键与金属晶体
1.对金属晶体的组成、性质的正确理解
(1)金属单质和合金都属于金属晶体。
(2)金属晶体中含有金属阳离子,但没有阴离子。
(3)金属导电的微粒是自由电子,电解质溶液导电的微粒是自由移动的阳离子和阴离
子;前者导电过程中不生成新物质,为物理变化,后者导电过程中有新物质生成,为化学变化。因而,两者导电的本质不同。
2.金属晶体熔、沸点的比较
金属晶体熔点变化差别较大。如汞在常温下是液体,熔点很低(-38.9 ℃),而铁(1535
℃)等金属熔点很高。这是由于金属阳离子与自由电子的静电作用(金属键)不同而造成的差
别。
金属晶体的熔、沸点高低和金属键的强弱有关。金属原子价电子数越多,离子半径越
小,金属离子与自由电子的作用力就越强,晶体的熔、沸点就越高,反之越低。
例如:元素周期表中碱金属单质的熔、沸点从上到下逐渐降低——价电子数相同,离
子半径逐渐增大。
下列关于金属键的叙述中,不正确的是( )
A.金属键是金属阳离子和自由电子这两种带异性电荷的微粒间的强烈相互作用,其
实质与离子键类似,也是一种静电作用
B.金属键可以看作是许多原子共用许多电子所形成的强烈的相互作用,所以与共价
键类似,也有方向性和饱和性
C.金属键是带异性电荷的金属阳离子和自由电子间的相互作用,故金属键无饱和性
和方向性
D.构成金属键的自由电子在整个金属内部的三维空间中做自由运动
下列关于金属性质和原因的描述不正确的是( )
A.金属一般具有银白色光泽,是物理性质,与金属键没有关系
B.金属具有良好的导电性,是因为金属晶体中共享了金属原子的价电子,形成了
“电子气”,在外电场的作用下自由电子定向移动便形成了电流
C.金属具有良好的导热性能,是因为自由电子通过与金属原子发生碰撞,传递了能
量
D.Na、Mg、Al的沸点依次升高,是因为半径依次减小,价电子数依次增多
考点2离子晶体
1.离子晶体的结构特点
(1)离子晶体微粒之间的作用力是离子键,由于离子键没有方向性和饱和性,故离子晶体一
般采取密堆积方式。(2)离子晶体中存在的微粒是阳离子和阴离子,离子晶体的化学式只表示晶体中阴、阳离子
的个数比,而不是表示其分子组成。
(3)离子晶体中,离子半径越小,离子所带电荷越多,离子键越强。
2.离子晶体的性质
性质 原因
离子晶体有较高的熔、沸点和难挥发性。离子晶体中有较强的离子键,熔化或汽化
熔、沸
时需消耗较多的能量。同种类型的离子晶体,离子半径越小,离子键越强,熔、沸
点
点越高
硬而脆。离子晶体表现出较高的硬度。但当晶体受到冲击力作用时,部分离子键发
硬度
生断裂,导致晶体破碎
离子晶体中,阴、阳离子不能自由移动,离子晶体不导电。熔融状态或溶于水时,
导电性
解离成自由移动的离子而导电
溶解性 大多数离子晶体易溶于极性溶剂(如水)中,难溶于非极性溶剂(如汽油、苯、CCl )中
4
延展性 无延展性
3.常见离子晶体的晶胞结构
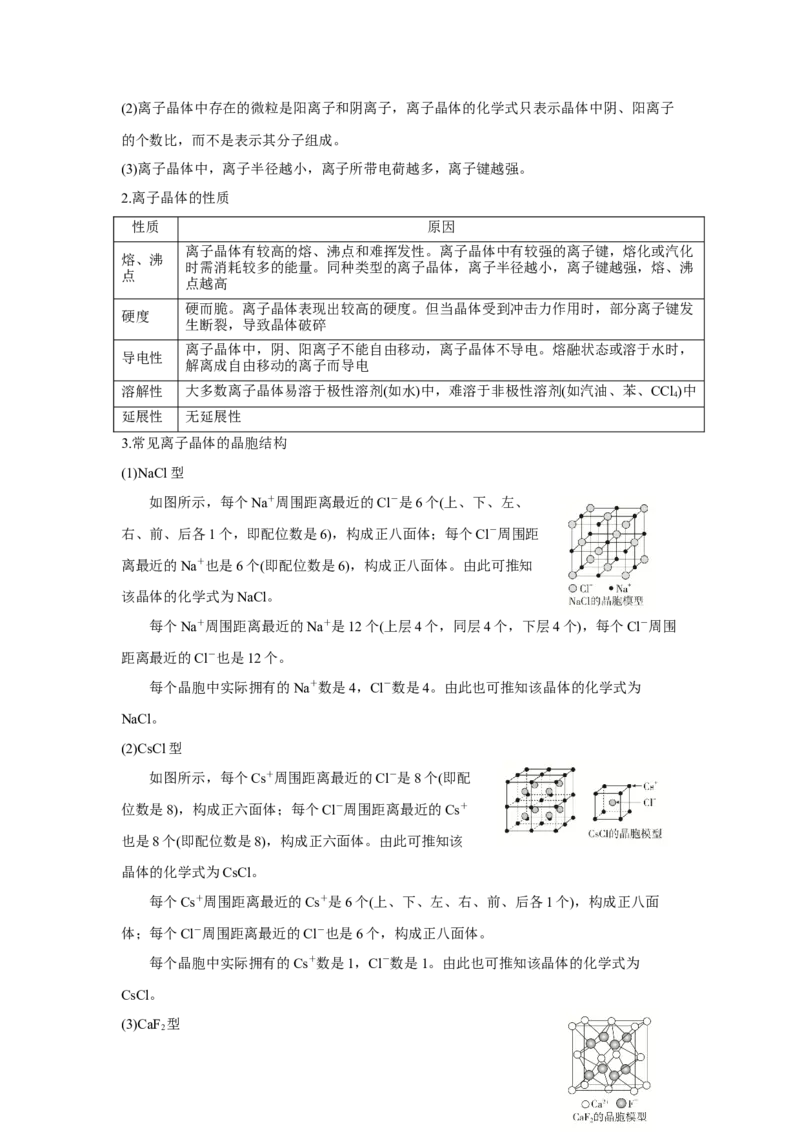
(1)NaCl型
如图所示,每个Na+周围距离最近的Cl-是6个(上、下、左、
右、前、后各1个,即配位数是6),构成正八面体;每个Cl-周围距
离最近的Na+也是6个(即配位数是6),构成正八面体。由此可推知
该晶体的化学式为NaCl。
每个Na+周围距离最近的Na+是12个(上层4个,同层4个,下层4个),每个Cl-周围
距离最近的Cl-也是12个。
每个晶胞中实际拥有的Na+数是4,Cl-数是4。由此也可推知该晶体的化学式为
NaCl。
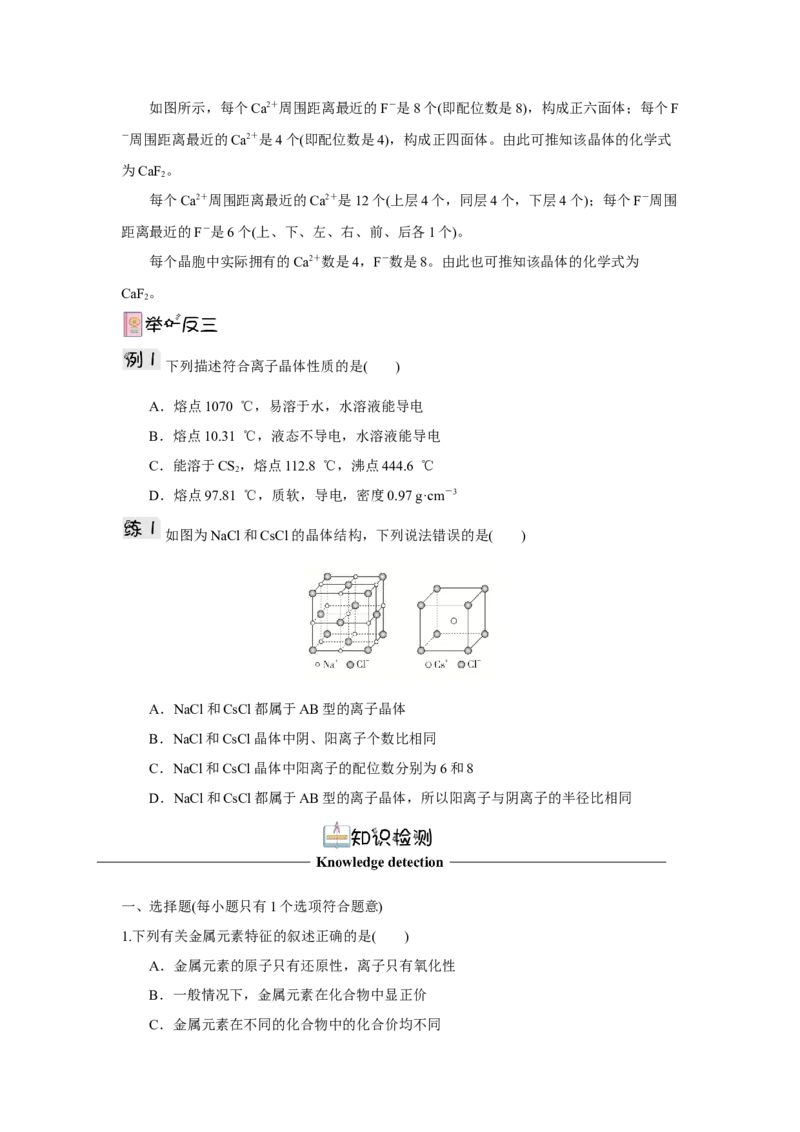
(2)CsCl型
如图所示,每个Cs+周围距离最近的Cl-是8个(即配
位数是8),构成正六面体;每个Cl-周围距离最近的Cs+
也是8个(即配位数是8),构成正六面体。由此可推知该
晶体的化学式为CsCl。
每个Cs+周围距离最近的Cs+是6个(上、下、左、右、前、后各1个),构成正八面
体;每个Cl-周围距离最近的Cl-也是6个,构成正八面体。
每个晶胞中实际拥有的Cs+数是1,Cl-数是1。由此也可推知该晶体的化学式为
CsCl。
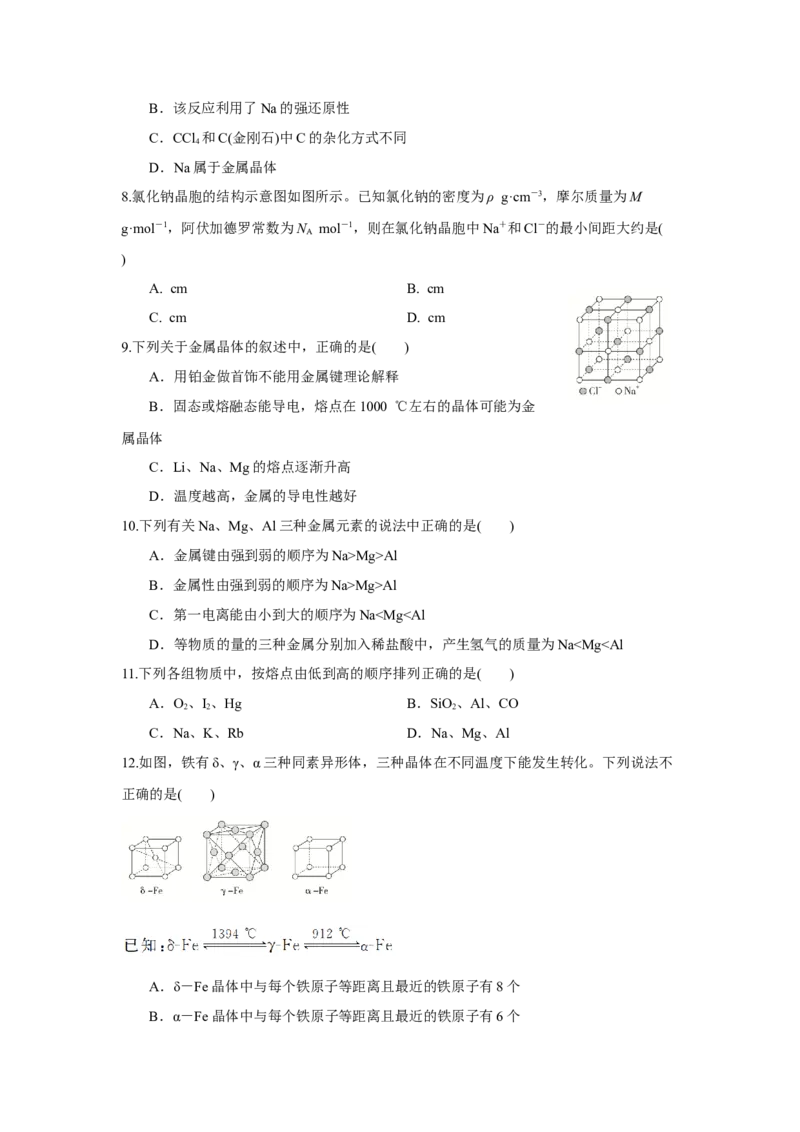
(3)CaF 型
2如图所示,每个Ca2+周围距离最近的F-是8个(即配位数是8),构成正六面体;每个F
-周围距离最近的Ca2+是4个(即配位数是4),构成正四面体。由此可推知该晶体的化学式
为CaF 。
2
每个Ca2+周围距离最近的Ca2+是12个(上层4个,同层4个,下层4个);每个F-周围
距离最近的F-是6个(上、下、左、右、前、后各1个)。
每个晶胞中实际拥有的Ca2+数是4,F-数是8。由此也可推知该晶体的化学式为
CaF 。
2
下列描述符合离子晶体性质的是( )
A.熔点1070 ℃,易溶于水,水溶液能导电
B.熔点10.31 ℃,液态不导电,水溶液能导电
C.能溶于CS,熔点112.8 ℃,沸点444.6 ℃
2
D.熔点97.81 ℃,质软,导电,密度0.97 g·cm-3
如图为NaCl和CsCl的晶体结构,下列说法错误的是( )
A.NaCl和CsCl都属于AB型的离子晶体
B.NaCl和CsCl晶体中阴、阳离子个数比相同
C.NaCl和CsCl晶体中阳离子的配位数分别为6和8
D.NaCl和CsCl都属于AB型的离子晶体,所以阳离子与阴离子的半径比相同
一、选择题(每小题只有1个选项符合题意)
1.下列有关金属元素特征的叙述正确的是( )
A.金属元素的原子只有还原性,离子只有氧化性
B.一般情况下,金属元素在化合物中显正价
C.金属元素在不同的化合物中的化合价均不同D.金属元素的单质在常温常压下均为金属晶体
2.有关离子晶体的下列说法不正确的是( )
A.离子晶体在熔融状态时都能导电
B.离子晶体具有较高的熔、沸点,较大的硬度
C.离子晶体中阴、阳离子个数比为1∶1
D.氯化钠溶于水时离子键被破坏
3.银是导电性最好的金属材料,银能导电的原因是( )
A.金属银晶体中银离子与自由电子间的相互作用力较大
B.银晶体中的自由电子在外加电场的作用下可发生定向移动
C.银晶体中的银离子在外加电场的作用下可发生定向移动
D.银晶体在外加电场作用下可失去电子
4.下列关于金属键或金属的性质说法正确的是( )
①金属的导电性是由金属阳离子和自由电子的定向移动实现的 ②金属键是金属阳离子和
自由电子之间存在的强烈的静电吸引作用 ③第三周期金属元素Na、Mg、Al的沸点依次
升高 ④金属键没有方向性和饱和性,金属中的电子在整个三维空间运动,属于整个金属
A.①② B.②③
C.③④ D.①④
5.氟在自然界中常以CaF 的形式存在。下列关于CaF 的表述正确的是( )
2 2
A.CaF 中的化学键为离子键,因此CaF 在熔融状态下能导电
2 2
B.F-的半径小于Cl-,则CaF 的熔点低于CaCl
2 2
C.阴、阳离子数目之比为2∶1的物质,均与CaF 晶体结构相同
2
D.Ca2+与F-间只存在静电吸引
6.下列叙述正确的是( )
A.金属受外力作用时常常发生变形而不易折断,这是由于金属原子之间有较强的作
用
B.通常情况下,金属里的自由电子会发生定向移动而形成电流
C.金属导热是借助自由电子的运动,把能量从温度高的部分传到温度低的部分
D.金属的导电性随温度的升高而减弱
7.利用反应CCl +4Na=====C(金刚石)+4NaCl可实现人工合成金刚石。下列有关说法错误
4
的是( )
A.C(金刚石)具有很高的熔、沸点B.该反应利用了Na的强还原性
C.CCl 和C(金刚石)中C的杂化方式不同
4
D.Na属于金属晶体
8.氯化钠晶胞的结构示意图如图所示。已知氯化钠的密度为ρ g·cm-3,摩尔质量为M
g·mol-1,阿伏加德罗常数为N mol-1,则在氯化钠晶胞中Na+和Cl-的最小间距大约是(
A
)
A. cm B. cm
C. cm D. cm
9.下列关于金属晶体的叙述中,正确的是( )
A.用铂金做首饰不能用金属键理论解释
B.固态或熔融态能导电,熔点在1000 ℃左右的晶体可能为金
属晶体
C.Li、Na、Mg的熔点逐渐升高
D.温度越高,金属的导电性越好
10.下列有关Na、Mg、Al三种金属元素的说法中正确的是( )
A.金属键由强到弱的顺序为Na>Mg>Al
B.金属性由强到弱的顺序为Na>Mg>Al
C.第一电离能由小到大的顺序为Na