文档内容
3.3 盐类的水解(精练)
题组一 盐类水解原理
1.下列物质的水溶液呈酸性的是
A.NH Cl B.NaCl C.CHCOONa D.NaCO
4 3 2 3
【答案】A
【解析】A.氯化铵为强酸弱碱盐,铵根离子水解使得溶液显酸性,A符合题意;
B.NaCl为强酸强碱盐,溶液呈中性,B与题意不符;
C.CHCOONa为弱酸强碱盐,溶液中醋酸根离子水解生成醋酸和氢氧根离子,溶液呈碱性,C与题意不
3
符;
D.NaCO 溶液中碳酸根离子水解生成氢氧根离子,溶液显碱性,D与题意不符;
2 3
故选A。
2.(2022·湖北武汉·高二期末)下列溶液呈中性的是
A. 溶液 B. 溶液
C. 溶液 D. 溶液
【答案】C
【解析】A.FeCl 为强酸弱碱盐,铁离子水解溶液显酸性,故A错误;
3
B.NaCO 为强碱弱酸盐,碳酸根离子水解溶液显碱性,故B错误;
2 3
C.NaCl溶液中氯化钠是强酸强碱盐,溶液显中性,故C正确;
D.CHCOOH为酸,在溶液中电离出氢离子,其溶液呈酸性,故D错误;
3
答案选C。
3.(2022·新疆·叶城县第八中学高二期末)下列盐溶液因水解而显酸性的是
A.NaHSO B.NaHCO C.NaHPO D.NH Cl
4 3 2 4 4
【答案】D
【解析】A.NaHSO 是强酸的酸式盐,在水中电离产生Na+、H+、 ,而使溶液显酸性,A不符合题意;
4
B.NaHCO 是强碱弱酸盐,在溶液中 发生水解反应,消耗水电离产生的H+、HCO、OH-,最终达
3 2 3
到平衡时,溶液中c(OH-)>c(H+),使溶液显碱性,B不符合题意;C.NaHPO 是强碱弱酸盐,在溶液中 发生水解作用,消耗水电离产生的H+,产生 、OH-,使
2 4
溶液显碱性;同时溶液中存在 的电离作用, 电离产生H+和 ,使溶液显酸性。由于其水解
作用大于电离作用,因此最终达到平衡时,溶液中c(OH-)>c(H+),溶液显碱性,C不符合题意;
D.NH Cl是强酸弱碱盐,在溶液中 发生水解作用,消耗水电离产生的OH-,反应产生NH ·H O、
4 3 2
H+,最终达到平衡时,溶液中c(H+)>c(OH-),使溶液显酸性,D符合题意;
故合理选项是D。
题组二 盐类水解的规律及应用
1.物质的量浓度相同的下列溶液中,按pH由小到大的顺序排列的是( )
A.NaCO、NaHCO 、NaCl、NH Cl
2 3 3 4
B.NaCO、NaHCO 、NH Cl、NaCl
2 3 3 4
C.(NH )SO 、NH Cl、NaNO 、NaS
4 2 4 4 3 2
D.NH Cl、(NH )SO 、NaS、NaNO
4 4 2 4 2 3
【答案】C
【解析】CO的水解程度大于HCO的,pH:NaCO >NaHCO ,故选项A、B不符合要求;NH水解使
2 3 3
NH Cl溶液、(NH )SO 溶液显酸性,相同物质的量浓度时,(NH )SO 溶液中NH浓度大于NH Cl溶液中
4 4 2 4 4 2 4 4
NH浓度,则pH:(NH )SO <NH Cl,NaNO 不水解,S2-水解使NaS溶液显碱性,选项C符合要求,选
4 2 4 4 3 2
项D不符合要求。
2.(2022·重庆八中高二阶段练习)室温下,往0.001mol/L的氨水中滴入几滴酚酞试液时,溶液呈现粉红
色。现采取下列措施,其中能使滴有酚酞的氨水溶液颜色变浅的是
A.往溶液中加入0.1mol/L的氨水
B.往溶液中加入 晶体
C.往溶液中加入 固体
D.往溶液中加入 溶液
【答案】B
【解析】A.往溶液中滴入0.1mol·L-1的氨水,NH •H O NH ++OH-的平衡向正反应方向移动,增大了
3 2 4
氢氧根离子的浓度,溶液颜色变深,故A错误;
B.加固体醋酸铵,铵根离子浓度增大影响大于醋酸根离子水解影响,增大了铵根离子的浓度,NH •H O
3 2NH ++OH-的平衡向逆反应方向移动,降低了氢氧根离子的浓度,溶液颜色变浅,故B正确;
4
C.往溶液中加入CHCOONa固体,醋酸钠水解溶液呈碱性,增大了氢氧根离子的浓度,溶液颜色变深,
3
故C错误;
D.加固体氢氧化钠,增大了氢氧根离子的浓度,溶液颜色加深,故D错误;
故选B。
3.(2021·北京·中国农业大学附属中学高二期中)常温下,物质的量浓度均为0.10 mol/L的下列物质的水
溶液,pH>7的是
A.CuCl B.NaCl C.KOH D.HNO
2 3
【答案】C
【解析】A.CuCl 是强酸弱碱盐,在溶液中Cu2+会发生水解反应,消耗水电离产生的OH-变为 Cu(OH) ,
2 2
同时产生H+,水电离平衡正向移动,最终达到平衡水溶液中c(H+)>c(OH-),溶液显酸性,溶液pH<7,A
不符合题意;
B.NaCl是强酸强碱盐,不水解,溶液中c(H+)=c(OH-),因此溶液显中性,则溶液pH=7,B不符合题意;
C.KOH是一元强碱,在水中完全电离产生OH-,使溶液显碱性,在常温下溶液pH>7,C符合题意;
D.HNO 是一元强酸,在水中完全电离产生H+,使溶液中c(H+)>c(OH-),溶液显酸性,则溶液pH<7,D
3
不符合题意;
故合理选项是C。
4.(2022·吉林辽源·高二期末)室温下,下列溶液中 最大的是
A. 的氨水 B. 的 溶液
C. 的 溶液 D. 的 溶液
【答案】B
【解析】A.0.1 molL−1 的氨水中铵根离子来源于一水合氨的电离,但是电离很微弱,故其中的铵根离子
是很少的,A不符合⋅题意;
B.B、C、D三种溶液中,0.1 molL−1 的NH HSO 溶液中,铵根离子有少部分发生了水解,由于硫酸氢根
4 4
离子在水溶液中会电离出氢离子,⋅而氢离子又会抑制铵根离子的水解,故0.1 molL−1 硫酸氢铵溶液中的铵
根离子是最多的,B符合题意; ⋅
C.B、C、D三种溶液中,0.1 molL−1 的NH HCO 溶液,铵根离子有少部分发生了水解,由于碳酸氢根会
4 3
水解产生氢氧根离子,而氢氧根离⋅子又会促进铵根离子的水解,故故0.1 molL−1 硫酸氢铵溶液中的铵根离
⋅子是最少的,C不符合题意;
D.B、C、D三种溶液中,0.1 molL−1 的NH NO 溶液,铵根离子有少部分发生了水解,但不受硝酸根离
4 3
子的影响,故0.1 molL−1硝酸铵溶液⋅ 中的铵根离子浓离居于三者中间,D不符合题意;
故选B。 ⋅
5.常温下,盐酸与氨水混合,所得溶液pH=7,则此溶液中
A.c( )c(Cl-) D.无法确定c( )与c(Cl-)的关系
【答案】B
【解析】常温下,盐酸与氨水混合,根据电荷守恒可知,c( )+c( )=c(Cl-)+c(OH-),因为所得溶液
pH=7,则+c( )=c(OH-),所以c( )=c(Cl-),B项符合题意。
故选B。
题组三 盐类水解方程式书写
1.(2022·吉林·长春博硕学校高二期末)下列离子方程式中,属于水解反应的是
A.CHCOOH+H O CHCOO-+ H O+ B.SO +H O HSO + H+
3 2 3 3 2 2
C.CO + H O HCO + OH- D.HCO + H O CO + H O+
2 2 3
【答案】C
【解析】A.CHCOOH+H O CHCOO-+ H O+是醋酸电离出醋酸根离子和一水合氢离子,故A不符
3 2 3 3
合题意;
B.SO +H O HSO + H+是生成亚硫酸,亚硫酸电离出氢离子和亚硫酸氢根,故B不符合题意;
2 2
C.CO + H O HCO + OH-是碳酸根水解生成碳酸氢根和氢氧根,故C符合题意;
2
D.HCO + H O CO + H O+是碳酸氢根电离出氢离子和碳酸根离子,故D不符合题意。
2 3
综上所述,答案为C。
2.(2021·吉林·榆树市第一高级中学校高二期中)下列反应中,不属于盐类水解反应的是A.NH + H O NH •H O + H+ B.HCO + H O CO + H O+
2 3 2 2 3
C.Al3+ + 3H O Al(OH) + 3H+ D.S2-+ H O HS- + OH-
2 3 2
【答案】B
【解析】A. 铵根离子发生水解反应生成一水合氨和氢离子,水解方程式为NH + H O NH •H O +
2 3 2
H+,氢离子浓度大于氢氧根离子浓度,溶液呈酸性,故A不符合 ;
B. HO+为水合氢离子,该式可表示为HCO CO + H+,属于电离方程式,不是水解方程式,故B符
3
合;
C. 铝离子发生水解反应生成Al(OH) 和H+,水解方程式为Al3+ + 3H O Al(OH) + 3H+,氢离子浓度
3 2 3
大于氢氧根离子浓度,溶液呈酸性,故C不符合;
D. S2-+H O HS-+OH-为水解反应,但硫离子结合消耗掉氢离子,造成氢氧根离子浓度大于氢离子浓度,
2
溶液呈碱性,⇌故D不符合;
故选B。
3.下列水解离子方程式正确的是
A.Fe3++3H O Fe(OH) ↓+3H+ B.Br-+H O HBr+OH-
2 3 2
C.CO +H O HCO+2OH- D.NH +H O NH •H O+H+
2 2 3 2 3 2
【答案】D
【解析】A.铁离子在水中部分水解生成氢氧化铁和氢离子,离子方程式为:Fe3++3H O Fe(OH) +3H+,
2 3
A项错误;
B.溴离子属于强酸阴离子,不水解,B项错误;
C.碳酸根离子为多元弱酸的酸根离子,分步水解,以第一步为主,离子方程式为CO +H O HCO
2
+OH-,C项错误;
D.铵根离子水解生成一水合氨和氢离子,离子方程式为:NH +H O NH •H O+ H+,D项正确;
2 3 2
答案选D。
4.下列离子方程式中,属于水解反应的是
A.CHCOOH+HO CHCOO-+HO+ B.SO +HO +H+
3 2 3 3 2 2C. +OH- +HO D. +HO NH ·H O+H+
2 2 3 2
【答案】D
【解析】A.醋酸与水作用生成阴阳离子,属于醋酸电离方程式,不属于水解反应方程式,A错误;
B.SO +HO +H+,属于二氧化硫和水反应,并电离出氢离子的过程,不属于水解反应,B错误;
2 2
C. +OH- +HO是 与OH-之间发生化学反应的离子方程式,不属于水解反应方程式,
2
C错误;
D. +HO NH ·H O+H+是 与水反应生成弱电解质NH •H O和H+,属于 水解反应方程式,
2 3 2 3 2
D正确;
故选D。
5.下列离子方程式中,属于水解反应的是
A.CHCOOH+H O CHCOO-+H O+ B.SO +H O HSO
3 2 3 3 2 2 2 3
C.HCO +OH- CO +H O D.NH +H O NH •H O+H+
2 2 3 2
【答案】D
【解析】A.CHCOOH+H O CHCOO-+H O+表示弱酸CHCOOH在水中电离的电离方程式,不属于
3 2 3 3 3
盐水解反应的离子方程式,A不符合题意;
B.SO +H O HSO 表示SO 溶于水,与水反应产生HSO ,该反应是可逆反应,不属于盐水解反应的
2 2 2 3 2 2 3
离子方程式,B不符合题意;
C.HCO +OH- CO +H O表示碳酸的酸式盐与碱反应产生正盐和水反应的离子方程式,而不能表示
2
盐水解反应的离子方程式,C不符合题意;
D.NH +H O NH •H O+H+表示铵盐的NH 与水电离产生的OH-结合形成弱碱NH •H O和H+,水电
2 3 2 3 2
离平衡被破坏,促进水的电离,最终达到平衡时溶液中c(H+)>c(OH-),溶液显酸性,是表示盐的水解平衡
的离子方程式,D符合题意;
故合理选项是D。
6.(2021·江西·吉安县第三中学高二阶段练习)下列反应不属于水解反应或水解方程式不正确的是①HCl+HO HO++Cl-
2 3
②AlCl +3HO=Al(OH) +3HCl
3 2 3
③CO +2HO HCO+2OH-
2 2 3
④碳酸氢钠溶液:HCO +HO CO +H O+
2 3
⑤HS-的水解:HS-+HO S2-+HO+
2 3
⑥NaAlO 与NaHCO 溶液混合:AlO +HCO +HO=Al(OH) ↓+CO
2 3 2 3
A.①②③④ B.①②③⑥ C.②③⑤⑥ D.全部
【答案】D
【解析】①HCl+HO HO++Cl-属于HCl的电离方程式,但是HCl是强酸,能完全电离;
2 3
②AlCl +3HO=Al(OH) +3HCl为AlCl 的水解方程式,但水解是微弱的,应用“ ”表示;
3 2 3 3
③多元弱酸根离子的水解要分步进行,所以,CO +2HO HCO+2OH-水解方程式错误;
2 2 3
④碳酸氢钠溶液:HCO +HO CO +H O+为HCO 的电离方程式;
2 3
⑤HS-+HO S2-+HO+为HS-的电离方程式;
2 3
⑥NaAlO 与NaHCO 溶液反应方程式:AlO +HCO +HO=Al(OH) ↓+CO 不属于水解反应;
2 3 2 3
故不属于水解反应或水解方程式不正确的是:①②③④⑤⑥,故答案选D。
7.(2022·全国·高二课时练习)下列水解离子方程式正确的是
A.NH +2HO NH ·H O +HO+
2 3 2 3
B.CO +2HO 2OH- + HCO
2 2 3
C.Fe3++3HO Fe(OH) ↓+3H+
2 3
D.Cl+HO H++Cl-+HClO
2 2
【答案】A
【解析】A.一水合氨是弱碱,铵根发生水解反应生成一水合氨和氢离子,水解离子方程式为
,A正确;B.碳酸根分步水解,且以第一步水解反应为主,水解离子方程式为 ,B错误;
C.水解反应是微弱的,不产生沉淀,水解离子方程式为 ,C错误;
D.氯气和水反应生成HCl和HClO是氧化还原反应,不是水解反应,D错误;
故选:A。
8.(2021·全国·高二专题练习)写出下列盐溶于水后发生水解反应的离子方程式。
(1)CH COONa___________
3
。
(2)NH Cl___________
4
。
(3)Na CO___________
2 3
。
(4)Al(SO )___________
2 4 3
。
【答案】(1)CH COO-+HO CHCOOH+OH-
3 2 3
(2)NH +HO NH ·H O+H+
2 3 2
(3)CO +HO HCO +OH-,HCO +HO HCO+OH-
2 2 2 3
(4)Al3++3HO Al(OH) +3H+
2 3
【解析】(1)CH COO-水解生成CHCOOH和OH-,水解方程式为:CHCOO-+HO CHCOOH+OH-,
3 3 3 2 3
故答案为:CHCOO-+HO CHCOOH+OH-;
3 2 3
(2)NH 水解生成NH ·H O和H+,水解方程式为:NH +HO NH ·H O+H+,故答案为:NH +HO
3 2 2 3 2 2
NH ·H O+H+;
3 2
(3)CO 水解生成HCO 和OH-,HCO 能继续水解生成HCO 和OH-,水解方程式为:CO +HO
2 3 2HCO +OH-,HCO +HO HCO+OH-,故答案为:CO +HO HCO +OH-,HCO +HO
2 2 3 2 2
HCO+OH-;
2 3
(4)Al3+水解生成Al(OH) 和H+,水解方程式为:Al3++3HO Al(OH) +3H+,故答案为:Al3++3HO
3 2 3 2
Al(OH) +3H+。
3
题组四 影响盐类水解的因素
1.下列粒子能影响水的电离平衡,且能使水的电离平衡向右移动的是
A.CHCOOH B.OH- C.CO D.Cl-
3
【答案】C
【解析】A.醋酸电离得到氢离子,增大了氢离子浓度,抑制了水电离,水的电离平衡向左移动,A错误;
B.增大OH-的浓度,抑制了水电离,水的电离平衡向左移动,B错误;
C.CO 水解,促进了水电离,水的电离向右移动,C正确;
D.Cl-不水解不电离,不影响水的电离,D错误;
故选C。
2.(2022·全国·高二课时练习)能够使CHCOONa溶液pH增大且水解程度也增大的条件是
3
A.加水 B.升温 C.加压 D.加CHCOONa固体
3
【答案】B
【解析】A.醋酸钠溶液显碱性,加水促进CHCOONa水解,但是氢氧根离子浓度减小,pH减小,故A
3
错误;
B.水解过程为吸热过程,升温促进CHCOONa水解,碱性增强,pH增大,故B正确;
3
C.反应没有气体参与,因此加压水解平衡不移动,故C错误;
D.加CHCOONa固体,增大了醋酸钠的浓度,水解平衡右移,但CHCOONa水解程度减小,故D错误。
3 3
故选B。
3.(2022·全国·高二课时练习)一定条件下,CHCOONa溶液中下列说法正确的是
3
A.加入冰醋酸, 增大B.通入HCl,平衡正向移动,溶液pH增大
C.加入NaOH固体,平衡正向移动,pH减小
D.稀释溶液,平衡正向移动, 增大
【答案】A
【解析】A. = ,加入冰醋酸,K 不变,氢离子浓度增大,所以该比值增大,A正确;
a
B.溶液中存在水解平衡CHCOO-+H O CHCOOH+OH-,通入HCl,消耗氢氧根,平衡正向移动,HCl
3 2 3
会电离出大量氢离子,溶液pH会减小,B错误;
C.NaOH可以电离出大量氢氧根,平衡逆向移动,溶液碱性增强,pH增大,C错误;
D.稀释溶液,促进水解,平衡正向移动, 即水解平衡常数,只与温度有关,温度不
变则该值不变,D错误;
综上所述答案为A。
4.(2021·河北正中实验中学高二阶段练习)下列溶液在加水不断稀释过程中数值保持增大的是
A.在0.1 mol/L HF溶液中
B.在0.1 mol/L CH COONa溶液中
3
C.在0.1 mol/L盐酸溶液中c(OH-)
D.在0.1 mol/L HClO溶液中
【答案】C
【解析】A.在0.1 mol/L HF溶液中加水稀释,c(HF)、c(F-)都减小,所以 减小,A不符合题意;
B.在0.1 mol/L CH COONa溶液中存在水解平衡:CHCOO-+H O CHCOOH+OH-,加水稀释,水解平
3 3 2 3
衡正向移动,导致 减小,B不符合题意;
C.在0.1 mol/L盐酸溶液中加水稀释,溶液中c(H+)减小,由于溶液中存在水的电离平衡,c(H+)∙c(OH-)=K ,c(H+)减小,则溶液中c(OH-)增大,C符合题意;
w
D.在0.1 mol/L HClO溶液中存在电离平衡:HClO H++ClO-, =
,K、K 只与温度有关,温度不变K、K 不变,所以加水稀释过程中,
a w a w
不变,D不符合题意;
故合理选项是C。
5.为配制NH 的浓度与 的浓度比为1∶1的溶液,可在 溶液中加入
①适量的HCl ②适量的NaCl ③适量的 ④适量的NaOH
A.①② B.③ C.③④ D.④
【答案】B
【解析】①加入适量的HCl,溶液中氯离子浓度增大,则溶液中c( )<c(Cl-),故①不符合题意;
②加入适量的NaCl,溶液中氯离子的浓度增加,铵根离子浓度不变,因此c( )<c(Cl-),故②不符合题
意;
③加入适量 ,增加溶液中铵根离子的浓度,并保持氯离子浓度不变,故③符合题意;
④加入适量NaOH,会发生反应: +OH-=NH∙H O, 越来越少,氯离子浓度不变,导致c( )
3 2
<c(Cl-),故④不符合题意;
答案选B。
6.(2022·全国·高二课时练习)一定条件下,NH Cl溶液中存在如下平衡:NH +H O NH •H O+H+,下
4 2 3 2
列说法正确的是
A.稀释溶液,平衡正向移动, 增大B.通入少量HCl气体,平衡逆向移动,K 减小
h
C.加入少量NaOH固体,平衡正向移动,溶液pH减小
D.升高温度, 增大
【答案】D
【解析】A.由水解方程式可知, 为铵根离子的水解平衡常数,平衡常数仅为温度的函
数,故温度不变,平衡常数不变,故稀释溶液,平衡正向移动, 不变,A错误;
B.平衡常数仅为温度的函数,故温度不变,平衡常数不变,通入少量HCl气体,平衡逆向移动,K 不变,
h
B错误;
C.加入少量NaOH固体,则溶液中H+浓度减小,导致平衡正向移动,溶液pH增大,C错误;
D.由于盐类水解反应是一个吸热反应,故升高温度,化学平衡正向移动,则c(H+)增大,c( )减小,故
增大,D正确;
故答案为:D。
7.在一定条件下,NaS溶液中存在水解平衡: 。下列说法正确的是
2
A.稀释溶液,水解平衡常数增大 B.升高温度, 减小
C.加入CuSO 固体,HS-浓度减小 D.加入NaOH固体,溶液pH减小
4
【答案】C
【解析】A.水解平衡常数只与温度有关,溶液稀释时温度不变,水解平衡常数就不变,A错误;
B.盐的水解反应是吸热反应,升高温度,水解平衡正向移动,溶液中c(HS-)增大,c(S2-)减小,因此
增大,B错误;C.加入CuSO 固体,Cu2+与溶液中的S2-反应产生CuS沉淀,使溶液中c(S2-)减小,水解平衡逆向移动,最
4
终达到平衡时溶液中HS-浓度减小,C正确;
D.加入NaOH固体,碱电离产生OH-,使溶液中c(OH-)增大,水解平衡逆向移动,但平衡移动的趋势是
微弱的,最终达到盐水解平衡时溶液中的c(OH-)增大,溶液的pH增大,D错误;
故合理选项是C。
题组五 三大守恒及离子浓度大小比较
1.下列关于0.1mol/LNaHCO 溶液中微粒浓度的关系式正确的是( )
3
A.c(CO )>c(HCO)
2 3
B.c(Na+)>c(HCO )>c(OH-)>c(H+)
C.c(Na+)=2[c(H CO)+c(HCO )+c(CO )]
2 3
D.c(Na+)+c(H+)=c(OH-)+c(HCO )+c(CO )
【答案】B
【解析】A.常温下,NaHCO 是强碱弱酸酸式盐,碳酸氢根离子水解程度大于电离程度,则c(CO )<
3
c(HCO),故A错误;
2 3
B.NaHCO 是强碱弱酸酸式盐,碳酸氢根离子水解程度大于电离程度,溶液呈碱性,则c(OH-)>c(H+),根
3
据电荷守恒可知:c(Na+)>c(HCO -),则溶液中离子浓度大小为:c(Na+)>c(HCO -)>c(OH-)>c(H+),故B
3 3
正确;
C.溶液中存在物料守恒,根据物料守恒得:c(CO )+c(HCO-)+c(H CO)=c(Na+),故C错误;
3 2 3
D.溶液呈存在电荷守恒,根据电荷守恒得:c(Na+)+c(H+)=2c(CO )+c(HCO-)+c(OH-),故D错误;
3
故选B。
2.(2022·辽宁·新民市第一高级中学高二期末)常温下,下列有关电解质溶液中相关微粒的物质的量浓度
关系不正确的是
A.0.1mol·L-1CHCOONa溶液中:c(CHCOO-)<c(Na+)
3 3
B.0.1mol·L-1NH Cl溶液中:c( )+c(H+)=c(Cl-)+c(OH-)
4C.0.1mol·L-1NaClO溶液:c(Na+)=c(ClO-)+c(HClO)
D.浓度均为0.1mol·L-1NH Cl、NH HSO 溶液中,c( )的大小顺序: NH Cl>NH HSO
4 4 4 4 4 4
【答案】D
【解析】A.CHCOONa为强碱弱酸盐,在溶液中CHCOO-发生水解,从而使其浓度减小,所以:
3 3
c(CHCOO-)<c(Na+),A正确;
3
B.0.1mol·L-1NH Cl溶液中含有c( )、c(H+)、c(Cl-)、c(OH-)等离子,溶液中存在电荷守恒:c( )
4
+c(H+)=c(Cl-)+c(OH-),B正确;
C.0.1mol·L-1NaClO溶液中,ClO-水解生成HClO和OH-,溶液中存在物料守恒:c(Na+)=c(ClO-)
+c(HClO),C正确;
D.等浓度NH Cl、NH HSO 溶液中,NH Cl中发生 水解,从而使c( )减小,而NH HSO 中,虽
4 4 4 4 4 4
然 也发生水解,但水解受硫酸氢根电离产生H+的抑制,所以c( )的大小顺序:NH Cl<
4
NH HSO ,D不正确;
4 4
故选D。
3.(2022·辽宁·渤海大学附属高级中学高二阶段练习)已知NaHB在水溶液中存在关系式:c(Na+)=c(HB-)
+c(B2-),下列说法中正确的是
A.HB的电离方程式为:①HB H++HB-,②HB- H++B2-
2 2
B.NaHB溶液中的离子浓度c(N⇌a+)>c(HB-)>c(H+)>⇌c(OH-)
C.NaHB水溶液呈碱性
D.c(Na+)+c(H+)=c(HB-)+c(B2-)+c(OH-)
【答案】B
【解析】A.由分析可知,HB的电离方程式为:①HB=H++HB-,②HB- H++B2-,故A错误;
2 2
B.NaHB为盐溶液且HB-只电离不水解,则溶液中氢离子浓度大于氢氧根⇌离子浓度;溶液中的离子浓度
c(Na+)>c(HB-)>c(H+)>c(OH-),故B正确;
C.由B分析可知,NaHB水溶液呈酸性,故C错误;
D.由电荷守恒可知,c(Na+)+c(H+)=c(HB-)+2c(B2-)+c(OH-),故D错误;
故选B。
4.(2021·广东·深圳实验学校高二阶段练习)下列各项关系中正确的是A.已知NaHSO 溶液显酸性,则溶液中c( )①>③
4 4 2 4 4 4 4
【答案】C
【解析】A. 既能发生电离: ,也能发生水解: ,已
知NaHSO 溶液显酸性,说明电离大于水解,则溶液中c( )>c(H SO ),故A错误;
3 2 3
B.0.2mol·L-1CHCOOH溶液与0.1mol·L-1NaOH溶液等体积混合,溶质为等浓度的CHCOOH和
3 3
CHCOONa,依据溶液液中电荷守恒和物料守恒得出:2c(H+)-2c(OH-)=c(CH COO-)-c(CHCOOH),故B错
3 3 3
误;
C.常温下pH=2的稀硫酸中c(H+)=0.01mol/L,一水合氨为弱碱,所以pH=12的氨水浓度远大于
0.01mol/L,二者等体积混合,碱过量,溶液呈碱性,故C正确;
D.氯离子、硫酸根对铵根离子的水解没有影响,但硫酸铵可以电离生成2个铵根离子,硫酸氢根会电离
出氢离子抑制铵根离子的水解,所以三种溶液c( )大小关系为②>③>①,故D错误;
答案选C。
5.(2022·浙江·高二期末)室温下,取20mL0.1mol·L-1某二元酸HA,滴加0.2mol·L-1NaOH溶液。已知:
2
HA=H++HA-,HA- H++A2-。下列说法不正确的是
2
A.0.1mol·L-1HA溶液中有c(H+)-c(OH-)-c(A2-)=0.1mol·L-1
2
B.当用去NaOH溶液体积10mL时,溶液的pH<7,此时溶液中有c(A2-)=c(H+)-c(OH-)
C.当滴加至中性时,溶液中c(Na+)=c(HA-)+2c(A2-),用去NaOH溶液的体积小于10mL
D.当用去NaOH溶液体积20mL时,此时溶液中有c(Na+)=2c(HA-)+2c(A2-)
【答案】C
【解析】A.HA第一步电离能完全电离,则HA-的浓度为0.1mol/L,HA- H++A2-,因此c(A2-)
2
+c(HA-)=0.1mol/L,根据电荷守恒,c(H+)=c(OH-)+2c(A2-)+c(HA-),则c(H+)-c(OH-)-c(A2-)=0.1mol/L,A正确;
B.当用去NaOH溶液体积为10mL,则此时溶剂全为NaHA,因HA- H++A2-,溶液pH<7,溶液中氢离
子分为HA-电离出的氢离子和水电离出的氢离子,其中水电离出的氢离子浓度等于氢氧根离子浓度,则c(H+)-c(OH-)=HA-电离出的氢离子浓度,则c(A2-)= c(H+)-c(OH-),B正确;
C.滴加至中性,氢离子浓度和氢氧根离子浓度相同,根据电荷守恒,c(Na+)=c(HA-)+2c(A2-),如用去
NaOH溶液体积小于10mL,则溶液为NaHA和HA的混合液,此时溶液呈酸性,故用去NaOH溶液的体
2
积一定大于10mL,C错误;
D.当用去NaOH溶液体积为20mL时,此时溶液中溶质为NaA,A2-水解生成HA-,根据物料守恒,可得
2
c(Na+)=2c(HA-)+2c(A2-),D正确;
故答案选C。
6.某二元弱酸的酸式盐NaHA溶液,若pH<7,则溶液中各离子浓度的关系不正确的是
A.c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
B.c(Na+)+c(H+)=c(HA-)+2c(A2-)+c(OH-)
C.c(H+)+c(A2-)=c(OH-)+c(H A)
2
D.c(Na+)=c(HA-)+c(H A)+2c(A2-)
2
【答案】D
【解析】A.因为电离和水解都较弱,所以溶液中离子浓度大小关系为:c(Na+)>c(HA-)>c(H+)>c(A2
-)>c(OH-)。A项正确;
B.根据电荷守恒有:c(H+)+c(Na+)=c(OH-)+2c(A2-)+c(HA-),B项正确;
C.根据电荷守恒有:c(H+)+c(Na+)=c(OH-)+2c(A2-)+c(HA-),根据物料守恒有:c(Na+)=c(HA-)+c(A2-)
+c(H A)。消去两式中c(Na+)项,得c(H+)+c(H A)=c(OH-)+c(A2-)。C项正确;
2 2
D.根据物料守恒有:c(Na+)=c(HA-)+c(A2-)+c(H A)。D项错误;
2
答案选D。
7.将20 mL 0.4 mol·L–1硝酸铵溶液跟50 mL 0.1 mol·L–1氢氧化钡溶液混合,则混合溶液中各离子浓度的大
小顺序是
A.[NO ]>[OH-]>[NH ]>[Ba2+] B.[NO ]>[Ba2+]>[OH-]>[NH ]
C.[Ba2+]>[NO ]>[OH-]>[NH ] D.[NO ]>[Ba2+]>[NH ]>[OH-]
【答案】B
【解析】20mL0.4mol/L硝酸铵溶液中硝酸铵的物质的量为20mL×10-3L×0.4mol/L=0.008mol,50mL0.1mol/L
氢氧化钡溶液中氢氧化钡的物质的量为50mL×10-3L×0.1mol/L=0.005mol,硝酸铵和氢氧化钡混合以后发生
反应:2NH NO +Ba(OH) =Ba(NO)+2NH•H O,则反应后,70mL溶液的组成为:剩余氢氧化钡
4 3 2 3 2 3 2
0.001mol,生成的硝酸钡0.004mol,生成的一水合氨0.008mol,在体积一样的前提下,物质的量越大,浓度越大,故[ ]>[Ba2+],而氨水能电离出少量且相等的铵根和氢氧根,氢氧化钡中还有0.002mol的氢氧
根,所以[OH-]>[ ],故离子浓度大小顺序为:[ ]>[Ba2+]>[OH-]>[ ],故答案选B。
8.将0.2mol• L-1Ba (OH) 溶液与0.05mol• L-1NaHSO 溶液等体积混合后,下列几种离子浓度大小顺序正确
2 4
的是
A.c(Ba2+ )>c(OH- )>c(Na+ )>c(SO )
B.c(Na+ )>c(OH- )>c(Ba2+ )>c(SO )
C.c(Na+ )>c(Ba2+ )>c(OH- )>c(SO )
D.c(OH- )>c(Ba2+ )>c(Na+ )>c(SO )
【答案】D
【解析】0.2mol•L-1 溶液与0.05mol•L-1NaHSO 溶液等体积混合后, 过量,所以 与
4
NaHSO 反应后所得溶液中c(Ba2+)=0.075mol•L-1 ,c(OH-)=0.175mol•L-1,c(Na+)=0.025mol•L-1,c(
4
)几乎为零,则 c(OH- )>c(Ba2+ )>c(Na+ )>c( ),故答案选D。
9.将0.2mol/L的Ba(OH) 溶液与0.05mol/L NaHSO 溶液等体积混合后,下列几种离子浓度大小顺序正确
2 4
的是
A.c(Ba2+)>c(OH-)>c(Na+)>c( ) B.c(OH-)>c(Na+)>c(Ba2+)>c( )
C.c(Na+)>c(Ba2+)>c(OH-)>c( ) D.c(OH-)>c(Ba2+)>c(Na+)>c( )
【答案】D
【解析】将0.2mol/L的Ba(OH) 溶液与0.05mol/L NaHSO 溶液等体积混合后,假设反应前溶液体积均是
2 4
1L,反应中氢氧化钡过量,生成0.05mol硫酸钡沉淀、0.05mol水,反应后溶液中钡离子的物质的量是
0.2mol-0.05mol=0.15mol,氢氧根的物质的量是0.2mol×2-0.05mol=0.35mol,钠离子的物质的量是
0.05mol,由于硫酸钡难溶,则离子浓度大小顺序为c(OH-)>c(Ba2+)>c(Na+)>c( ),答案选D。
10.向10mL 0.1mol/L NH Al(SO ) 溶液中,滴加等浓度Ba(OH) 溶液x mL,下列叙述正确的是
4 4 2 2A.x=10时,溶液中有 、Al3+、 , 且c( )>c(Al3+)
B.x=10时, 溶液中有 、 、 , 且c( )>c( )
C.x=30时, 溶液中有Ba2+、 、 OH-,且c(OH- ) c(Al3+),故A正确;
B.x=10时,10mL0.1molL−1Ba(OH) 溶液中有0.001molBa2+,0.002molOH−,混合后生成0.001mol硫酸钡沉
2
⋅
淀,剩余0.001mol SO 。生成 ×10−3mol氢氧化铝沉淀,剩余 ×10−3molAl3+,没有 生成,故B错误;
C.x=30时,混合后生成0.002mol硫酸钡沉淀,剩余0.001molBa2+,OH−过量,生成0.001molAlO−,能把
2
Al3+和NH 都反应完,还剩余0.001mol OH−,加上一水合氨电离生成铵根离子和氢氧根离子,此时
c(OH- )>c ( ),故C项错误;
D.x=30时,混合后生成0.002mol硫酸钡沉淀,剩余0.001mol Ba2+,OH−过量,则溶液中存在
0.001molAlO−,铵根离子和氢氧根离子反应生成一水合氨,氢氧根离子剩余0.001mol,一水合氨电离生成
2
铵根离子和氢氧根离子,此时c(OH−)>c(Ba2+),故D项错误。
11.向10 mL0.1 mol·L-1NH Al(SO ) 溶液中,滴加等浓度Ba(OH) 溶液x mL。下列叙述正确的是
4 4 2 2
A.x=10时, 溶液中有NH +、AlO-、SO 2-, 且c(NH +)>c(SO 2-)
4 2 4 4 4
B.x=10时, 溶液中有NH +、Al3+、SO 2-, 且c(NH +)>c(Al3+)
4 4 4
C.x=30时, 溶液中有Ba2+、AlO-、OH-, 且c(OH-)c(Al3+),正确;
4
C.当x=30时,0.001 mol的NH Al(SO ) 与0.003 mol Ba(OH) 反应,生成0.002 mol BaSO 、0.001 mol
4 4 2 2 4
NaAlO 、0.001 mol NH •H O,且剩余0.001 mol Ba2+和0.001 mol OH-,由于NH •H O也是一种碱,存在电
2 3 2 3 2
离平衡:NH •H O NH ++ OH-,使得溶液中c(OH-)大于0.001 mol,c(OH-)>c(AlO-),错误;
3 2 4 2
D.由C中分析可知,溶液中含有Ba2+、AlO-、OH-,其中溶液中c(OH-)大于0.001 mol,含有0.001 mol
2
Ba2+,c(OH-)>c(Ba2+),错误。
答案选B。
12.(2022·广东广州·高二期末)用0.lmol/LNaOH溶液滴定20.00 mL 0.1 mol/L醋酸溶液,用酚酞作指示
剂,滴定过程中溶液pH随加入的NaOH溶液体积的变化如下图所示。下列说法不正确的是
A.a点对应的溶液中:c(CHCOO-)>c(Na+)>c(H+)>c(OH-)
3
B.b点 c(Na+)=c(CHCOO-),V=20mL
3 1
C.c点n(CHCOO-)大于b点
3
D.滴定终点时,c(Na+)+c(H+)=c(CHCOO-)+c(OH-)
3
【答案】B
【解析】A.a点时,V(NaOH)=10mL,则反应结束后n(CHCOONa)=n(CHCOOH),此时溶液的pH<7,
3 3
表明对应的溶液中以CHCOOH的电离为主,所以溶液中:c(CHCOO-)>c(Na+)>c(H+)>c(OH-),A正确;
3 3
B.b点时,溶液的pH=7,则溶液中CHCOONa与CHCOOH共存,依据电荷守恒得 c(Na+)
3 3
+c(H+)=c(CHCOO-)+c(OH-),而c(H+)=c(OH-),所以c(Na+)=c(CHCOO-),但此时CHCOOH有剩余,V<
3 3 3 1
20mL,B不正确;
C.c点时,CHCOOH与NaOH完全反应,而b点CHCOOH有剩余,则c点n(CHCOO-)大于b点,C正
3 3 3
确;
D.滴定终点时,溶液为CHCOONa溶液,依据电荷守恒可得,c(Na+)+c(H+)=c(CHCOO-)+c(OH-),D正确;
3 3
故选B。13.(2022·黑龙江·嫩江市第一中学校高二开学考试)室温下,下列混合溶液中,各离子浓度的关系正确
的是
A.pH=12的氨水溶液与pH=2的盐酸溶液等体积混合:c( )>c(Cl—)>c(OH—)>c(H+)
B.浓度均为0.1mol·L-1的硫酸氢铵溶液与氢氧化钠溶液等体积混合:c(Na+)>c( )>c( )>c(H+)>c(OH
—)
C.浓度均为0.1mol·L-1的小苏打溶液与烧碱溶液等体积混合:c(Na+)+c(H+)=2c( )+c(OH—)
D.浓度均为0.1mol·L-1的醋酸溶液与氢氧化钠溶液等体积混合:c(Na+)=c(CHCOO—)> c(OH—)=c(H+)
3
【答案】A
【解析】A.pH=12的氨水溶液与pH=2的盐酸溶液等体积混合后,氨水过量,溶液呈碱性,则溶液中离子
浓度的大小顺序为c( )>c(Cl—)>c(OH—)>c(H+),故A正确;
B.浓度均为0.1mol∙L-1的硫酸氢铵溶液与氢氧化钠溶液等体积混合反应生成等物质的量的硫酸钠和硫酸铵,
溶液中钠离子的物质的量和硫酸根离子的物质的量相等,故B错误;
C.浓度均为0.1mol∙L-1的小苏打溶液与烧碱溶液等体积混合恰好反应生成碳酸钠,溶液中存在的电荷守恒
关系为c(Na+)+c(H+)=2c( )+c(HCO )+c(OH—),故C错误;
D.浓度均为0.1mol•L-1的醋酸溶液与氢氧化钠溶液等体积混合恰好反应生成醋酸钠,醋酸钠在溶液中水解
使溶液呈碱性,溶液中氢氧根离子浓度大于氢离子浓度,故D错误;
故选A。
14.(2021·云南·西盟佤族自治县第一中学高二阶段练习)常温下,在所得下列溶液中,各离子浓度的关
系正确的是
A.浓度均为0.1mol•L-1的醋酸溶液与氢氧化钠溶液等体积混合:c(Na+)=c(CH COO-)>c(OH-)=c(H+)
3
B.pH=12的氨水与pH=2的盐酸等体积混合:c(NH )>c(Cl-)>c(H+)>c(OH-)
C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH COO-)>c(H+)>c(OH-)
3
D.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)=c(NO )
【答案】D
【解析】A.浓度均为0.1mol•L-1的醋酸溶液与氢氧化钠溶液等体积混合,反应后溶质为醋酸钠,醋酸根离子部分水解,溶液呈碱性,则c(Na+)>c(CHCOO-)、c(OH-)>c(H+),正确的离子浓度大小为:
3
c(Na+)>c(CHCOO-)>c(OH-)>c(H+),故A错误;
3
B.pH=12的氨水与pH=2的盐酸等体积混合,由于氨水为弱碱,混合液中氨水过量,溶液呈碱性,则c
(OH-)>c(H+),根据电荷守恒可知c(NH )>c(Cl-),所以溶液中离子浓度大小为:c(NH )>
c(Cl-)>c(OH-)>c(H+),故B错误;
C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液,溶液呈酸性,则c(H+)>c(OH-),溶液中存
在电荷守恒c(H+)+c(Na+)=c(CHCOO-)+c(OH-),则c(Na+)<c(CHCOO-),水电离程度较小,
3 3
则溶液中存在c(CHCOO-)>c(Na+)>c(H+)>c(OH-),故C错误;
3
D.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液,该溶液呈酸性,硝酸钠为强酸强碱盐,加盐酸的
过程中始终存在c(Na+)=c(NO ),故D正确;
故选:D。
题组六 盐类的水解的应用
1.(2022·甘肃武威·高二期末)下列过程或现象与盐类的水解无关的是
A.加热氯化铁溶液的颜色变深
B.CaCO 的饱和溶液pH约为9.3
3
C.0.1mol/LAlCl 溶液中c(Al3+)<0.1mol/L
3
D.NaHCO 做发酵粉时加入柠檬酸后效果更好
3
【答案】D
【解析】A.加热可促进铁离子水解,则颜色加深与水解有关,故A错误;
B.饱和溶液中碳酸根离子水解显碱性,pH约为9.3与水解有关,故B错误;
C. 0.1mol/LAlCl 溶液中c(Al3+)<0.1mol/L是因为Al3+的水解消耗了部分Al3+,与水解有关,故C错误;
3
D.柠檬酸与NaHCO 反应生成二氧化碳气体,与水解无关,故D正确;
3
故答案选D。
2.(2022·全国·高二专题练习)下列各组离子因发生相互促进的水解反应而不能大量共存的是
A.NH Al(SO ) 溶液中:Na+、Mg2+、HCO 、NO
4 4 2
B.pH=1的溶液中:Fe2+、Al3+、NO 、Cl-C.常温下,水电离出的c(H+)=1×10-12mol•L-1的溶液中:Al3+、Ca2+、NO 、Cl-
D.加入铝粉产生氢气的溶液中:Cu2+、NH 、HCO 、Br-
【答案】A
【解析】A.NH Al(SO ) 溶液中,NH +和Al3+水解溶液呈酸性,HCO -水解呈碱性,因发生相互促进的水
4 4 2 4 3
解反应而不能大量共存,故A符合题意;
B.pH=1的溶液中:Fe2+、H+、NO -发生氧化还原反应不能大量共存,故B不符合题意;
3
C.常温下,水电离出的c(H+)=1×10-12mol·L-1的溶液呈酸性或碱性,在酸性条件下Al3+、Ca2+、NO -、Cl
3
-能大量共存,碱性条件会生成氢氧化铝沉淀不能大量共存,故C不符合题意;
D.加入铝粉产生氢气的溶液,呈强酸性或强碱性:Cu2+、NH +在碱性条件下不共存,HCO -在酸性和碱性
4 3
条件下均不能大量共存,与相互促进的水解不能大量共存无关,故D不符合题意;
故选A。
3.(2021·云南省通海县第二中学高二阶段练习)下列关于盐类水解反应的应用说法正确的是
①可以把FeCl 固体直接溶于水制FeCl 溶液
3 3
②用NaHCO 与Al (SO ) 两种溶液作泡沫灭火剂
3 2 4 3
③Mg粉投入到饱和NH Cl溶液中无明显现象
4
④草木灰与铵态氮肥不能混合施用
⑤实验室盛NaCO 溶液的试剂瓶不能用磨口玻璃塞
2 3
⑥热的纯碱溶液去油污效果好
A.①②③④ B.②③④⑤ C.②④⑤⑥ D.①②④⑥
【答案】C
【解析】①FeCl 固体直接溶于水,会发生水解生成氢氧化铁,从而使制得的FeCl 溶液中出现浑浊,①不
3 3
正确;
②NaHCO 与Al (SO ) 两种溶液混合后发生双水解反应,生成氢氧化铝胶体和二氧化碳气体,能够灭火,
3 2 4 3
可以用作泡沫灭火剂,②正确;
③NH Cl溶液中, +H O NH ·H O+H+,生成的H+与Mg粉反应,从而生成H,所以有气泡逸出,
4 2 3 2 2
③不正确;
④草木灰的主要成分为KCO,CO2-+H O HCO -+OH-,生成的OH-与铵态氮肥中的 结合生成一水
2 3 3 2 3
合氨,一水合氨分解生成氨气挥发出去,所以不能混合施用,④正确;⑤NaCO 溶液中发生反应CO2-+H O HCO -+OH-,生成的OH-会腐蚀玻璃,所以盛放NaCO 溶液的试
2 3 3 2 3 2 3
剂瓶不能用磨口玻璃塞,⑤正确;
⑥热的纯碱溶液中CO2-+H O HCO -+OH-平衡正向移动,OH-增大,对油污的水解起促进作用,所以去
3 2 3
油污效果好,⑥正确;
从而得出②④⑤⑥正确,故选C。
4.下列事实与盐类的水解无关的是
A.用明矾净水
B.用稀盐酸清除铁锈
C.用热的纯碱溶液清洗油污
D.配制FeCl 溶液时,先将氯化铁固体溶于浓盐酸中,再稀释至所需浓度
3
【答案】B
【解析】A.将明矾净水,发生反应Al3++3H O Al(OH) +3H+,生成的Al(OH) 胶体能吸附水中的悬浮颗
2 3 3
粒物,并发生沉降,从而达到净水目的,A不符合题意;
B.铁锈的主要成分为氧化铁,用稀盐酸清除铁锈时,发生反应Fe O+6HCl=2FeCl +3H O,与水解反应无
2 3 3 2
关,B符合题意;
C.热的纯碱溶液中存在下列反应:CO +H O HCO +OH-,生成的OH-能促进油污的水解,从而达到
2
清洗油污的目的,C不符合题意;
D.配制FeCl 溶液时,为抑制FeCl 水解,先将氯化铁固体溶于浓盐酸中,再稀释至所需浓度,D不符合
3 3
题意;
故选B。
5.(2021·山东济宁·高二期中)化学与生活生产密切相关,下列事实与盐类水解无关的是
A.古代用草木灰的水溶液来洗涤衣物
B.“管道通”中含有铝粉和苛性钠,用于疏通下水道
C.氯化铵溶液可做金属焊接中的除锈剂
D.向 中加入水,加热蒸干,最后焙烧固体得到
【答案】B
【解析】A.草木灰的主要成分是碳酸钾,碳酸钾水解使溶液显碱性,油污在碱性条件下易被除去,与盐
类水解有关,A错误;
B.铝与氢氧化钠溶液反应生成氢气,增大管道内气压用于疏通下水道,与盐类水解无关,B正确;
C.铵根离子水解,有H+生成,使溶液显酸性,H+与铁锈反应,能起到除锈的作用,与盐类水解有关,C错误;
D.在加热的条件下,TiCl 水解得TiO xHO和HCl,最后焙烧得到TiO,与盐类水解有关,D错误;
4 2 2 2
故选B。 ⋅
6.(2022·青海西宁·高二期末)下列事实或操作与盐类水解无关的是
A.配制FeCl 溶液时,要滴加少量的盐酸
3
B.加热蒸干并灼烧NaSO 溶液,得到NaSO 固体
2 3 2 4
C.焊接时用NH Cl溶液除锈
4
D.浓的硫化钠溶液有臭味
【答案】B
【解析】A.配制FeCl 溶液时,滴加少量的盐酸是为了抑制Fe3+的水解;
3
B.加热蒸干并灼烧Na SO 溶液,得到NaSO 固体,是因为NaSO 被空气中的氧气氧化,与水解无关;
2 3 2 4 2 3
C.焊接时用NH Cl溶液除锈,是因为NH +水解使溶液呈酸性;
4 4
D.浓的硫化钠溶液有臭味,是因为S2-水解生成HS;
2
故答案选B。
题组七 盐类水解的综合运用
1.在25℃条件下,将 的 溶液加水稀释过程中,下列说法正确的是
A.能使 的水解常数 增大 B.溶液中 不变
C.能使溶液中 增大 D.此过程中,溶液中所有离子浓度均减小
【答案】B
【解析】A.水解常数 只受温度影响,不会改变,错误;
B.溶液中 = 不变,正确;
C.加水稀释过程中,铵根离子水解程度变大,导致溶液中 减小,错误;
D.此过程中, = 不变,稀释过程中溶液氢离子浓度减小,则氢氧根离子浓度变大,错误。
故选B。
2.常温下向20mL0.1mol•L-1CHCOOH溶液中逐滴加入0.1mol•L-1NaOH溶液,其pH变化曲线如图所示(忽
3
略温度变化)。下列说法中错误的是A.a点表示的溶液中c(CHCOO-)略小于10-3mol∙L-1
3
B.b、d点表示的溶液 的值b=d
C.c点表示CHCOOH和NaOH恰好反应完全
3
D.b点表示的溶液中c(CHCOO−)>c(Na+)>c(H+)>c(OH-)
3
【答案】C
【解析】A.a点表示的溶液中,依据质子守恒c(CHCOO-)+c(OH-)=c(H+)=10-3mol∙L-1,则c(CHCOO-)略小
3 3
于10-3mol∙L-1,A正确;
B.K (CHCOOH)= ,b、d点溶液的温度相同,K (CHCOOH)相同,则
a 3 a 3
表示的溶液的值b=d,B正确;
C.若CHCOOH和NaOH恰好反应完全,则生成CHCOONa溶液呈碱性,而c点表示溶液的pH=7,则应
3 3
为CHCOOH有剩余,C错误;
3
D.b点溶液pH<7,溶液中的溶质为CHCOOH和CHCOONa,且以CHCOOH的电离为主,所以溶液中
3 3 3
c(CHCOO−)>c(Na+)>c(H+)>c(OH-),D正确;
3
故选C。
3.(2022·江西省余干第一中学高二开学考试)按要求完成下列问题。
(1)25°C时,pH试纸测得0.1 mol/L醋酸溶液的pH约为3,则估算出醋酸的电离常数约为___________;
向10 mL此溶液中加水稀释的 值将___________(填“增大”、“减小”或“无法确定”)
(2)常温下,已知HA为二元弱酸,溶液M由20 mLl mol·L-1NaHA溶液与20 mL 1mol·L-1NaOH溶液等体积
2
混合而得,则溶液M的pH___________7(填“>”“<”或“=”), 溶液M中各微粒的浓度关系正确的是___________。
A.c(A2-)+c(HA-)+c(OH-)=c(Na+ )+c(H+)
B.c(HA-)+c(H A)+c(H+)=c(OH-)
2
C.c(A2-)+c(HA-)+c(H A)=lmol·L-l
2
D.c(Na+)> c(A2-)> c(OH-)>c(H+)
【答案】(1) 10-5 增大
(2) > D
【解析】(1)25℃时,pH试纸测得0.1 mol/L醋酸溶液的pH约为3,则c(H+)=10-3 mol/L,所以醋酸的电
离常数K= ;
向10 mL该溶液中加水稀释,溶液中c(H+)、c(CHCOOH)都减小,电离平衡正向移动,导致c(H+)有所增加,
3
而c(CHCOOH)进一步减小,即c(CHCOOH)减小的倍数大于c(H+),故稀释后溶液中 增大;
3 3
(2)常温下,已知HA为二元弱酸,溶液M由20 mL1 mol·L-1NaHA溶液与20 mL1 mol·L-1NaOH溶液等
2
体积混合而得,二者恰好反应产生NaA,该盐是强碱弱酸盐,A2-水解消耗水电离产生的H+,使水的电离
2
平衡正向移动,最终达到平衡时溶液中c(OH-)>c(H+),溶液显碱性,故所得溶液M的pH>7;
A.根据电荷守恒可得:2c(A2-)+c(HA-)+c(OH-)=c(Na+)+c(H+),A错误;
B.根据质子守恒可得:c(HA-)+2c(H A)+c(H+)=c(OH-),B错误;
2
C.混合后体积为原来两倍,根据元素守恒可得c(A2-)+c(HA-)+c(H A)=0.5 mol·L-1,C错误;
2
D.M溶液为NaA,根据盐的组成可知c(Na+)>c(A2-);A2-发生水解反应,消耗水电离产生的H+,使水的
2
电离平衡正向移动,最终达到平衡时溶液中c(OH-)>c(H+),但盐的水解程度是微弱的,主要以盐电离产生
的离子存在,盐电离产生的离子浓度c(A2-)远大于水解产生的c(OH-),故该溶液中离子浓度大小关系为:
c(Na+)>c(A2-)>c(OH-)>c(H+),D正确;
故选D。
3. I.84消毒液在生活中有广泛的应用,其主要成分是NaCl和NaClO。
资料:HClO的电离常数为K=4.7×10-8;HCO 的电离常数为K =4.3×10-7,K =5.6×10-11;HClO的氧化性
a 2 3 a1 a2
和杀菌消毒效果强于ClO-。
84消毒液和医用酒精都是重要的消毒剂。某实验小组同学围绕“84消毒液能否与医用酒精混合使用”这一
问题进行了如下实验。序
实验操作 实验现象
号
分别取40 mL 84消毒液和医用酒精混合均 溶液温度由20℃升高至23℃,并产生大量气泡,略有
Ⅰ
匀,并测量溶液温度变化 刺激性气味,溶液颜色无明显变化
分别取40 mL医用酒精和蒸馏水混合均
Ⅱ 溶液中无明显现象
匀,水浴加热至23℃
分别取_______mL 84消毒液和蒸馏水混合
Ⅲ 溶液中无明显现象,略有刺激性气味
均匀,水浴加热至23℃
(1)84消毒液溶液呈_______(填“酸性”或“碱性”)。
(2)实验Ⅲ中应分别取_______mL 84消毒液和蒸馏水混合均匀。
(3)由实验现象推断,84消毒液和医用酒精_______(填“能”或“不能”)混合使用。
(4)84消毒液可由氯气与NaOH溶液反应制得。为了防止消毒液在存储过程中失效,通常要在84消毒液中
残余一定量的NaOH,请运用平衡移动原理解释NaOH的作用:( 用离子方程式表示并配以必要的文字说
明) _______。
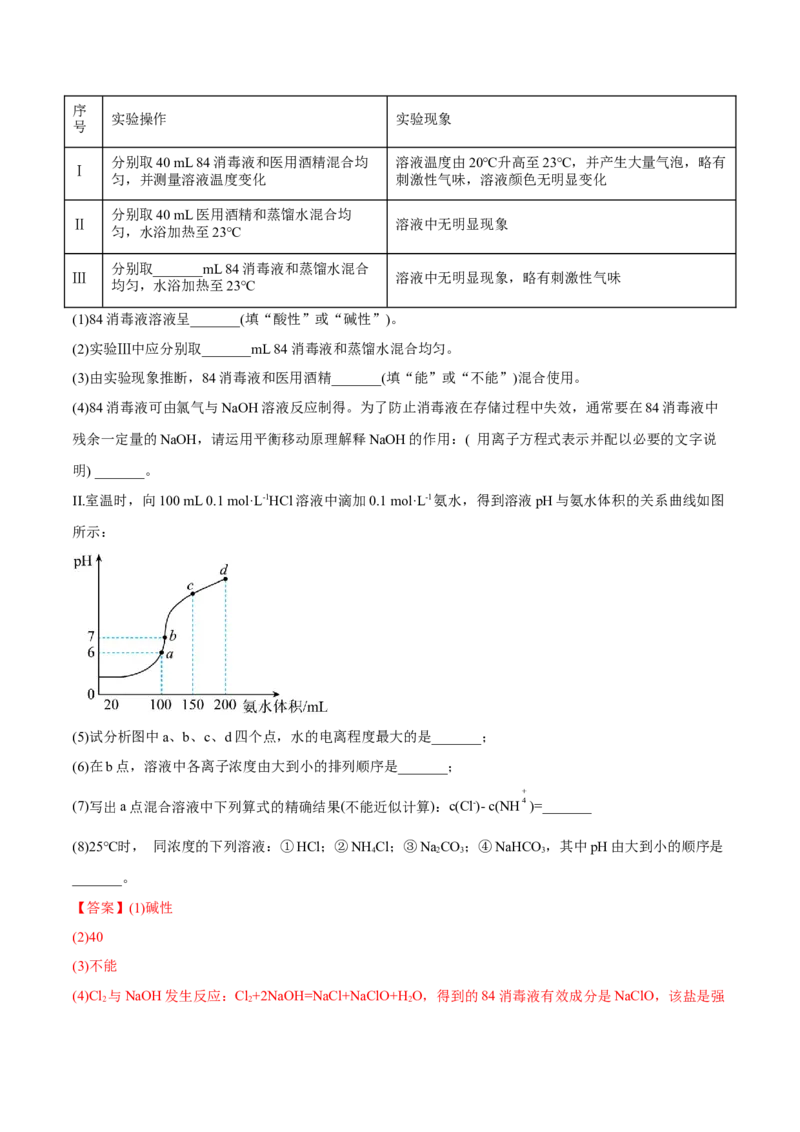
II.室温时,向100 mL 0.1 mol·L-1HCl溶液中滴加0.1 mol·L-1氨水,得到溶液pH与氨水体积的关系曲线如图
所示:
(5)试分析图中a、b、c、d四个点,水的电离程度最大的是_______;
(6)在b点,溶液中各离子浓度由大到小的排列顺序是_______;
(7)写出a点混合溶液中下列算式的精确结果(不能近似计算):c(Cl-)- c(NH )=_______
(8)25℃时, 同浓度的下列溶液:①HCl;②NH Cl;③NaCO;④NaHCO ,其中pH由大到小的顺序是
4 2 3 3
_______。
【答案】(1)碱性
(2)40
(3)不能
(4)Cl 与NaOH发生反应:Cl+2NaOH=NaCl+NaClO+H O,得到的84消毒液有效成分是NaClO,该盐是强
2 2 2碱弱酸盐,在溶液中发生水解反应:ClO−+H O OH−+HClO,消耗水电离产生的H+,使水的电离平衡
2
正向移动,最终达到平衡时,溶液中c(OH-)>c(H+),溶液显碱性。向其中加入NaOH使c(OH−)增大,平衡
逆向移动,使c(HClO)减小,HClO分解速率减慢,因此消毒液更稳定,所以为了防止消毒液在存储过程中
失效,通常要在84消毒液中残余一定量的NaOH;
(5)a
(6)c( )=c(Cl-)> c(H+)=c(OH-)
(7)(10-6-10-8)mol/L
(8)③④②①
【解析】(1)“84消毒液”(主要成分为NaClO),次氯酸钠为强碱弱酸盐,次氯酸根离子水解,溶液
显碱性;
(2)采用控制变量法进行研究,因此实验III要取40 mL84消毒液和蒸馏水混合均匀,水浴加热至23℃,
然后根据实验现象的不同与上面的两个实验进行对比;答案为40;
(3)由实验现象推断,84消毒液和医用酒精混合,会发生化学反应,故不能混合使用;答案为不能;
(4)Cl 与NaOH发生反应:Cl+2NaOH=NaCl+NaClO+H O,得到的84消毒液有效成分是NaClO,该盐
2 2 2
是强碱弱酸盐,在溶液中发生水解反应:ClO−+H O OH−+HClO,消耗水电离产生的H+,使水的电离
2
平衡正向移动,最终达到平衡时,溶液中c(OH-)>c(H+),溶液显碱性。向其中加入NaOH使c(OH−)增大,
平衡逆向移动,使c(HClO)减小,HClO分解速率减慢,因此消毒液更稳定,所以为了防止消毒液在存储过
程中失效,通常要在84消毒液中残余一定量的NaOH;
(5)室温时,向100 mL 0.1 mol·L-1HCl溶液中滴加0.1 mol·L-1氨水,根据图中信息可知,图中a、b、c、d
四个点分别为完全中和生成氯化铵,氯化铵为强酸弱碱盐水解促进水的电离、过了a点后碱过量均抑制水
的电离,且氨过量越多抑制程度越大,故水的电离程度最大的是a;
(6)在b点,溶液呈中性c(H+)=c(OH-),盐酸和氨水完全中和后氨水略过量,为氯化铵和一水合氨的混合
溶液,根据电荷守恒有c( )+ c(H+)=c(Cl-)+ c(OH-),故c( )=c(Cl-),各离子浓度由大到小的排列顺序
是c( )=c(Cl-)> c(H+)=c(OH-);
(7)a点混合溶液中pH=6,c(H+)=10-6mol/L,c(OH-)=10-8mol/L,根据电荷守恒有c( )+ c(H+)=c(Cl-)+c(OH-),故c(Cl-)- c(NH )= c(H+)- c(OH-)=10-6mol/L-10-8mol/L=(10-6-10-8)mol/L;
(8)①HCl为强酸,完全电离,pH小于7;②NH Cl溶液中,铵离子水解,溶液显示酸性,pH小于7,
4
但水解是微弱的,pH大于同浓度的盐酸的pH;③NaCO 溶液中,碳酸根离子水解,溶液显示碱性,溶液
2 3
pH>7;④NaHCO ,碳酸氢根离子水解,溶液显示碱性,溶液pH>7,但水解程度小于同浓度的NaCO
3 2 3
溶液,pH小于同浓度的碳酸钠溶液;根据以上分析,可知pH值由大到小的顺序为:③④②①。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育