文档内容
3.3 盐类的水解(精讲)
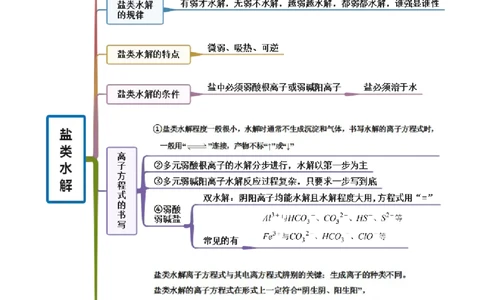
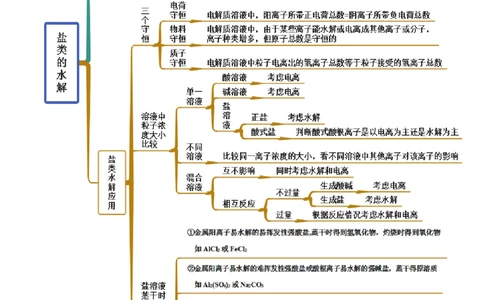
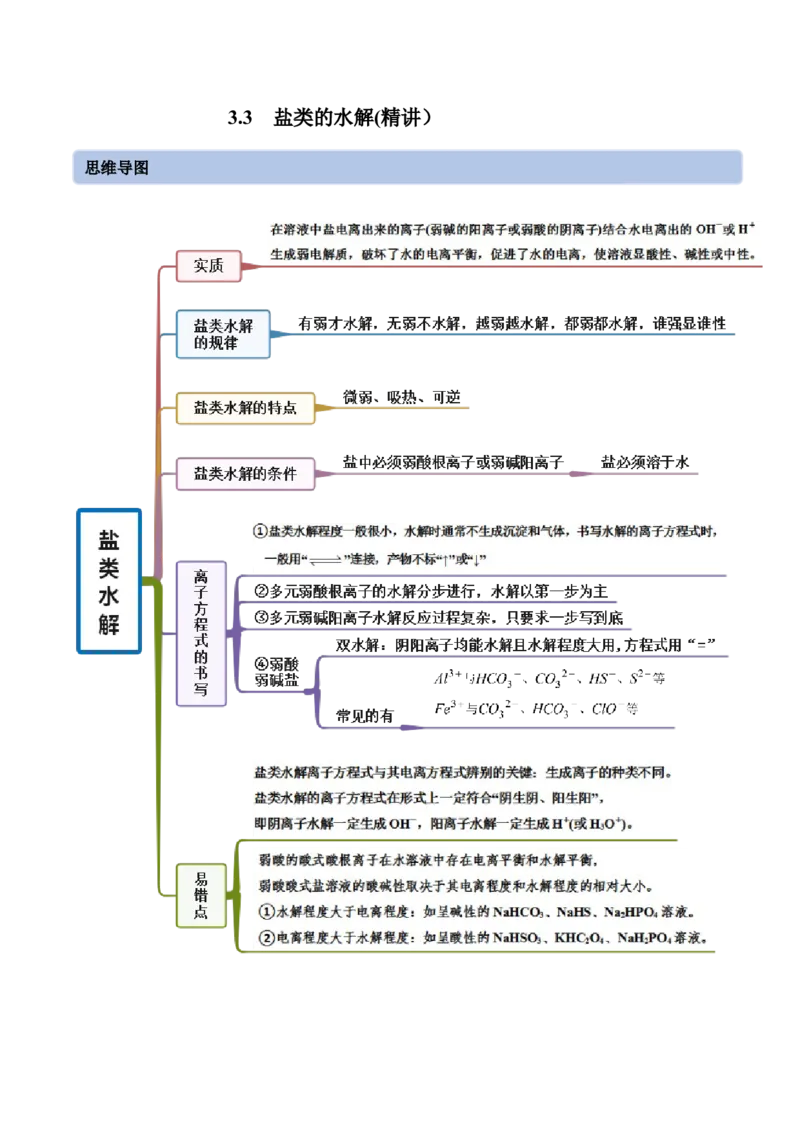
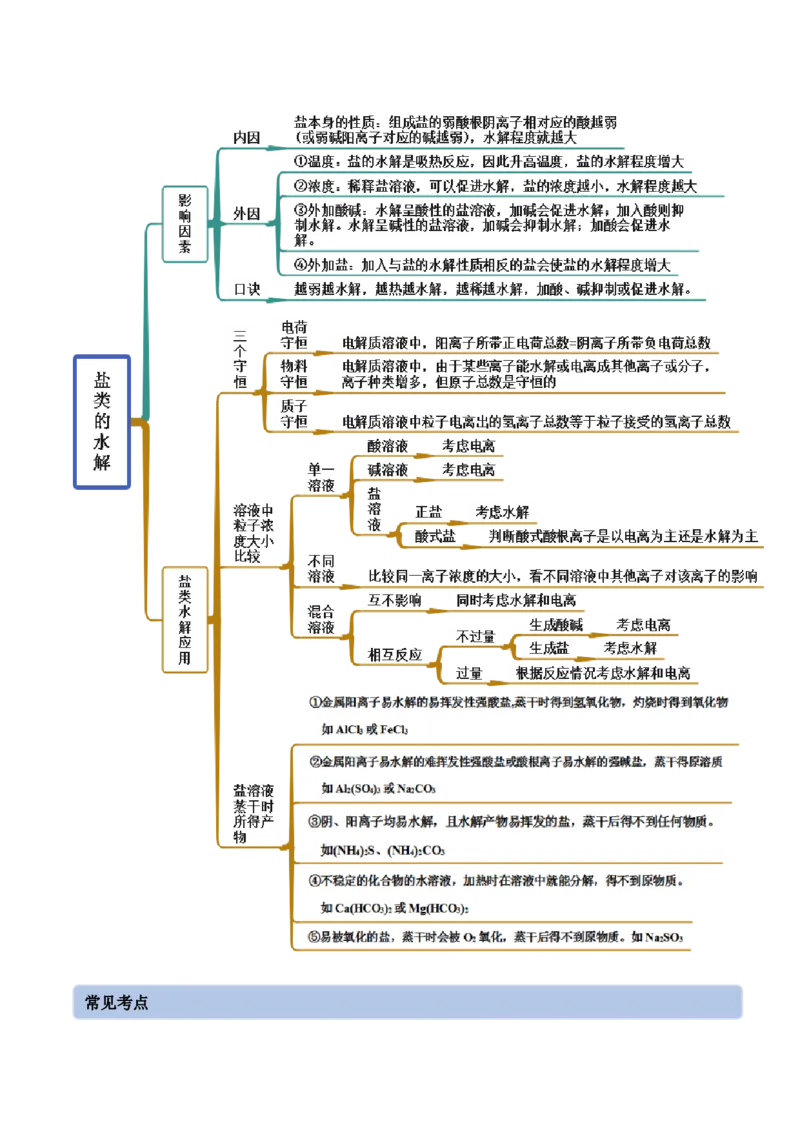
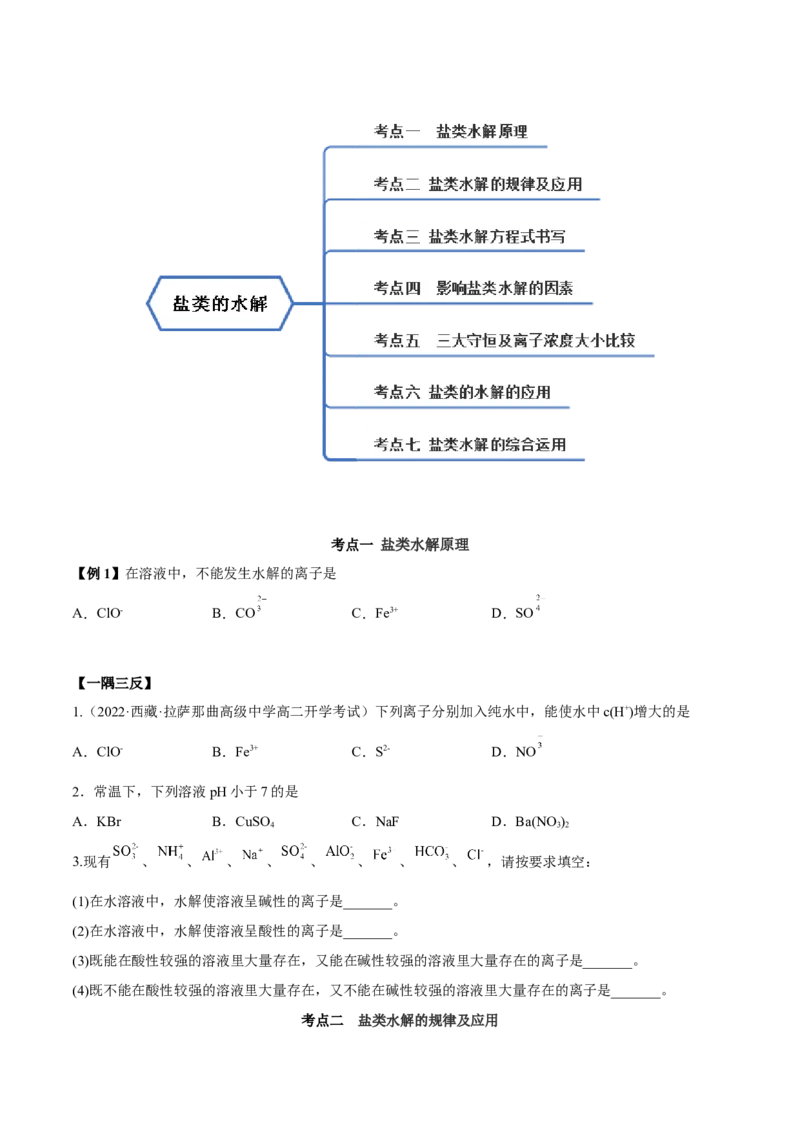
思维导图常见考点考点一 盐类水解原理
【例1】在溶液中,不能发生水解的离子是
A.ClO- B.CO C.Fe3+ D.SO
【一隅三反】
1.(2022·西藏·拉萨那曲高级中学高二开学考试)下列离子分别加入纯水中,能使水中c(H+)增大的是
A.ClO- B.Fe3+ C.S2- D.NO
2.常温下,下列溶液pH小于7的是
A.KBr B.CuSO C.NaF D.Ba(NO )
4 3 2
3.现有 、 、 、 、 、 、 、 、 ,请按要求填空:
(1)在水溶液中,水解使溶液呈碱性的离子是_______。
(2)在水溶液中,水解使溶液呈酸性的离子是_______。
(3)既能在酸性较强的溶液里大量存在,又能在碱性较强的溶液里大量存在的离子是_______。
(4)既不能在酸性较强的溶液里大量存在,又不能在碱性较强的溶液里大量存在的离子是_______。
考点二 盐类水解的规律及应用【例2】pH=4的醋酸和氯化铵溶液中,水的电离程度前者与后者比较为( )
A.大于 B.小于
C.等于 D.无法确定
【一隅三反】
1.下列有关盐类水解的叙述正确的是( )
A.溶液呈中性的盐一定是强酸、强碱反应生成的盐
B.含有弱酸根离子的盐的水溶液一定呈碱性
C.盐溶液的酸碱性主要取决于形成盐的酸和碱的相对强弱
D.强酸强碱盐的水溶液一定呈中性
2.由一价离子组成的四种盐溶液:AC、BD、AD、BC各1 mol·L-1,在室温下,前两种溶液的pH=7,
第三种溶液的pH>7,最后一种溶液的pH<7,则下列说法正确的是( )
A B C D
碱性 AOH>BOH AOH<BOH AOH>BOH AOH<BOH
酸性 HC>HD HC>HD HC<HD HC<HD
3(2022山东)物质的量浓度相同的下列各物质的溶液,由水电离出的c(H+)由大到小的顺序是( )
①NaHSO ②NaHCO ③NaCO ④NaSO
4 3 2 3 2 4
A.④③②① B.①②③④
C.③②④① D.③④②①
考点三 盐类水解方程式书写
【例3-1】(2022·全国·高二专题练习)在一定条件下发生下列反应,其中属于盐类水解反应的是
A.
B.
C.
D.
【例3-2】NH Cl;NaSO ;KHCO ;Fe(NO );KHSO;NaCO;NaAlO ;KClO,以上盐中有些能发生
4 2 4 3 3 3 4 2 3 2 4
水解反应,写出能发生水解反应的盐对应的离子方程式:
(1)________ ___(写离子方程式)
(2)__________ _(写离子方程式)
(3)___________ (写离子方程式)(4)___________ (写离子方程式)
(5)___________ (写离子方程式)
【一隅三反】
1.(2022·甘肃武威·高二期末)下列反应中,属于水解反应且使溶液显酸性的是
A. +H O NH ·H O+H+ B. +H O +H O+
2 3 2 2 3
⇌ ⇌
C.S2-+H O HS-+OH- D.NH +H O +OH-
2 3 2
⇌ ⇌
2.(2022·全国·高二课时练习)在一定条件下发生下列反应,其中属于盐类水解反应的是
A.NH +2H O NH ·H O+HO+ B.HCO +H O HO++CO
2 3 2 3 2 3
C.HS-+H O+ HS+HO D.Cl+H O H++Cl-+HClO
3 2 2 2 2
3.写出下列盐溶液水解反应的离子方程式:
(1)NaF:____ 。
(2)NH NO :____ 。
4 3
(3)CuSO :____ 。
4
(4)NaHCO :____ 。
3
(5)CH COONa:____ 。
3
考点四 影响盐类水解的因素
【例4-1】(2022·全国·高二课时练习)在0.1mol/LFeCl 溶液中存在Fe3++3H O Fe(OH) +3H+的水解平
3 2 3
衡,下列说法中正确的是
A.加FeCl 固体,平衡正向移动,水解程度增大
3
B.稍微加热,促进水解,c(H+)增大,pH减小
C.加NaOH固体,与铁离子反应,平衡逆向移动
D.通入HCl气体,平衡逆向移动,铁离子水解常数减小
【例4-2】(2022·全国·高二课时练习)为使 溶液中 的值减小,可加入的物质是
A.适量的 固体 B.适量的 固体C.通入适量的 气体 D.适量的 固体
【一隅三反】
1.(2022·全国·高二课时练习)室温时,下列操作能使浓度均为0.01mol·L-1的①CHCOOH溶液
3
②CHCOONa溶液中c(CHCOO-)都增大的是
3 3
A.升高温度 B.加水稀释 C.加入少量硫酸 D.加入少量NaOH固体
2.(2022·全国·高二课时练习)0.1mol/L 溶液中,由于 的水解,使得 。如果
要使 更接近于0.1mol/L,可采取的措施是
A.加入少量氢氧化钠 B.加入少量水
C.加入少量盐酸 D.加热
3.(2022·全国·高二课时练习)一定条件下, 溶液中存在平衡: 。下
列说法错误的是
A.加入 固体,溶液 增大 B.通入 ,平衡向正反应方向移动
C.升高温度, 增大 D.加水稀释, 浓度减小,平衡常数变小
考点五 三大守恒及离子浓度大小比较
【例5-1】常温下,等物质的量浓度的下列溶液中 最大的是
A. B. C. D.
【例5-2】有等物质的量浓度的下列四种溶液:a. 、b. 、C. 、d.
,其中 大小关系判断正确的是
A. B.
C. D.
【例5-3】(2022·陕西·富平县蓝光中学高二期末)某酸式盐NaHY的水溶液显碱性,下列叙述正确的是
A.该酸式盐溶液中离子浓度关系:[Na+]>[HY-]>[OH-]>[H+]B.HY-的水解方程式:HY-+HO HO++Y2–
2 3
C.该酸式盐溶液中离子浓度关系:[Na+]>[Y2–] >[HY-]>[OH-]>[H+]
D.HY的电离方程式:HY 2H++Y2–
2 2
【例5-4】(2021·全国·高二课时练习)25 ℃时,下列有关溶液中微粒的物质的量浓度关系正确的是
A.0.1 mol·L-1 CHCOONa溶液与0.1 mol·L-1HCl溶液等体积混合:c(Na+)=c(Cl-)>c(CHCOO-)>c(OH-)
3 3
B.0.1 mol·L-1 NH Cl溶液与0.1 mol·L-1氨水等体积混合(pH>7):c(NH ·H O)>c(NH )>c(Cl-)>c(OH-)
4 3 2
C.0.1 mol·L-1 Na CO 溶液与0.1 mol·L-1 NaHCO 溶液等体积混合: c(Na+)=c(CO )+c(HCO )+
2 3 3
c(HCO)
2 3
D.0.1 mol·L-1 Na C O 溶液与0.1 mol·L-1 HCl溶液等体积混合(H C O 为二元弱酸):2c(C O )+c(HC O )
2 2 4 2 2 4 2 2
+c(OH-)=c(Na+)+c(H+)
【例5-5】25℃时,在20mL0.1mol/LNaOH溶液中逐滴加入0.2mol/L醋酸溶液,pH曲线如图所示,有关粒
子浓度关系的比较中,错误的是
A.A点,c(Na+)>c(OH-)>c(CH COO-)>c(H+)
3
B.B点,c(H+)=c(OH-),c(Na+)=c(CH COO-)
3
C.C点,c(CHCOO-)+c(CH COOH)=2c(Na+)
3 3
D.C点,c(CHCOO-)>c(Na+)>c(H+)>c(OH-)
3
【一隅三反】
1.(2022·全国·高二课时练习)下列五种混合溶液,由分别为 的两种溶液等体积混合而成:
① 与 ② 与
③ 与 ④ 与
⑤ 与 , 由大到小排序正确的是A.①>④>③>②>⑤ B.①>③>⑤>④>②
C.②>④>③>⑤>① D.②>③>④>⑤>①
2.4种混合溶液:分别由等体积0.1mol/L的两溶液混合而成:①NH Cl与CHCOONa ②NH Cl与
4 3 4
HCl ③NH Cl与NaCl ④NH Cl与NH ·H O(混合液呈碱性),下列各项排序正确的是
4 4 3 2
A.c(NH ):①<③<②<④ B.溶液中c(H+):①<③<②<④
C.pH:②<①<④<③ D.c(NH ·H O):①<③<④<②
3 2
3.现有0.1mol/LNa CO 溶液,对溶液中离子浓度关系的描述,不正确的是
2 3
A.c(Na+)+c(H+)=c(OH-)+2c(CO )+c(HCO )
B.c(H+)+c(HCO )+2c(H CO)=c(OH-)
2 3
C.c(Na+)=2[c(H CO)+c(CO )+c(HCO )]
2 3
D.c(Na+)+c(H+)=c(OH-)+2c(CO )+c(HCO )+c(H CO)
2 3
4.下列各溶液中,各粒子的物质的量浓度关系正确的是
A.0.1mol/LNa CO 溶液中:c(Na+) + c(H+) = c(CO 2-) + c(HCO -) + c(OH-)
2 3 3 3
B.0.1mol/L(NH )SO 溶液中:c(SO 2-) > c(NH +) > c(H+) > c(OH-)
4 2 4 4 4
C.0.1mol/LNaHCO 溶液中:c(OH-) = 2c(H CO) + c(HCO -) + c(H+)
3 2 3 3
D.0.1mol/LNa S溶液中:c(Na+) = 2c(S2-) +2c(HS-) + 2c(H S)
2 2
5.室温下,下列溶液中粒子浓度关系正确的是
A.NaS溶液:c(Na+)>c(HS-)>c(OH-)>c(H S)
2 2
B.NaCO 溶液: c(OH-)=c(H+)+c( )+c(H CO)
2 3 2 3
C.NaCO 溶液:c(Na+)+c(H+)=2c( )+c(OH-)
2 3
D.0.1mol/L的NaHCO 溶液中:c(Na+)>c( )>c(OH-)>c(H+)>c( )
3
6.(2022·重庆八中高二阶段练习)下列溶液中各微粒的浓度关系正确的是
A.常温下,将 溶液与 溶液等体积混合溶液显碱性,B.在纯碱溶液中存在:
C.常温下,向 溶液中加入适量的NaOH,得到 的混合溶液:
D. 的一元酸HX和 的一元碱MOH等体积混合:
考点六 盐类的水解的应用
【例6-1】(2021·吉林江城中学高二期中)在蒸发皿中用酒精灯加热蒸干下列物质的溶液然后灼烧,可以
得到该物质固体的是
A.AlCl B.NaSO C.CuSO D.KMnO
3 2 3 4 4
【例6-2】(2021·云南省楚雄天人中学高二阶段练习)下列有关问题与盐类的水解有关的是
①NH Cl与ZnCl 溶液可作焊接金属时的除锈剂
4 2
②NaHCO 与Al (SO ) 两种溶液可作泡沫灭火剂
3 2 4 3
③草木灰与铵态氮肥不能混合施用
④实验室中盛放NaCO 溶液的试剂瓶不能用磨口玻璃塞
2 3
⑤加热蒸干CuCl 溶液得到Cu(OH) 固体
2 2
⑥要除去FeCl 溶液中混有的Fe2+,通入氧化剂Cl
3 2
A.①②③⑥ B.②③④⑥ C.全部 D.①②③④⑤
【一隅三反】
1.(2022·陕西·富平县蓝光中学高二期末)下列表述中,与盐类水解无关的是
A.明矾和FeCl 可作净水剂 B.盛放NaOH溶液的试剂瓶不能用玻璃塞
3
C.热的纯碱溶液去污能力增强 D.NH Cl与ZnCl 溶液可作焊接中的除锈剂
4 2
2.(2022·陕西宝鸡·高二期末)下列表述中,与盐类水解有关的是
①明矾和FeCl 可作净水剂
3
②为保存FeCl 溶液,要在溶液中加少量铁粉
2
③AlCl 溶液蒸干,灼烧,最后得到的主要固体产物是Al O
3 2 3
④NH Cl与ZnCl 溶液可作焊接中的除锈剂
4 2
⑤实验室盛放NaOH溶液的试剂瓶应用橡皮塞,而不能用玻璃塞⑥用NaHCO 与Al (SO ) 两种溶液可作泡沫灭火剂
3 2 4 3
⑦草木灰与铵态氮肥不能混合施用
A.①②③⑤⑥⑦ B.①③④⑥⑦ C.①③⑤⑥⑦ D.全有关
3.(2022·辽宁·沈阳二中高二阶段练习)在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列
关于离子共存说法中正确的是
A.d点对应的溶液中大量存在:Na+、K+、ClO-、Cl-
B.b点对应的溶液中大量存在:Fe2+、Ba2+、K+、
C.c点对应的溶液中大量存在:Na+、Ba2+、Cl-、
D.a点对应的溶液中大量存在: 、Na+、I-、Fe2+
考点七 盐类水解的综合运用
【例7】(2022·江苏·灌南县第二中学高二阶段练习)25℃时,醋酸、次氯酸、碳酸和亚硫酸电离平衡常数
分别为:醋酸K=1.75×10-5;次氯酸K=2.95×10-8;碳酸K=4.30×10-7,K=5.61×10-11;亚硫酸K=1.54×10-2,
1 2 1
K=1.02×10-7。
2
(1)写出碳酸的第一级电离平衡常数表达式K=____。
1
(2)在相同条件下,等浓度的CHCOO-、ClO-、 和 溶液中结合H+能力最强的是_____。
3
(3)已知下面三个数据:6.3×10-4、5.6×10-4、6.2×10-10分别是下列有关的三种酸的电离常数,若已知下列反应
可以发生:NaCN+HNO=HCN+NaNO ;NaNO +HF=HNO +NaF。由此可判断下列叙述不正确的是____。
2 2 2 2
A.K(HF)=6.3×10-4 B.K(HNO)=6.2×10-10
a a 2
C.三种酸的强弱顺序为HF>HNO>HCN D.K(HCN)<K(HNO)<K(HF)
2 a a 2 a
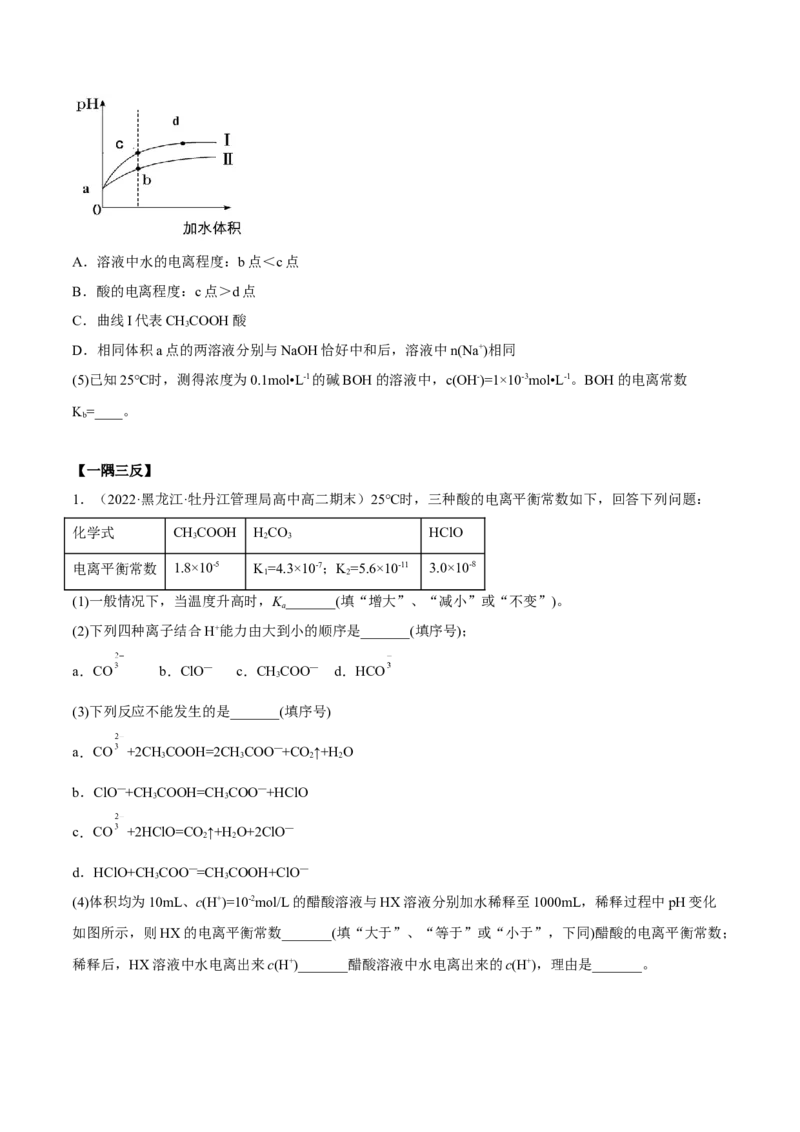
(4)25℃时,将pH和体积均相同的两种酸HCl和CHCOOH溶液分别稀释,其pH随加水体积的变化如图所
3
示,下列说法正确的是____。A.溶液中水的电离程度:b点<c点
B.酸的电离程度:c点>d点
C.曲线I代表CHCOOH酸
3
D.相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同
(5)已知25℃时,测得浓度为0.1mol•L-1的碱BOH的溶液中,c(OH-)=1×10-3mol•L-1。BOH的电离常数
K=____。
b
【一隅三反】
1.(2022·黑龙江·牡丹江管理局高中高二期末)25℃时,三种酸的电离平衡常数如下,回答下列问题:
化学式 CHCOOH HCO HClO
3 2 3
电离平衡常数 1.8×10-5 K=4.3×10-7;K=5.6×10-11 3.0×10-8
1 2
(1)一般情况下,当温度升高时,K _______(填“增大”、“减小”或“不变”)。
a
(2)下列四种离子结合H+能力由大到小的顺序是_______(填序号);
a.CO b.ClO— c.CHCOO— d.HCO
3
(3)下列反应不能发生的是_______(填序号)
a.CO +2CH COOH=2CH COO—+CO ↑+H O
3 3 2 2
b.ClO—+CH COOH=CH COO—+HClO
3 3
c.CO +2HClO=CO ↑+H O+2ClO—
2 2
d.HClO+CH COO—=CH COOH+ClO—
3 3
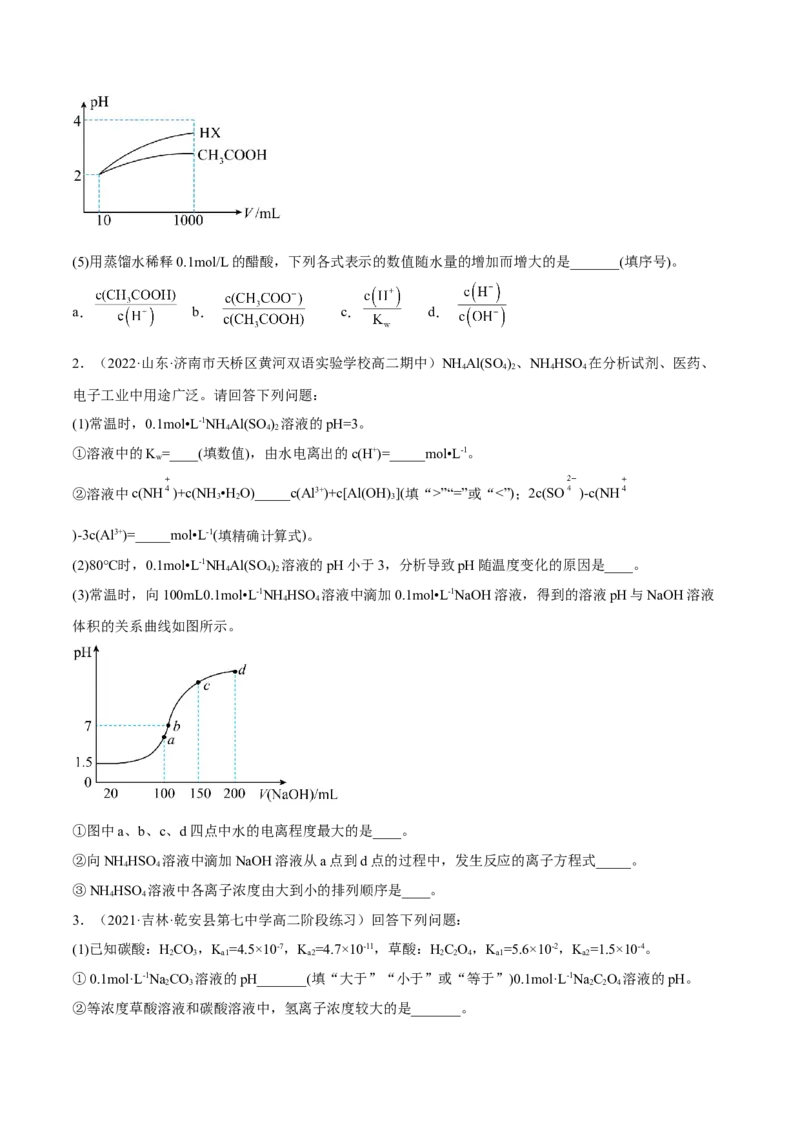
(4)体积均为10mL、c(H+)=10-2mol/L的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化
如图所示,则HX的电离平衡常数_______(填“大于”、“等于”或“小于”,下同)醋酸的电离平衡常数;
稀释后,HX溶液中水电离出来c(H+)_______醋酸溶液中水电离出来的c(H+),理由是_______。(5)用蒸馏水稀释0.1mol/L的醋酸,下列各式表示的数值随水量的增加而增大的是_______(填序号)。
a. b. c. d.
2.(2022·山东·济南市天桥区黄河双语实验学校高二期中)NH Al(SO )、NH HSO 在分析试剂、医药、
4 4 2 4 4
电子工业中用途广泛。请回答下列问题:
(1)常温时,0.1mol•L-1NH Al(SO ) 溶液的pH=3。
4 4 2
①溶液中的K =____(填数值),由水电离出的c(H+)=_____mol•L-1。
w
②溶液中c(NH )+c(NH•H O)_____c(Al3+)+c[Al(OH) ](填“>”“=”或“<”);2c(SO )-c(NH
3 2 3
)-3c(Al3+)=_____mol•L-1(填精确计算式)。
(2)80℃时,0.1mol•L-1NH Al(SO ) 溶液的pH小于3,分析导致pH随温度变化的原因是____。
4 4 2
(3)常温时,向100mL0.1mol•L-1NH HSO 溶液中滴加0.1mol•L-1NaOH溶液,得到的溶液pH与NaOH溶液
4 4
体积的关系曲线如图所示。
①图中a、b、c、d四点中水的电离程度最大的是____。
②向NH HSO 溶液中滴加NaOH溶液从a点到d点的过程中,发生反应的离子方程式_____。
4 4
③NH HSO 溶液中各离子浓度由大到小的排列顺序是____。
4 4
3.(2021·吉林·乾安县第七中学高二阶段练习)回答下列问题:
(1)已知碳酸:HCO,K =4.5×10-7,K =4.7×10-11,草酸:HC O,K =5.6×10-2,K =1.5×10-4。
2 3 a1 a2 2 2 4 a1 a2
①0.1mol·L-1NaCO 溶液的pH_______(填“大于”“小于”或“等于”)0.1mol·L-1NaC O 溶液的pH。
2 3 2 2 4
②等浓度草酸溶液和碳酸溶液中,氢离子浓度较大的是_______。③若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种粒子浓度大小的顺序正确的是_______(填字
母)。
a.c(H+)>c( )>c( )>c( )
b.c( )>c( )>c( )>c( )
c.c(H+)>c( )>c( )>c( )
d.c(H CO)>c( )>c( )>c( )
2 3
(2)SO 会对环境和人体健康带来极大的危害,工业上采取多种方法减少SO 的排放,回答下列方法中的问
2 2
题。
方法1(双碱法):用NaOH溶液吸收SO ,并用CaO使NaOH再生
2
NaOH溶液 NaSO 溶液
2 3
①写出过程ⅰ的离子方程式:_______;
②CaO在水中存在如下转化:CaO(s)+HO(l)=Ca(OH) (s) Ca2+(aq)+2OH-(aq)
2 2
从平衡移动的角度,简述过程ⅱ中NaOH再生的原理:_______。
方法2:用氨水除去SO
2
③已知25℃,NH ·H O的K=1.8×10-5,HSO 的K =1.4×10-2,K =6.0×10-8。若氨水的浓度为2.0mol·L-1,
3 2 b 2 3 a1 a2
溶液中的c(OH-)=_______mol·L-1。将SO 通入该氨水中,当c(OH-)降至1.0×10-7mol·L-1时,溶液中的
2
=_______。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育