文档内容
第三章 烃的衍生物
第三节 醛 酮
本节内容在高中化学所介绍的含氧衍生物(醇、醛、羧酸)中,醛起着承上启下的作用,向前
联系着醇,向后联系着羧酸,它既可引入羟基又可引入羧基,在官能团的转化、化学键的结构变化
和有机合成中占有核心地位,同时通过探究学习也可以让学生学会自主构建化学知识体系的方法。
课程目标 学科素养
1.从官能团和化学键可能的断键部位预 a.宏观辨识与微观探析:从官能团的角度认识有机化
测乙醛的化学性质,并能在结构分析和实
合物的分类,通过对乙醛的认识,明确官能团和醛类
验事实的基础上书写相关反应的化学方程
式,强化“结构决定性质”的观念。 特征性质的特征关系,形成“结构决定性质的”观
2.能够结合分子结构特点,运用类比迁 念。
移的方法预测其他醛类物质的主要性质。
b.证据推理与模型认知:通过实验探究掌握醛基的特
3.能根据官能团的特点和性质区别醛和
征反应和能被弱氧化剂氧化的重要性质,建立醛类认
酮,以丙酮为例认识酮的主要化学性质。
知模型,并能运用认知模型解决实际问题。
c.科学态度和社会责任:通过乙醛的学习,认识醛类
对环境和健康的影响,形成环境保护意识,养成节约
适度、绿色低碳的生活方式。
教学重点:乙醛的化学性质
教学难点:乙醛的化学性质
讲义 教具
【导入新课】
自然界的许多植物中含有醛,其中有些具有特殊的香味,可作为植物香料使用。
【学习任务一】认识醛类物质1. 醛的定义
2. 醛的官能团
3. 饱和一元醛的通式
4. 常见的醛及其物理性质、应用
【讲解】
1. 醛是由烃基(或氢原子)与醛基相连而构成的化合物,简写为RCHO。
2. 醛的官能团:醛基(—CHO)
3. 饱和一元醛的通式为C H O。
n 2n
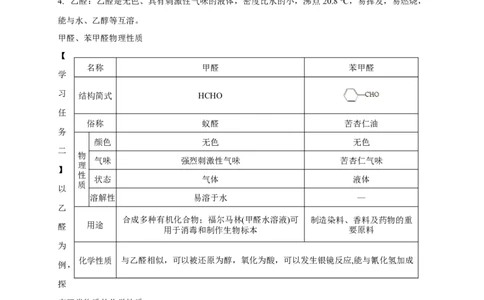
4. 乙醛:乙醛是无色、具有刺激性气味的液体,密度比水的小,沸点 20.8 ℃,易挥发,易燃烧,
能与水、乙醇等互溶。
甲醛、苯甲醛物理性质
【
名称 甲醛 苯甲醛
学
习 结构简式 HCHO
任
俗称 蚁醛 苦杏仁油
务
颜色 无色 无色
二
物
气味 强烈刺激性气味 苦杏仁气味
理
】
性
状态 气体 液体
质
以
溶解性 易溶于水 —
乙
合成多种有机化合物;福尔马林(甲醛水溶液)可 制造染料、香料及药物的重
醛 用途
用于消毒和制作生物标本 要原料
为
化学性质 与乙醛相似,可以被还原为醇,氧化为酸,可以发生银镜反应,能与氰化氢加成
例,
探
究醛类物质的化学性质
[环节一]
书写乙醛的结构简式,搭建其分子的结构模型,分析乙醛的结构特点
【讲解】
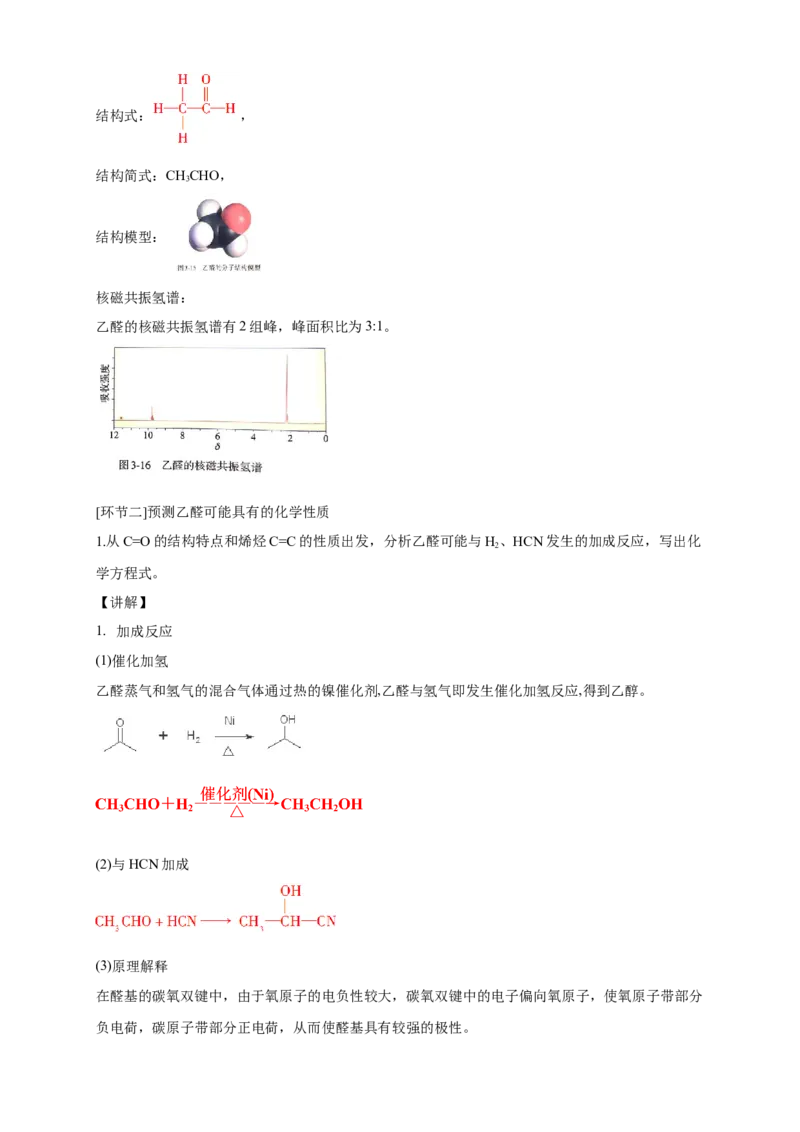
1. 乙醛
分子式:C HO,
2 4结构式: ,
结构简式:CHCHO,
3
结构模型:
核磁共振氢谱:
乙醛的核磁共振氢谱有2组峰,峰面积比为3:1。
[环节二]预测乙醛可能具有的化学性质
1.从C=O的结构特点和烯烃C=C的性质出发,分析乙醛可能与H、HCN发生的加成反应,写出化
2
学方程式。
【讲解】
1. 加成反应
(1)催化加氢
乙醛蒸气和氢气的混合气体通过热的镍催化剂,乙醛与氢气即发生催化加氢反应,得到乙醇。
(2)与HCN加成
(3)原理解释
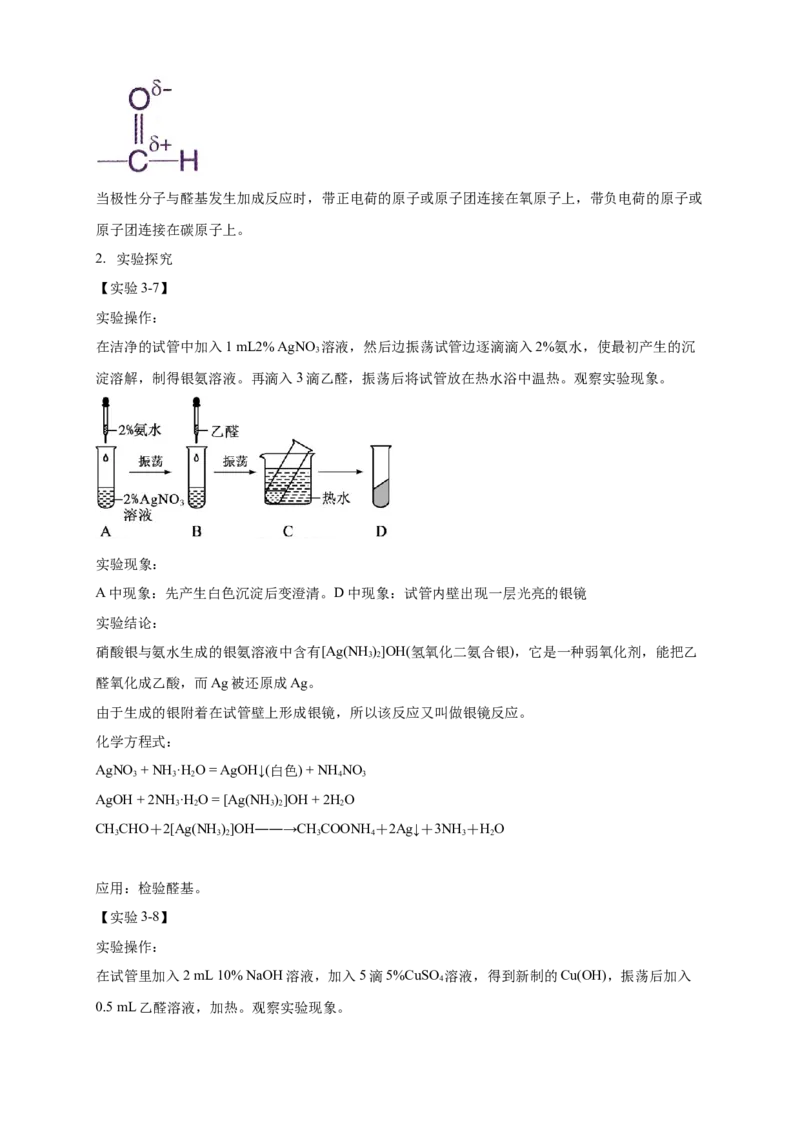
在醛基的碳氧双键中,由于氧原子的电负性较大,碳氧双键中的电子偏向氧原子,使氧原子带部分
负电荷,碳原子带部分正电荷,从而使醛基具有较强的极性。当极性分子与醛基发生加成反应时,带正电荷的原子或原子团连接在氧原子上,带负电荷的原子或
原子团连接在碳原子上。
2. 实验探究
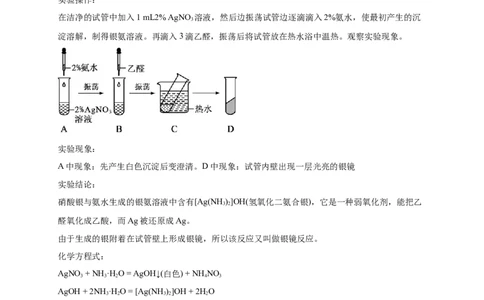
【实验3-7】
实验操作:
在洁净的试管中加入1 mL2% AgNO 溶液,然后边振荡试管边逐滴滴入2%氨水,使最初产生的沉
3
淀溶解,制得银氨溶液。再滴入3滴乙醛,振荡后将试管放在热水浴中温热。观察实验现象。
实验现象:
A中现象:先产生白色沉淀后变澄清。D中现象:试管内壁出现一层光亮的银镜
实验结论:
硝酸银与氨水生成的银氨溶液中含有[Ag(NH)]OH(氢氧化二氨合银),它是一种弱氧化剂,能把乙
3 2
醛氧化成乙酸,而Ag被还原成Ag。
由于生成的银附着在试管壁上形成银镜,所以该反应又叫做银镜反应。
化学方程式:
AgNO + NH ·H O = AgOH↓(白色) + NH NO
3 3 2 4 3
AgOH + 2NH ·H O = [Ag(NH)]OH + 2HO
3 2 3 2 2
CHCHO+2[Ag(NH)]OH――→CHCOONH+2Ag↓+3NH +HO
3 3 2 3 4 3 2
应用:检验醛基。
【实验3-8】
实验操作:
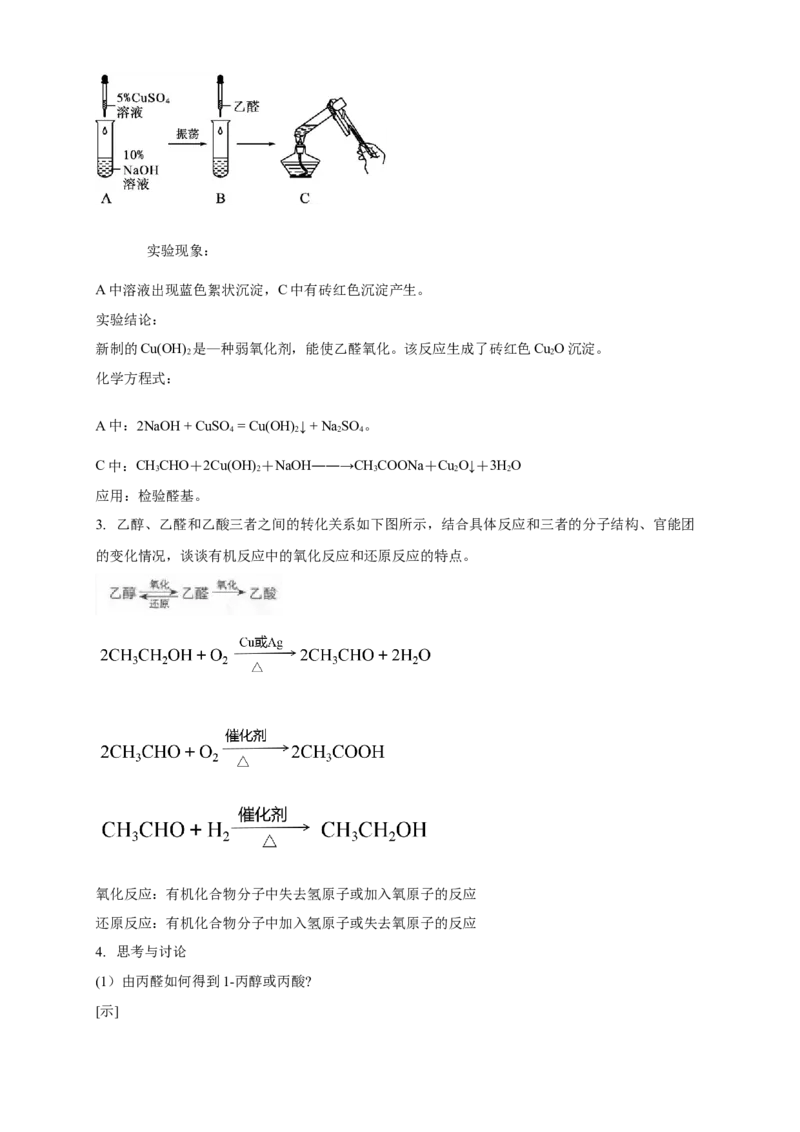
在试管里加入2 mL 10% NaOH溶液,加入5滴5%CuSO 溶液,得到新制的Cu(OH),振荡后加入
4
0.5 mL乙醛溶液,加热。观察实验现象。实验现象:
A中溶液出现蓝色絮状沉淀,C中有砖红色沉淀产生。
实验结论:
新制的Cu(OH) 是—种弱氧化剂,能使乙醛氧化。该反应生成了砖红色Cu O沉淀。
2 2
化学方程式:
A中:2NaOH + CuSO = Cu(OH) ↓ + NaSO 。
4 2 2 4
C中:CHCHO+2Cu(OH) +NaOH――→CHCOONa+Cu O↓+3HO
3 2 3 2 2
应用:检验醛基。
3. 乙醇、乙醛和乙酸三者之间的转化关系如下图所示,结合具体反应和三者的分子结构、官能团
的变化情况,谈谈有机反应中的氧化反应和还原反应的特点。
氧化反应:有机化合物分子中失去氢原子或加入氧原子的反应
还原反应:有机化合物分子中加入氢原子或失去氧原子的反应
4. 思考与讨论
(1)由丙醛如何得到1-丙醇或丙酸?
[示](2)苯甲醛在空气中久置,在客器内壁会出现苯甲酸的结晶,这是为什么?
[提示]苯甲醛在空气中久置被氧化为苯甲酸
(3) 乙醛能不能使酸性高锰酸钾溶液褪色?
[提示]酸性高锰酸钾溶液属于强氧化剂,故乙醛能使酸性高锰酸钾溶液褪色
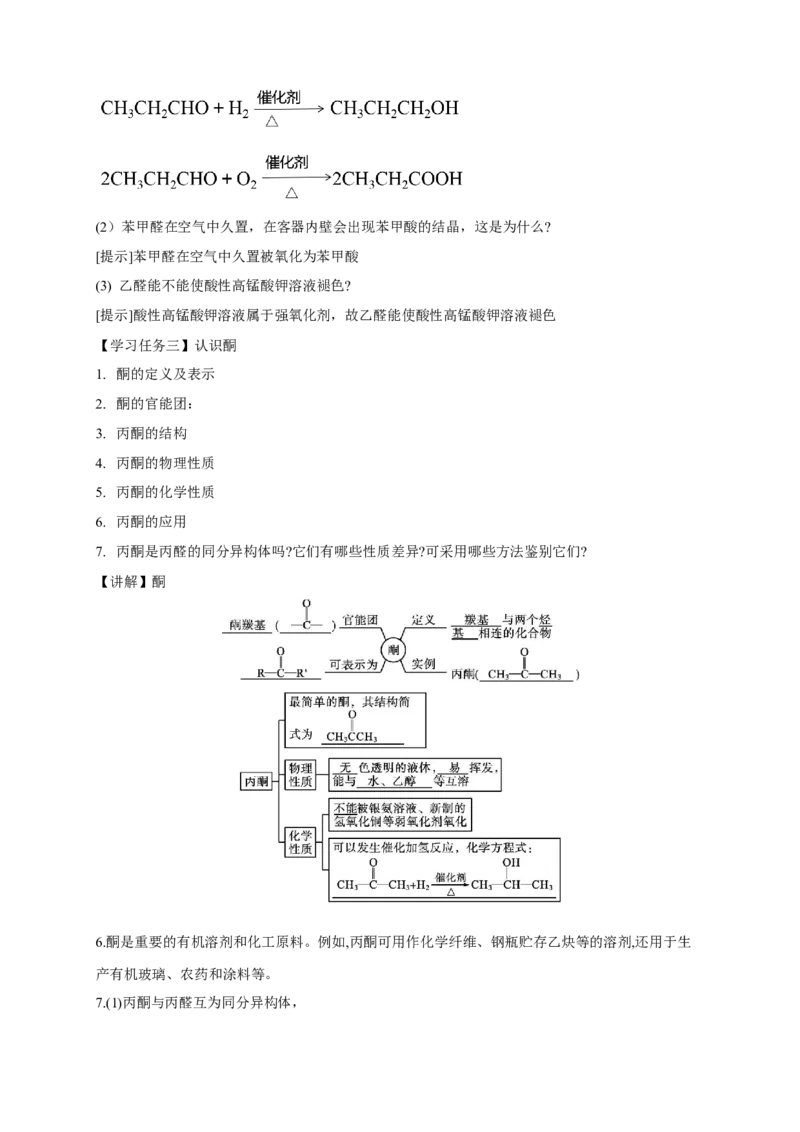
【学习任务三】认识酮
1. 酮的定义及表示
2. 酮的官能团:
3. 丙酮的结构
4. 丙酮的物理性质
5. 丙酮的化学性质
6. 丙酮的应用
7. 丙酮是丙醛的同分异构体吗?它们有哪些性质差异?可采用哪些方法鉴别它们?
【讲解】酮
6.酮是重要的有机溶剂和化工原料。例如,丙酮可用作化学纤维、钢瓶贮存乙炔等的溶剂,还用于生
产有机玻璃、农药和涂料等。
7.(1)丙酮与丙醛互为同分异构体,(2)丙酮可发生还原反应,却不与银氨溶液和新制的氢氧化铜反应。丙醛可发生氧化反应、还原反应、
与银氨溶液和新制的氢氧化铜反应。
(3)丙酮与丙醛可用银氨溶液和新制的氢氧化铜反应。
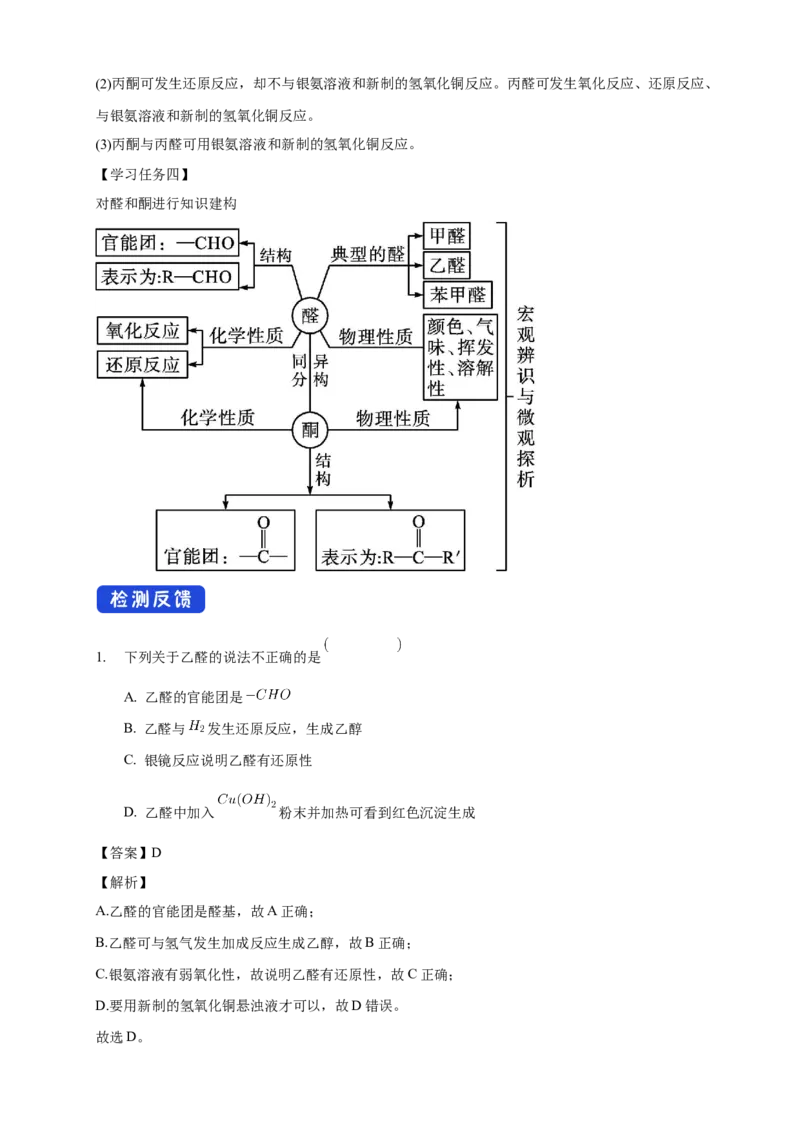
【学习任务四】
对醛和酮进行知识建构
1. 下列关于乙醛的说法不正确的是
A. 乙醛的官能团是
B. 乙醛与 发生还原反应,生成乙醇
C. 银镜反应说明乙醛有还原性
D. 乙醛中加入 粉末并加热可看到红色沉淀生成
【答案】D
【解析】
A.乙醛的官能团是醛基,故A正确;
B.乙醛可与氢气发生加成反应生成乙醇,故B正确;
C.银氨溶液有弱氧化性,故说明乙醛有还原性,故C正确;
D.要用新制的氢氧化铜悬浊液才可以,故D错误。
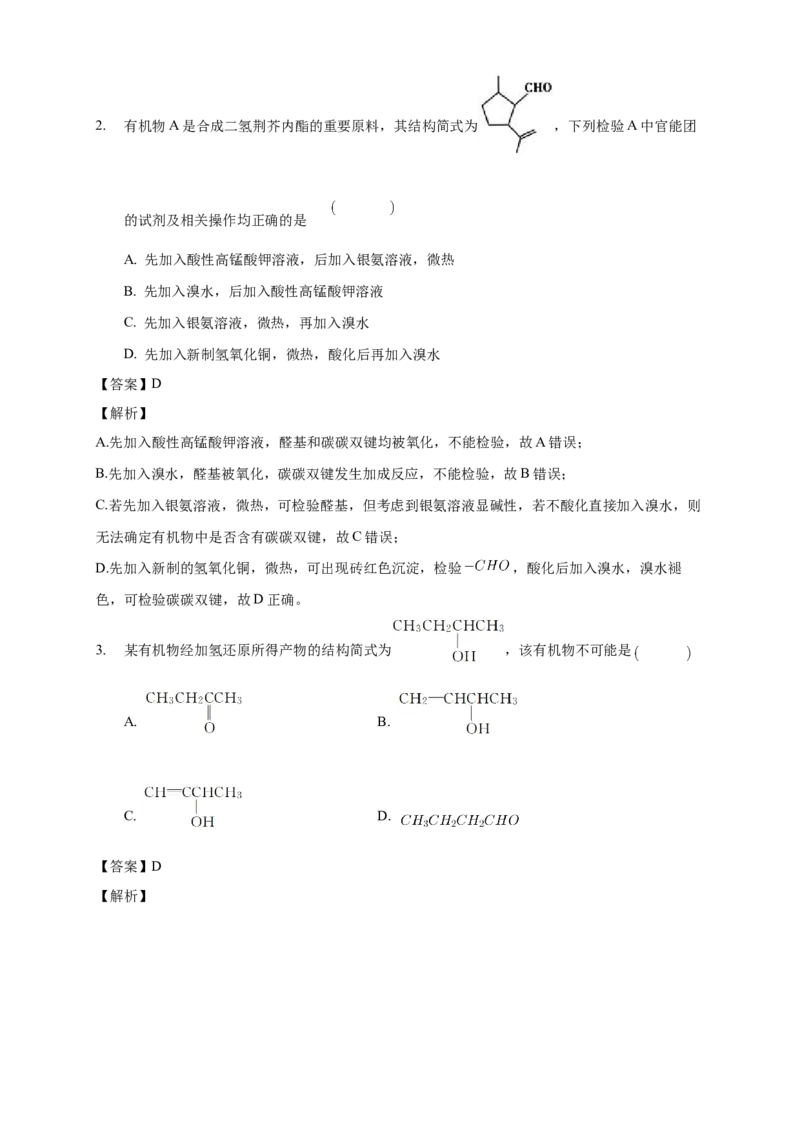
故选D。2. 有机物A是合成二氢荆芥内酯的重要原料,其结构简式为 ,下列检验A中官能团
的试剂及相关操作均正确的是
A. 先加入酸性高锰酸钾溶液,后加入银氨溶液,微热
B. 先加入溴水,后加入酸性高锰酸钾溶液
C. 先加入银氨溶液,微热,再加入溴水
D. 先加入新制氢氧化铜,微热,酸化后再加入溴水
【答案】D
【解析】
A.先加入酸性高锰酸钾溶液,醛基和碳碳双键均被氧化,不能检验,故A错误;
B.先加入溴水,醛基被氧化,碳碳双键发生加成反应,不能检验,故B错误;
C.若先加入银氨溶液,微热,可检验醛基,但考虑到银氨溶液显碱性,若不酸化直接加入溴水,则
无法确定有机物中是否含有碳碳双键,故C错误;
D.先加入新制的氢氧化铜,微热,可出现砖红色沉淀,检验 ,酸化后加入溴水,溴水褪
色,可检验碳碳双键,故D正确。
3. 某有机物经加氢还原所得产物的结构简式为 ,该有机物不可能是
A. B.
C. D.
【答案】D
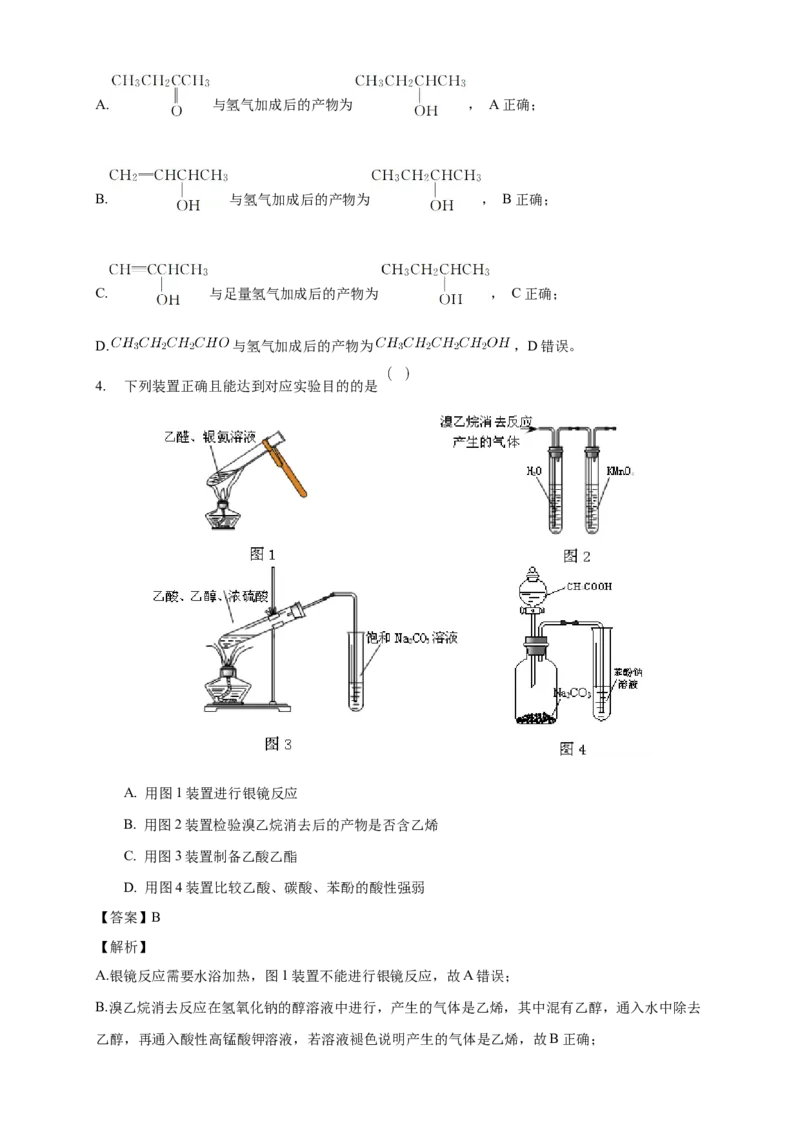
【解析】A. 与氢气加成后的产物为 , A正确;
B. 与氢气加成后的产物为 , B正确;
C. 与足量氢气加成后的产物为 , C正确;
D. 与氢气加成后的产物为 ,D错误。
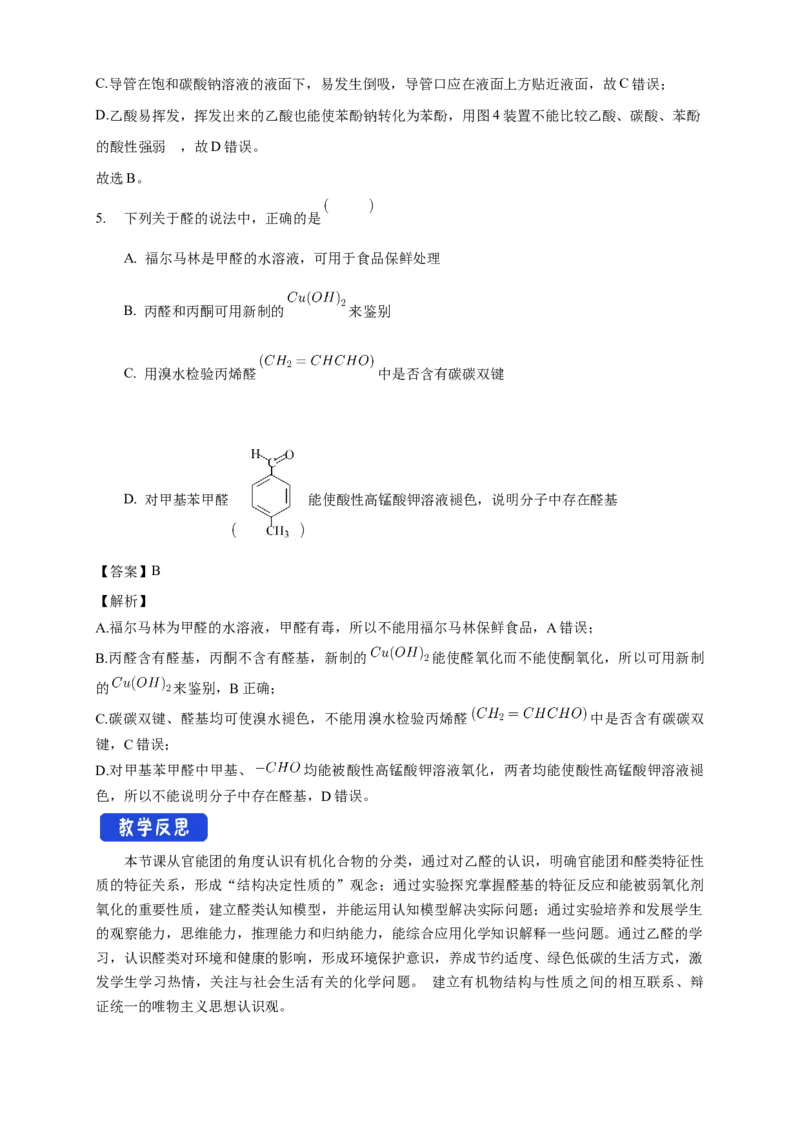
4. 下列装置正确且能达到对应实验目的的是
A. 用图1装置进行银镜反应
B. 用图2装置检验溴乙烷消去后的产物是否含乙烯
C. 用图3装置制备乙酸乙酯
D. 用图4装置比较乙酸、碳酸、苯酚的酸性强弱
【答案】B
【解析】
A.银镜反应需要水浴加热,图1装置不能进行银镜反应,故A错误;
B.溴乙烷消去反应在氢氧化钠的醇溶液中进行,产生的气体是乙烯,其中混有乙醇,通入水中除去
乙醇,再通入酸性高锰酸钾溶液,若溶液褪色说明产生的气体是乙烯,故B正确;C.导管在饱和碳酸钠溶液的液面下,易发生倒吸,导管口应在液面上方贴近液面,故C错误;
D.乙酸易挥发,挥发出来的乙酸也能使苯酚钠转化为苯酚,用图4装置不能比较乙酸、碳酸、苯酚
的酸性强弱 ,故D错误。
故选B。
5. 下列关于醛的说法中,正确的是
A. 福尔马林是甲醛的水溶液,可用于食品保鲜处理
B. 丙醛和丙酮可用新制的 来鉴别
C. 用溴水检验丙烯醛 中是否含有碳碳双键
D. 对甲基苯甲醛 能使酸性高锰酸钾溶液褪色,说明分子中存在醛基
【答案】B
【解析】
A.福尔马林为甲醛的水溶液,甲醛有毒,所以不能用福尔马林保鲜食品,A错误;
B.丙醛含有醛基,丙酮不含有醛基,新制的 能使醛氧化而不能使酮氧化,所以可用新制
的 来鉴别,B正确;
C.碳碳双键、醛基均可使溴水褪色,不能用溴水检验丙烯醛 中是否含有碳碳双
键,C错误;
D.对甲基苯甲醛中甲基、 均能被酸性高锰酸钾溶液氧化,两者均能使酸性高锰酸钾溶液褪
色,所以不能说明分子中存在醛基,D错误。
本节课从官能团的角度认识有机化合物的分类,通过对乙醛的认识,明确官能团和醛类特征性
质的特征关系,形成“结构决定性质的”观念;通过实验探究掌握醛基的特征反应和能被弱氧化剂
氧化的重要性质,建立醛类认知模型,并能运用认知模型解决实际问题;通过实验培养和发展学生
的观察能力,思维能力,推理能力和归纳能力,能综合应用化学知识解释一些问题。通过乙醛的学
习,认识醛类对环境和健康的影响,形成环境保护意识,养成节约适度、绿色低碳的生活方式,激
发学生学习热情,关注与社会生活有关的化学问题。 建立有机物结构与性质之间的相互联系、辩
证统一的唯物主义思想认识观。