文档内容
第三节 乙醇与乙酸
第 1 课时 乙醇
课后篇巩固提升
夯实基础·轻松达标
1.下列物质不能氧化乙醇的是( )
A.氧气 B.酸性高锰酸钾溶液
C.酸性重铬酸钾溶液 D.稀硫酸
答案D
解析乙醇可在氧气中燃烧生成二氧化碳和水,也可与O 发生催化氧化生成乙醛;乙醇可被强氧化剂酸
2
性高锰酸钾溶液或酸性重铬酸钾溶液氧化成乙酸,但不能被稀硫酸氧化。
2.比较乙烷和乙醇的分子结构,下列说法错误的是 ( )
A.两个碳原子以单键相连
B.分子里都含6个相同的氢原子
C.乙基与一个氢原子相连就是乙烷分子
D.乙基与一个羟基相连就是乙醇分子
答案B
解析乙烷和乙醇的结构简式分别为CHCH 和CHCHOH,乙醇分子中有3种等效氢原子,所以B选
3 3 3 2
项错误。
3.下列有关乙醇的物理性质的应用的说法不正确的是 ( )
A.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中药的有效成分
C.由于乙醇能够以任意比溶解于水,所以酒厂可以勾兑各种浓度的酒
D.从化学学科角度看,俗语“酒香不怕巷子深”中包含乙醇容易挥发的性质
答案A
解析乙醇与水能以任意比混溶,无法用分液法将乙醇中的水除去。
4.已知分子中含有羟基的物质都能与钠反应产生氢气。
乙醇、乙二醇( )、丙三醇( )分别与足量金属钠作用,产生等量的氢气。则这三
种醇的物质的量之比为( )
A.6∶3∶2 B.1∶2∶3
C.3∶2∶1 D.4∶3∶2
答案A解析醇分子中羟基个数与被置换的氢原子个数之比为1∶1。三种醇与钠反应放出等量的氢气,则三
1 1
种醇提供的羟基数相同,因此三种醇的物质的量之比为1∶
∶
=6∶3∶2。
2 3
5.下列醇不能发生催化氧化的是( )
A.CHOH B.
3
C. D.
答案C
解析醇的催化氧化断裂的化学键是O—H键和连接羟基的碳原子上的C—H键。C项中连接羟基的
碳原子上没有C—H键,故不能发生催化氧化。
6.将等质量的铜片在酒精灯上加热后,分别插入下列溶液中,最终导致铜片质量增加的是( )
A.硝酸 B.稀盐酸
C.Ca(OH) 溶液 D.乙醇
2
答案C
解析铜片在酒精灯上加热,发生化学反应:2Cu+O 2CuO,使质量增加。当遇到硝酸和稀盐酸后,发
2
生反应的化学方程式分别为CuO+2HNO Cu(NO )+H O、CuO+2HCl CuCl +H O,反而使铜片
3 3 2 2 2 2
质量减少;当遇到乙醇时发生化学反应:CuO+CH CHOH CHCHO+H O+Cu,CuO被还原为Cu,反
3 2 3 2
应前后铜片质量不变;当遇到Ca(OH) 溶液时,CuO不与它反应,故加热后的铜片比原铜片质量增加。
2
故正确答案为C。
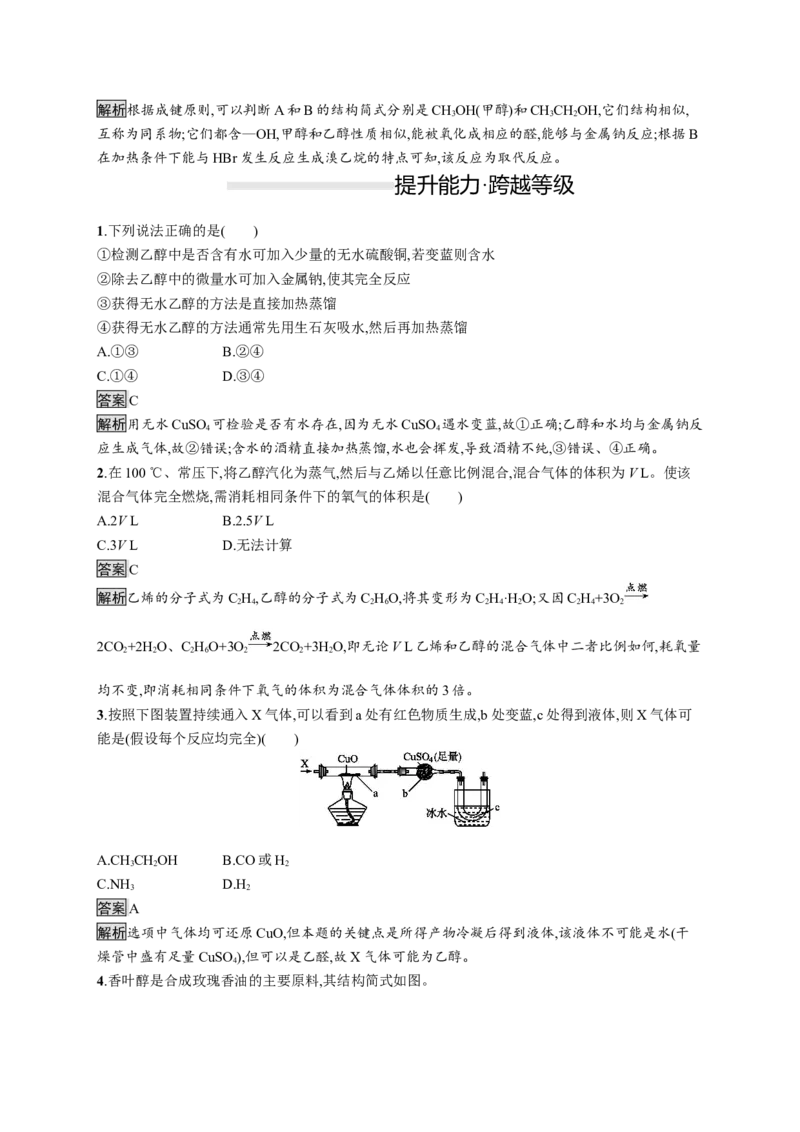
7.如图是A分子的球棍模型和B分子的空间充填模型,回答下列问题:
(1)A和B的关系是 。
(2)写出A分子在催化剂存在条件下加热和氧气反应的化学方程式:
。
(3)写出B分子和金属钠反应的化学方程式: 。
(4)B在加热条件下能够与HBr发生反应生成溴乙烷,该反应类型是 。
答案(1)同系物
(2)2CH OH+O 2HCHO+2H O
3 2 2
(3)2CH CHOH+2Na 2CHCHONa+H ↑
3 2 3 2 2
(4)取代反应解析根据成键原则,可以判断A和B的结构简式分别是CHOH(甲醇)和CHCHOH,它们结构相似,
3 3 2
互称为同系物;它们都含—OH,甲醇和乙醇性质相似,能被氧化成相应的醛,能够与金属钠反应;根据B
在加热条件下能与HBr发生反应生成溴乙烷的特点可知,该反应为取代反应。
提升能力·跨越等级
1.下列说法正确的是( )
①检测乙醇中是否含有水可加入少量的无水硫酸铜,若变蓝则含水
②除去乙醇中的微量水可加入金属钠,使其完全反应
③获得无水乙醇的方法是直接加热蒸馏
④获得无水乙醇的方法通常先用生石灰吸水,然后再加热蒸馏
A.①③ B.②④
C.①④ D.③④
答案C
解析用无水CuSO 可检验是否有水存在,因为无水CuSO 遇水变蓝,故①正确;乙醇和水均与金属钠反
4 4
应生成气体,故②错误;含水的酒精直接加热蒸馏,水也会挥发,导致酒精不纯,③错误、④正确。
2.在100 ℃、常压下,将乙醇汽化为蒸气,然后与乙烯以任意比例混合,混合气体的体积为V L。使该
混合气体完全燃烧,需消耗相同条件下的氧气的体积是( )
A.2V L B.2.5V L
C.3V L D.无法计算
答案C
解析乙烯的分子式为C H,乙醇的分子式为C HO,将其变形为C H·HO;又因C H+3O
2 4 2 6 2 4 2 2 4 2
2CO+2H O、C HO+3O 2CO+3H O,即无论V L乙烯和乙醇的混合气体中二者比例如何,耗氧量
2 2 2 6 2 2 2
均不变,即消耗相同条件下氧气的体积为混合气体体积的3倍。
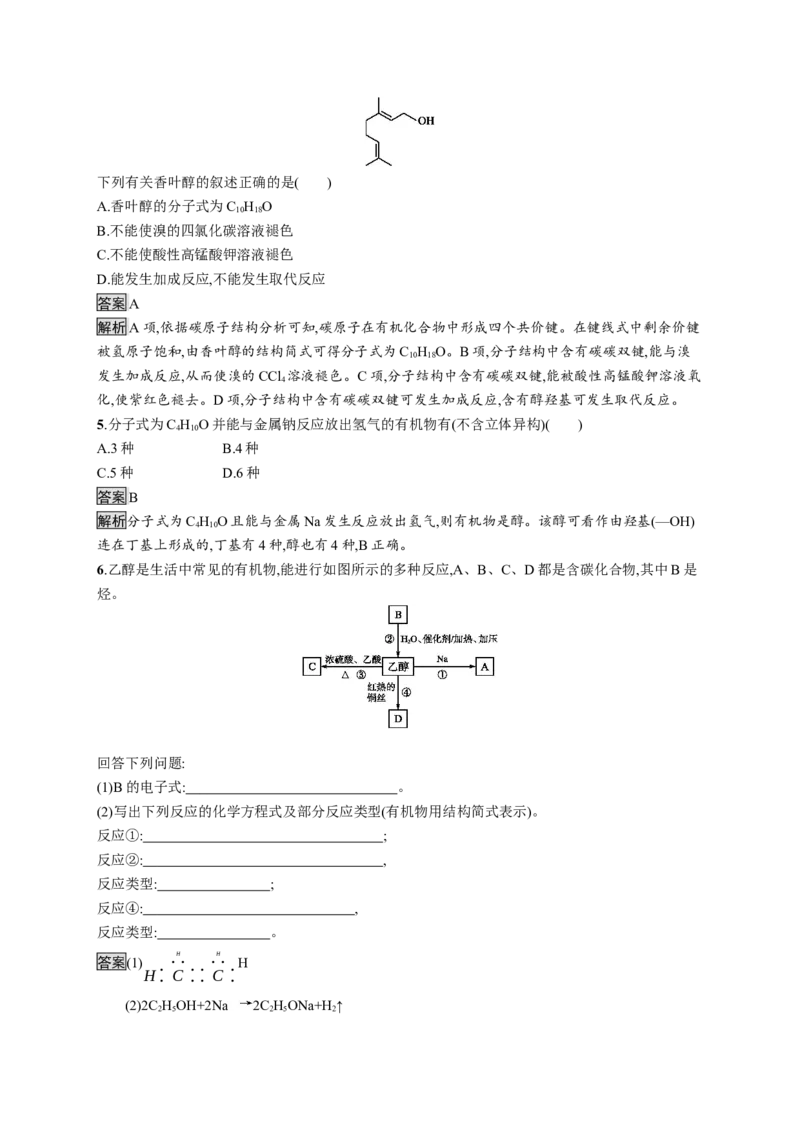
3.按照下图装置持续通入X气体,可以看到a处有红色物质生成,b处变蓝,c处得到液体,则X气体可
能是(假设每个反应均完全)( )
A.CHCHOH B.CO或H
3 2 2
C.NH D.H
3 2
答案A
解析选项中气体均可还原CuO,但本题的关键点是所得产物冷凝后得到液体,该液体不可能是水(干
燥管中盛有足量CuSO ),但可以是乙醛,故X气体可能为乙醇。
4
4.香叶醇是合成玫瑰香油的主要原料,其结构简式如图。下列有关香叶醇的叙述正确的是( )
A.香叶醇的分子式为C H O
10 18
B.不能使溴的四氯化碳溶液褪色
C.不能使酸性高锰酸钾溶液褪色
D.能发生加成反应,不能发生取代反应
答案A
解析A项,依据碳原子结构分析可知,碳原子在有机化合物中形成四个共价键。在键线式中剩余价键
被氢原子饱和,由香叶醇的结构简式可得分子式为C H O。B项,分子结构中含有碳碳双键,能与溴
10 18
发生加成反应,从而使溴的CCl 溶液褪色。C项,分子结构中含有碳碳双键,能被酸性高锰酸钾溶液氧
4
化,使紫红色褪去。D项,分子结构中含有碳碳双键可发生加成反应,含有醇羟基可发生取代反应。
5.分子式为C H O并能与金属钠反应放出氢气的有机物有(不含立体异构)( )
4 10
A.3种 B.4种
C.5种 D.6种
答案B
解析分子式为C H O且能与金属Na发生反应放出氢气,则有机物是醇。该醇可看作由羟基(—OH)
4 10
连在丁基上形成的,丁基有4种,醇也有4种,B正确。
6.乙醇是生活中常见的有机物,能进行如图所示的多种反应,A、B、C、D都是含碳化合物,其中B是
烃。
回答下列问题:
(1)B的电子式: 。
(2)写出下列反应的化学方程式及部分反应类型(有机物用结构简式表示)。
反应①: ;
反应②: ,
反应类型: ;
反应④: ,
反应类型: 。
H H
答案(1) ·· ·· H
H· C ·· C ·
· ·· ·
(2)2C HOH+2Na 2C HONa+H ↑
2 5 2 5 2CH CH+H O CHCHOH 加成反应 2CHCHOH+O 2CHCHO+2H O 氧化
2 2 2 3 2 3 2 2 3 2
反应
解析(2)乙醇与钠发生反应生成乙醇钠和氢气。乙烯与水发生加成反应生成乙醇。乙醇与氧气在铜
作催化剂和加热条件下发生氧化反应生成乙醛。
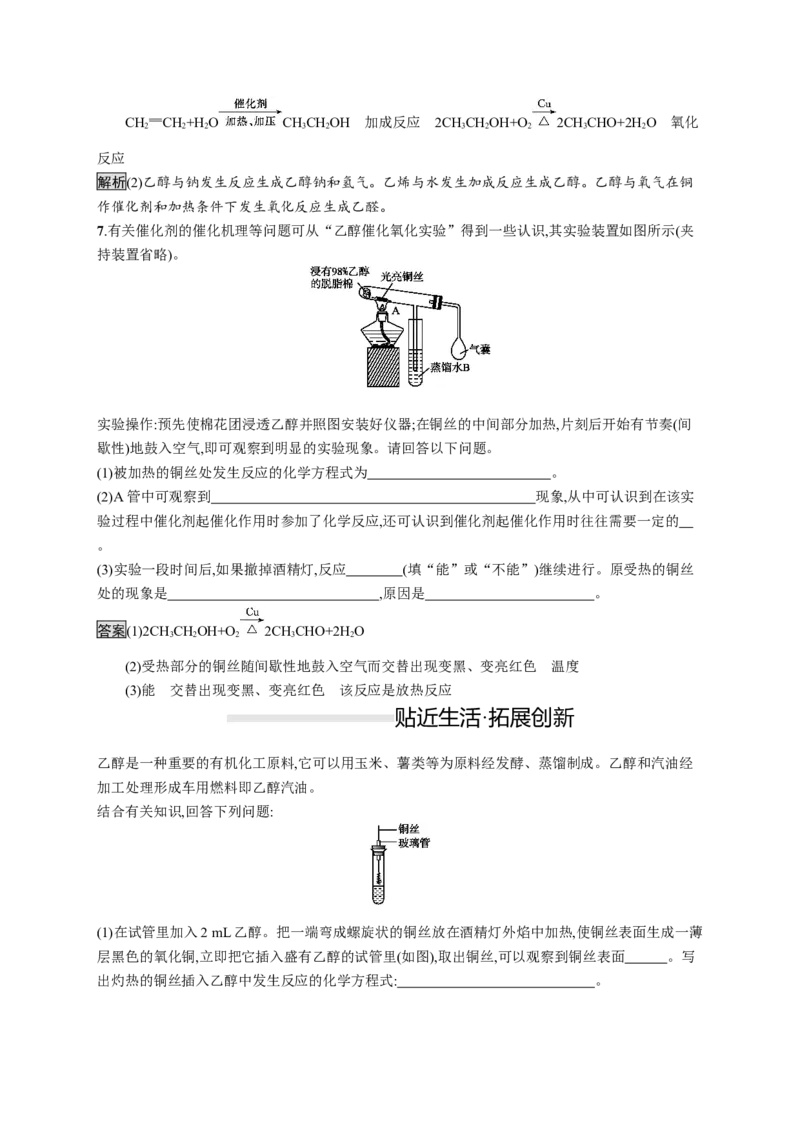
7.有关催化剂的催化机理等问题可从“乙醇催化氧化实验”得到一些认识,其实验装置如图所示(夹
持装置省略)。
实验操作:预先使棉花团浸透乙醇并照图安装好仪器;在铜丝的中间部分加热,片刻后开始有节奏(间
歇性)地鼓入空气,即可观察到明显的实验现象。请回答以下问题。
(1)被加热的铜丝处发生反应的化学方程式为 。
(2)A管中可观察到 现象,从中可认识到在该实
验过程中催化剂起催化作用时参加了化学反应,还可认识到催化剂起催化作用时往往需要一定的
。
(3)实验一段时间后,如果撤掉酒精灯,反应 (填“能”或“不能”)继续进行。原受热的铜丝
处的现象是 ,原因是 。
答案(1)2CH CHOH+O 2CHCHO+2H O
3 2 2 3 2
(2)受热部分的铜丝随间歇性地鼓入空气而交替出现变黑、变亮红色 温度
(3)能 交替出现变黑、变亮红色 该反应是放热反应
贴近生活·拓展创新
乙醇是一种重要的有机化工原料,它可以用玉米、薯类等为原料经发酵、蒸馏制成。乙醇和汽油经
加工处理形成车用燃料即乙醇汽油。
结合有关知识,回答下列问题:
(1)在试管里加入2 mL乙醇。把一端弯成螺旋状的铜丝放在酒精灯外焰中加热,使铜丝表面生成一薄
层黑色的氧化铜,立即把它插入盛有乙醇的试管里(如图),取出铜丝,可以观察到铜丝表面 。写
出灼热的铜丝插入乙醇中发生反应的化学方程式: 。(2)乙醇汽油作为一种新型车用燃料,符合我国的能源战略,推广使用乙醇汽油的好处是
(写出一条即可)。
(3)对于驾驶员酒后驾车,可对其呼出的气体进行检验,所利用的化学反应如下:
KCr O(橙色)+3C HOH+4H SO
2 2 7 2 5 2 4
Cr (SO )(绿色)+3CH CHO+7H O+KSO
2 4 3 3 2 2 4
被检测的气体成分是 ,上述反应中的氧化剂是 ,还原剂是 。
答案(1)变红 2CHCHOH+O 2CHCHO+2H O
3 2 2 3 2
(2)减少污染(合理即可)
(3)乙醇 KCr O C HOH
2 2 7 2 5
解析(1)乙醇能将氧化铜还原为单质Cu,故铜丝表面黑色部分变红;CH CHOH在Cu作催化剂并加热
3 2
的条件下被O 氧化为乙醛(CHCHO)。(3)乙醇具有还原性,K Cr O 具有氧化性,二者可发生氧化还原
2 3 2 2 7
反应。