文档内容
乙醇与乙酸
【教学目标】
知识与技能:
1.知道官能团的概念;
2.了解乙醇的物理性质,掌握乙醇的结构和化学性质;
3.知道乙酸的物理性质,乙酸的分子组成和结构,了解乙酸的化学性质;
4.了解酯化反应的概念,了解酯化反应实验的装罝特点并能够独立完成该实验。
过程与方法:
1.通过建立乙醇、乙酸分子的立体结构模型来学习“结构-性质-用途”研究烃的衍生物
的程序和方法;
2.通过学习乙酸的性质,使学生体会利用比较、归纳、概括等方法得到科学结论的过程;
3.通过乙醇的分子结构与化学性质的学习,充分理解官能团对性质的影响,学会通过事
物的表象分析事物本质的方法。
情感态度与价值观:
1.知道乙醇在日常生活、工业生产中的广泛应用,形成运用知识解决实际问题的意识;
2.通过新旧知识的联系,激发学生学习的兴趣和求知欲望;
3.通过学生实验,培养学生求实、严谨的优良品质;
4.对学生进行“本质决定现象”,“由个别到一般”的辩证唯物主义思维方法的训练。
【教学重难点】
重点:
1.官能团的概念、乙醇、乙酸的组成;
2.乙醇的取代反应与氧化反应;
3.乙酸的酸性和酯化反应。
难点:使学生建立乙醇和乙酸分子的立体结构模型,并能从结构角度初步认识乙醇的氧
化、乙酸的酯化两个重要反应。
【教学过程】
知识点一:乙醇
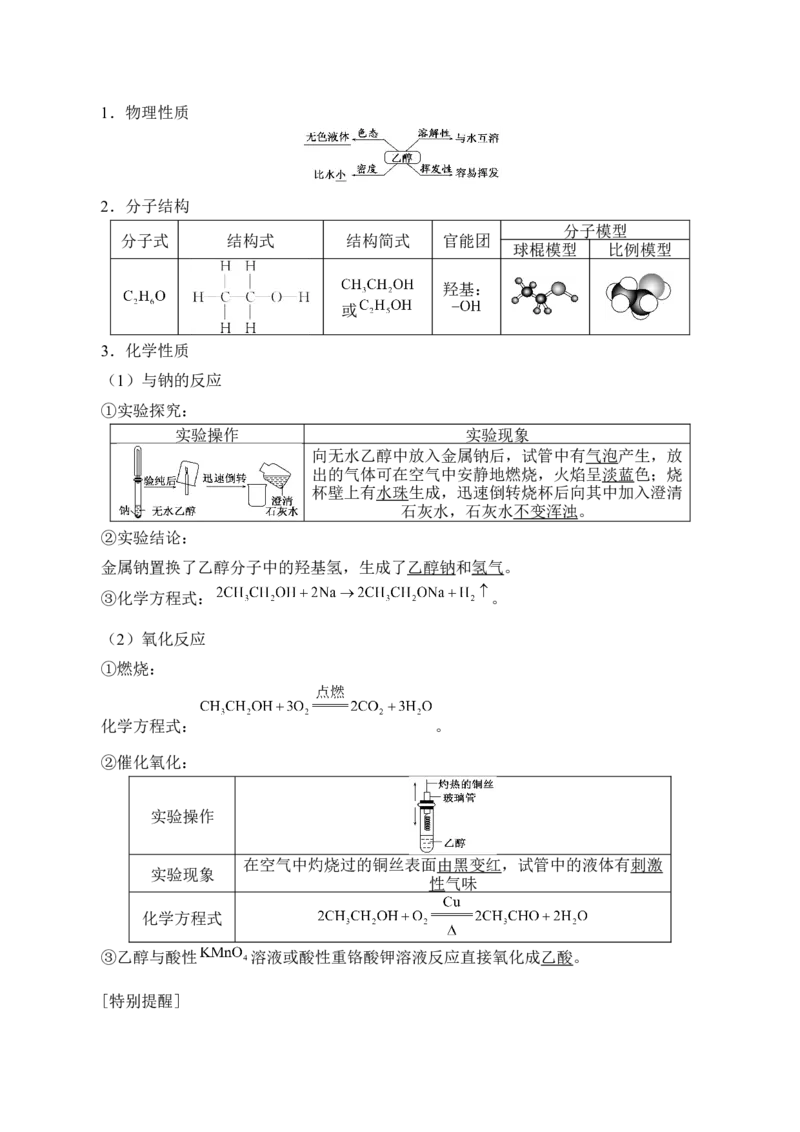
基础:自主落实1.物理性质
2.分子结构
分子模型
分子式 结构式 结构简式 官能团
球棍模型 比例模型
羟基:
或
3.化学性质
(1)与钠的反应
①实验探究:
实验操作 实验现象
向无水乙醇中放入金属钠后,试管中有气泡产生,放
出的气体可在空气中安静地燃烧,火焰呈淡蓝色;烧
杯壁上有水珠生成,迅速倒转烧杯后向其中加入澄清
石灰水,石灰水不变浑浊。
②实验结论:
金属钠置换了乙醇分子中的羟基氢,生成了乙醇钠和氢气。
③化学方程式: 。
(2)氧化反应
①燃烧:
化学方程式: 。
②催化氧化:
实验操作
在空气中灼烧过的铜丝表面由黑变红,试管中的液体有刺激
实验现象
性气味
化学方程式
③乙醇与酸性 溶液或酸性重铬酸钾溶液反应直接氧化成乙酸。
[特别提醒]钠(或其他活泼金属)只能置换羟基上的氢,不能置换其他氢。
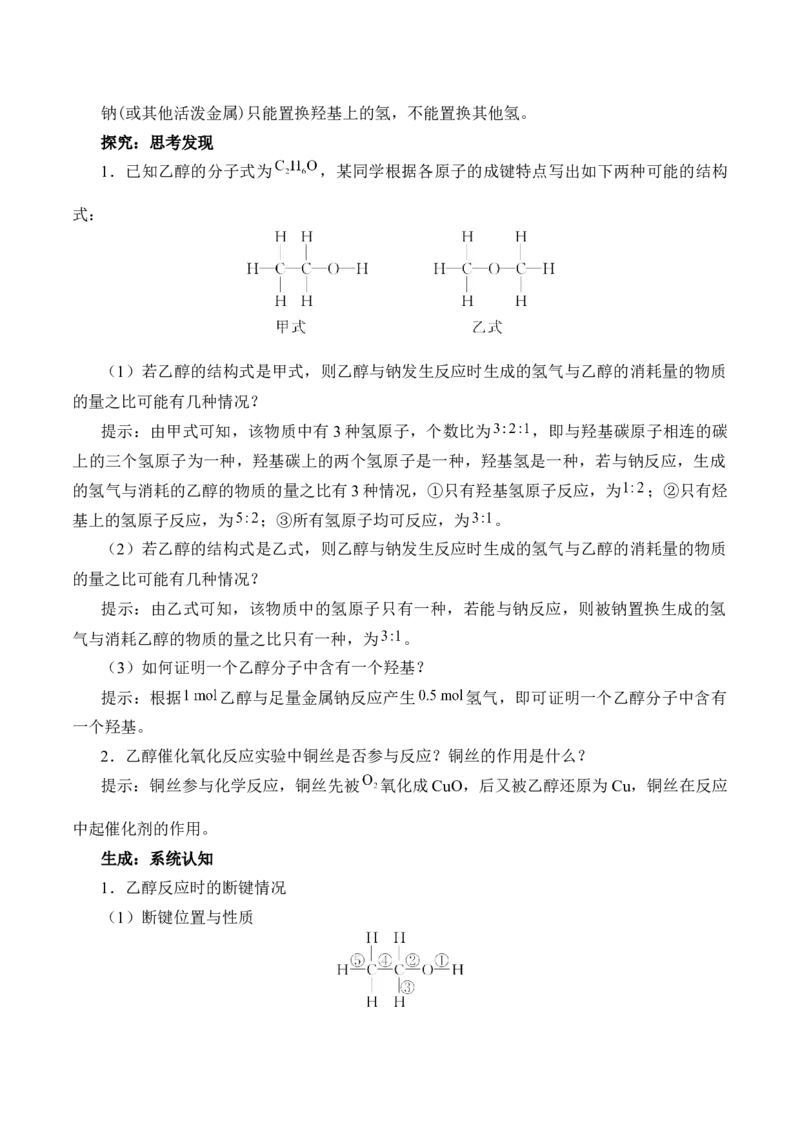
探究:思考发现
1.已知乙醇的分子式为 ,某同学根据各原子的成键特点写出如下两种可能的结构
式:
(1)若乙醇的结构式是甲式,则乙醇与钠发生反应时生成的氢气与乙醇的消耗量的物质
的量之比可能有几种情况?
提示:由甲式可知,该物质中有3种氢原子,个数比为 ,即与羟基碳原子相连的碳
上的三个氢原子为一种,羟基碳上的两个氢原子是一种,羟基氢是一种,若与钠反应,生成
的氢气与消耗的乙醇的物质的量之比有3种情况,①只有羟基氢原子反应,为 ;②只有烃
基上的氢原子反应,为 ;③所有氢原子均可反应,为 。
(2)若乙醇的结构式是乙式,则乙醇与钠发生反应时生成的氢气与乙醇的消耗量的物质
的量之比可能有几种情况?
提示:由乙式可知,该物质中的氢原子只有一种,若能与钠反应,则被钠置换生成的氢
气与消耗乙醇的物质的量之比只有一种,为 。
(3)如何证明一个乙醇分子中含有一个羟基?
提示:根据 乙醇与足量金属钠反应产生 氢气,即可证明一个乙醇分子中含有
一个羟基。
2.乙醇催化氧化反应实验中铜丝是否参与反应?铜丝的作用是什么?
提示:铜丝参与化学反应,铜丝先被 氧化成CuO,后又被乙醇还原为Cu,铜丝在反应
中起催化剂的作用。
生成:系统认知
1.乙醇反应时的断键情况
(1)断键位置与性质乙醇的性质 键的断裂
与钠反应 断①键
燃烧 断①②③④⑤键
催化氧化 断①③键
(2)注意
①乙醇与钠的反应比水与钠的反应要缓和得多,这说明乙醇分子羟基中的氢原子不如水
分子羟基中的氢原子活泼。
② 乙醇与足量钠反应,产生 ,该关系可延伸为 羟基( )跟足量
钠反应产生 。
2.乙醇催化氧化的实质
总反应的化学方程式为 ,反应中Cu作催化剂。
演练:应用体验
1.判断正误(正确的打“√”,错误的打“×”)。
(1)乙醇结构中有 ,所以乙醇溶解于水,可以电离出 而显碱性(×)
(2)乙醇燃烧生成二氧化碳和水,说明乙醇具有氧化性(×)
(3)乙醇与钠反应可以产生氢气,所以乙醇显酸性(×)
(4)乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中羟基上的氢原子活泼
(√)
2.下列说法中,不正确的是( )
A.乙醇与金属钠反应时,是乙醇分子中羟基中的 键断裂
B.检验乙醇中是否含有水,可加入少量无水硫酸铜,若变蓝则含水
C.乙醇在一定条件下可氧化成
D.甲烷、乙烯、苯、乙醇都是无色不溶于水的有机化合物解析:选D。与金属钠反应生成乙醇钠,是乙醇分子中羟基中的 键断裂;检验乙醇
中是否含有水可用无水硫酸铜作检验试剂,若变蓝则表明乙醇中含水;乙醇在酸性 溶
液中可氧化成乙酸;甲烷、乙烯、苯都不溶于水,但乙醇却能与水以任意比例混溶。
知识点二:乙酸
基础:自主落实
1.分子结构
分子式 结构式 结构简式 官能团 比例模型
羧基:
2.物理性质
俗名 颜色 状态 气味 溶解性 挥发性
强烈刺激性气
醋酸 无色 液体 易溶于水 易挥发
味
当温度低于 时,乙酸凝结成像冰一样的晶体,故又称冰醋酸。
3.化学性质
(1)断键位置与性质
(2)弱酸性
乙 酸 是 一 元 弱 酸 , 具 有 酸 的 通 性 。 在 水 中 部 分 电 离 , 电 离 方 程 式 为
,其酸性比碳酸的酸性强。
根据如下转化关系,写出相应的化学方程式
① ;
② ;
③ ;
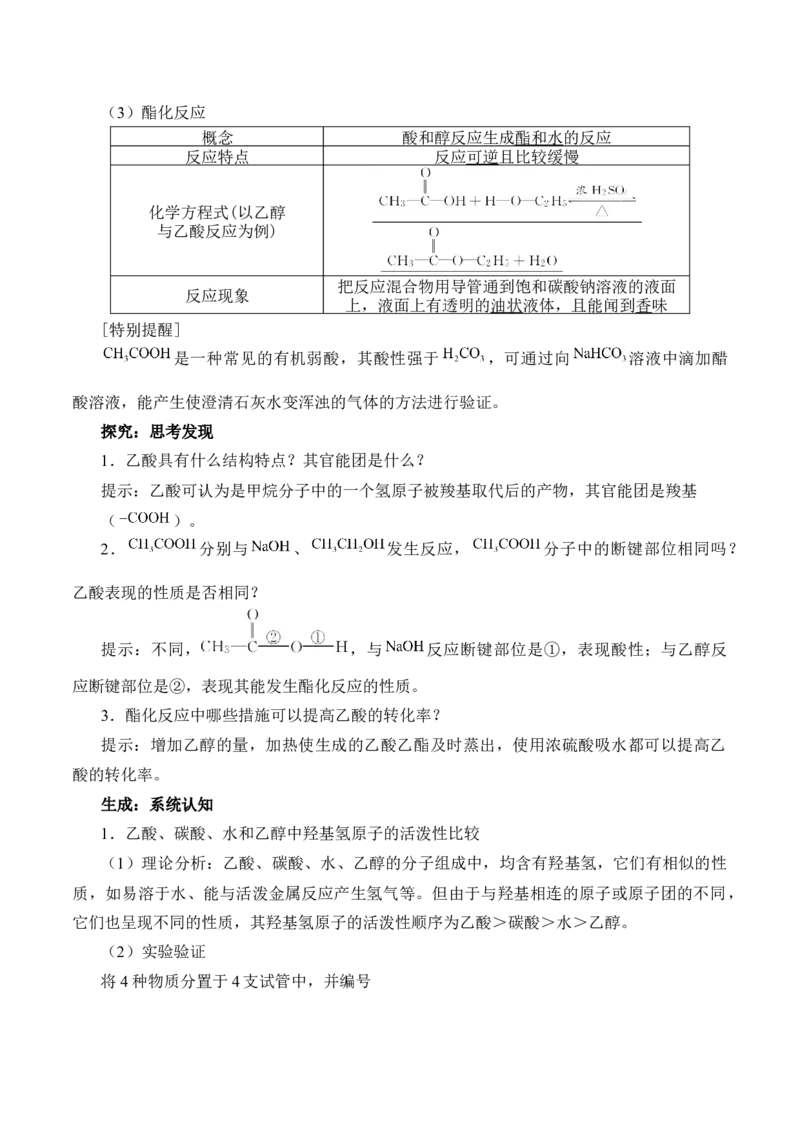
④ 。(3)酯化反应
概念 酸和醇反应生成酯和水的反应
反应特点 反应可逆且比较缓慢
化学方程式(以乙醇
与乙酸反应为例)
把反应混合物用导管通到饱和碳酸钠溶液的液面
反应现象
上,液面上有透明的油状液体,且能闻到香味
[特别提醒]
是一种常见的有机弱酸,其酸性强于 ,可通过向 溶液中滴加醋
酸溶液,能产生使澄清石灰水变浑浊的气体的方法进行验证。
探究:思考发现
1.乙酸具有什么结构特点?其官能团是什么?
提示:乙酸可认为是甲烷分子中的一个氢原子被羧基取代后的产物,其官能团是羧基
( )。
2. 分别与 、 发生反应, 分子中的断键部位相同吗?
乙酸表现的性质是否相同?
提示:不同, ,与 反应断键部位是①,表现酸性;与乙醇反
应断键部位是②,表现其能发生酯化反应的性质。
3.酯化反应中哪些措施可以提高乙酸的转化率?
提示:增加乙醇的量,加热使生成的乙酸乙酯及时蒸出,使用浓硫酸吸水都可以提高乙
酸的转化率。
生成:系统认知
1.乙酸、碳酸、水和乙醇中羟基氢原子的活泼性比较
(1)理论分析:乙酸、碳酸、水、乙醇的分子组成中,均含有羟基氢,它们有相似的性
质,如易溶于水、能与活泼金属反应产生氢气等。但由于与羟基相连的原子或原子团的不同,
它们也呈现不同的性质,其羟基氢原子的活泼性顺序为乙酸>碳酸>水>乙醇。
(2)实验验证
将4种物质分置于4支试管中,并编号① ,② ,
③
Ⅰ.实验过程:
操作 现象 结论(—OH中氢原子活泼性顺序)
四种物质各取少量于试管
③、④变红,其他不
中,各加入紫色石蕊溶液 ③、④>①、②
变红
两滴
在③、④试管中,各加入
④中产生气体 ④>③
少量碳酸钠溶液
①产生气体,反应迅
在①、②中各加入少量金
速,②产生气体,反 ①>②
属钠
应缓慢
Ⅱ.实验结论:
羟基氢的活泼性:乙醇<水<碳酸<乙酸。
2.酯化反应实验
(1)实验装置
(2)导气管末端未伸入液面以下的目的是为了防止倒吸。
(3)饱和 溶液的作用
①与挥发出来的乙酸发生反应,生成可溶于水的乙酸钠,便于闻乙酸乙酯的香味。
②溶解挥发出来的乙醇。
③减小乙酸乙酯在水中的溶解度,使液体分层,便于得到酯。
(4)酯化反应实验中的四个注意问题
①注意防暴沸:反应试管中常加入几片碎瓷片或沸石防暴沸。
②注意浓硫酸的作用:催化剂、吸水剂。
③注意试剂的添加顺序:不能先加浓硫酸,以防止液体飞溅;通常的顺序是乙醇→浓硫
酸→乙酸。
④注意酯的分离:对于生成的酯,通常用分液漏斗进行分液,将酯和饱和碳酸钠溶液分
离。
演练:应用体验1.分别将一小块钠投入下列物质中,能生成氢气,但生成氢气的速率最慢的是( )
A.乙酸 B.碳酸
C.乙醇 D.水
解析:选C。四种物质均能与钠反应生成氢气,但四种物质的分子中,羟基 H最不活泼
的是乙醇,所以生成氢气速率最慢的是乙醇。
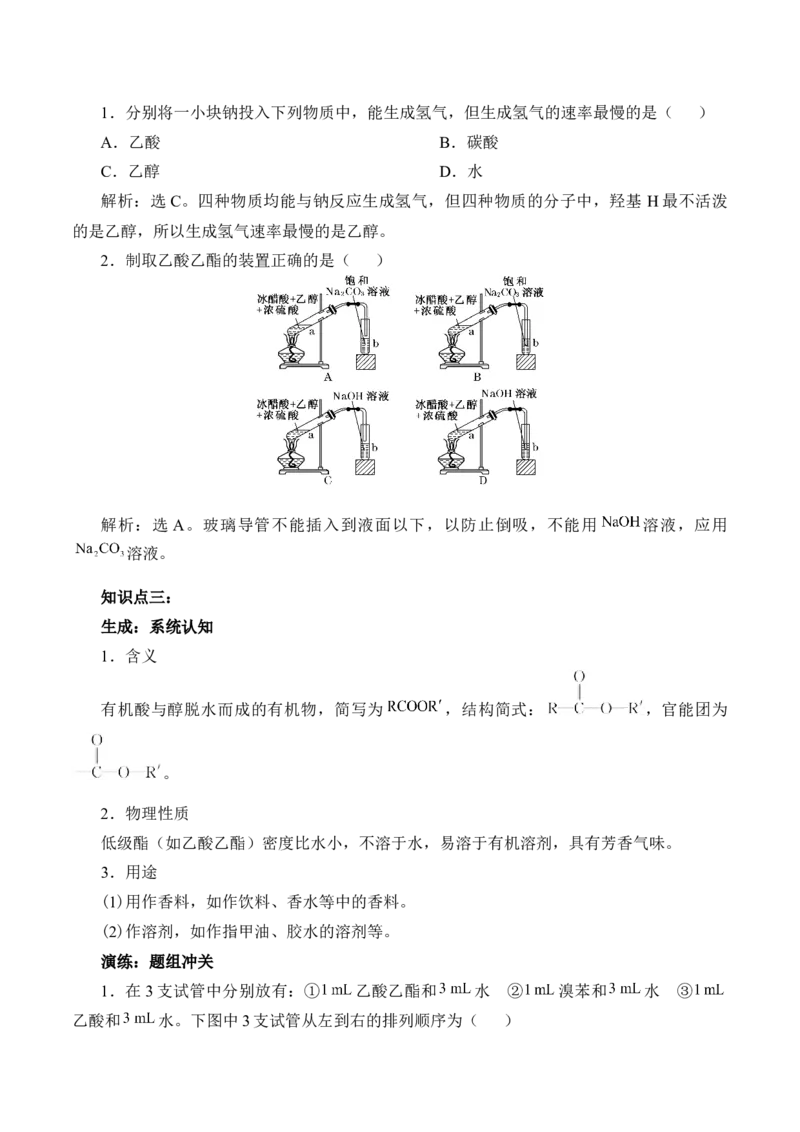
2.制取乙酸乙酯的装置正确的是( )
解析:选 A。玻璃导管不能插入到液面以下,以防止倒吸,不能用 溶液,应用
溶液。
知识点三:
生成:系统认知
1.含义
有机酸与醇脱水而成的有机物,简写为 ,结构简式: ,官能团为
。
2.物理性质
低级酯(如乙酸乙酯)密度比水小,不溶于水,易溶于有机溶剂,具有芳香气味。
3.用途
(1)用作香料,如作饮料、香水等中的香料。
(2)作溶剂,如作指甲油、胶水的溶剂等。
演练:题组冲关
1.在3支试管中分别放有:① 乙酸乙酯和 水 ② 溴苯和 水 ③
乙酸和 水。下图中3支试管从左到右的排列顺序为( )A.①②③ B.①③②
C.②①③ D.②③①
解析:选D。几种液体的密度: ,溶解性:溴苯和乙酸乙酯
不溶于水,而乙酸与水混溶,可知三支试管的排列顺序为②③①。
2.酯类物质广泛存在于香蕉、梨等水果中。某实验小组从梨中分离出一种酯,然后将分
离出的酯水解,得到乙酸和另一种分子式为 的物质。下列分析不正确的是( )
A. 分子中含有羟基
B.实验小组分离出的酯可表示为
C. 可与金属钠发生反应
D.这种酯易溶于水
解析:选D。低级酯(含碳原子数较少)难溶于水,D项不正确。