文档内容
第 2 课时 乙酸
[核心素养发展目标] 1.了解乙酸的物理性质和用途,培养“科学态度与社会责任”。2.掌
握乙酸的组成结构和化学性质,培养“变化观念与平衡思想”。3.掌握酯化反应的原理和实
质,了解其实验操作,提高“证据推理与模型认知”能力。
一、乙酸
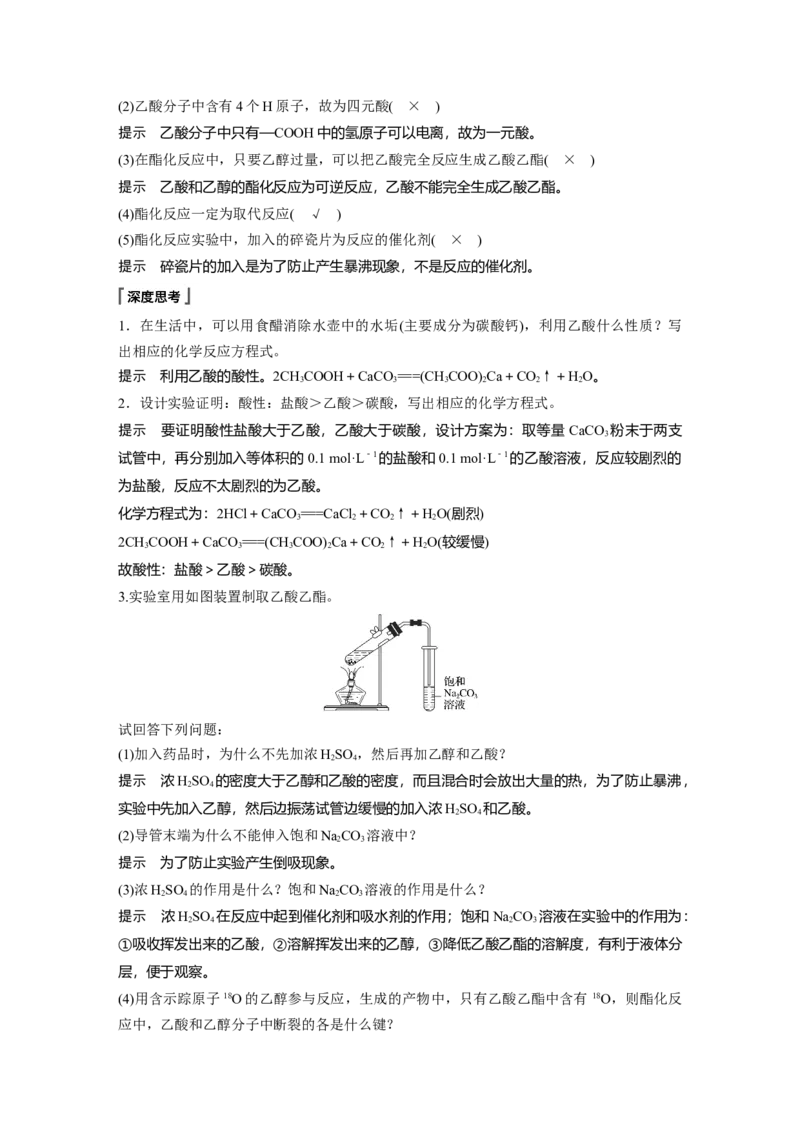
(一)乙酸的组成和结构
分子式 结构式 结构简式 官能团
C
2
H
4
O
2
CH
3
COOH 羧基( 或—
COOH)
(二)乙酸的性质
1.物理性质
乙酸是一种有强烈刺激性气味的无色液体,当温度低于熔点时,会凝结成类似冰一样的晶体,
所以纯净的乙酸又叫冰醋酸,易溶于水和乙醇。
2.化学性质
(1)弱酸性
CHCOOH
3
(2)酯化反应
①概念:酸与醇反应生成酯和水的反应。
②实验探究
实验操作
实验现象 饱和NaCO 溶液的液面上有无色透明油状液体生成,且能闻到香味
2 3
化学方程式
+H—O—CH CH +HO
2 3 2
(1)可以用水鉴别乙醇和乙酸( × )
提示 乙醇和乙酸都易溶于水。(2)乙酸分子中含有4个H原子,故为四元酸( × )
提示 乙酸分子中只有—COOH中的氢原子可以电离,故为一元酸。
(3)在酯化反应中,只要乙醇过量,可以把乙酸完全反应生成乙酸乙酯( × )
提示 乙酸和乙醇的酯化反应为可逆反应,乙酸不能完全生成乙酸乙酯。
(4)酯化反应一定为取代反应( √ )
(5)酯化反应实验中,加入的碎瓷片为反应的催化剂( × )
提示 碎瓷片的加入是为了防止产生暴沸现象,不是反应的催化剂。
1.在生活中,可以用食醋消除水壶中的水垢(主要成分为碳酸钙),利用乙酸什么性质?写
出相应的化学反应方程式。
提示 利用乙酸的酸性。2CHCOOH+CaCO ===(CHCOO) Ca+CO↑+HO。
3 3 3 2 2 2
2.设计实验证明:酸性:盐酸>乙酸>碳酸,写出相应的化学方程式。
提示 要证明酸性盐酸大于乙酸,乙酸大于碳酸,设计方案为:取等量CaCO 粉末于两支
3
试管中,再分别加入等体积的0.1 mol·L-1的盐酸和0.1 mol·L-1的乙酸溶液,反应较剧烈的
为盐酸,反应不太剧烈的为乙酸。
化学方程式为:2HCl+CaCO ===CaCl +CO↑+HO(剧烈)
3 2 2 2
2CHCOOH+CaCO ===(CHCOO) Ca+CO↑+HO(较缓慢)
3 3 3 2 2 2
故酸性:盐酸>乙酸>碳酸。
3.实验室用如图装置制取乙酸乙酯。
试回答下列问题:
(1)加入药品时,为什么不先加浓HSO ,然后再加乙醇和乙酸?
2 4
提示 浓HSO 的密度大于乙醇和乙酸的密度,而且混合时会放出大量的热,为了防止暴沸,
2 4
实验中先加入乙醇,然后边振荡试管边缓慢的加入浓HSO 和乙酸。
2 4
(2)导管末端为什么不能伸入饱和NaCO 溶液中?
2 3
提示 为了防止实验产生倒吸现象。
(3)浓HSO 的作用是什么?饱和NaCO 溶液的作用是什么?
2 4 2 3
提示 浓HSO 在反应中起到催化剂和吸水剂的作用;饱和NaCO 溶液在实验中的作用为:
2 4 2 3
①吸收挥发出来的乙酸,②溶解挥发出来的乙醇,③降低乙酸乙酯的溶解度,有利于液体分
层,便于观察。
(4)用含示踪原子18O的乙醇参与反应,生成的产物中,只有乙酸乙酯中含有 18O,则酯化反
应中,乙酸和乙醇分子中断裂的各是什么键?提示 据信息,反应的原理应如下所示:
即反应中,乙酸断裂的是C—O单键,乙醇断裂的是O—H单键,即酸脱羟基醇脱氢。
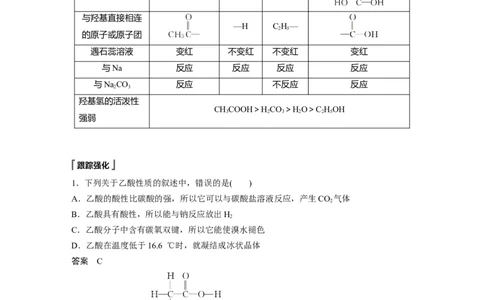
乙酸、水、乙醇、碳酸的性质比较
名称 乙酸 水 乙醇 碳酸
分子结构 CHCOOH H—OH C HOH
3 2 5
与羟基直接相连
—H C H—
2 5
的原子或原子团
遇石蕊溶液 变红 不变红 不变红 变红
与Na 反应 反应 反应 反应
与NaCO 反应 不反应 反应
2 3
羟基氢的活泼性
CHCOOH>HCO>HO>C HOH
3 2 3 2 2 5
强弱
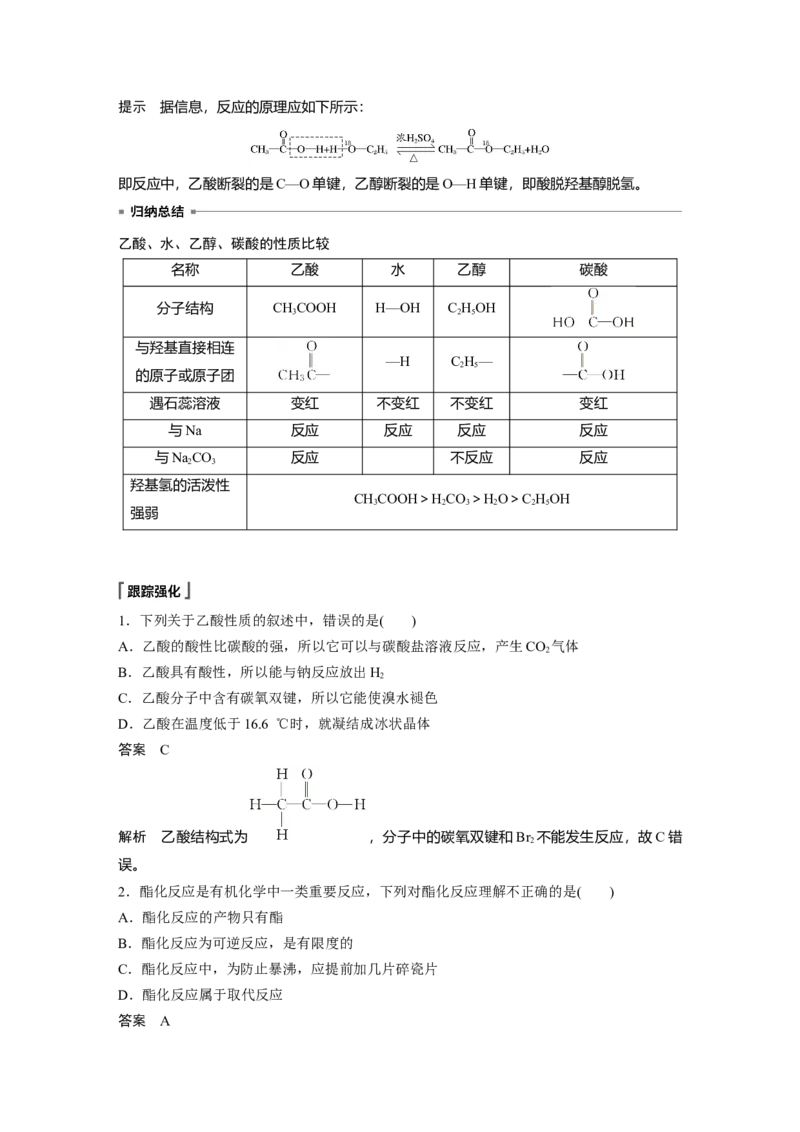
1.下列关于乙酸性质的叙述中,错误的是( )
A.乙酸的酸性比碳酸的强,所以它可以与碳酸盐溶液反应,产生CO 气体
2
B.乙酸具有酸性,所以能与钠反应放出H
2
C.乙酸分子中含有碳氧双键,所以它能使溴水褪色
D.乙酸在温度低于16.6 ℃时,就凝结成冰状晶体
答案 C
解析 乙酸结构式为 ,分子中的碳氧双键和Br 不能发生反应,故C错
2
误。
2.酯化反应是有机化学中一类重要反应,下列对酯化反应理解不正确的是( )
A.酯化反应的产物只有酯
B.酯化反应为可逆反应,是有限度的
C.酯化反应中,为防止暴沸,应提前加几片碎瓷片
D.酯化反应属于取代反应
答案 A解析 酯化反应的产物为酯和水。
3.实验室制取乙酸乙酯的主要步骤如下:
①在甲试管(如图)中加入3 mL乙醇、2 mL浓硫酸和2 mL乙酸的混合溶液。
②按图连接好装置(装置气密性良好)并加入混合液,用小火均匀地加热3~5 min。
③待试管乙收集到一定量产物后停止加热,撤出试管乙,并用力振荡,然后静置待分层。
④分离出乙酸乙酯层,洗涤、干燥。
(1)反应中浓硫酸的作用是______________________________________________________。
(2)上述实验中饱和碳酸钠溶液的作用是________(填字母)。
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
(3)欲将乙试管中的物质分离开以得到乙酸乙酯,必须使用的仪器有________________;分
离时,乙酸乙酯应该从仪器________(填“下口放出”或“上口倒出”)。
答案 (1)作催化剂和吸水剂
(2)BC
(3)分液漏斗 上口倒出
解析 (2)饱和碳酸钠溶液的作用是:①中和乙酸并吸收部分乙醇;②降低乙酸乙酯的溶解
度有利于分层析出。
(3)分离互不相溶的液体应采用分液法,上层液体从分液漏斗的上口倒出,下层液体从分液
漏斗的下口放出。
二、乙醇与乙酸的结构、性质比较及应用
1.乙醇在化学变化中的断键规律
①键断裂:和Na 反应,和乙酸发生酯化反应。
①键和③键同时断裂:发生催化氧化反应。
2.乙酸在化学变化中的断键规律
①键断裂:显示酸性。②键断裂:发生酯化反应。
3.在应用中,若题目有机物分子结构中含有—OH或 ,可根据乙醇和乙酸的性质
进行判断及推演。
(1)乙醇和乙酸分子中都含有O—H共价键,故两者水溶液都呈酸性( × )
提示 乙醇分子中所含官能团为羟基(—OH),乙酸分子中所含官能团为羧基( ),
羧基中的氢原子可以发生电离,羟基(—OH)中的氢原子不能发生电离,故乙醇呈中性,乙
酸呈酸性。
(2)乙醇和乙酸在一定条件下发生酯化反应时,乙醇分子脱去羟基、乙酸分子脱去氢原子(
× )
提示 在酯化反应中,乙醇分子脱去氢原子,乙酸分子脱去羟基。
(3)乙酸分子中也含有C—H共价键和O—H共价键,故乙酸也可以和氧气发生催化氧化反应
( × )
提示 乙醇发生催化氧化的原理为O—H键断裂及和羟基相连的碳原子上的C—H键断裂,
而乙酸的结构为 ,和—OH相连的为 ,故不能发生催化氧化。
1.(2019·天津高一检测)某有机物的结构简式为 。下列关于该有机物
的叙述中,不正确的是( )
A.能与NaHCO 发生反应并放出二氧化碳
3
B.能在催化剂作用下与HCl发生加成反应
C.不能使酸性KMnO 溶液和溴水褪色
4
D.在浓硫酸作催化剂条件下能和乙醇发生酯化反应生成酯
答案 C
解析 该有机物分子中含有 、—COOH两种官能团,其中—COOH能和NaHCO
3
反应放出 CO ,能在浓硫酸作催化剂条件下发生酯化反应生成酯; 能使酸性
2
KMnO 溶液褪色,也能和Br 及HCl发生加成反应。
4 2
2.(2018·山西晋中高三高考适应性调研)芳樟醇和橙花叔醇是决定茶叶花甜香的关键物质。芳樟醇和橙花叔醇的结构如图所示,下列有关叙述正确的是( )
A.橙花叔醇的分子式为C H O
15 28
B.芳樟醇和橙花叔醇互为同分异构体
C.芳樟醇和橙花叔醇与H 完全加成后的产物互为同系物
2
D.二者均能发生取代反应、加成反应、还原反应,但不能发生氧化反应
答案 C
解析 根据橙花叔醇的结构,C原子数为15,O原子数为1,其不饱和度为3,则其H原子
数为15×2+2-3×2=26,则橙花叔醇的分子式为C H O,A错误;芳樟醇的分子式为
15 26
C H O,芳樟醇与橙花叔醇不属于同分异构体,B错误;芳樟醇和橙花叔醇与氢气加成后
10 18
产物的分子式分别是C H O、C H O,两者都属于醇,且分子中只含有1个羟基,碳的连
10 22 15 32
接方式相同,因此芳樟醇和橙花叔醇与氢气加成后的产物互为同系物,C正确;两种有机物
分子中含有的官能团都是碳碳双键和羟基,可以发生取代反应、加成反应、还原反应,碳碳
双键能被酸性高锰酸钾溶液氧化,因此芳樟醇和橙花叔醇都能发生氧化反应,D错误。
3.某有机物的结构简式如图所示,下列说法中不正确的是( )
A.1 mol该有机物和过量的金属钠反应最多可以生成1.5 mol H
2
B.该物质最多消耗Na、NaOH、NaHCO 的物质的量之比为3∶2∶2
3
C.可以用酸性KMnO 溶液检验其中的碳碳双键
4
D.该物质能够在催化剂作用下被氧化为含有—CHO的有机物
答案 C
解析 A项,金属钠可以和羟基、羧基反应生成H,1 mol该有机物中含有1 mol羟基和2
2
mol羧基,故1 mol该有机物与过量的金属钠反应最多可以生成1.5 mol H ,正确;B项,
2
NaOH、NaHCO 均只能与该有机物中的羧基反应,正确;C项,该有机物中羟基和碳碳双
3
键都能使酸性KMnO 溶液褪色,无法用酸性KMnO 溶液检验其中的碳碳双键,错误;D项,
4 4
该有机物中含有—CHOH,可以被氧化为—CHO,正确。
2
4.下表为某有机物与各种试剂的反应现象,则这种有机物可能是( )
试剂 钠 溴水 NaHCO 溶液
3
现象 放出气体 褪色 放出气体A.CH==CH—CH —OH
2 2
B.
C.CH==CH—COOH
2
D.CHCOOH
3
答案 C
解析 A项中的物质不与NaHCO 反应,B项中的物质不与Na、NaHCO 反应,D项中的物
3 3
质不与溴反应。故选C。
课时对点练
A组 基础对点练
题组一 乙酸的结构与性质
1.下列说法不正确的是( )
A.乙醇、乙酸的沸点和熔点都比C H、C H 的沸点和熔点高
2 6 2 4
B.乙酸能和碳酸钠反应生成二氧化碳气体,说明乙酸的酸性强于碳酸
C.乙酸和乙醇生成乙酸乙酯的反应属于酸碱中和反应
D.乙酸分子中虽然有4个氢原子,但乙酸是一元酸
答案 C
解析 乙酸和乙醇生成乙酸乙酯的反应属于酯化反应。
2.下列物质中,能与醋酸发生反应的是( )
①石蕊溶液 ②乙醇 ③乙醛 ④金属铝 ⑤氧化镁 ⑥碳酸钠 ⑦氢氧化铜
A.①③④⑤⑥⑦ B.②③④⑤
C.①②④⑤⑥⑦ D.全部
答案 C
解析 醋酸具有酸的通性,可使石蕊溶液变红色,可与 Al、MgO、NaCO 、Cu(OH) 等发
2 3 2
生反应,可与乙醇发生酯化反应生成乙酸乙酯,但不能与乙醛发生反应。
题组二 酯化反应与实验探究
3.(2018·合肥一中月考)实验室采用如图所示装置制备乙酸乙酯,实验结束后,取下盛有饱
和碳酸钠溶液的试管,再沿该试管内壁缓缓加入1 mL紫色石蕊溶液,发现紫色石蕊溶液存
在于饱和碳酸钠溶液层与乙酸乙酯液层之间(整个过程不振荡试管),下列有关该实验的描述
不正确的是( )A.制备的乙酸乙酯中混有乙酸和乙醇杂质
B.该实验中浓硫酸的作用是催化剂和吸水剂
C.饱和碳酸钠溶液的主要作用是降低乙酸乙酯的溶解度及吸收乙醇、中和乙酸
D.石蕊层为三色环,由上而下的颜色依次是蓝、紫、红
答案 D
解析 A项,因为乙醇、乙酸都易挥发,所以制取的乙酸乙酯中含有乙醇和乙酸杂质,正确;
B项,制取乙酸乙酯的实验中,浓硫酸作催化剂和吸水剂,正确;C项,乙酸乙酯在饱和碳
酸钠溶液中的溶解度小于在水中的溶解度,同时碳酸钠溶液可以吸收乙醇、中和乙酸,正确;
D项,紫色石蕊溶液的上面与乙酸乙酯接触,因乙酸乙酯中混有乙酸,石蕊溶液变红,下面
与饱和NaCO 溶液接触,饱和NaCO 溶液呈碱性,石蕊溶液变蓝,故石蕊层由上而下的颜
2 3 2 3
色依次是红、紫、蓝,错误。
4.下图是分离乙酸乙酯、乙酸和乙醇混合物的实验操作流程图。
在上述实验过程中,所涉及的三次分离操作分别是( )
A.①蒸馏、②过滤、③分液
B.①分液、②蒸馏、③蒸馏
C.①蒸馏、②分液、③分液
D.①分液、②蒸馏、③结晶、过滤
答案 B
解析 乙酸乙酯在饱和碳酸钠溶液中溶解度很小,而乙酸和乙醇易溶于水,所以第一步用分
液的方法分离;然后得到的A中含有乙酸钠和乙醇,由于乙酸钠的沸点高,故第二步用蒸
馏的方法分离出乙醇;第三步,加硫酸将乙酸钠转变为乙酸,再蒸馏得到乙酸。
题组三 乙醇、乙酸性质比较及应用
5.下列物质中可以用来区分乙醇、乙酸和氢氧化钠溶液的试剂是( )
A.金属钠 B.酸性KMnO 溶液
4
C.NaCO 溶液 D.紫色石蕊溶液
2 3
答案 D
解析 金属钠和乙醇、乙酸和氢氧化钠溶液反应都生成氢气,故无法区分,A错误;酸性KMnO 溶液能和乙醇反应,紫红色褪去,但乙酸和氢氧化钠溶液与酸性KMnO 溶液混合均
4 4
无现象,故无法区分,故B错误;NaCO 溶液和乙酸反应会生成CO 气体,但乙醇、NaOH
2 3 2
溶液和NaCO 溶液互溶无现象,故C项无法区分;乙醇和紫色石蕊溶液互溶,无现象,乙
2 3
酸能使紫色石蕊溶液变红色,NaOH溶液能使紫色石蕊溶液变蓝色,故D正确。
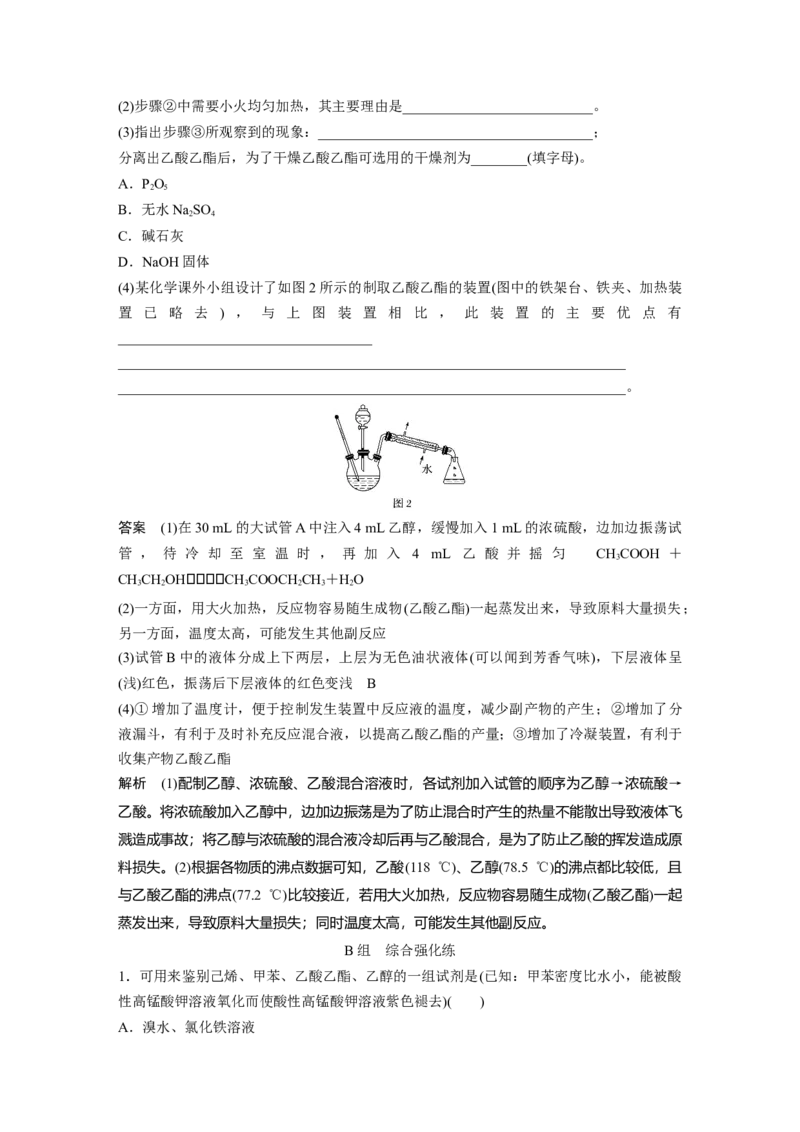
6.某有机物M的结构简式为 ,下列有关M性质的叙述中错误的是(
)
A.M的水溶液呈酸性,能和NaHCO 反应生成CO 气体
3 2
B.M和金属钠完全反应时,二者的物质的量之比为1∶3
C.M和NaOH完全反应时,二者的物质的量之比为1∶3
D.M在浓HSO 作用下,既可以和乙酸反应,又能和乙醇反应
2 4
答案 C
解析 由M的结构简式知,羧基呈酸性,可以和NaHCO 反应,也可以和金属钠及NaOH
3
反应,醇羟基呈中性,只和金属钠反应,而和NaOH不反应,故M和NaOH完全反应时,
二者的物质的量之比应为1∶1,故C错误;羧基及醇羟基可以分别和醇及羧酸发生酯化反
应,故D正确。
7.(2018·海南农垦中学月考)查阅资料可知以下数据:
物质 乙醇 乙酸 乙酸乙酯 浓硫酸
沸点/℃ 78.5 118 77.2 338.0
某学生在实验室制取乙酸乙酯的主要步骤如下:
①在30 mL大试管A中按体积比1∶4∶4配制浓硫酸、乙醇和乙酸的混合溶液。
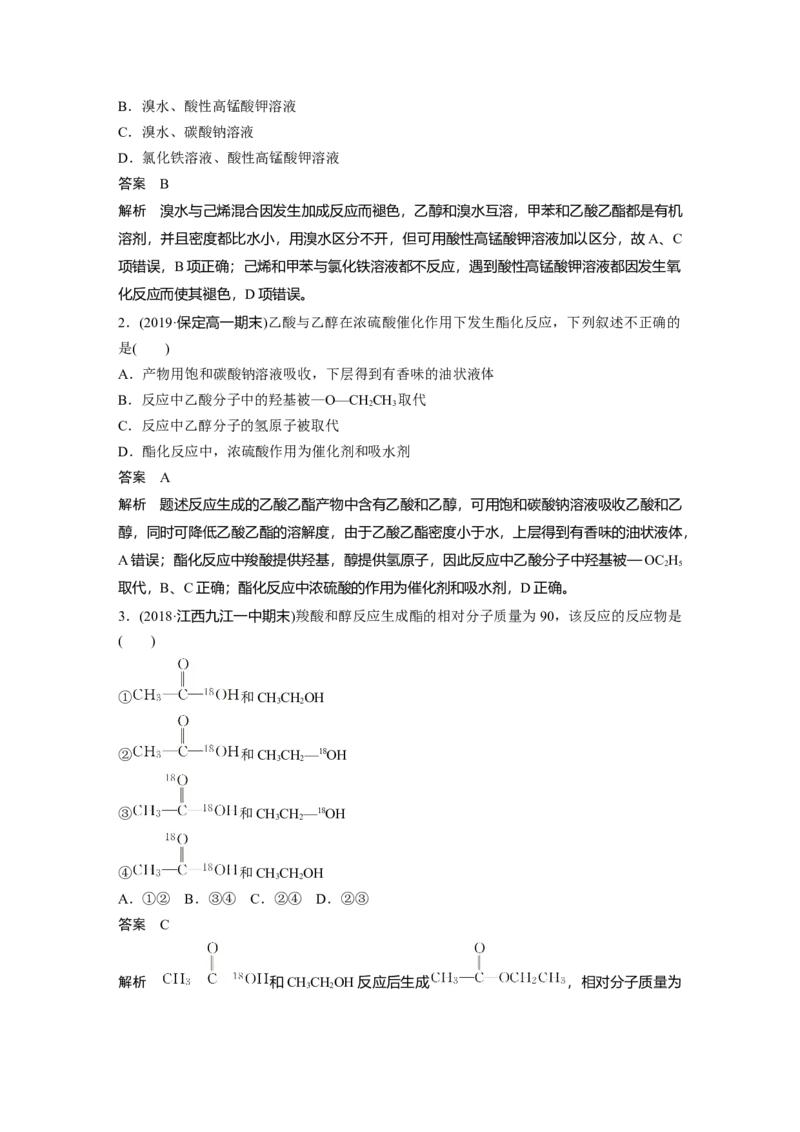
②按如图1所示连接好装置(装置气密性良好),用小火均匀地加热装有混合溶液的大试管A
5~10 min。
③待试管B收集到一定量的产物后停止加热,撤去试管B并用力振荡,然后静置分层。
④分离出乙酸乙酯层,洗涤、干燥。
请根据题目要求回答下列问题:
(1)配制①中混合溶液的主要操作步骤为_______________________________;
写出制取乙酸乙酯的化学方程式:____________________________________。(2)步骤②中需要小火均匀加热,其主要理由是___________________________。
(3)指出步骤③所观察到的现象:_______________________________________;
分离出乙酸乙酯后,为了干燥乙酸乙酯可选用的干燥剂为________(填字母)。
A.PO
2 5
B.无水NaSO
2 4
C.碱石灰
D.NaOH固体
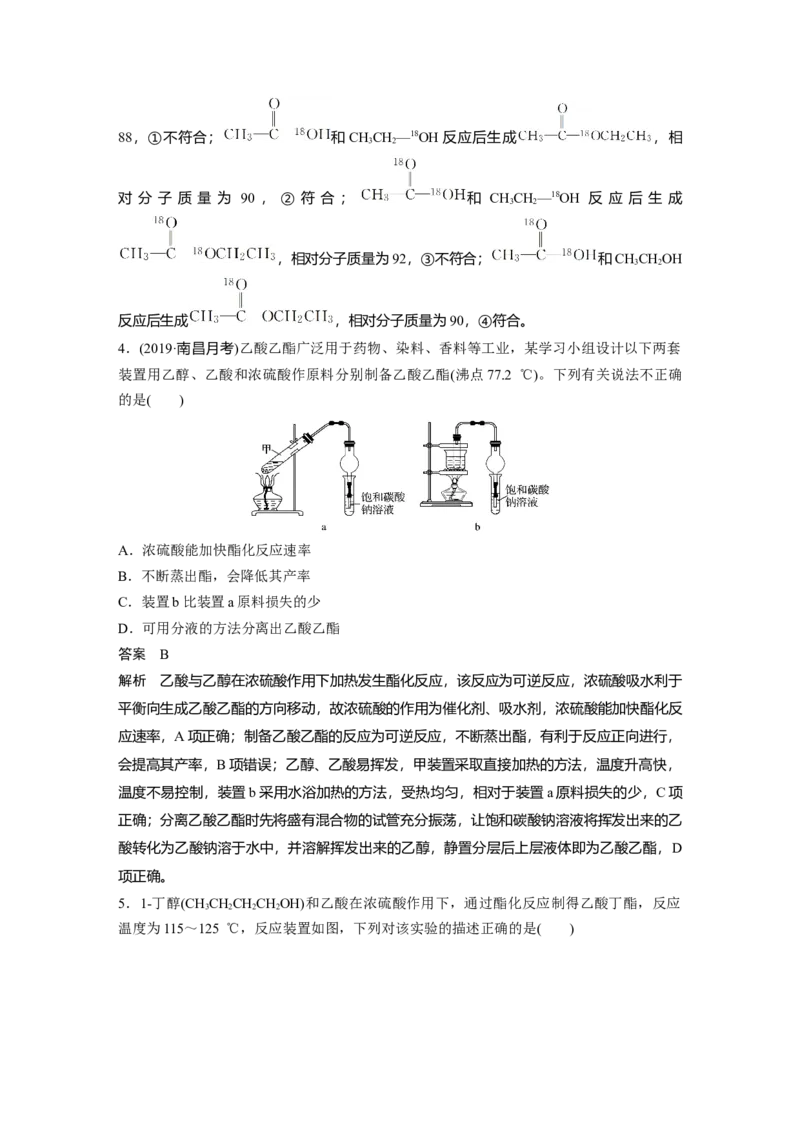
(4)某化学课外小组设计了如图2所示的制取乙酸乙酯的装置(图中的铁架台、铁夹、加热装
置 已 略 去 ) , 与 上 图 装 置 相 比 , 此 装 置 的 主 要 优 点 有
____________________________________
________________________________________________________________________
________________________________________________________________________。
答案 (1)在30 mL的大试管A中注入4 mL乙醇,缓慢加入1 mL的浓硫酸,边加边振荡试
管 , 待 冷 却 至 室 温 时 , 再 加 入 4 mL 乙 酸 并 摇 匀 CHCOOH +
3
CHCHOHCHCOOCH CH+HO
3 2 3 2 3 2
(2)一方面,用大火加热,反应物容易随生成物(乙酸乙酯)一起蒸发出来,导致原料大量损失;
另一方面,温度太高,可能发生其他副反应
(3)试管B中的液体分成上下两层,上层为无色油状液体(可以闻到芳香气味),下层液体呈
(浅)红色,振荡后下层液体的红色变浅 B
(4)①增加了温度计,便于控制发生装置中反应液的温度,减少副产物的产生;②增加了分
液漏斗,有利于及时补充反应混合液,以提高乙酸乙酯的产量;③增加了冷凝装置,有利于
收集产物乙酸乙酯
解析 (1)配制乙醇、浓硫酸、乙酸混合溶液时,各试剂加入试管的顺序为乙醇→浓硫酸→
乙酸。将浓硫酸加入乙醇中,边加边振荡是为了防止混合时产生的热量不能散出导致液体飞
溅造成事故;将乙醇与浓硫酸的混合液冷却后再与乙酸混合,是为了防止乙酸的挥发造成原
料损失。(2)根据各物质的沸点数据可知,乙酸(118 ℃)、乙醇(78.5 ℃)的沸点都比较低,且
与乙酸乙酯的沸点(77.2 ℃)比较接近,若用大火加热,反应物容易随生成物(乙酸乙酯)一起
蒸发出来,导致原料大量损失;同时温度太高,可能发生其他副反应。
B组 综合强化练
1.可用来鉴别己烯、甲苯、乙酸乙酯、乙醇的一组试剂是(已知:甲苯密度比水小,能被酸
性高锰酸钾溶液氧化而使酸性高锰酸钾溶液紫色褪去)( )
A.溴水、氯化铁溶液B.溴水、酸性高锰酸钾溶液
C.溴水、碳酸钠溶液
D.氯化铁溶液、酸性高锰酸钾溶液
答案 B
解析 溴水与己烯混合因发生加成反应而褪色,乙醇和溴水互溶,甲苯和乙酸乙酯都是有机
溶剂,并且密度都比水小,用溴水区分不开,但可用酸性高锰酸钾溶液加以区分,故A、C
项错误,B项正确;己烯和甲苯与氯化铁溶液都不反应,遇到酸性高锰酸钾溶液都因发生氧
化反应而使其褪色,D项错误。
2.(2019·保定高一期末)乙酸与乙醇在浓硫酸催化作用下发生酯化反应,下列叙述不正确的
是( )
A.产物用饱和碳酸钠溶液吸收,下层得到有香味的油状液体
B.反应中乙酸分子中的羟基被—O—CH CH 取代
2 3
C.反应中乙醇分子的氢原子被取代
D.酯化反应中,浓硫酸作用为催化剂和吸水剂
答案 A
解析 题述反应生成的乙酸乙酯产物中含有乙酸和乙醇,可用饱和碳酸钠溶液吸收乙酸和乙
醇,同时可降低乙酸乙酯的溶解度,由于乙酸乙酯密度小于水,上层得到有香味的油状液体,
A错误;酯化反应中羧酸提供羟基,醇提供氢原子,因此反应中乙酸分子中羟基被—OC H
2 5
取代,B、C正确;酯化反应中浓硫酸的作用为催化剂和吸水剂,D正确。
3.(2018·江西九江一中期末)羧酸和醇反应生成酯的相对分子质量为90,该反应的反应物是
( )
① 和CHCHOH
3 2
② 和CHCH—18OH
3 2
③ 和CHCH—18OH
3 2
④ 和CHCHOH
3 2
A.①② B.③④ C.②④ D.②③
答案 C
解析 和CHCHOH反应后生成 ,相对分子质量为
3 288,①不符合; 和CHCH—18OH反应后生成 ,相
3 2
对 分 子 质 量 为 90 , ② 符 合 ; 和 CHCH—18OH 反 应 后 生 成
3 2
,相对分子质量为92,③不符合; 和CHCHOH
3 2
反应后生成 ,相对分子质量为90,④符合。
4.(2019·南昌月考)乙酸乙酯广泛用于药物、染料、香料等工业,某学习小组设计以下两套
装置用乙醇、乙酸和浓硫酸作原料分别制备乙酸乙酯(沸点77.2 ℃)。下列有关说法不正确
的是( )
A.浓硫酸能加快酯化反应速率
B.不断蒸出酯,会降低其产率
C.装置b比装置a原料损失的少
D.可用分液的方法分离出乙酸乙酯
答案 B
解析 乙酸与乙醇在浓硫酸作用下加热发生酯化反应,该反应为可逆反应,浓硫酸吸水利于
平衡向生成乙酸乙酯的方向移动,故浓硫酸的作用为催化剂、吸水剂,浓硫酸能加快酯化反
应速率,A项正确;制备乙酸乙酯的反应为可逆反应,不断蒸出酯,有利于反应正向进行,
会提高其产率,B项错误;乙醇、乙酸易挥发,甲装置采取直接加热的方法,温度升高快,
温度不易控制,装置b采用水浴加热的方法,受热均匀,相对于装置a原料损失的少,C项
正确;分离乙酸乙酯时先将盛有混合物的试管充分振荡,让饱和碳酸钠溶液将挥发出来的乙
酸转化为乙酸钠溶于水中,并溶解挥发出来的乙醇,静置分层后上层液体即为乙酸乙酯,D
项正确。
5.1-丁醇(CHCHCHCHOH)和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应
3 2 2 2
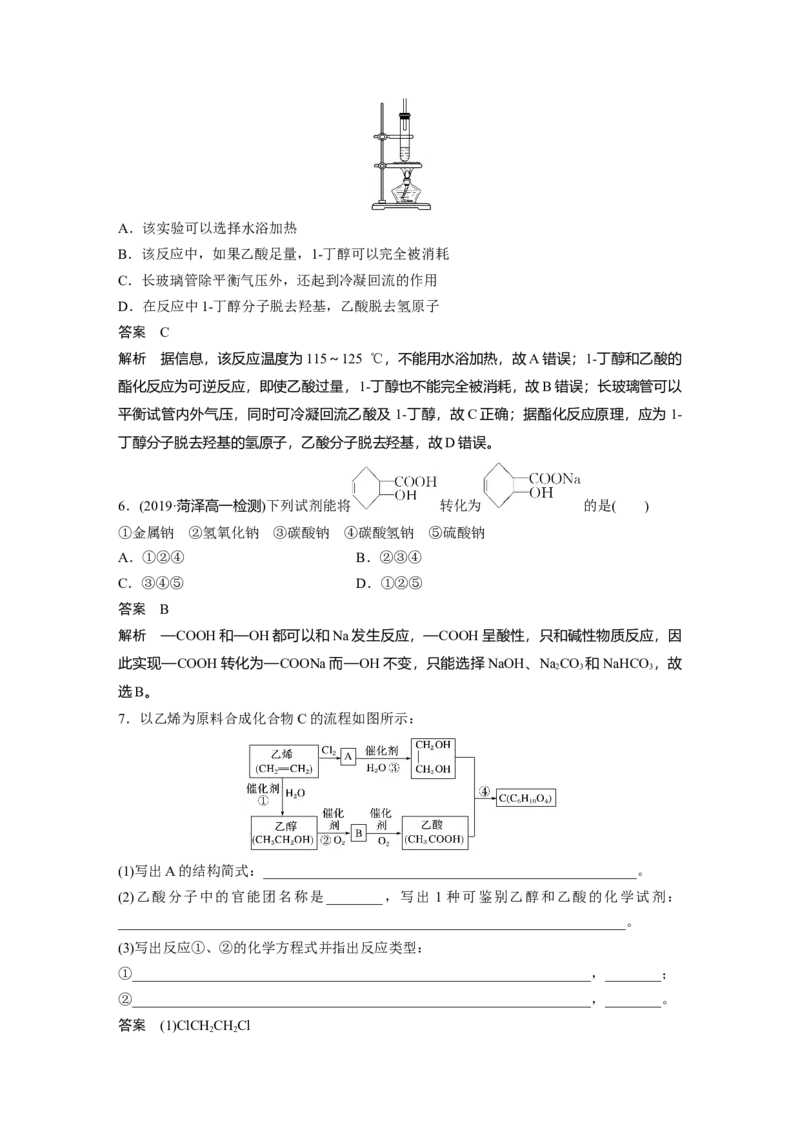
温度为115~125 ℃,反应装置如图,下列对该实验的描述正确的是( )A.该实验可以选择水浴加热
B.该反应中,如果乙酸足量,1-丁醇可以完全被消耗
C.长玻璃管除平衡气压外,还起到冷凝回流的作用
D.在反应中1-丁醇分子脱去羟基,乙酸脱去氢原子
答案 C
解析 据信息,该反应温度为115~125 ℃,不能用水浴加热,故A错误;1-丁醇和乙酸的
酯化反应为可逆反应,即使乙酸过量,1-丁醇也不能完全被消耗,故B错误;长玻璃管可以
平衡试管内外气压,同时可冷凝回流乙酸及 1-丁醇,故C正确;据酯化反应原理,应为1-
丁醇分子脱去羟基的氢原子,乙酸分子脱去羟基,故D错误。
6.(2019·菏泽高一检测)下列试剂能将 转化为 的是( )
①金属钠 ②氢氧化钠 ③碳酸钠 ④碳酸氢钠 ⑤硫酸钠
A.①②④ B.②③④
C.③④⑤ D.①②⑤
答案 B
解析 —COOH和—OH都可以和Na发生反应,—COOH呈酸性,只和碱性物质反应,因
此实现—COOH转化为—COONa而—OH不变,只能选择NaOH、NaCO 和NaHCO ,故
2 3 3
选B。
7.以乙烯为原料合成化合物C的流程如图所示:
(1)写出A的结构简式:_____________________________________________________。
(2)乙酸分子中的官能团名称是________,写出 1 种可鉴别乙醇和乙酸的化学试剂:
________________________________________________________________________。
(3)写出反应①、②的化学方程式并指出反应类型:
①_________________________________________________________________,________;
②_________________________________________________________________,________。
答案 (1)ClCH CHCl
2 2(2)羧基 紫色石蕊溶液(或碳酸钠溶液或其他合理答案)
(3)①CH==CH+HO――→CHCHOH 加成反应
2 2 2 3 2
②2CHCHOH+O――→2CHCHO+2HO 氧化反应
3 2 2 3 2
解析 乙烯含有碳碳双键,与氯气发生加成反应生成A,A的结构简式为ClCH CHCl,A
2 2
与水反应生成乙二醇。乙烯和水发生加成反应生成乙醇,乙醇催化氧化生成乙醛,即B是
乙醛。乙醛再氧化生成乙酸,乙酸与乙二醇发生酯化反应生成 C,结构简式为CHCOOCH
3 2
—CHOOCCH 。
2 3
(1)根据以上分析可知A的结构简式为ClCH CHCl。
2 2
(2)乙酸的官能团是羧基,乙酸显酸性,乙醇为中性,则鉴别乙酸和乙醇的化学试剂可以是
紫色石蕊溶液,也可以是碳酸钠溶液。
8.(2018·江西奉新一中高一期末)A~I是常见有机物,A是烃,E的分子式为C HO ,H为
4 8 2
有香味的油状物质。
已知:CHCHBr+NaOH――→CHCHOH+NaBr
3 2 3 2
(1)0.2 mol A 完 全 燃 烧 生 成 17.6 g CO 和 7.2 g H O , 则 A 的 结 构 简 式 为
2 2
________________________________________________________________________。
(2)D分子中含有官能团的名称为_____________________________________________。
(3)①的反应类型为_________________________________________________________。
(4)G可能具有的性质为________(填字母)。
a.与钠反应 b.与NaOH溶液反应
c.易溶于水
(5)请写出②和⑦的化学方程式:
反应②________________________________________________________________________;
反应⑦________________________________________________________________________。
答案 (1)CH ==CH (2)羧基 (3)加成反应 (4)ac (5)2CH CHOH+O――→2CHCHO+
2 2 3 2 2 3
2HO HOCH CHOH+2CHCOOHCHCOOCH CHOOCCH +2HO
2 2 2 3 3 2 2 3 2
解析 17.6 g CO 的物质的量n(CO)==0.4 mol,7.2 g H O的物质的量n(H O)==0.4 mol,
2 2 2 2
已知A是一种烃,根据元素守恒可知0.2 mol A中n(C)=0.4 mol,n(H)=0.4 mol×2=0.8
mol,则1 mol A中n(C)=2 mol,n(H)=4 mol,则A为CH==CH ,A与水加成生成B,B
2 2
为CHCHOH,则C为乙醛,D为乙酸,乙醇和乙酸发生酯化反应生成E,E为乙酸乙酯;
3 2
乙烯与氢气加成生成I,I为乙烷;乙烯与溴加成生成F,F为1,2-二溴乙烷;1,2-二溴乙烷发
生已知所给的反应生成G,G为乙二醇;乙二醇和乙酸反应生成H,H为二乙酸乙二酯。(1)根据以上分析可知A为乙烯,A的结构简式为CH==CH。
2 2
(2)D为乙酸,乙酸分子中含有羧基。
(3)反应①为CH==CH 与水在一定条件下发生加成反应生成CHCHOH。
2 2 3 2
(4)G 为 HOCH CHOH 。乙 二醇与金属钠反应的化学方程式为 HOCH CHOH +
2 2 2 2
2Na―→NaOCH CHONa+H↑,a正确;醇不能与NaOH溶液反应,b错误;乙二醇易溶
2 2 2
于水,c正确。
(5)反应②:乙醇在Cu作催化剂条件下发生氧化反应,反应的化学方程式为2CHCHOH+
3 2
O― 2―CHCH→O + 2HO , 反 应 ⑦ : HOCH CHOH +
2 3 2 2 2
2CHCOOHCHCOOCH CHOOCCH +2HO。
3 3 2 2 3 2