文档内容
第 2 课时 烷烃的性质
课后篇巩固提升
夯实基础·轻松达标
1.下列有关有机化合物的说法不正确的是( )
A.有机化合物都易燃烧
B.有机化合物中一定含碳元素
C.有机化合物的熔点、沸点一般较低
D.有机化合物使我们的物质世界更加丰富多彩
答案A
解析某些有机物不能燃烧,如CCl 可作灭火剂。
4
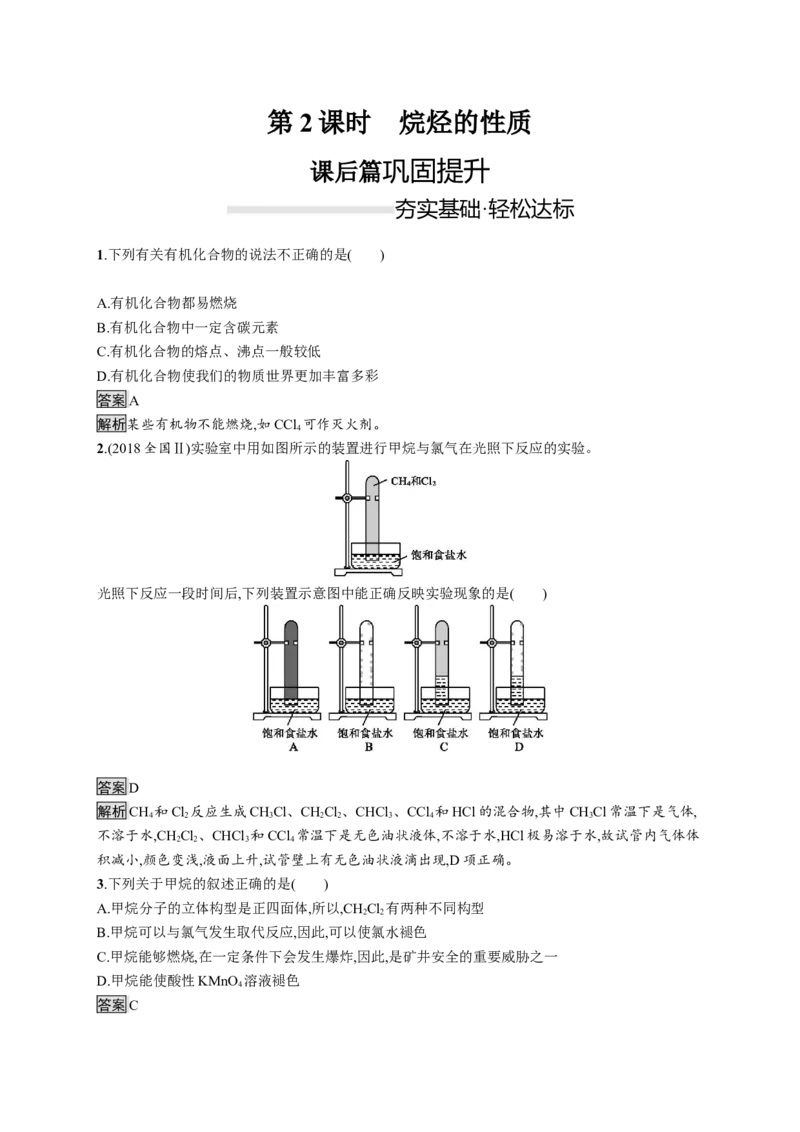
2.(2018全国Ⅱ)实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。
光照下反应一段时间后,下列装置示意图中能正确反映实验现象的是( )
答案D
解析CH 和Cl 反应生成CHCl、CHCl、CHCl 、CCl 和HCl的混合物,其中CHCl常温下是气体,
4 2 3 2 2 3 4 3
不溶于水,CH Cl、CHCl 和CCl 常温下是无色油状液体,不溶于水,HCl极易溶于水,故试管内气体体
2 2 3 4
积减小,颜色变浅,液面上升,试管壁上有无色油状液滴出现,D项正确。
3.下列关于甲烷的叙述正确的是( )
A.甲烷分子的立体构型是正四面体,所以,CH Cl 有两种不同构型
2 2
B.甲烷可以与氯气发生取代反应,因此,可以使氯水褪色
C.甲烷能够燃烧,在一定条件下会发生爆炸,因此,是矿井安全的重要威胁之一
D.甲烷能使酸性KMnO 溶液褪色
4
答案C解析A项,由于甲烷分子是正四面体结构,四个顶点上任意两个氢原子都是相邻关系,故CHCl 只有
2 2
一种构型。B项,CH 能跟氯气在光照下反应,与氯水不反应。D项,CH 比较稳定,不能被酸性KMnO
4 4 4
溶液氧化。
4.鉴别甲烷、一氧化碳和氢气3种无色气体的方法是,将它们( )
A.先后通入溴水和澄清石灰水
B.点燃后罩上涂有澄清石灰水的烧杯
C.点燃,先后罩上干燥的冷烧杯和涂有澄清石灰水的烧杯
D.点燃后罩上涂有澄清石灰水的烧杯,通入溴水
答案C
解析CH、CO和H 与溴水、澄清石灰水都不反应,A项不可选。CH 和CO燃烧都生成CO,B、D
4 2 4 2
项不可选。干燥的冷烧杯可检验燃烧产物中是否有水生成,涂有澄清石灰水的烧杯可检验燃烧产物
中是否有CO 生成。
2
5.下列关于CH 和 的叙述正确的是 ( )
4
A.均能用通式C H 来表示
n 2n+2
B.与所有烷烃互为同分异构体
C.它们物理、化学性质相同
D.通常情况下前者是气体,后者是液体
答案A
解析因二者均为烷烃,都符合通式C H ,A正确;它们与其他烷烃互为同系物,B错误;二者的化学性
n 2n+2
质相似,但物理性质不同,C错误;分子中所含碳原子数小于或等于4的烷烃常温下是气体,D错误。
6.有两种气态烷烃的混合物,在标准状况下,其密度为1.16 g·L-1,则关于此混合物组成的说法正确的是
( )
A.一定有甲烷
B.一定有乙烷
C.可能是甲烷和己烷的混合物
D.可能是乙烷和丙烷的混合物
答案A
解析标准状况下,该混合物的平均摩尔质量为22.4 L·mol-1×1.16 g·L-1=26 g·mol-1,在烷烃中,只有甲烷
的摩尔质量小于26 g·mol-1,所以一定有甲烷,另一种气态烷烃不能确定。
7.取标准状况下的CH 和过量O 的混合气体840 mL点燃,将燃烧后所得的气体混合物用过量碱石灰
4 2
吸收,碱石灰质量增加0.6 g。计算:
(1)经碱石灰吸收后所剩气体的体积(标准状况下)为 。
(2)原混合气体中CH 与O 的体积比为 。
4 2
答案(1)0.336 L (2)1∶4
44
解析(1)由CH+2O CO+2H O可知,完全燃烧后产生的CO 的质量为0.6 g× =0.33 g,即物质的
4 2 2 2 2
800.84 L
量为0.007 5 mol,CH 与O 共有 =0.037 5 mol。由化学方程式CH+2O
4 2 22.4 L·mol-1 4 2
CO+2H O可知,参与反应的混合气体的物质的量为0.007 5 mol(CH )+0.015 mol(O )=0.022 5 mol,故
2 2 4 2
剩余氧气的物质的量为0.037 5 mol-0.022 5 mol=0.015 mol,即经碱石灰吸收后所剩气体的体积(标准
状况下)为0.015 mol×22.4 L·mol-1=0.336 L。
(2)原混合气体中CH 与O 的物质的量之比为0.007 5 mol∶(0.015+0.015)mol=0.007
4 2
5∶0.03=1∶4,由相同条件下气体的物质的量之比等于气体的体积比可知,原混合气体中CH 与O 的
4 2
体积比为1∶4。
提升能力·跨越等级
1.下列叙述错误的是( )
A.在通常情况下,甲烷与强酸、强碱、强氧化剂都不反应
B.甲烷化学性质比较稳定,不能被任何氧化剂氧化
C.甲烷与氯气反应无论生成CHCl、CHCl、CHCl 还是CCl ,都属于取代反应
3 2 2 3 4
D.甲烷的四种有机取代物都不溶于水
答案B
解析甲烷的性质比较稳定,在通常情况下,不与强酸、强碱、强氧化剂反应,但甲烷能在空气中燃烧,A
正确,B错误;甲烷在光照条件下与氯气发生取代反应,生成四种有机产物,分别是CHCl、CHCl、
3 2 2
CHCl 和CCl ,且均不溶于水,故C、D均正确。
3 4
2.若1 mol某链状烷烃燃烧后,测得产物中含有m mol CO 和n mol CO,则该烷烃分子中氢原子的个数
2
为 ( )
A.m+n B.2(m+n)
C.m-n+2 D.2(n+m+1)
答案D
解析由题意可知,该链状烷烃分子中含有(m+n)个碳原子,根据链状烷烃的通式可得该链状烷烃分子
中含有2(m+n+1)个氢原子。
3.下列说法正确的是( )
A.碳碳间以单键结合,碳原子剩余价键全部与氢原子结合的烃一定是饱和链烃
B.分子式符合C H 的碳氢化合物一定是烷烃
n 2n+2
C.正戊烷分子中所有的碳原子均在同一条直线上
D.碳、氢原子个数比为1∶3的烷烃有两种
答案B
解析A项中,环烷烃也符合要求,但它不是链烃,属于环烃;C项中,由碳原子的成键方式和键角特征知,
正戊烷中碳原子呈锯齿状排列,因此所有碳原子不在同一直线上;D项中,分子中n(C)∶n(H)=1∶3的
烷烃必为C H,一定是乙烷。
2 6
4.燃烧0.1 mol两种气态碳氢化合物的混合物,生成3.58 L CO (标准状况)和3.6 g HO,则混合气体中(
2 2
)
A.一定有甲烷 B.一定有乙烷C.一定无甲烷 D.一定有丙烷
答案A
3.58 L 3.6 g
解析生成的n(CO)= =0.16 mol,生成的n(H O)= =0.2 mol,因此该
2 22.4 L·mol-1 2 18 g·mol-1
气态混合物的平均分子组成为C H,而分子中碳原子数小于1.6的碳氢化合物只有甲烷,故另一种碳
1.6 4
氢化合物应为分子中氢原子数为4、碳原子数大于或等于2的气态碳氢化合物。
5.在常温、常压下,取下列四种气态烷烃各1 mol,分别在足量的氧气中燃烧,消耗氧气最多的是( )
A.CH B.C H C.C H D.C H
4 3 8 4 10 2 6
答案C
y y
解析设此气态烷烃的分子式为CH,其完全燃烧的化学方程式为CH+(x+ )O xCO+ HO,则1
x y x y 2 2 2
4 2
y y
mol烷烃完全燃烧时耗氧量为(x+ ) mol,将上述选项中分子式中相应数值分别代入(x+ ) mol,比较
4 4
可知C H 耗氧量最多。
4 10
6.(1)乙烷的电子式为 ,分子式为C H 的链状烷烃中m为 ,分子式
m 20
为C H 的链状烷烃中n为 ,与CO 密度(同温同压)相同的气态链状烷烃的分子式为 。
8 n 2
(2)若CH、C H、C H、C H 四种烷烃的质量均为1 g,在足量O 中燃烧,消耗O 最多的是
4 2 6 3 8 4 10 2 2
。
H H
答案(1) ·· ·· H 9 18 C H (2)CH
H· C · C · 3 8 4
· · ·
·· ··
H H
解析(1)根据链状烷烃通式为C H 可求出m为9,n为18,密度与CO 相同的气态链状烷烃的相对分
n 2n+2 2
子质量为44,由14n+2=44可求出n为3,即分子式为C H。
3 8
y y
(2)若四种烷烃的质量同为1 g,消耗O 的多少取决于CH 中“ ”的大小,“ ”的值越大,消耗O
2 x y 2
x x
越多,此题中消耗O 最多的是CH。
2 4
贴近生活·拓展创新
“立方烷”是一种新合成的碳氢化合物,其分子为正方体结构,其碳架结构如图所示。
(1)立方烷的分子式为 。
(2)该立方烷与氯气发生取代反应,生成的一氯代物有 种,生成的二氯代物有 种。
(3)若要使1 mol“立方烷”的所有氢原子全部被氯原子取代,需要 mol氯气。
答案(1)C H (2)1 3 (3)8
8 8
解析(1)1个立方烷分子中有8个碳原子,分布在立方烷各顶点。氢原子数目可根据碳原子最多形成4
个价键来考虑。由于每个碳原子与其他碳原子均已形成3个C—C键,故只能与1个氢原子结合。(2)由于该分子结构是正方体,8个顶点的位置全部一样,所以立方烷只有一种一氯代物。根据正
方体中两顶点的相对位置只有3种情况,所以二氯代物应有3种。
(3)根据取代反应的特点,完全取代8 mol H原子,需8 mol Cl原子,同时生成8 mol氯化氢,故共需
要8 mol Cl。
2