文档内容
2019-2020学年高一化学期末复习专项提升卷(人教版2019必修第二册)
专项 01 常见物质间的转化关系
1.(2020·山东省微山县第二中学高一月考)下列说法正确的是( )
A.单质 氧化物 酸或碱 盐,铁单质可以按上述关系进行转化
B.若a、b、c分别为S、SO 、HSO ,则可以通过一步反应实现如图所示的转化
3 2 4
C.太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置
D.单质硅常用于制造光导纤维
【答案】C
【解析】A.Fe与氧气反应生成氧化铁或四氧化三铁,但氧化铁或四氧化三铁与水不反应,所以氧化物−→
水酸或碱不能实现,故A错误;
B. 若a、b、c分别为S、SO 、HSO ,b→c不能一步实现,故B错误;
3 2 4
C.硅元素位于第三周期第ⅣA族元素,位于金属元素与非金属元素的交界处,故C正确;
D.二氧化硅常用来制造光导纤维,故D错误;
故答案选:C。
2.(2020·北京和平街第一中学高一期中)研究表明,氮氧化物(NO )和二氧化硫在形成雾霾时与大气中的
x
氨有关,其转化关系如图所示:
下列关于雾霾及其形成的叙述中,不正确的是
A.与燃料燃烧有关 B.涉及氧化还原反应、化合反应等
C.雾霾中含有NH NO 和(NH )SO D.NH 是形成无机颗粒物的催化剂
4 3 4 2 4 3
【答案】D
【解析】A.根据图示,燃料燃烧产生的颗粒物形成雾霾,则雾霾形成与燃料燃烧有关,故A正确;
B.如图所示,S元素的化合价升高,化合价发生变化,属于氧化还原反应,三氧化硫和水反应生成硫酸,属于化合反应,则B正确;
C.根据图示,NH NO 和(NH )SO 构成无机颗粒物,无机颗粒物形成雾霾,故C正确;
4 3 4 2 4
D.根据NH 参与反应转化为铵盐,为反应物,不是催化剂,故D错误;
3
答案选D。
3.(2020·安徽省屯溪一中高一开学考试)如图所示是一系列含硫化合物的转化关系(反应中生成的水已
略去),其中说法正确的是
A.反应①说明SO 具有漂白性,反应②说明SO 具有酸性
2 2
B.反应②中生成物n(NaSO ):n(NaHSO)=1:1时,则反应物n(SO ):n(NaOH)=1:2
2 3 3 2
C.反应③④⑤均属于氧化还原反应
D.工业上可利用反应②和反应④回收SO
2
【答案】D
【解析】A.反应①中先变蓝后褪色显然是因为KIO 的还原产物先是I 后是I-,体现了SO 具有还原性,
3 2 2
反应②属于酸性氧化物和碱的反应,体现了SO 具有酸性,故A错误;
2
B.根据元素守恒,当n(NaSO ):n(NaHSO)=1:1时,n(SO ):n(NaOH)=2:3,故B错误;
2 3 3 2
C.反应④是非氧化还原反应,故C错误;
D.反应②吸收了二氧化硫,反应④放出了SO ,可以通过2个反应回收二氧化硫,故D正确;
2
故选D。
4.(2020·安徽师范大学附属中学高一期中)已知氨气可以与灼热的氧化铜反应得到氮气和金属铜,用如
图中的装置可以实现该反应。实验时C中粉末逐渐变为红色,D中出现无色液体。下列有关说法正确的是
( )A.装置C中氧化剂和还原剂的物质的量之比为2:3
B.装置B中加入的物质可以是碱石灰或无水氯化钙
C.装置D中液体可以使干燥的红色石蕊试纸变蓝
D.装置A中加入的固体,可以是NH HCO 或NH Cl
4 3 4
【答案】C
【解析】A. 装置C中氨气可以与灼热的氧化铜反应得到氮气和金属铜,N元素化合价由-3升高为0,铜元
素化合价由+2降低为0,根据得失电子守恒,氧化剂和还原剂的物质的量之比为3:2,故A错误;
B. 无水氯化钙能吸收氨气(与氨气反应),所以装置B中加入的物质可以是碱石灰,不能是无水氯化钙,
故B错误;
C. 装置D中液体是氨水,可以使干燥的红色石蕊试纸变蓝,故C正确;
D. NHCl加热分解为氨气和氯化氢,试管口温度降低,氯化氢和氨气化合生成氯化铵,不能用加热氯化铵
4
来制备氨气,故D错误;
故选C。
5.制备硅单质时,主要化学反应如下:
①SiO+2C Si+2CO↑ ②Si+2Cl SiCl ③SiCl +2H Si+4HCl
2 2 4 4 2
下列对上述三个反应的叙述中,不正确的是
A.①③为置换反应
B.①②③均为氧化还原反应
C.②为化合反应
D.三个反应的反应物中硅元素均被还原
【答案】D
【解析】A、①属于置换反应、③属于置换反应,故A不符合题意;
B、这三个反应方程式中都有元素化合价升降,所以都属于氧化还原反应,故B不符合题意;
C、②由两种物质生成一种物质,所以为化合反应,故C不符合题意;D、①中Si元素得电子被还原、②中Si元素失电子被氧化、③中Si元素得电子被还原,故D符合题意。
6.(2020·甘肃省张掖市第二中学高一开学考试)A、B、C是中学化学常见的三种物质,它们之间的相互
转化关系如图(部分反应条件及产物略去)。
(1)若A是一种黄色单质固体,则B→C的化学方程式为____。
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为____,试用化学方程式表示该物质与水的反应
____。将C长期露置于空气中,最后将变成物质D,D的化学式为____。
(3)若C是红棕色气体,A是一种能使湿润的红色石蕊试纸变蓝的气体。请结合所学知识,写出实验室制取
A的化学方程式____。
【答案】(1)2SO +O 2SO
2 2 3
(2)过氧化钠 2NaO+2H O=4NaOH+O NaCO
2 2 2 2 2 3
(3)2NH Cl+Ca(OH) CaCl +2NH↑+2H O
4 2 2 3 2
【解析】
【分析】 (1)若A是一种黄色单质固体,为S,硫被氧气氧化变为二氧化硫,二氧化硫被氧气氧化生成三
氧化硫,则B→C的化学方程式为2SO +O 2SO ;
2 2 3
(2)若A是一种活泼金属,C是淡黄色固体,则C为过氧化钠,A为金属钠,过氧化钠与水反应生成氢氧化
钠和氧气,其化学方程式表示该物质与水的反应2NaO+2H O=4NaOH+O ,将过氧化钠长期露置于空气中,
2 2 2 2
过氧化钠和二氧化碳反应生成碳酸钠,则D的化学式为NaCO;
2 3
(3)若C是红棕色气体,A是一种能使湿润的红色石蕊试纸变蓝的气体,则A为氨气,B为一氧化氮,C为
二氧化氮,实验室制取氨气用氯化铵和氢氧化钙加热反应,其化学方程式2NH Cl+Ca(OH)
4 2
CaCl +2NH↑+2H O。
2 3 2
7.(2020·阜新市第二高级中学高一月考)非金属单质A经下图所示的过程可转化为含氧酸D,已知D为
强酸,请回答下列问题:(1)若A在常温下是固体,B是能使品红溶液褪色的有刺激性气味的无色气体:
①D的化学式:_________;
②在工业生产中,B气体大量排放,被雨水吸收后形成____________污染环境。
(2)若A在常温下为气体,C是红棕色气体。
①C的化学式为:_________;
②D的浓溶液在常温下可与铜反应并生成C气体,该反应的化学方程式为:___________,该反应___(填
“属于”或“不属于”)氧化还原反应。
【答案】(1)H SO 酸雨
2 4
(2)NO Cu+4HNO (浓)=Cu(NO)+2NO↑+2H O 属于
2 3 3 2 2 2
【解析】 (1)A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体,则A为S单质,B为
SO ,C为SO ,D为HSO 。
2 3 2 4
①由以上分析可知D是硫酸,化学式为HSO ,故答案为:HSO ;
2 4 2 4
②在工业生产中大量排放的SO 气体被雨水吸收后形成了酸雨而污染了环境,故答案为:酸雨;
2
(2)若A在常温下为气体,C是红棕色的气体,则A应为N,B为NO,C为NO ,D为HNO。
2 2 3
①由以上分析可知C为NO ,故答案为:NO ;
2 2
②D的浓溶液在常温下可与铜反应并生成C气体,反应的化学方程式为
Cu+4HNO (浓)=Cu(NO)+2NO↑+2H O,该反应中Cu的化合价升高,N的化合价降低,属于氧化还原反应,
3 3 2 2 2
故答案为:Cu+4HNO (浓)=Cu(NO)+2NO↑+2H O;属于。
3 3 2 2 2
【点睛】
解答本题的关键是物质的颜色和框图中的“连续氧化”特征,也是解答本题的突破口。本题的易错点为A的
判断,要注意A属于非金属单质。
8.A、B、C、D、E代表的物质为单质或化合物,它们之间的相互转化关系如图所示。A为地壳中含量仅
次于氧的非金属元素的单质,其晶体结构与金刚石相似。
请回答:
(1)单质A的化学式为________,它的最高化合价为________。(2)B 的 化 学 式 为 ________ , B 和 碳 反 应 生 成 A 和 E 的 化 学 方 程 式 是
_______________________________________________________________。
(3)C的化学式为________,D的化学式为________。
【答案】(1)Si +4
(2)SiO SiO+2CSi+2CO↑
2 2
(3)CaSiO NaSiO
3 2 3
【解析】这是一道关于元素及其化合物的推断题,其中“A为地壳中含量仅次于氧的非金属元素的单质”
是该题的“题眼”。由该“题眼”可知 A是Si。分析题图,结合B能生成C、D、E,可以推出B是
SiO,E是CO,C是CaSiO ,D是NaSiO。
2 3 2 3
9.(2020·威远县连界一中高一月考)燃煤的烟气中含有 SO ,为了治理雾霾天气,工厂采用多种方法实
2
现烟气脱硫。
Ⅰ.(1)“湿式吸收法”利用吸收剂与 SO 发生反应从而脱硫。下列试剂中适合用作该法吸收剂的是_____(填
2
字母序号)。
a. 石灰乳 b.CaCl 溶液
2
(2)某工厂利用含 SO 的烟气处理含Cr O2-的酸性废水,吸收塔中反应后的铬元素以Cr3+形式存在,具体
2 2 7
流程如下:
①用 SO 处理含铬废水时,利用了 SO 的_____性。
2 2
②吸收塔中发生反应的离子方程式为_____。
Ⅱ.石灰-石膏法和烧碱法是常用的烟气脱硫法。石灰-石膏法的吸收反应为Ca(OH) +SO= CaSO↓+H O。吸
2 2 3 2
收产物亚硫酸钙由管道输送至氧化塔氧化,反应为2CaSO+O +4H O =2CaSO ·2H O。其流程如图:
3 2 2 4 2
烧碱法的吸收反应为2NaOH+SO =Na SO +H O。该法的特点是氢氧化钠碱性强、吸收快、效率高。其流程
2 2 3 2
如图:已知:
试剂 Ca(OH) NaOH
2
价格(元/kg) 0.36 2.9
吸收 SO 的成本(元/mol) 0.027 0.232
2
(3)石灰-石膏法和烧碱法相比,石灰-石膏法的优点是_______,缺点是_______。
(4)某学习小组在石灰-石膏法和烧碱法的基础上,设计一个改进的、能实现物料循环的烟气脱硫方案,流
程图中的甲、乙、丙各是_____、_____、_____(填化学式)
【答案】(1)a
(2)还原 3SO +Cr O2-+2H+=2Cr3++3SO2-+H O
2 2 7 4 2
(3)原料便宜,成本低 吸收慢,效率低
(4)NaOH Ca(OH) NaSO
2 2 3
【解析】Ⅰ(1)二氧化硫与氯化钙不能发生反应,而与氢氧化钙可以反应生成亚硫酸钙,因为氢氧化钙
溶解度不大,所以用石灰乳来吸收二氧化硫,故答案为:a;
(2)①重铬酸根具有强氧化性,二氧化硫具有还原性,则可以用 SO 处理含铬废水,故答案为:还原;
2
②吸收塔中为二氧化硫与重铬酸根发生氧化还原反应,其发生反应的离子方程式为3SO +Cr O2-+2H+=2Cr3+
2 2 7
+3SO2-+H O,故答案为:3SO +Cr O2-+2H+=2Cr3++3SO2-+H O;
4 2 2 2 7 4 2
Ⅱ(3)对比两个流程可知,基本反应原理都为二氧化硫与碱发生反应,氢氧化钙原料廉价易得,成本低,
但氢氧化钙溶解度不大,吸收慢,效率低,故答案为:原料便宜,成本低;吸收慢,效率低;
(4)分析流程并对比前两个流程可知,该流程的目的是改进前两个流程的缺点,即氢氧化钙吸收效率低,
应用吸收效率较高的氢氧化钠,则甲为氢氧化钠,又氢氧化钠成本高,需要循环利用,则可用氢氧化钙制
备氢氧化钠,则乙为氢氧化钙,由此可推知丙为亚硫酸钠,亚硫酸钠与氢氧化钙可以发生复分解反应生成
氢氧化钠和亚硫酸钙,实现氢氧化钠的再生,降低成本,故答案为:NaOH;Ca(OH) ;NaSO 。
2 2 3
10.(2020·四川省射洪中学高一月考)研究氮的循环和转化对生产、生活有重要的价值。I.(1)写出实验室制备氨气的化学方程式________ 。
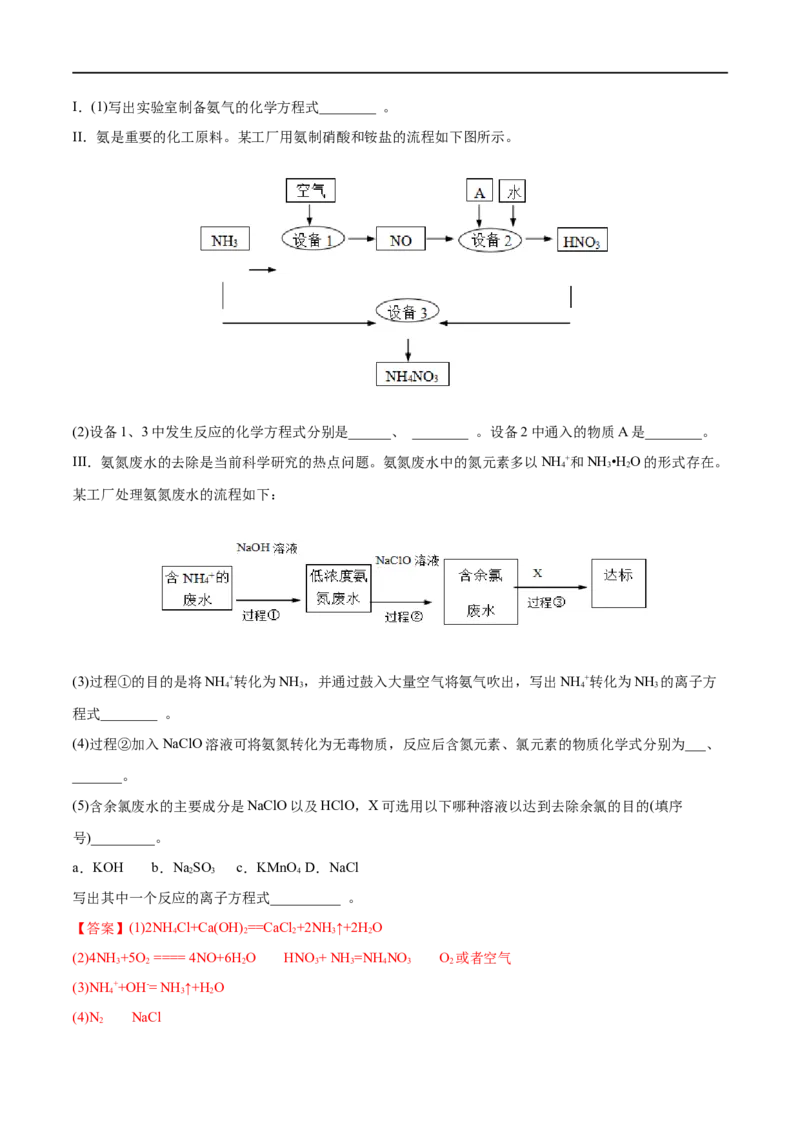
II.氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如下图所示。
(2)设备1、3中发生反应的化学方程式分别是______、 ________ 。设备2中通入的物质A是________。
III.氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以NH +和NH •H O的形式存在。
4 3 2
某工厂处理氨氮废水的流程如下:
(3)过程①的目的是将NH +转化为NH ,并通过鼓入大量空气将氨气吹出,写出NH +转化为NH 的离子方
4 3 4 3
程式________ 。
(4)过程②加入NaClO溶液可将氨氮转化为无毒物质,反应后含氮元素、氯元素的物质化学式分别为___、
_______。
(5)含余氯废水的主要成分是NaClO以及HClO,X可选用以下哪种溶液以达到去除余氯的目的(填序
号)_________。
a.KOH b.NaSO c.KMnO D.NaCl
2 3 4
写出其中一个反应的离子方程式__________ 。
【答案】(1)2NH Cl+Ca(OH) ==CaCl +2NH↑+2H O
4 2 2 3 2
(2)4NH +5O ==== 4NO+6H O HNO+ NH =NHNO O 或者空气
3 2 2 3 3 4 3 2
(3)NH ++OH-= NH ↑+H O
4 3 2
(4)N NaCl
2(5)b
(6)SO 2-+ClO-= SO 2-+Cl-或者SO 2-+HClO= SO 2-+Cl-+H+
3 4 3 4
【解析】I.(1)实验室用NH Cl和Ca(OH) 制备氨气,其反应的化学方程式为:
4 2
2NH Cl+Ca(OH) ==CaCl +2NH↑+2H O。答案:2NH Cl+Ca(OH) ==CaCl +2NH↑+2H O。
4 2 2 3 2 4 2 2 3 2
II.(2)设备1中是NH 和O 发生反应,化学方程式为4NH +5O ==== 4NO+6H O;设备II中是HNO 和
3 2 3 2 2 3
NH 发生反应,发生反应的化学方程式是HNO+ NH =NHNO 。设备2中发生的反应为:4NO+O +H O=4
3 3 3 4 3 2 2
HNO,所以通入的物质A是O 或者空气。答案:4NH +5O ==== 4NO+6H O;HNO+ NH =NHNO ;O 或
3 2 3 2 2 3 3 4 3 2
者空气。
III.(3)过程①的目的是将NH +转化为NH ,并通过鼓入大量空气将氨气吹出,使NH +转化为NH ,反应
4 3 4 3
的离子方程式为:NH ++OH-= NH ↑+H O 。答案:NH ++OH-= NH ↑+H O。
4 3 2 4 3 2
(4)过程②加入NaClO溶液可将氨氮转化为无毒物质,反应的方程式为:3NaClO+ 2NH =3NaCl+N
3 2
+3H O,所以含氮元素、氯元素的物质化学式为N 、NaCl 。 答案:N ;NaCl。
2 2 2
(5)含余氯废水的主要成分是NaClO和HClO,要除去需加入还原性物质NaSO ,反应的离子方程式为:
2 3
SO 2-+ClO-= SO 2-+Cl-和SO 2-+HClO= SO 2-+Cl-+H+。答案:b;SO 2-+ClO-= SO 2-+Cl-或SO 2-+HClO= SO 2-
3 4 3 4 3 4 3 4
+Cl-+H+。
11.(2020·河北省隆化存瑞中学高一期中)由三种短周期非金属元素形成的常见单质A、B、C,在一定
条件下有如下反应:A+B→甲(气) ,B+C→乙(气),请根据不同情况回答下列问题:
(1)若标准状况下A、B、C、甲、乙均为气体,且甲和乙化合生成固体丙时有白烟产生。
①丙的化学式是 _________ ,丙中含有的化学键类型为 ______________
②工厂常用气体甲检验装有气体C的管道是否泄漏,请写出该反应的化学方程式 ______________
(2)若常温下B为固体,A、C为气体且气体乙有刺激性气味,甲在空气中充分燃烧可生成乙。
①乙的化学式是 ___________
②向氢氧化钠溶液中通人过量的乙,所发生反应的离子方程式是 ________________________
③将乙与(1)中某单质的水溶液充分反应可生成两种强酸,该反应的化学方程式是___________________
【答案】(1)NH Cl 离子键、极性共价键 8NH +3Cl=N +6NHCl
4 3 2 2 4
(2) SO SO +OH-=HSO - SO +Cl+2H O=2HCl+H SO
2 2 3 2 2 2 2 4
【解析】【分析】(1)若在标准状况下A、B、C、甲、乙均为气体,且甲和乙化合生成固体丙时有白烟
产生,应是氯化氢与氨气反应生成氯化铵,则丙为NH Cl,甲、乙分别为HCl、NH 中的一种,结合转化
4 3
关系可知B为H,A、C分别是Cl、N 的一种。
2 2 2
(2)若常温下B为固体,A、C为气体,且气体乙有刺激性气味,甲在空气中充分燃烧可生成乙,结合转化关系可推知,B为S、A为H、C为O、甲为HS、乙为SO 。
2 2 2 2
【详解】(1)①丙为氯化铵,其化学式为NH Cl,NH Cl中铵根离子与氯离子之间是离子键,铵根离子中
4 4
氮原子与氢原子之间是极性共价键,所以化学键类型为离子键、极性共价键,故答案为:NH Cl;离子键、
4
极性共价键。
②甲是HCl、NH 中的一种,C分别是Cl、N 的一种,工厂常用NH 检验装有Cl 的管道是否泄漏,则甲
3 2 2 3 2
是NH ,C是Cl,其反应的化学方程式:8NH +3Cl=N +6NHCl,故答案为:8NH +3Cl=N +6NHCl。
3 2 3 2 2 4 3 2 2 4
(2)①乙是二氧化硫,其化学式是SO ,故答案为:SO 。
2 2
②乙为SO ,氢氧化钠溶液中通入过量的SO ,其化学反应方程式为:SO +NaOH=NaHSO ,离子反应方
2 2 2 3
程式为:SO +OH-=HSO - ,故答案为:SO +OH-=HSO - 。
2 3 2 3
③乙为SO ,与Cl 的水溶液充分反应可生成两种强酸,即盐酸和硫酸,其化学反应化学方程式是
2 2
SO +Cl+2H O=2HCl+H SO ,故答案为:SO +Cl+2H O=2HCl+H SO 。
2 2 2 2 4 2 2 2 2 4
12.(2020·湖北省鄂州高中高一月考)X、Y、Z 是中学化学常见的三种物质,它们之间的相互转化关系
如下(X、Y、Z、E、F 为英文字母,部分反应条件及产物略去)
I.若Y是一种易溶于水,且能使品红溶液褪色的无色刺激性气味的气体。
(1)Y气体的大量排放会形成酸雨,在工业上可以用足量氨水吸收,化学方程式为_____。
(2)Z的水溶液可以制得某种强酸 E。实验室用 98%的浓 E(ρ = 1.84g·cm−3)溶液配制l.5mol·L−1稀 E 溶
液240 mL。
① 制该稀 E 溶液需要使用的玻璃仪器有胶头滴管、量筒、烧杯、玻璃棒 和_____ ;
II.若Z是淡黄色固体粉末。
在呼吸面具或潜水艇中由Z和 CO 制备氧气的化学反应方程式为_____。
2
III.若Z是红棕色气体。
(1)试写出 Z 与水反应制备另一种强酸 F 的化学方程式_____。
(2)2.0g铜镁合金完全溶解于100mL 密度为 1.40g·mL−1质量分数为 63%的浓F溶液中,得到Z 和
NO(Z和NO 均为浓F 溶液的还原产物)的混合气体1792mL(标准状况),向反应后的溶液中加入
2 4 2 4
1.0mol·L−1NaOH 溶液,当金属离子全部沉淀,得到3.7g沉淀。则合金中铜与镁的物质的量之比为_____,
加入 NaOH 溶液的体积为_____ mL 。
【答案】2NH HO+SO =(NH)SO +H O 250mL容量瓶 2NaO+2CO =2Na CO+O
3 2 2 4 2 3 2 2 2 2 2 3 2
3NO +H O=2H⋅NO +NO 2:3 1300
2 2 3【解析】I.(1)根据分析,Y为SO ,SO 的大量排放会形成酸雨,在工业上可以用足量氨水吸收,生成亚
2 2
硫酸铵和水,其反应的化学方程式为:2NH HO+SO =(NH)SO +H O,故答案为:
3 2 2 4 2 3 2
2NH HO+SO =(NH)SO +H O。 ⋅
3 2 2 4 2 3 2
(2)⋅①二氧化硫氧化生成三氧化硫,三氧化硫溶于水得硫酸,E是硫酸。实验室用98%浓硫酸
(ρ=1.84mgcm−3)溶液配制1.5molL−1稀硫酸溶液240mL,依据配制溶液的步骤可知,需用的玻璃仪器有胶
头滴管、量⋅ 筒、烧杯、玻璃棒、⋅250mL容量瓶,故答案为:250mL容量瓶。
II. 根据分析,Z为NaO,在呼吸面具或潜水艇中NaO 和CO 制备O 的化学反应方程式为:
2 2 2 2 2 2
2NaO+2CO =2Na CO+O ,故答案为:2NaO+2CO =2Na CO+O 。
2 2 2 2 3 2 2 2 2 2 3 2
III.(1) Z为NO ,X为N 或NH ,Y为NO,NO 与HO反应生成HNO 和NO,其化学反应方程式为:
2 2 3 2 2 3
3NO +H O=2HNO +NO,故答案为:3NO +H O=2HNO +NO。
2 2 3 2 2 3
(2)F为HNO,金属离子全部沉淀时,得到3.7g沉淀为氢氧化铜和氢氧化镁,所以沉淀中氢氧根离子的
3
质量为3.7g−2g=1.7g,氢氧根离子的物质的量为: ,根据电荷守恒可知,金属提
供的电子的物质的量等于氢氧根离子的物质的量,设铜、镁合金中Cu、Mg的物质的量分别为xmol、
ymol,则: ,计算得出: ,所以合金中铜与镁的物质的量之比是0.02:
0.03=2:3;标准状况下,NO 和NO 混合气体的物质的量为: ,设二氧
2 2 4
化氮的物质的量为amol,则四氧化二氮的物质的量为(0.08−a)mol,根据电子转移守恒可知,
a×1+(0.08−a)×2×1=0.1,计算得出:a=0.06mol,则NO 的物质的量为0.02mol,根据钠离子守恒可知,氢
2 4
氧化钠的物质的量等于反应后溶液中硝酸钠的物质的量,根据氮元素守恒可知,硝酸钠的物质的量为:
−0.06mol−0.02mol×2=1.3mol,所以需要氢氧化钠溶液的体积为:,故答案为:2:3;1300。