文档内容
2021-2022 学年高二化学重难点专题突破
模块三 晶体结构与性质
专题 10 常见晶体模型及晶胞计算
一.选择题
1.下面有关晶体的叙述中,不正确的是( )
A.金刚石为立体网状结构,由共价键形成的碳原子环中,最小的环上有6个碳原子
B.氯化钠晶体中,每个Na+周围紧邻且距离相等的Na+共有6个
C.氯化铯晶体中,每个Cs+周围紧邻8个Cl-
D.干冰晶体中,每个CO 分子周围紧邻12个CO 分子
2 2
答案:B
解析:金刚石中由共价键构成的最小环状结构中有6个碳原子;NaCl晶体中,每个Na+周围紧邻6个
Cl-,每个Na+周围紧邻12个Na+;氯化铯晶体中,每个Cs+周围紧邻8个Cl-,每个Cs+周围紧邻6个Cs
+;干冰晶体中,每个CO 分子周围紧邻12个CO 分子。
2 2
2.KO 的晶体结构与NaCl相似,KO 可以看作是Na+的位置用K+代替,Cl-的位置用O代替,则下
2 2
列对于KO 晶体结构的描述正确的是( )
2
A.与K+距离相等且最近的O2-共有8个
B.与K+距离相等且最近的O2-构成的多面体是正八面体
C.与K+距离相等且最近的K+有8个
D.一个KO 晶胞中的K+和O粒子数均为8
2
答案:B
解析:K+位于晶胞棱心,与K+距离相等且最近的O2-位于顶角和面心,共有6个,故A错误;与K+
距离相等且最近的O2-共有6个,构成正八面体,K+位于正八面体中心,故B正确;K+位于晶胞棱心,则
被横平面、竖平面和正平面共有,且每一个平面有4个K+距离最近,共4×3=12个,故C错误;K+位于
晶胞棱心和体心,数目为12×1/4+1=4,O2-位于顶角和面心,数目为8×1/8+6×1/2=4,即一个KO 晶胞
2
中的K+和O2-粒子数均为4个,故D错误。
3、下图是从NaCl或CsCl晶体结构图中分割出来的部分结构图,其中属于从 NaCl晶体中分割出来的
结构图是( )
A.图①和图③ B.图②和图③
C.图①和图④ D.只有图④解析:根据NaCl的晶体结构( ),在每个Na+周围最近的等距离的Cl-有6个(上、下、左、
右、前、后),故①正确;从NaCl晶体中分割可得图④结构。
答案:C
4、甲烷晶体的晶胞结构如图所示,下列说法正确的是( )
A.甲烷晶胞中的球只代表1个C原子
B.晶体中1个CH 分子有12个紧邻的CH 分子
4 4
C.甲烷晶体熔化时需克服共价键
D.1个CH 晶胞中含有8个CH 分子
4 4
答案 B
解析 题图所示的甲烷晶胞中的球代表的是1个甲烷分子,并不是1个C原子,A错误;由甲烷晶胞分析,
位于晶胞的顶点的某一个甲烷分子与其距离最近的甲烷分子有 3个,而这3个甲烷分子在晶胞的面上,因
此每个都被2个晶胞共用,故与1个甲烷分子紧邻的甲烷分子数目为3×8×=12,B正确;甲烷晶体是分子
晶体,熔化时克服范德华力,C错误;甲烷晶胞属于面心立方晶胞,该晶胞中甲烷分子的个数为8×+6×=
4,D错误。
5.科学家把C 和K掺杂在一起制造出的化合物具有超导性能,其晶胞如图所示。该化合物中的K原子和
60
C 分子的个数比为( )
60
A.3∶1 B.1∶3
C.1∶20 D.20∶1
解析:根据晶胞结构可以判断该晶胞中含C 分子数目为8×+1=2,含K原子数目为2×6×=6,所以
60
K原子与C 分子的个数比为3∶1。
60
答案:A
6、中学教材上介绍的干冰晶体是一种立方面心结构,如图所示,即每8个CO 构成立方体,且在6个面的
2
中心又各占据1个CO 分子,在每个CO 周围距离a(其中a为立方体棱长)的CO 有( )
2 2 2A.4个 B.8个 C.12个 D.6个
答案 C
解析 在每个CO 周围距离a的CO 即为每个面心上的CO 分子,在X、Y、Z三个方向上各有4个,所以
2 2 2
应为12个。
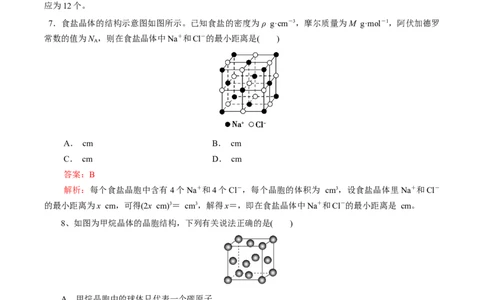
7.食盐晶体的结构示意图如图所示。已知食盐的密度为ρ g·cm-3,摩尔质量为M g·mol-1,阿伏加德罗
常数的值为N ,则在食盐晶体中Na+和Cl-的最小距离是( )
A
A. cm B. cm
C. cm D. cm
答案:B
解析:每个食盐晶胞中含有4个Na+和4个Cl-,每个晶胞的体积为 cm3,设食盐晶体里Na+和Cl-
的最小距离为x cm,可得(2x cm)3= cm3,解得x=,即在食盐晶体中Na+和Cl-的最小距离是 cm。
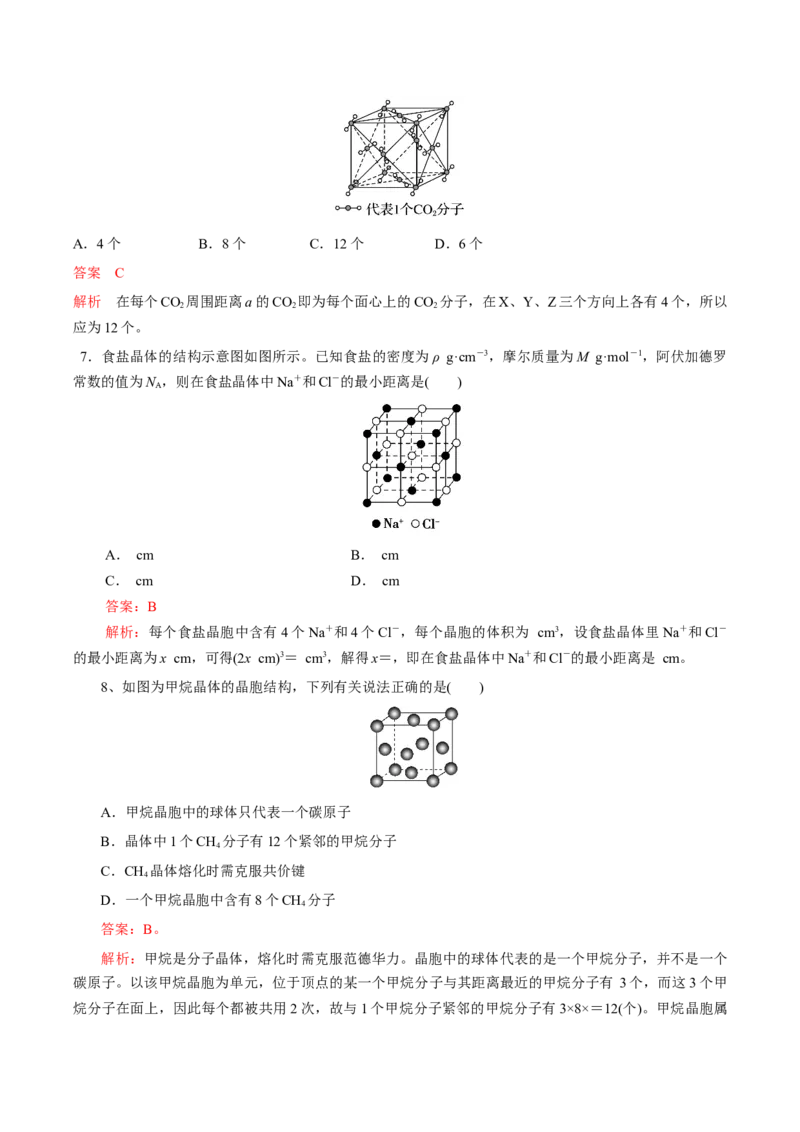
8、如图为甲烷晶体的晶胞结构,下列有关说法正确的是( )
A.甲烷晶胞中的球体只代表一个碳原子
B.晶体中1个CH 分子有12个紧邻的甲烷分子
4
C.CH 晶体熔化时需克服共价键
4
D.一个甲烷晶胞中含有8个CH 分子
4
答案:B。
解析:甲烷是分子晶体,熔化时需克服范德华力。晶胞中的球体代表的是一个甲烷分子,并不是一个
碳原子。以该甲烷晶胞为单元,位于顶点的某一个甲烷分子与其距离最近的甲烷分子有 3个,而这3个甲
烷分子在面上,因此每个都被共用2次,故与1个甲烷分子紧邻的甲烷分子有3×8×=12(个)。甲烷晶胞属于面心立方晶胞,该晶胞含有甲烷的分子个数为8×+6×=4(个)。综上所述,只有B项正确。
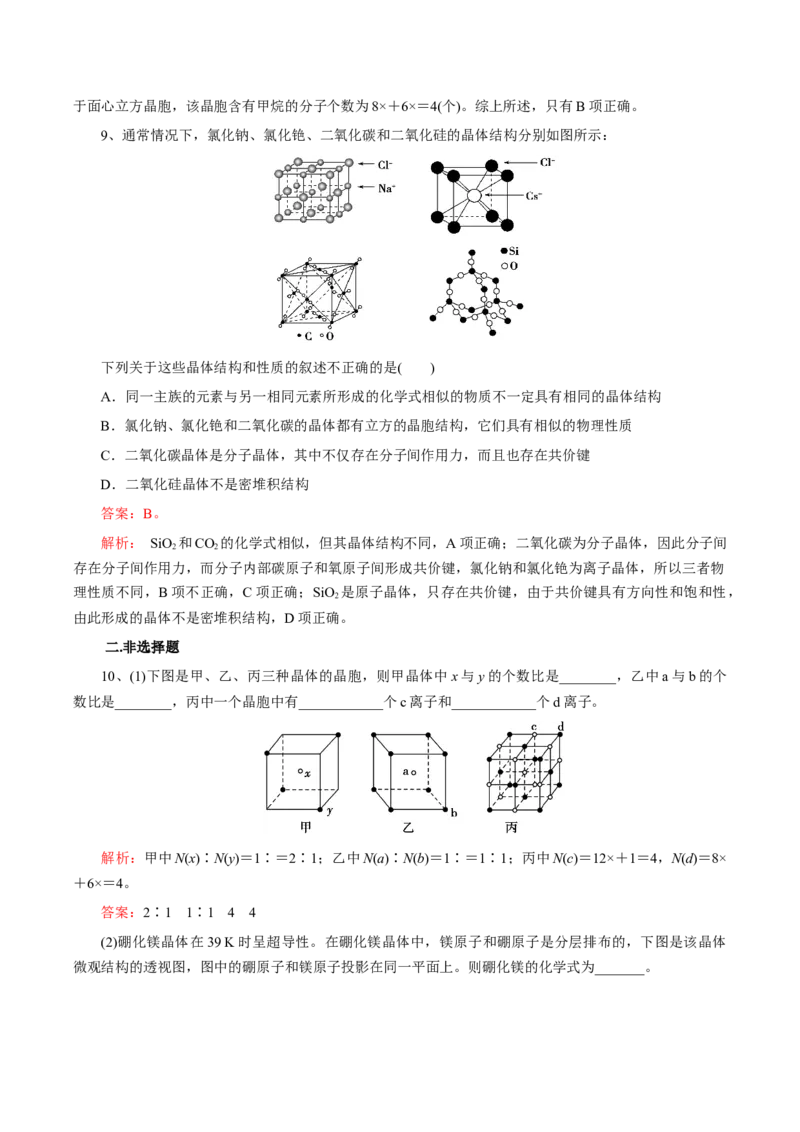
9、通常情况下,氯化钠、氯化铯、二氧化碳和二氧化硅的晶体结构分别如图所示:
下列关于这些晶体结构和性质的叙述不正确的是( )
A.同一主族的元素与另一相同元素所形成的化学式相似的物质不一定具有相同的晶体结构
B.氯化钠、氯化铯和二氧化碳的晶体都有立方的晶胞结构,它们具有相似的物理性质
C.二氧化碳晶体是分子晶体,其中不仅存在分子间作用力,而且也存在共价键
D.二氧化硅晶体不是密堆积结构
答案:B。
解析: SiO 和CO 的化学式相似,但其晶体结构不同,A项正确;二氧化碳为分子晶体,因此分子间
2 2
存在分子间作用力,而分子内部碳原子和氧原子间形成共价键,氯化钠和氯化铯为离子晶体,所以三者物
理性质不同,B项不正确,C项正确;SiO 是原子晶体,只存在共价键,由于共价键具有方向性和饱和性,
2
由此形成的晶体不是密堆积结构,D项正确。
二.非选择题
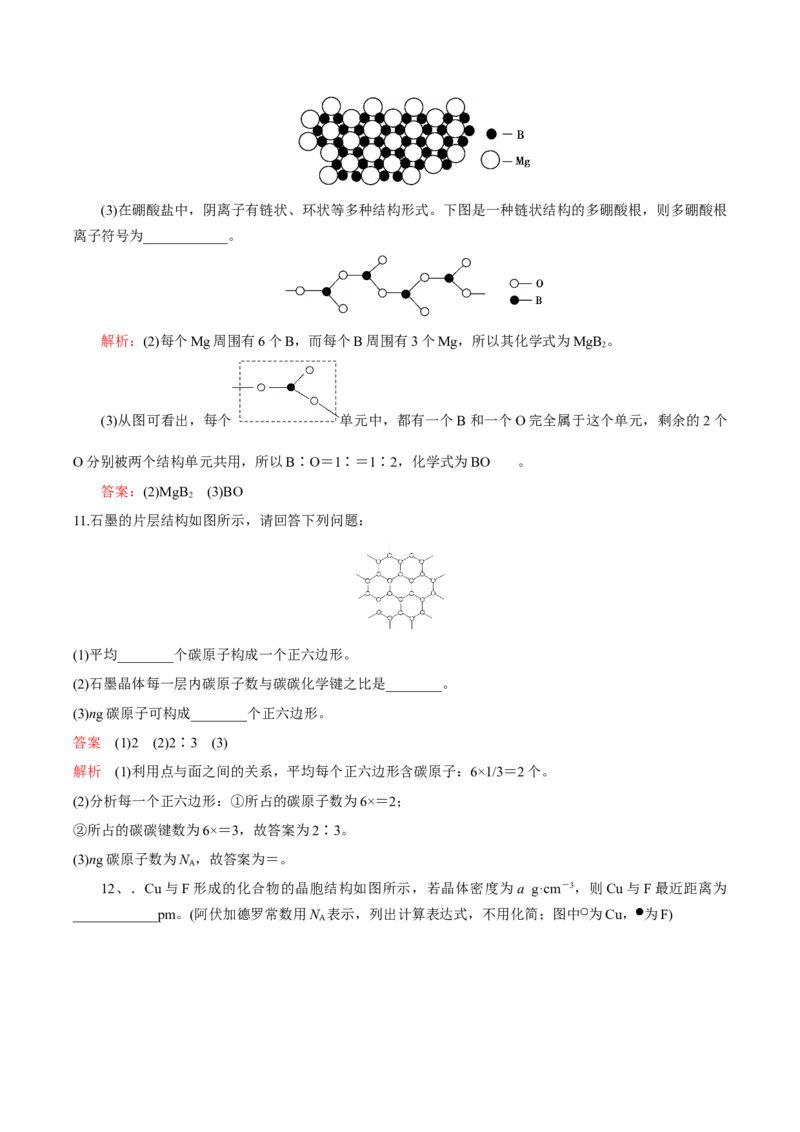
10、(1)下图是甲、乙、丙三种晶体的晶胞,则甲晶体中x与y的个数比是________,乙中a与b的个
数比是________,丙中一个晶胞中有____________个c离子和____________个d离子。
解析:甲中N(x)∶N(y)=1∶=2∶1;乙中N(a)∶N(b)=1∶=1∶1;丙中N(c)=12×+1=4,N(d)=8×
+6×=4。
答案:2∶1 1∶1 4 4
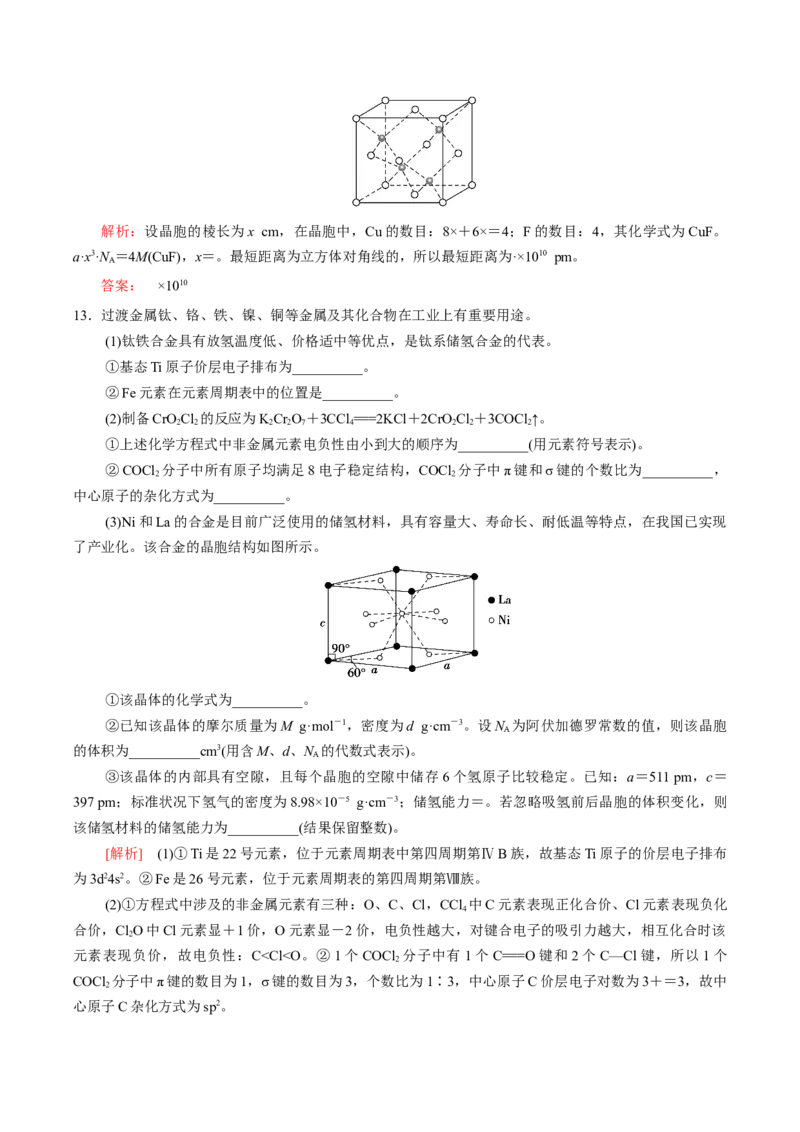
(2)硼化镁晶体在39 K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,下图是该晶体
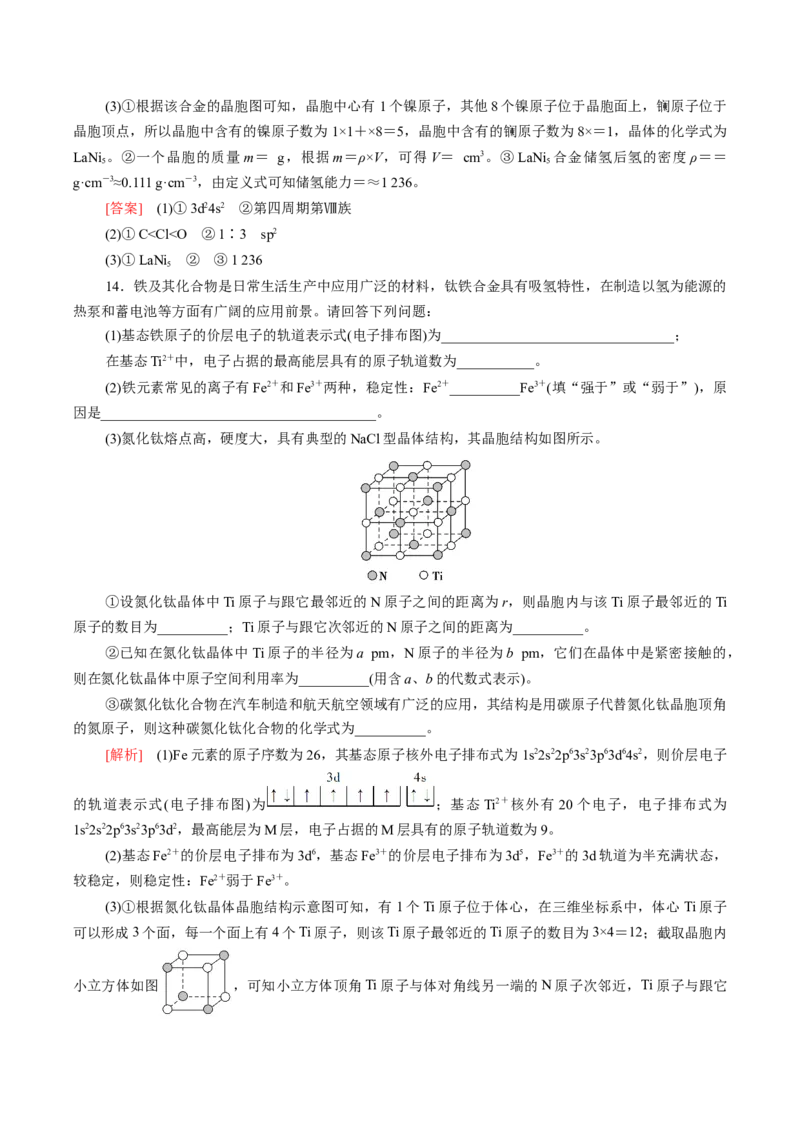
微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为_______。(3)在硼酸盐中,阴离子有链状、环状等多种结构形式。下图是一种链状结构的多硼酸根,则多硼酸根
离子符号为____________。
解析:(2)每个Mg周围有6个B,而每个B周围有3个Mg,所以其化学式为MgB 。
2
(3)从图可看出,每个 单元中,都有一个B和一个O完全属于这个单元,剩余的2个
O分别被两个结构单元共用,所以B∶O=1∶=1∶2,化学式为BO 。
答案:(2)MgB (3)BO
2
11.石墨的片层结构如图所示,请回答下列问题:
(1)平均________个碳原子构成一个正六边形。
(2)石墨晶体每一层内碳原子数与碳碳化学键之比是________。
(3)ng碳原子可构成________个正六边形。
答案 (1)2 (2)2∶3 (3)
解析 (1)利用点与面之间的关系,平均每个正六边形含碳原子:6×1/3=2个。
(2)分析每一个正六边形:①所占的碳原子数为6×=2;
②所占的碳碳键数为6×=3,故答案为2∶3。
(3)ng碳原子数为N ,故答案为=。
A
12、.Cu与F形成的化合物的晶胞结构如图所示,若晶体密度为 a g·cm-3,则Cu与F最近距离为
____________pm。(阿伏加德罗常数用N 表示,列出计算表达式,不用化简;图中 为Cu, 为F)
A解析:设晶胞的棱长为x cm,在晶胞中,Cu的数目:8×+6×=4;F的数目:4,其化学式为CuF。
a·x3·N =4M(CuF),x=。最短距离为立方体对角线的,所以最短距离为·×1010 pm。
A
答案: ×1010
13.过渡金属钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途。
(1)钛铁合金具有放氢温度低、价格适中等优点,是钛系储氢合金的代表。
①基态Ti原子价层电子排布为__________。
②Fe元素在元素周期表中的位置是__________。
(2)制备CrOCl 的反应为KCr O+3CCl ===2KCl+2CrOCl+3COCl ↑。
2 2 2 2 7 4 2 2 2
①上述化学方程式中非金属元素电负性由小到大的顺序为__________(用元素符号表示)。
②COCl 分子中所有原子均满足8电子稳定结构,COCl 分子中π键和σ键的个数比为__________,
2 2
中心原子的杂化方式为__________。
(3)Ni和La的合金是目前广泛使用的储氢材料,具有容量大、寿命长、耐低温等特点,在我国已实现
了产业化。该合金的晶胞结构如图所示。
①该晶体的化学式为__________。
②已知该晶体的摩尔质量为M g·mol-1,密度为d g·cm-3。设N 为阿伏加德罗常数的值,则该晶胞
A
的体积为__________cm3(用含M、d、N 的代数式表示)。
A
③该晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子比较稳定。已知:a=511 pm,c=
397 pm;标准状况下氢气的密度为8.98×10-5 g·cm-3;储氢能力=。若忽略吸氢前后晶胞的体积变化,则
该储氢材料的储氢能力为__________(结果保留整数)。
[解析] (1)①Ti是22号元素,位于元素周期表中第四周期第ⅣB族,故基态Ti原子的价层电子排布
为3d24s2。②Fe是26号元素,位于元素周期表的第四周期第Ⅷ族。
(2)①方程式中涉及的非金属元素有三种:O、C、Cl,CCl 中C元素表现正化合价、Cl元素表现负化
4
合价,ClO中Cl元素显+1价,O元素显-2价,电负性越大,对键合电子的吸引力越大,相互化合时该
2
元素表现负价,故电负性:C