文档内容
高清视频学案
1 / 3
绚丽多彩的世界—身边的物质之一
第二讲 制取氧气
魏国福
了解氧气的工业制法及原理
熟练掌握氧气的实验室制法及原理
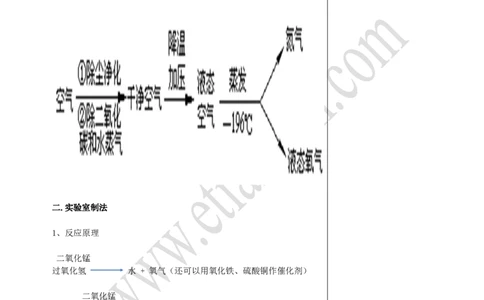
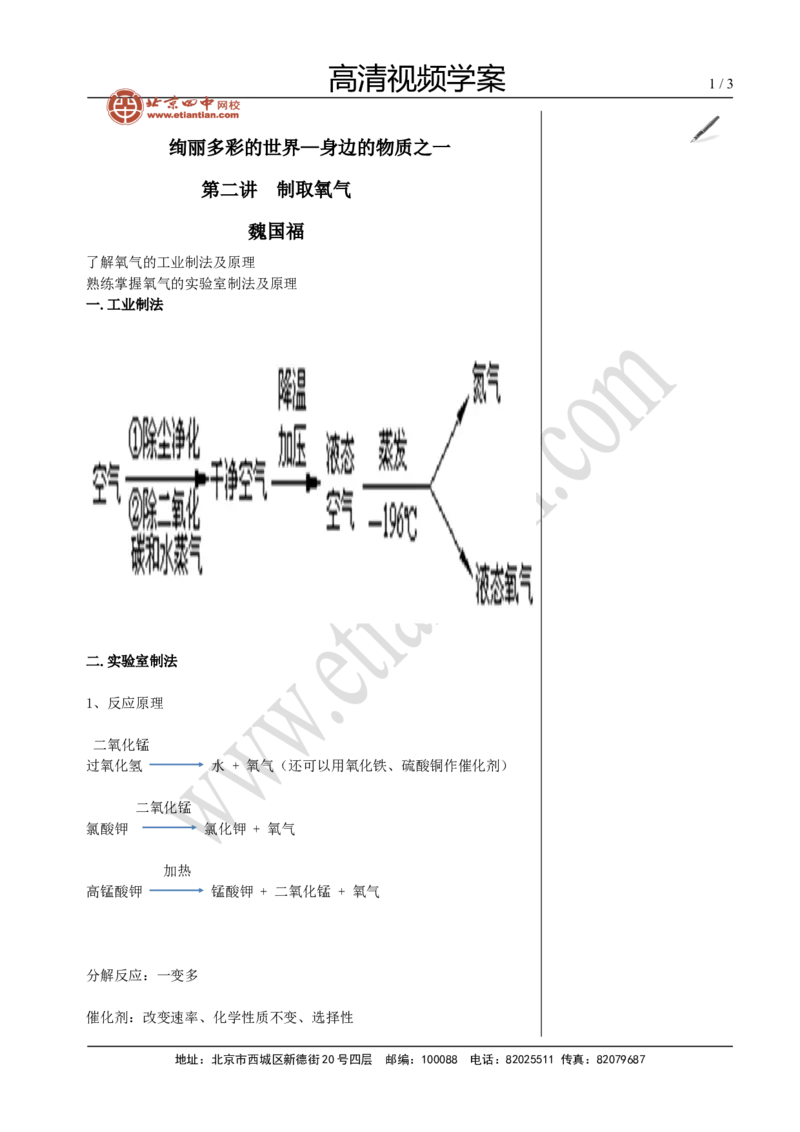
一.工业制法
二.实验室制法
1、反应原理
二氧化锰
过氧化氢 水 + 氧气(还可以用氧化铁、硫酸铜作催化剂)
二氧化锰
氯酸钾 氯化钾 + 氧气
加热
高锰酸钾 锰酸钾 + 二氧化锰 + 氧气
分解反应:一变多
催化剂:改变速率、化学性质不变、选择性
地址:北京市西城区新德街20号四层 邮编:100088 电话:82025511 传真:82079687高清视频学案
2 / 3
2,装置
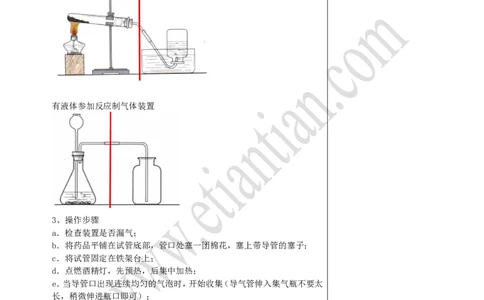
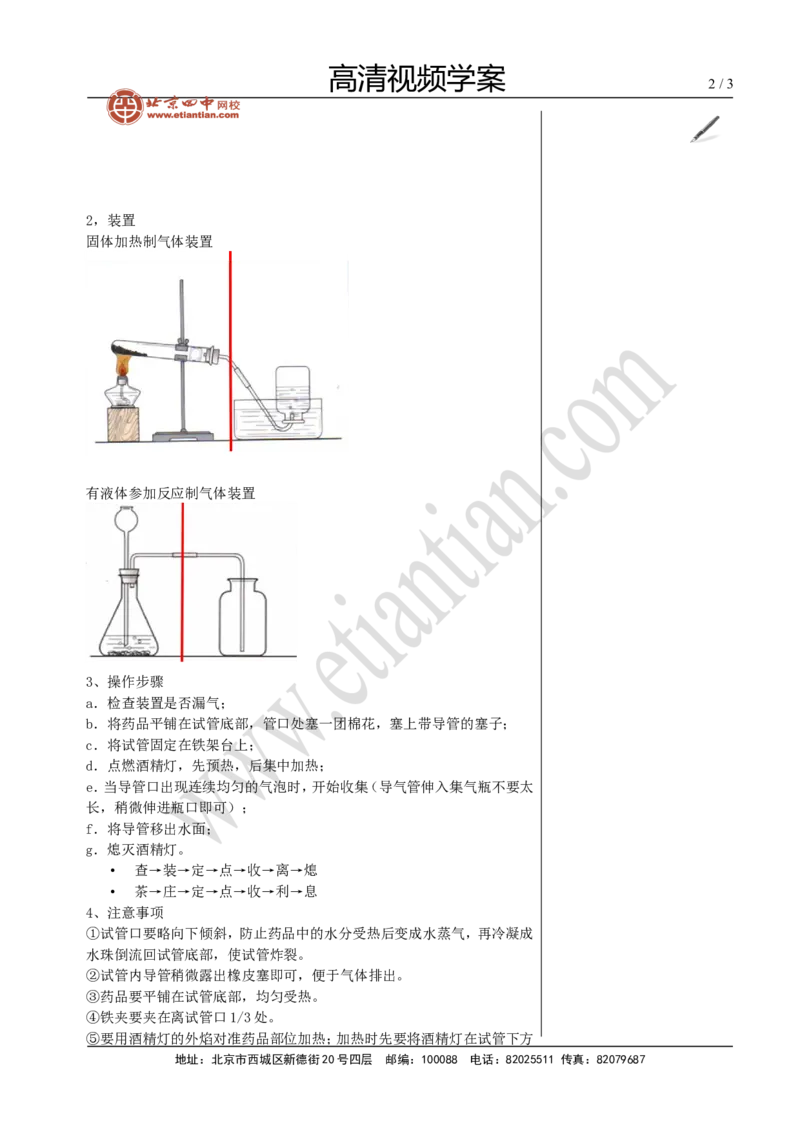
固体加热制气体装置
有液体参加反应制气体装置
3、操作步骤
a.检查装置是否漏气;
b.将药品平铺在试管底部,管口处塞一团棉花,塞上带导管的塞子;
c.将试管固定在铁架台上;
d.点燃酒精灯,先预热,后集中加热;
e.当导管口出现连续均匀的气泡时,开始收集(导气管伸入集气瓶不要太
长,稍微伸进瓶口即可);
f.将导管移出水面;
g.熄灭酒精灯。
• 查→装→定→点→收→离→熄
• 茶→庄→定→点→收→利→息
4、注意事项
①试管口要略向下倾斜,防止药品中的水分受热后变成水蒸气,再冷凝成
水珠倒流回试管底部,使试管炸裂。
②试管内导管稍微露出橡皮塞即可,便于气体排出。
③药品要平铺在试管底部,均匀受热。
④铁夹要夹在离试管口1/3处。
⑤要用酒精灯的外焰对准药品部位加热;加热时先要将酒精灯在试管下方
地址:北京市西城区新德街20号四层 邮编:100088 电话:82025511 传真:82079687高清视频学案
3 / 3
来回移动,让试管均匀受热,然后对准药品部位加热。
⑥用排水法集气时,集气瓶充满水后倒放入水槽中(瓶口要在水面下),导
管伸到瓶口处即可;用向上排空气法集气时,集气瓶正放,导管口要接近
集气瓶底部。
⑦用排水法集气时,应注意当气泡从导管口连续、均匀地放出时再收集,
否则收集的气体中混有空气。当集气瓶口有气泡冒出时,证明已满。
⑧停止反应时,应先把导管从水槽里拿出,再熄灭酒精灯(防止水倒流到
试管,导致试管炸裂)。
⑨收集满氧气的集气瓶应正放,并盖上玻璃片。
⑩用高锰酸钾制氧气时,试管口处应放一团棉花,防止高锰酸钾小颗粒进
入导管。
练习题
根据下列装置图回答问题。
A B C D E F G
• (1)标号仪器①的名称是 。
• (2)实验室用一定质量的高锰酸钾制取氧气,通过排水量测定所收
集到的氧气体积(装置选用A、F、G)。
• ①写出该反应的文字表达式 。
• ②若各装置的连接顺序是:a→b→c→d,F装置内导管(“b”或
“c”)该怎样延伸?请画出。
• ③根据高锰酸钾的质量算出的氧气体积为理论值。如果实际测得
氧气的体积大于理论值(水的体积测量准确),你认为原因是
。
• ④若改用氯酸钾和二氧化锰来制取氧气,则二氧化锰在反应前后
固体混合物中的质量分数将 (填“变大”、“变小”或
“不变”)
地址:北京市西城区新德街20号四层 邮编:100088 电话:82025511 传真:82079687