文档内容
2023 年贵州省中考化学试卷
1. 贵州省作为国家生态文明试验区,“十四五”期间被赋予建设新型综合能源基地的重要
战略地位。下列做法与助推生态文明建设不相符的是( )
A. 分类回收垃圾 B. 发展高耗能产业 C. 积极植树造林 D. 增加光伏发电
2. 正确的实验操作是实验成功的重要保障。下列基本实验操作正确的是( )
A. 检查气密性 B. 取用块状固体
C. 倾倒液体药品 D. 加热液体药品
3. 位于贵州省平塘县的500米口径球面射电望远镜被誉为“中国天眼”,其反射面面板由
金刚砂(SiC)制成。SiC中C的化合价为−4,则Si的化合价为( )
A. +4 B. 0 C. +2 D. −4
4. 我国传统节日端午节,有吃粽子、赛龙舟、挂艾草的习俗。艾草中含有的黄酮素
(C H O )有很高的药用价值。下列关于黄酮素的说法正确的是( )
15 10 2
A. 黄酮素属于氧化物
B. 黄酮素中含有氧气
C. 黄酮素分子由碳原子、氢原子和氧原子构成
D. 黄酮素中碳元素与氢元素的质量比为3:2
5. 探索燃烧的利用和控制,能更好地为人类服务。下列关于燃烧的说法错误的是( )
A. 燃烧属于化学变化,产生的能量被广泛应用
B. 把煤块粉碎成煤粉使用,可以使煤充分燃烧C. 炒菜油锅着火时,立刻盖上锅盖可以灭火
D. 把蜡烛伸入装有氧气的集气瓶中,蜡烛能立刻燃烧
6. 某同学对下列四个实验都分别设计了两种方案,其中两种方案均能达到实验目的的是
( )
序号 实验 方案一 方案二
A 除去CO 中的CO 点燃 通过灼热的炭层
2
B 除去CaO中的CaCO 高温煅烧 加足量的稀盐酸
3
取等量的固体,加入等量同温的 取样,加熟石灰混合
C 鉴别NaCl和N H NO 固体
4 3 水,溶解,测温度变化 研磨,闻气味
取样,加入足量稀硫
D 鉴别CuO粉末和木炭粉 取样,观察颜色
酸
A. A B. B C. C D. D
7. 自然界有一种含镁矿石,经处理后得到只含MgCO 和
3
Mg(OH) 的混合物,可作生产耐火材料氧化镁的原料。为确定
2
其组成,现各取wg样品两份,第一份样品加过量稀盐酸,生成
气体8.8g;第二份样品加热,固体质量与反应时间的变化关系
❑
如图所示,化学方程式:MgCO =MgO+CO ↑;
3 2
❑
Mg(OH) =MgO+H O↑。下列说法错误的是( )
2 2
A. MgCO 和Mg(OH) 的混合物可用作防火材料
3 2
B. 样品中MgCO 与Mg(OH) 的质量比为168:58
3 2
C. 第二份样品加热后,固体中镁元素的质量分数变大
D. 两份样品充分反应后,生成CO 气体的质量相等
2
8. 化学作为实用的、创造性的学科,在认识自然、服务社会中发挥着不可替代的作用。
(1)认识物质。空气是一种宝贵的资源,其中能供给呼吸的气体是 ______ 。
(2)人体健康。合理膳食是人体健康的基本保障。小明的早餐食谱为:馒头、鸡蛋、牛奶、
青菜,其中富含糖类的是 ______ 。适量饮用牛奶可补充 ______ 元素,能预防骨质疏松。
(3)粮食增产。常用的化肥有 CO(N H ) 、KCl、Ca(H PO ) 等,其中属于氮肥的是
2 2 2 4 2______ 。
(4)材料创造。汽车使用的材料有合金、塑料等,其中属于有机合成材料的是 ______ ;创
造始于丰富的想象力,如果让你设计未来汽车的材料,你希望材料具备的性能有 ______ 。
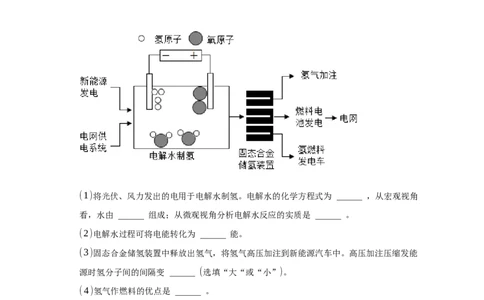
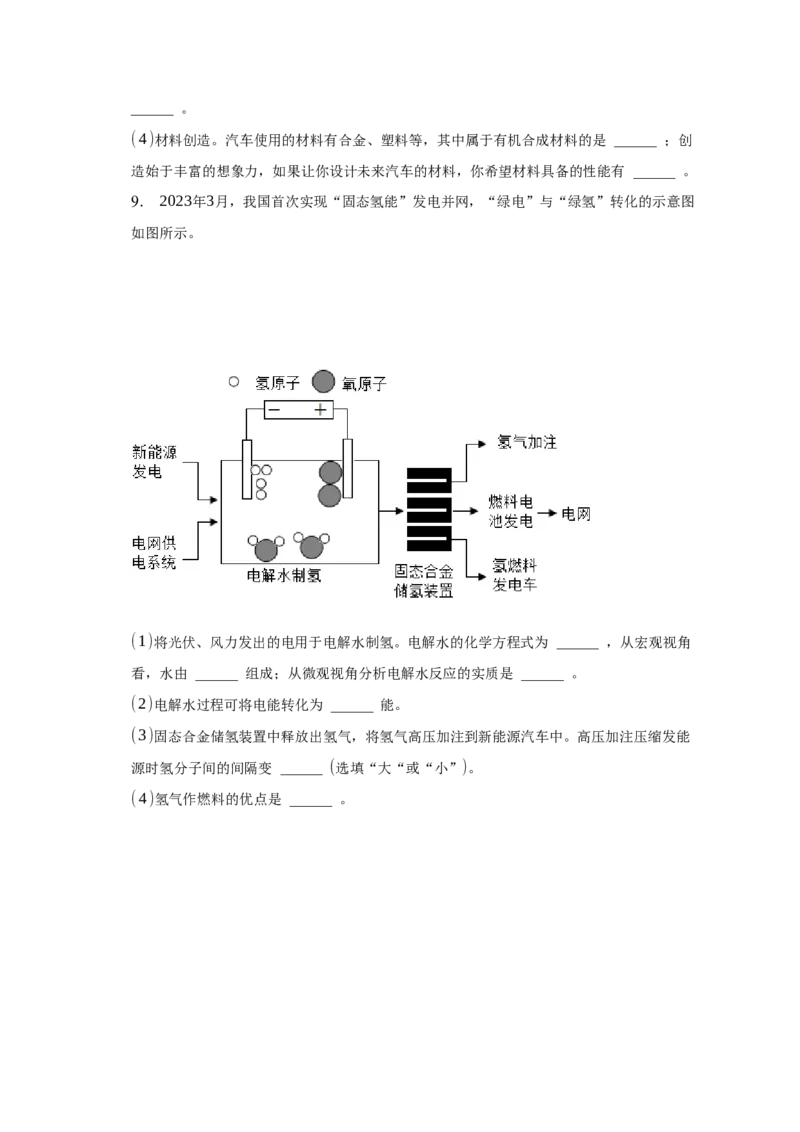
9. 2023年3月,我国首次实现“固态氢能”发电并网,“绿电”与“绿氢”转化的示意图
如图所示。
(1)将光伏、风力发出的电用于电解水制氢。电解水的化学方程式为 ______ ,从宏观视角
看,水由 ______ 组成;从微观视角分析电解水反应的实质是 ______ 。
(2)电解水过程可将电能转化为 ______ 能。
(3)固态合金储氢装置中释放出氢气,将氢气高压加注到新能源汽车中。高压加注压缩发能
源时氢分子间的间隔变 ______ (选填“大“或“小”)。
(4)氢气作燃料的优点是 ______ 。10. 化学是一门以实验为基础的学科。
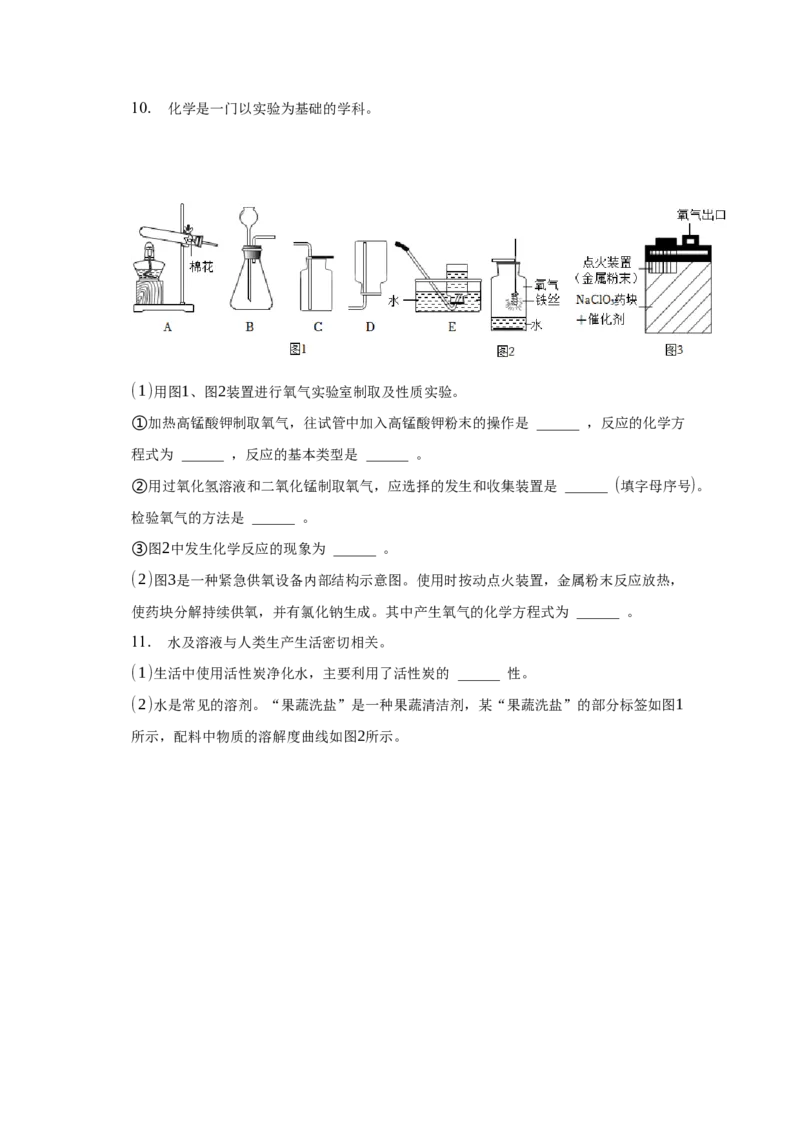
(1)用图1、图2装置进行氧气实验室制取及性质实验。
①加热高锰酸钾制取氧气,往试管中加入高锰酸钾粉末的操作是 ______ ,反应的化学方
程式为 ______ ,反应的基本类型是 ______ 。
②用过氧化氢溶液和二氧化锰制取氧气,应选择的发生和收集装置是 ______ (填字母序号)。
检验氧气的方法是 ______ 。
③图2中发生化学反应的现象为 ______ 。
(2)图3是一种紧急供氧设备内部结构示意图。使用时按动点火装置,金属粉末反应放热,
使药块分解持续供氧,并有氯化钠生成。其中产生氧气的化学方程式为 ______ 。
11. 水及溶液与人类生产生活密切相关。
(1)生活中使用活性炭净化水,主要利用了活性炭的 ______ 性。
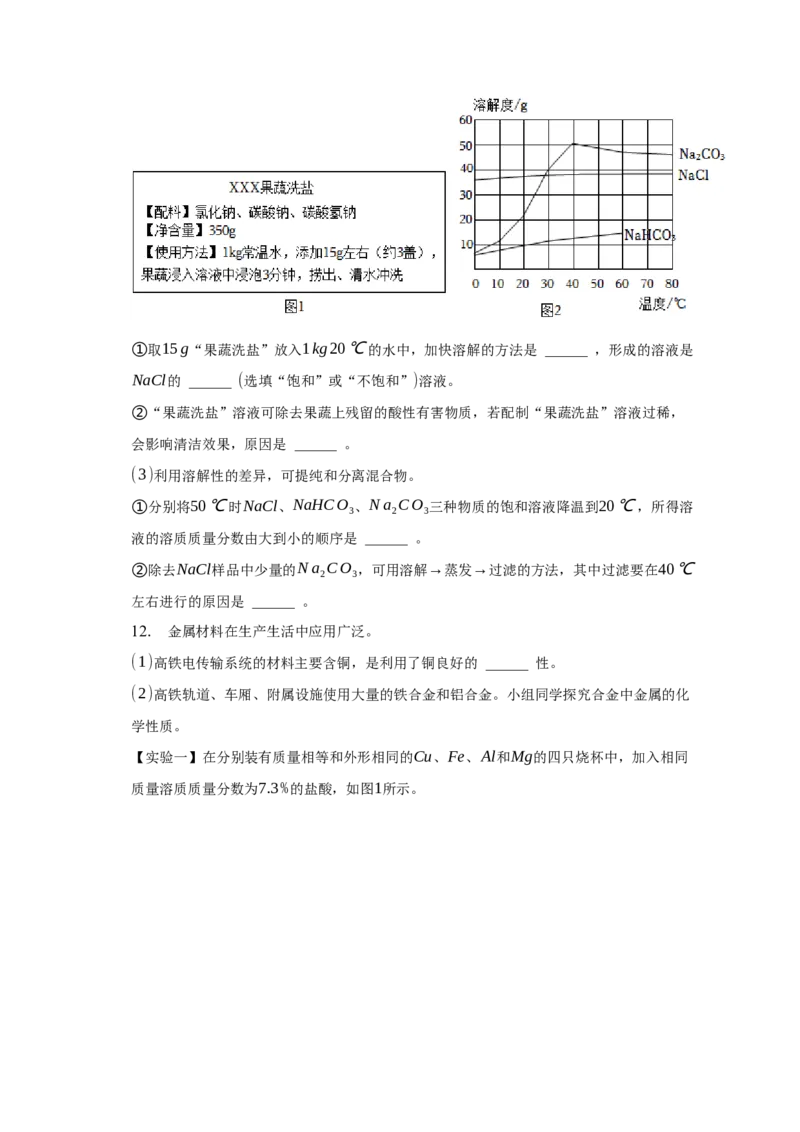
(2)水是常见的溶剂。“果蔬洗盐”是一种果蔬清洁剂,某“果蔬洗盐”的部分标签如图1
所示,配料中物质的溶解度曲线如图2所示。①取15g“果蔬洗盐”放入1kg20℃的水中,加快溶解的方法是 ______ ,形成的溶液是
NaCl的 ______ (选填“饱和”或“不饱和”)溶液。
②“果蔬洗盐”溶液可除去果蔬上残留的酸性有害物质,若配制“果蔬洗盐”溶液过稀,
会影响清洁效果,原因是 ______ 。
(3)利用溶解性的差异,可提纯和分离混合物。
①分别将50℃时NaCl、NaHCO 、Na CO 三种物质的饱和溶液降温到20℃,所得溶
3 2 3
液的溶质质量分数由大到小的顺序是 ______ 。
②除去NaCl样品中少量的Na CO ,可用溶解→蒸发→过滤的方法,其中过滤要在40℃
2 3
左右进行的原因是 ______ 。
12. 金属材料在生产生活中应用广泛。
(1)高铁电传输系统的材料主要含铜,是利用了铜良好的 ______ 性。
(2)高铁轨道、车厢、附属设施使用大量的铁合金和铝合金。小组同学探究合金中金属的化
学性质。
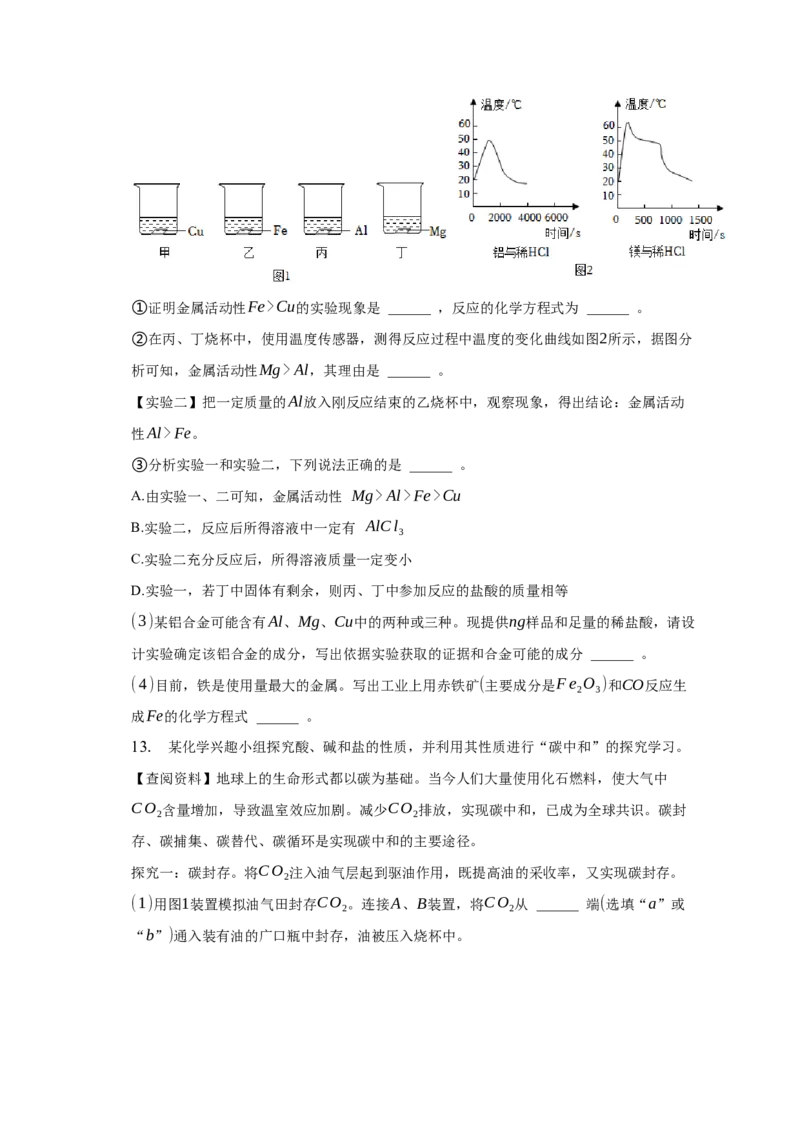
【实验一】在分别装有质量相等和外形相同的Cu、Fe、Al和Mg的四只烧杯中,加入相同
质量溶质质量分数为7.3%的盐酸,如图1所示。①证明金属活动性Fe>Cu的实验现象是 ______ ,反应的化学方程式为 ______ 。
②在丙、丁烧杯中,使用温度传感器,测得反应过程中温度的变化曲线如图2所示,据图分
析可知,金属活动性Mg>Al,其理由是 ______ 。
【实验二】把一定质量的Al放入刚反应结束的乙烧杯中,观察现象,得出结论:金属活动
性Al>Fe。
③分析实验一和实验二,下列说法正确的是 ______ 。
A.由实验一、二可知,金属活动性 Mg>Al>Fe>Cu
B.实验二,反应后所得溶液中一定有 AlCl
3
C.实验二充分反应后,所得溶液质量一定变小
D.实验一,若丁中固体有剩余,则丙、丁中参加反应的盐酸的质量相等
(3)某铝合金可能含有Al、Mg、Cu中的两种或三种。现提供ng样品和足量的稀盐酸,请设
计实验确定该铝合金的成分,写出依据实验获取的证据和合金可能的成分 ______ 。
(4)目前,铁是使用量最大的金属。写出工业上用赤铁矿(主要成分是Fe O )和CO反应生
2 3
成Fe的化学方程式 ______ 。
13. 某化学兴趣小组探究酸、碱和盐的性质,并利用其性质进行“碳中和”的探究学习。
【查阅资料】地球上的生命形式都以碳为基础。当今人们大量使用化石燃料,使大气中
CO 含量增加,导致温室效应加剧。减少CO 排放,实现碳中和,已成为全球共识。碳封
2 2
存、碳捕集、碳替代、碳循环是实现碳中和的主要途径。
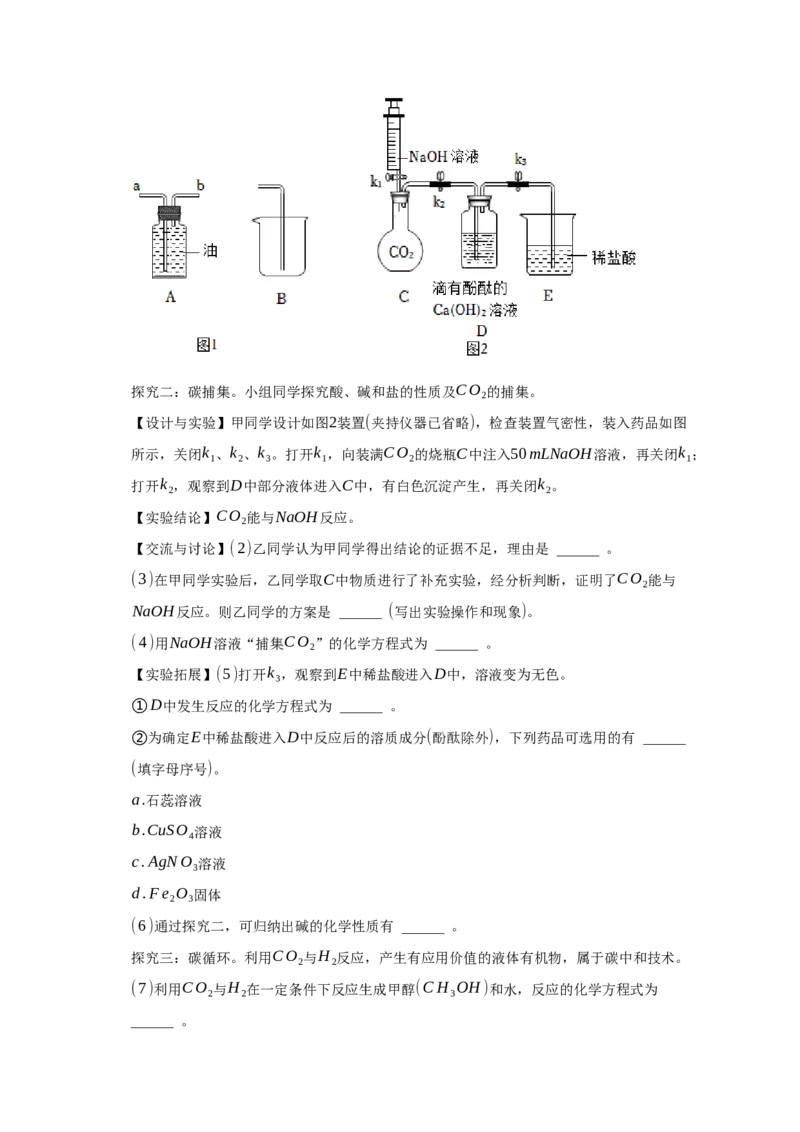
探究一:碳封存。将CO 注入油气层起到驱油作用,既提高油的采收率,又实现碳封存。
2
(1)用图1装置模拟油气田封存CO 。连接A、B装置,将CO 从 ______ 端(选填“a”或
2 2
“b”)通入装有油的广口瓶中封存,油被压入烧杯中。探究二:碳捕集。小组同学探究酸、碱和盐的性质及CO 的捕集。
2
【设计与实验】甲同学设计如图2装置(夹持仪器已省略),检查装置气密性,装入药品如图
所示,关闭k 、k 、k 。打开k ,向装满CO 的烧瓶C中注入50mLNaOH溶液,再关闭k ;
1 2 3 1 2 1
打开k ,观察到D中部分液体进入C中,有白色沉淀产生,再关闭k 。
2 2
【实验结论】CO 能与NaOH反应。
2
【交流与讨论】(2)乙同学认为甲同学得出结论的证据不足,理由是 ______ 。
(3)在甲同学实验后,乙同学取C中物质进行了补充实验,经分析判断,证明了CO 能与
2
NaOH反应。则乙同学的方案是 ______ (写出实验操作和现象)。
(4)用NaOH溶液“捕集CO ”的化学方程式为 ______ 。
2
【实验拓展】(5)打开k ,观察到E中稀盐酸进入D中,溶液变为无色。
3
①D中发生反应的化学方程式为 ______ 。
②为确定E中稀盐酸进入D中反应后的溶质成分(酚酞除外),下列药品可选用的有 ______
(填字母序号)。
a.石蕊溶液
b.CuSO 溶液
4
c.AgNO 溶液
3
d.Fe O 固体
2 3
(6)通过探究二,可归纳出碱的化学性质有 ______ 。
探究三:碳循环。利用CO 与H 反应,产生有应用价值的液体有机物,属于碳中和技术。
2 2
(7)利用CO 与H 在一定条件下反应生成甲醇(CH OH)和水,反应的化学方程式为
2 2 3
______ 。14. 氢气可作燃料,若40g氢气完全燃烧,需要氧气的质量是多少?(写出计算过程)。