文档内容
新情境下方程式的书写
1.陌生情境下非氧化还原反应方程式的书写
(1)依据广义水解原理书写
广义的水解观认为,无论是盐的水解还是非盐的水解,其最终结果都是参与反应的物质和水分别解离
成两部分,再重新组合成新的物质。
例1 写出亚硫酰氯(SOCl )在潮湿的空气中产生白雾的化学方程式: 。
2
例2 常用尿素[CO(NH ) ]除去工业废水中Cr3+,流程为:
2 2
含 ,完成该转化的离子方程式: 。
(2)根据“中和”原理或“强酸制弱酸”原理书写
例3 根据要求完成下列化学方程式:
(1)25 ℃,H C O 和HF两种酸的电离平衡常数如下:
2 2 4
H C O K =5.36×10-2 K =5.35×10-5
2 2 4 a1 a2
HF K=6.31×10-4
a
则H C O 溶液和NaF溶液反应的离子方程式为 。
2 2 4
(2)多硼酸盐四硼酸钠(Na B O )与硫酸反应可制硼酸(H BO ),写出反应的化学方程式: 。
2 4 7 3 3
解题思路 (1)判断三种酸(只看一步电离)H C O 、HF、HC
O-
电离H+的能力,即酸性的强弱,运用强酸制
2 2 4 2 4
弱酸即可写出方程式。
(2)联想Na SiO 与酸的反应,H BO 是弱酸。
2 3 3 3(3)应用“平衡转化”思想书写
例4 硫酸是一种重要的大宗工业化学品,应用广泛,可实现下列转化:
(1)过程Ⅰ的化学方程式为 。
(2)已知硫酸分子的结构为 ,过程Ⅱ生成了焦硫酸钠Na S O ,写出其阴离子的结构式:
2 2 7
;推测焦硫酸钠水溶液呈 (填“酸性”“中性”或“碱性”),用离子方程式表明原因:
。
(3) Na S O 高温下具有强氧化性,受热分解产生SO 气体。过程Ⅲ是将过量Na S O 固体与磁铁矿熔融
2 2 7 3 2 2 7
反应,产生了混合气体。写出Na S O 只与磁铁矿发生反应的总化学方程式:
2 2 7
。
(4)过量的焦硫酸(H S O )和苯在加热条件下反应得到苯磺酸,写出反应的化学方程式:
2 2 7
。
2.陌生情境下氧化还原反应方程式的书写
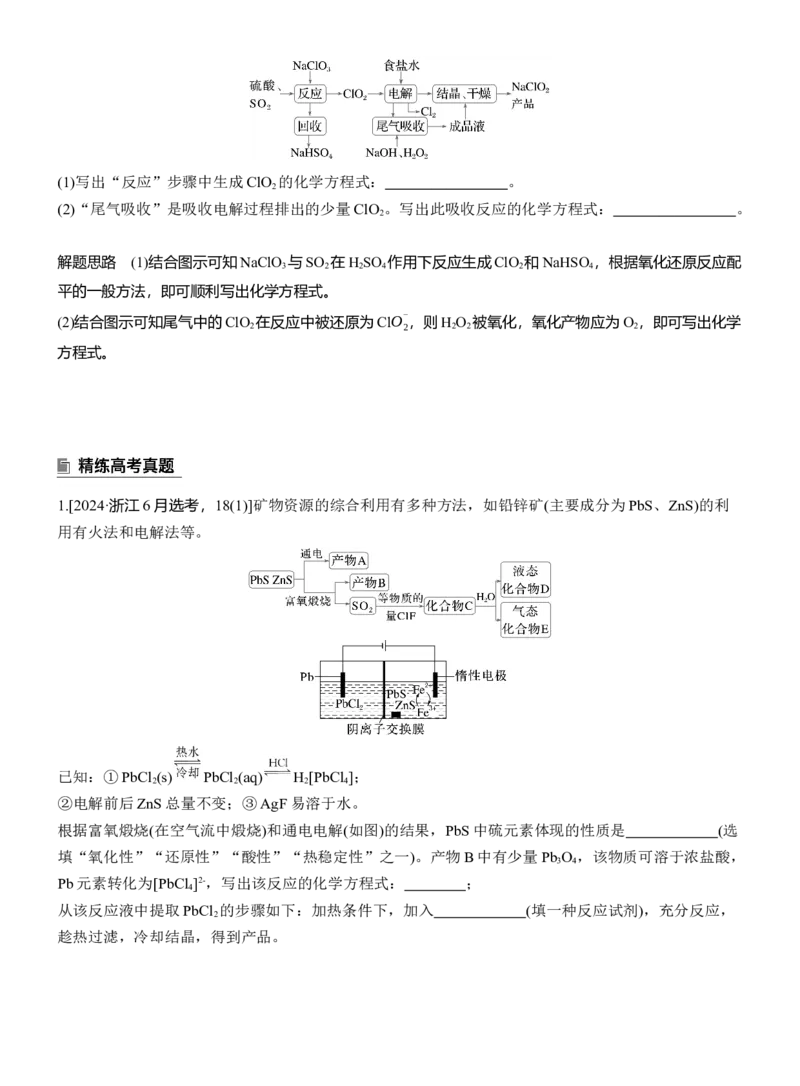
例5 NaClO 是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如图所示:
2(1)写出“反应”步骤中生成ClO 的化学方程式: 。
2
(2)“尾气吸收”是吸收电解过程排出的少量ClO 。写出此吸收反应的化学方程式: 。
2
解题思路 (1)结合图示可知NaClO 与SO 在H SO 作用下反应生成ClO 和NaHSO ,根据氧化还原反应配
3 2 2 4 2 4
平的一般方法,即可顺利写出化学方程式。
(2)结合图示可知尾气中的ClO
在反应中被还原为ClO-
,则H O 被氧化,氧化产物应为O ,即可写出化学
2 2 2 2 2
方程式。
1.[2024·浙江6月选考,18(1)]矿物资源的综合利用有多种方法,如铅锌矿(主要成分为PbS、ZnS)的利
用有火法和电解法等。
已知:①PbCl (s) PbCl (aq) H [PbCl ];
2 2 2 4
②电解前后ZnS总量不变;③AgF易溶于水。
根据富氧煅烧(在空气流中煅烧)和通电电解(如图)的结果,PbS中硫元素体现的性质是 (选
填“氧化性”“还原性”“酸性”“热稳定性”之一)。产物B中有少量Pb O ,该物质可溶于浓盐酸,
3 4
Pb元素转化为[PbCl ]2-,写出该反应的化学方程式: ;
4
从该反应液中提取PbCl 的步骤如下:加热条件下,加入 (填一种反应试剂),充分反应,
2
趁热过滤,冷却结晶,得到产品。2.[2024·北京,18(1)(2)]利用黄铜矿(主要成分为CuFeS ,含有SiO 等杂质)生产纯铜,流程示意图如下。
2 2
(1)矿石在焙烧前需粉碎,其作用是 。
(2)(NH ) SO 的作用是利用其分解产生的SO 使矿石中的铜元素转化为CuSO 。(NH ) SO 发生热分解的
4 2 4 3 4 4 2 4
化学方程式是 。
3.[2024·甘肃,15(1)(2)(3)]我国科研人员以高炉渣(主要成分为CaO,MgO,Al O 和SiO 等)为原料,对
2 3 2
炼钢烟气(CO 和水蒸气)进行回收利用,有效减少了环境污染,主要流程如图所示:
2
已知:K (CaSO )=4.9×10-5
sp 4
K (CaCO )=3.4×10-9
sp 3
(1)高炉渣与(NH ) SO 经焙烧产生的“气体”是 。
4 2 4
(2)“滤渣”的主要成分是CaSO 和 。
4
(3)“水浸2”时主要反应的化学方程式为 ,
该反应能进行的原因是 。
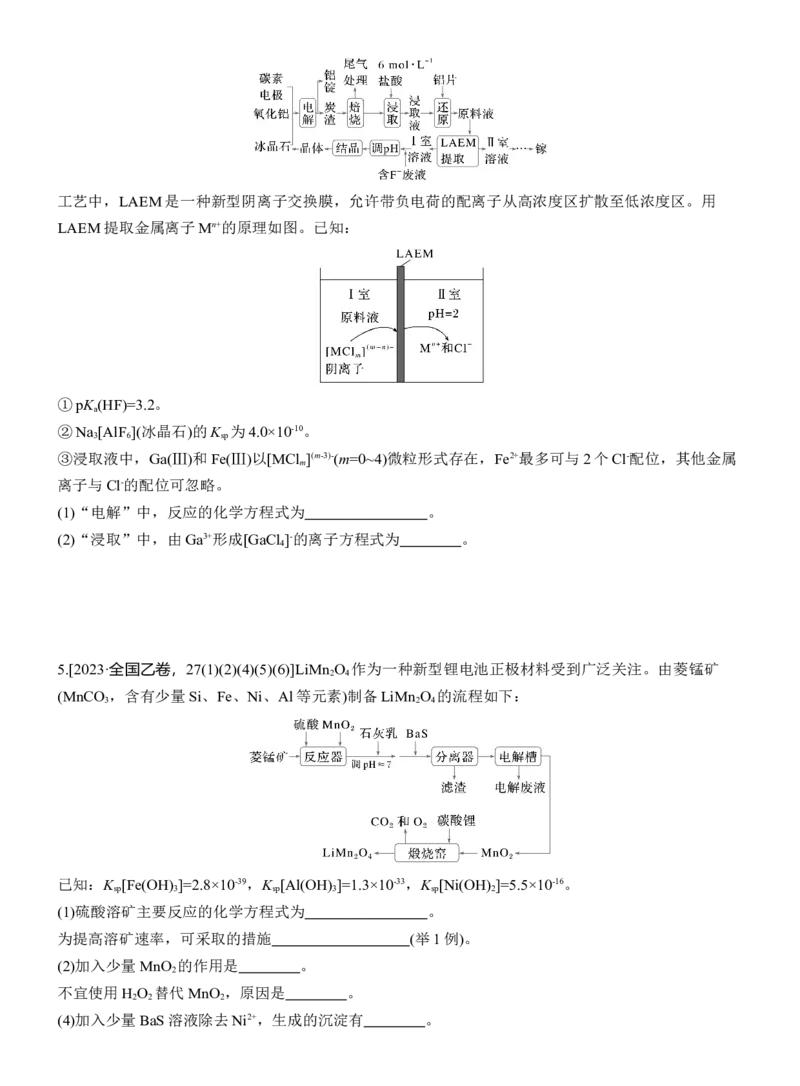
4.[2024·广东,18(1)(2)]镓(Ga)在半导体、记忆合金等高精尖材料领域有重要应用。一种从电解铝的副
产品炭渣(含C、Na、Al、F和少量的Ga、Fe、K、Ca等元素)中提取镓及循环利用铝的工艺如下。工艺中,LAEM是一种新型阴离子交换膜,允许带负电荷的配离子从高浓度区扩散至低浓度区。用
LAEM提取金属离子Mn+的原理如图。已知:
①pK(HF)=3.2。
a
②Na [AlF ](冰晶石)的K 为4.0×10-10。
3 6 sp
③浸取液中,Ga(Ⅲ)和Fe(Ⅲ)以[MCl ](m-3)-(m=0~4)微粒形式存在,Fe2+最多可与2个Cl-配位,其他金属
m
离子与Cl-的配位可忽略。
(1)“电解”中,反应的化学方程式为 。
(2)“浸取”中,由Ga3+形成[GaCl ]-的离子方程式为 。
4
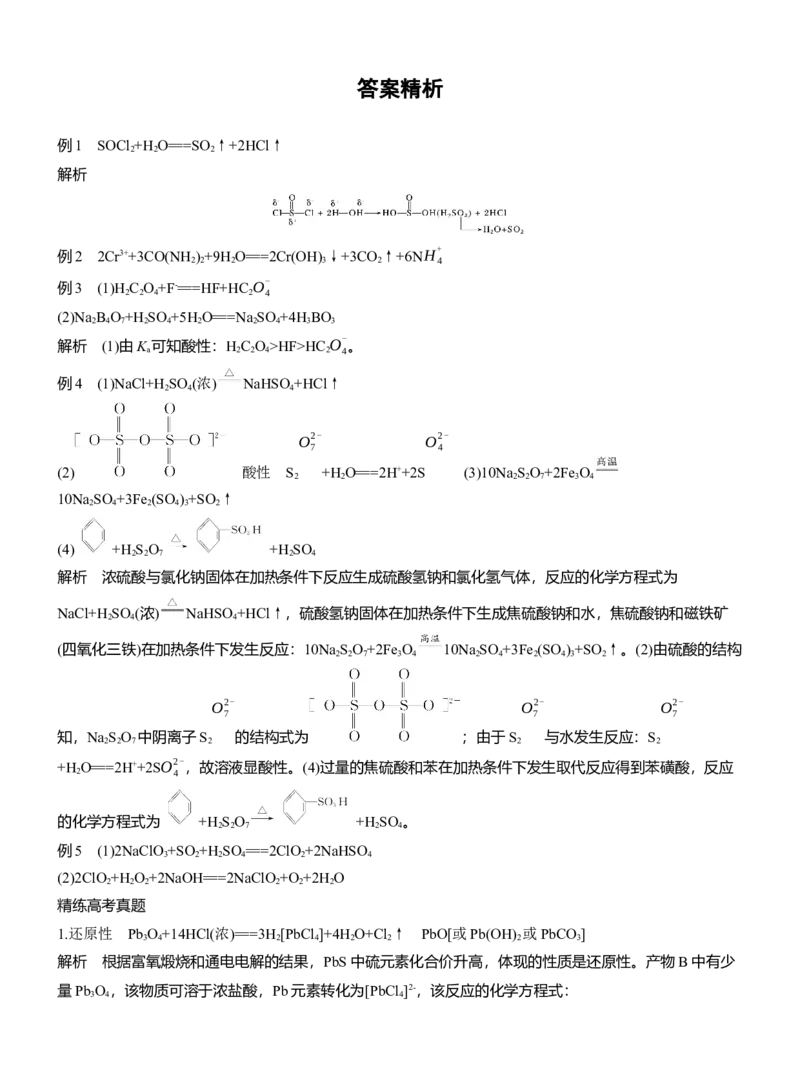
5.[2023·全国乙卷,27(1)(2)(4)(5)(6)]LiMn O 作为一种新型锂电池正极材料受到广泛关注。由菱锰矿
2 4
(MnCO ,含有少量Si、Fe、Ni、Al等元素)制备LiMn O 的流程如下:
3 2 4
已知:K [Fe(OH) ]=2.8×10-39,K [Al(OH) ]=1.3×10-33,K [Ni(OH) ]=5.5×10-16。
sp 3 sp 3 sp 2
(1)硫酸溶矿主要反应的化学方程式为 。
为提高溶矿速率,可采取的措施 (举1例)。
(2)加入少量MnO 的作用是 。
2
不宜使用H O 替代MnO ,原因是 。
2 2 2
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有 。(5)在电解槽中,发生电解反应的离子方程式为 。
随着电解反应进行,为保持电解液成分稳定,应不断 。电解废液可在反应器中循
环利用。
(6)煅烧窑中,生成LiMn O 反应的化学方程式是 。
2 4
6.[2023·江苏,17(1)]空气中CO 含量的控制和CO 资源利用具有重要意义。
2 2
燃煤烟气中CO 的捕集可通过如下所示的物质转化实现。
2
“吸收”后所得的KHCO 溶液与石灰乳反应的化学方程式为 ;
3
载人航天器内,常用LiOH固体而很少用KOH固体吸收空气中的CO ,其原因是 。
2答案精析
例1 SOCl +H O===SO ↑+2HCl↑
2 2 2
解析
例2 2Cr3++3CO(NH ) +9H O===2Cr(OH) ↓+3CO
↑+6NH+
2 2 2 3 2 4
例3 (1)H C O +F-===HF+HC
O-
2 2 4 2 4
(2)Na B O +H SO +5H O===Na SO +4H BO
2 4 7 2 4 2 2 4 3 3
解析 (1)由K 可知酸性:H C O >HF>HC
O-
。
a 2 2 4 2 4
例4 (1)NaCl+H SO (浓) NaHSO +HCl↑
2 4 4
O2- O2-
7 4
(2) 酸性 S +H O===2H++2S (3)10Na S O +2Fe O
2 2 2 2 7 3 4
10Na SO +3Fe (SO ) +SO ↑
2 4 2 4 3 2
(4) +H S O +H SO
2 2 7 2 4
解析 浓硫酸与氯化钠固体在加热条件下反应生成硫酸氢钠和氯化氢气体,反应的化学方程式为
NaCl+H SO (浓) NaHSO +HCl↑,硫酸氢钠固体在加热条件下生成焦硫酸钠和水,焦硫酸钠和磁铁矿
2 4 4
(四氧化三铁)在加热条件下发生反应:10Na S O +2Fe O 10Na SO +3Fe (SO ) +SO ↑。(2)由硫酸的结构
2 2 7 3 4 2 4 2 4 3 2
O2- O2- O2-
7 7 7
知,Na S O 中阴离子S 的结构式为 ;由于S 与水发生反应:S
2 2 7 2 2 2
+H
O===2H++2SO2-
,故溶液显酸性。(4)过量的焦硫酸和苯在加热条件下发生取代反应得到苯磺酸,反应
2 4
的化学方程式为 +H S O +H SO 。
2 2 7 2 4
例5 (1)2NaClO +SO +H SO ===2ClO +2NaHSO
3 2 2 4 2 4
(2)2ClO +H O +2NaOH===2NaClO +O +2H O
2 2 2 2 2 2
精练高考真题
1.还原性 Pb O +14HCl(浓)===3H [PbCl ]+4H O+Cl ↑ PbO[或Pb(OH) 或PbCO ]
3 4 2 4 2 2 2 3
解析 根据富氧煅烧和通电电解的结果,PbS中硫元素化合价升高,体现的性质是还原性。产物B中有少
量Pb O ,该物质可溶于浓盐酸,Pb元素转化为[PbCl ]2-,该反应的化学方程式:
3 4 4Pb O +14HCl(浓)===3H [PbCl ]+4H O+Cl ↑;根据已知①可判断要从该反应液中提取PbCl ,则所加试剂应
3 4 2 4 2 2 2
能消耗H+使平衡逆向移动,且不引入杂质,则步骤为加热条件下,加入PbO或Pb(OH) 或PbCO ,充分反
2 3
应,趁热过滤,冷却结晶。
2.(1)增大接触面积,加快反应速率,使反应更充分
(2)(NH ) SO 2NH ↑+SO ↑+H O
4 2 4 3 3 2
解析 (2)(NH ) SO 不稳定,易分解,产物中有NH 和SO ,发生热分解的化学方程式为(NH ) SO
4 2 4 3 3 4 2 4
2NH ↑+SO ↑+H O。
3 3 2
3.(1)NH (2)SiO (3)CaSO +(NH ) CO ===CaCO +(NH ) SO K (CaSO )>K (CaCO ),微溶的硫酸钙转化
3 2 4 4 2 3 3 4 2 4 sp 4 sp 3
为更难溶的碳酸钙
解析 (1)高炉渣的主要成分为CaO、MgO、Al O 和SiO 等,加入(NH ) SO 在400 ℃下焙烧,生成硫酸钙、
2 3 2 4 2 4
硫酸镁、硫酸铝,同时产生气体,该气体与烟气(CO 和水蒸气)反应,生成(NH ) CO ,所以该气体为
2 4 2 3
NH 。(2)焙烧后的固体有未反应的SiO 及反应产生的硫酸钙、硫酸镁、硫酸铝,经过水浸1,然后过滤,
3 2
滤渣为CaSO 以及未反应的SiO ,滤液溶质主要为硫酸镁、硫酸铝及硫酸铵,将滤液浓缩结晶,析出
4 2
NH Al(SO ) ·12H O,剩余富镁溶液。(3)滤渣含硫酸钙和SiO ,“水浸2”时,由于
4 4 2 2 2
K (CaSO )>K (CaCO ),CaSO 与加入的(NH ) CO 溶液反应转化为更难溶的碳酸钙,反应的化学方程式为
sp 4 sp 3 4 4 2 3
CaSO +(NH ) CO ===CaCO +(NH ) SO 。
4 4 2 3 3 4 2 4
4.(1)2Al O (熔融) 4Al+3O ↑ (2)Ga3++4Cl-===[GaCl ]-
2 3 2 4
解析 电解铝的副产品炭渣(含C、Na、Al、F和少量的Ga、Fe、K、Ca等元素)进行焙烧,金属转化为氧
化物,焙烧后的固体加入盐酸浸取,浸取液加入铝片将Fe3+进行还原,得到原料液,原料液利用LAEM提
取,[GaCl ]-通过交换膜进入Ⅱ室并转化为Ga3+,Ⅱ室溶液进一步处理得到镓,Ⅰ室溶液加入含F-的废液调
4
pH并结晶得到Na [AlF ]晶体用于电解铝。
3 6
(1)“电解”是电解熔融的氧化铝冶炼铝单质,反应的化学方程式为2Al O (熔融) 4Al+3O ↑。
2 3 2
(2)“浸取”中,由Ga3+形成[GaCl ]-的离子方程式为Ga3++4Cl-===[GaCl ]-。
4 4
5.(1)MnCO +H SO ===MnSO +H O+CO ↑ 粉碎菱锰矿(或搅拌、适当升高温度等) (2)将Fe2+氧化为Fe3+
3 2 4 4 2 2
Mn2+和生成的Fe3+可以催化H O 分解 (4)BaSO 、NiS
2 2 4
(5)Mn2++2H O H ↑+MnO ↓+2H+ 加入Mn(OH) (6)2Li CO +8MnO 4LiMn O +2CO ↑+O ↑
2 2 2 2 2 3 2 2 4 2 2
解析
(4)加入少量BaS溶液除去Ni2+,此时溶液中发生反应的离子方程式为Ba2++S2-+Ni2++SO2-
4
===BaSO ↓+NiS↓。(5)在电解槽中,Mn2+发生反应生成MnO ,离子方程式为Mn2++2H O
4 2 2
H ↑+MnO ↓+2H+。
2 2
6.KHCO +Ca(OH) ===CaCO +KOH+H O 相同质量的LiOH固体可吸收更多二氧化碳
3 2 3 2
解析 由图可知“吸收”后所得的KHCO 溶液与石灰乳反应生成的碳酸钙用于煅烧产生二氧化碳,产物
3
KOH可回收利用,故化学方程式为KHCO +Ca(OH) ===CaCO +KOH+H O。
3 2 3 2