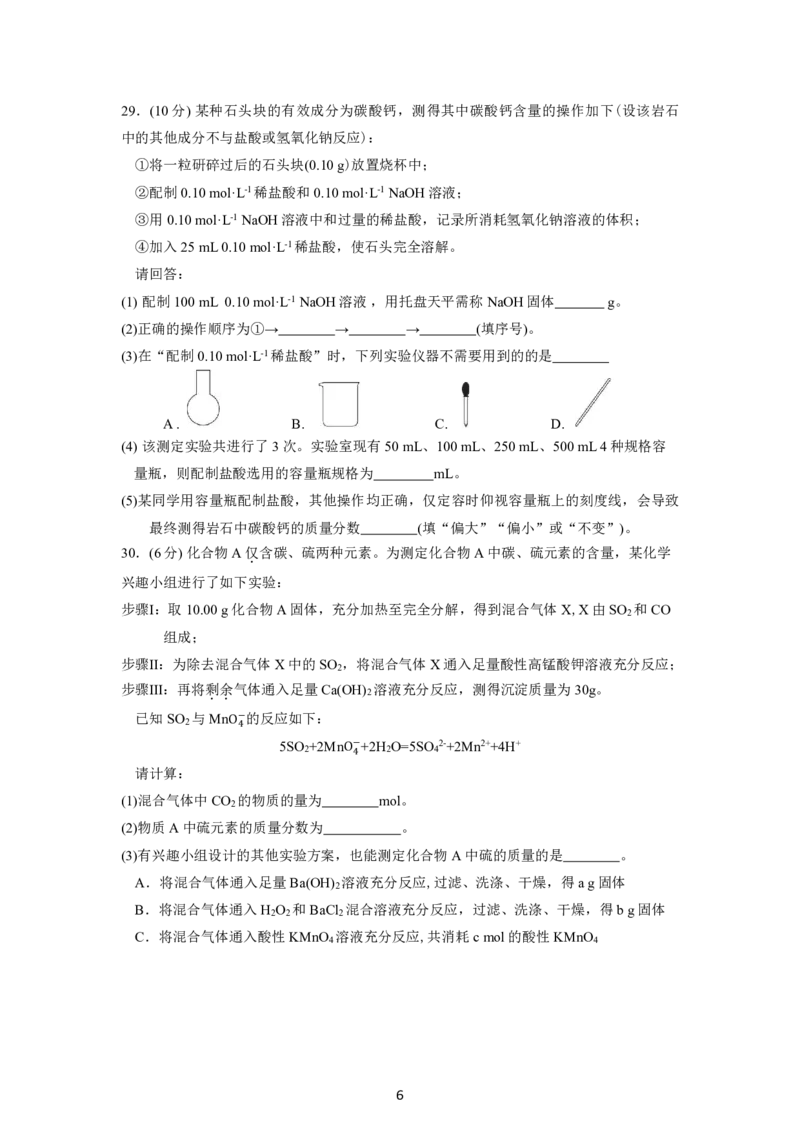文档内容
余姚中学 2025学年第二学期 4月质量检测高一化学学考试卷
命题:黄金萍 审题:胡洁玲
本试题卷分选择题和非选择题两部分,共6页,满分100分,考试时间60分钟。
考生注意:
1.答题前,请将自己的姓名等用黑色字迹的签字笔或钢笔填写在答题纸规定的位置上。
2.非选择题的答案必须使用黑色字迹的签字笔或钢笔写在答题纸上相应区域内,答案写在
本试题卷上无效。
3.可能用到的相对原子质量:H1 Li7 C12 O16 Na23 Mg24 Al27 S32 Cl35.5
Ca40 Fe56 Cu64 Ag108 I127 Ba137
选择题部分
一、选择题I(本大题共15小题,每小题2分,共30分。每小题列出的四个备选项中
只有一个是符合题目要求的,不选、多选、错选均不得分)
1.按物质的组成进行分类,Na O属于( )
2
A.氧化物 B.酸 C.碱 D.盐
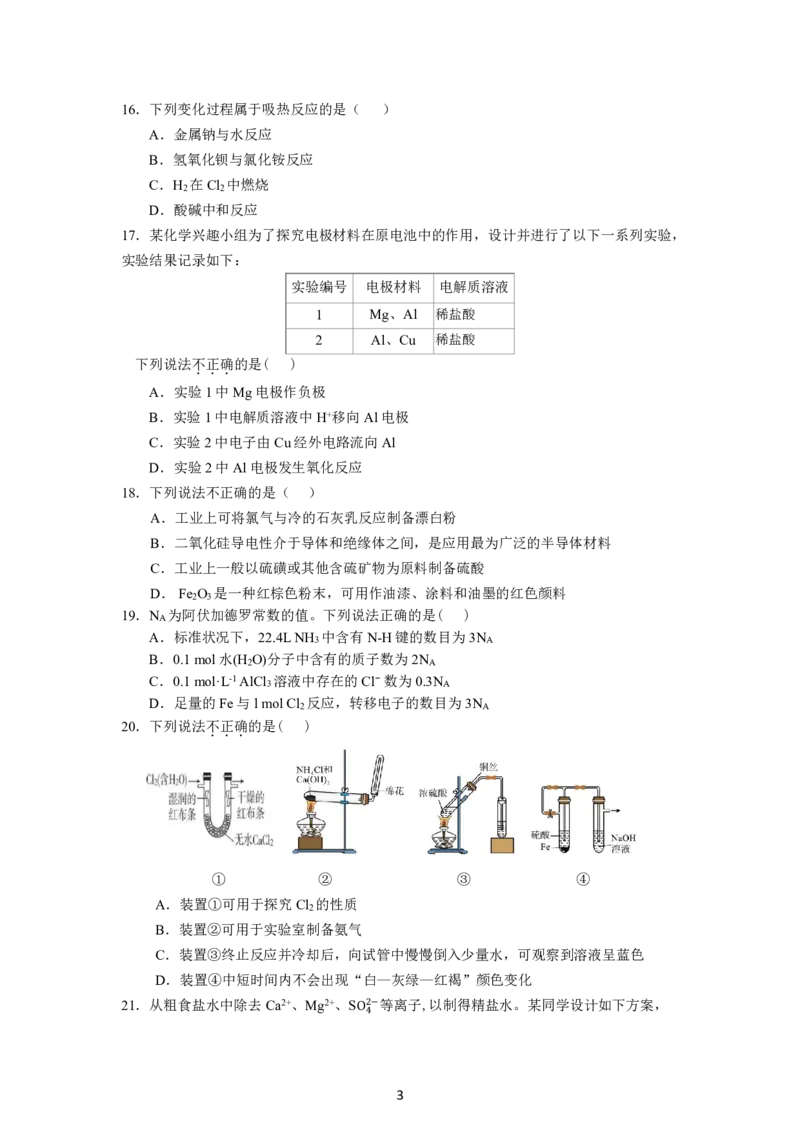
2.为了钠与水反应实验的安全,标注的图标中不
.
需要的是( )
A B C D
3.下列物质属于电解质的是( )
A.稀盐酸 B.Cu C.CO
2
D.Ba(OH)
2
4.下列分散系不
.
能
.
产生“丁达尔效应”的是( )
A.食盐溶液 B.氢氧化铁胶体 C.雾 D.有色玻璃
5.气体摩尔体积的单位是( )
A.mol·L-1 B.L·mol-1 C.L D.mol-1
6.反应2Na+2H O===2NaOH+H ↑中的还原产物是( )
2 2
A.Na B.H O C.NaOH D.H
2 2
7.下列说法不
.
正
.
确
.
的是( )
A.硅原子的结构示意图:
B.金刚石和石墨烯互为同素异形体
C.1H 、2H 、3H 互为同位素
2 2 2
D.甲烷分子的空间填充模型:
8.下列物质中化学键只
.
有
.
极性共价键的是( )
A.Br B.H O C.K S D.NaOH
2 2 2
9.下列说法不
.
正
.
确
.
的是( )
A.SO 可用于漂白纸浆以及草帽等编织物
2
B.碳酸氢钠可用于制造肥皂、玻璃等
1C.Na O 固体呈淡黄色,可用作潜水艇中的供氧剂
2 2
D.ClO 可用于自来水的杀菌消毒
2
10.下列说法不
.
正
.
确
.
的是( )
A.实验未用完的钠、钾、白磷可放回原试剂瓶
B.轻微烫伤或烧伤时,可先用洁净的冷水处理,降低局部温度
C.可通过盛有饱和Na CO 溶液的洗气瓶除去Cl 中的HCl
2 3 2
D.氯气泄漏时,应用浸有肥皂水的毛巾捂住口鼻向高处撤离
11.下列反应的离子方程式不
.
正
.
确
.
的是( )
A.CaCO 溶于盐酸:CaCO +2H+===Ca2++CO ↑+H O
3 3 2 2
B.Al O 溶于NaOH溶液:Al O +2OH−+3H O===2[Al(OH) ]−
2 3 2 3 2 4
C.用FeCl 溶液刻蚀覆铜板制作印刷电路板:2Fe3++Cu===2Fe2++Cu2+
3
D.用NaOH溶液吸收少量二氧化硫:OH−+SO ===HSO −
2 3
12.下表是元素周期表的一部分,W、X、Y、Z代表4种短周期主族元素,其中Z原子M
层电子数是K层的3倍。下列说法不
.
正
.
确
.
的是( )
W X
Y Z
A.简单气态氢化物的稳定性:W>X
B.原子半径:Y>X
C.Y与Z可能会组成离子化合物Y Z
2 2
D.Z的最高价氧化物对应水化物的酸性比W的强
13.下列说法正确的是( )
A.HBr分子中的共用电子对偏向Br,Br显正电性
B.氯化钠固体不能导电,因为固体内无离子
C.HClO中所有原子都满足8电子稳定结构
D.H O 的分解反应有共价键的断裂和生成
2 2
14.下列各组离子在给定条件下能大量共存的是( )
A.在某无色透明溶液中:K+、NH +、Cl−、MnO -
4 4
B.有大量SCN-的溶液:Na+、Fe3+、Cl-、SO2-
4
C.有SO 2-存在的溶液中:Mg2+、Br−、Ba2+、Cl−
4
D.使紫色石蕊试液变蓝的溶液中:Na+、CO 2-、Cl−、SO 2-
3 4
15.下列说法不正确的是( )
A.硬铝常用于制造飞机的外壳
B.新型无机非金属材料有新型陶瓷、碳纳米材料等
C.英国科学家道尔顿提出分子学说
D.测定雨水pH变化,pH计比pH试纸更精确
二、选择题II(本大题共10小题,每小题3分,共30分。每小题列出的四个备选项中只
有一个是符合题目要求的,不选、多选、错选均不得分)
216.下列变化过程属于吸热反应的是( )
A.金属钠与水反应
B.氢氧化钡与氯化铵反应
C.H 在Cl 中燃烧
2 2
D.酸碱中和反应
17.某化学兴趣小组为了探究电极材料在原电池中的作用,设计并进行了以下一系列实验,
实验结果记录如下:
实验编号 电极材料 电解质溶液
1 Mg、Al 稀盐酸
2 Al、Cu 稀盐酸
下列说法不正确的是( )
...
A.实验1中Mg电极作负极
B.实验1中电解质溶液中H+移向Al电极
C.实验2中电子由Cu经外电路流向Al
D.实验2中Al电极发生氧化反应
18.下列说法不正确的是( )
A.工业上可将氯气与冷的石灰乳反应制备漂白粉
B.二氧化硅导电性介于导体和绝缘体之间,是应用最为广泛的半导体材料
C.工业上一般以硫磺或其他含硫矿物为原料制备硫酸
D.Fe O 是一种红棕色粉末,可用作油漆、涂料和油墨的红色颜料
2 3
19.N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.标准状况下,22.4LNH 中含有N-H键的数目为3N
3 A
B.0.1mol水(H O)分子中含有的质子数为2N
2 A
C.0.1mol·L-1AlCl 溶液中存在的Cl−数为0.3N
3 A
D.足量的Fe与lmolCl 反应,转移电子的数目为3N
2 A
20.下列说法不
.
正
.
确
.
的是( )
① ② ③ ④
A.装置①可用于探究Cl 的性质
2
B.装置②可用于实验室制备氨气
C.装置③终止反应并冷却后,向试管中慢慢倒入少量水,可观察到溶液呈蓝色
D.装置④中短时间内不会出现“白—灰绿—红褐”颜色变化
21.从粗食盐水中除去Ca2+、Mg2+、S 等离子,以制得精盐水。某同学设计如下方案,
2−
O4
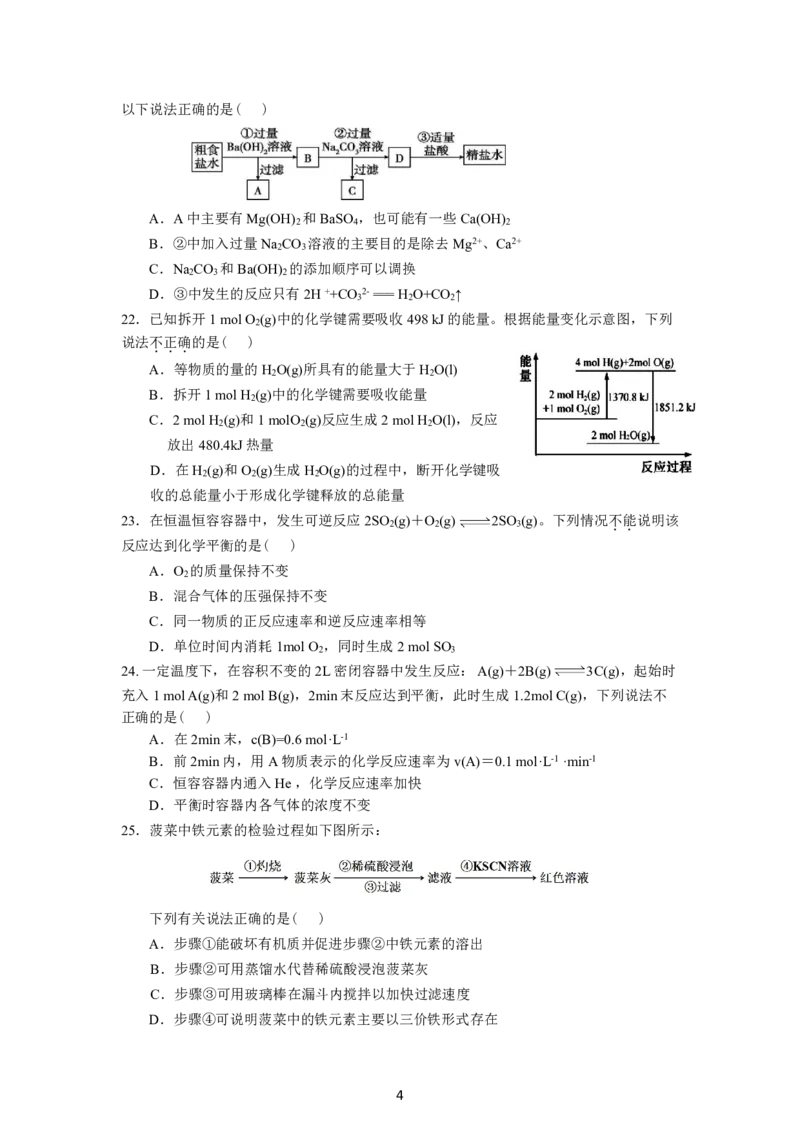
3以下说法正确的是( )
A.A中主要有Mg(OH) 和BaSO ,也可能有一些Ca(OH)
2 4 2
B.②中加入过量Na CO 溶液的主要目的是除去Mg2+、Ca2+
2 3
C.Na CO 和Ba(OH) 的添加顺序可以调换
2 3 2
D.③中发生的反应只有2H++CO 2-===H O+CO ↑
3 2 2
22.已知拆开1molO (g)中的化学键需要吸收498kJ的能量。根据能量变化示意图,下列
2
说法不正确的是( )
...
A.等物质的量的H O(g)所具有的能量大于H O(l)
2 2
B.拆开1molH (g)中的化学键需要吸收能量
2
C.2molH (g)和1molO (g)反应生成2molH O(l),反应
2 2 2
放出480.4kJ热量
D.在H (g)和O (g)生成H O(g)的过程中,断开化学键吸
2 2 2
收的总能量小于形成化学键释放的总能量
23.在恒温恒容容器中,发生可逆反应2SO 2 (g)+O 2 (g) 2SO 3 (g)。下列情况不 . 能 . 说明该
反应达到化学平衡的是( )
A.O 的质量保持不变
2
B.混合气体的压强保持不变
C.同一物质的正反应速率和逆反应速率相等
D.单位时间内消耗1molO ,同时生成2molSO
2 3
24.一定温度下,在容积不变的2L密闭容器中发生反应:A(g)+2B(g) 3C(g),起始时
充入1molA(g)和2molB(g),2min末反应达到平衡,此时生成1.2molC(g),下列说法不
正确的是( )
A.在2min末,c(B)=0.6mol·L-1
B.前2min内,用A物质表示的化学反应速率为v(A)=0.1mol·L-1·min-1
C.恒容容器内通入He,化学反应速率加快
D.平衡时容器内各气体的浓度不变
25.菠菜中铁元素的检验过程如下图所示:
下列有关说法正确的是( )
A.步骤①能破坏有机质并促进步骤②中铁元素的溶出
B.步骤②可用蒸馏水代替稀硫酸浸泡菠菜灰
C.步骤③可用玻璃棒在漏斗内搅拌以加快过滤速度
D.步骤④可说明菠菜中的铁元素主要以三价铁形式存在
4非选择题部分
三、非选择题(本大题共5小题,共40分)
26.(8分)
(1)①纯碱的化学式 ;②氯化氢的电子式
(2)Na SO 溶液进行焰色试验,可观察到 色的火焰。
2 4
(3)钠与水反应的离子方程式
27.(8分)氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧
化制硝酸的流程示意图。
请回答:
(1)氧化炉中发生的化学反应方程式为 。
(2)工业生产中为了盛装大量浓硝酸,可选择_______作为罐体材料。
A.镁 B.铜 C.铁 D.铝
(3)下列说法正确的是 。
A.“合成塔”中使H 的转化率为100%
2
B.“氨分离器”分离出氨气,利用氨气易液化的性质
C.向“吸收塔”里通入A的目的是将NO转化为NO
2
D.为避免硝酸生成尾气中的氮氧化物污染空气,可将其点燃处理
(4)在一定条件下,NH 与NO反应生成N 和H O,该反应体现NH 的 性。
3 2 2 3
28.(8分)一定温度下,在密闭容器中发生反应:N (g)+3H (g) 2NH (g)。键能是指气
2 2 3
态分子中1mol化学键解离成气态原子所吸收的能量,共价键的键能信息如表:
共价键 N—H N—N H—H N≡N O—H
键能/
391 161 436 946 463
(kJ·mol-1)
(1)该反应为 (填“吸热”或“放热”)反应。
(2)要增大该反应的反应速率,下列措施可行的是 (填字母)。
A.降低温度 B. 增大体积 C.加合适催化剂 D.充入N
2
(3)将1molN 和3molH 充入容积不变的2L密闭容器中发生反应,在2min末达到平衡,
2 2
测得此时的NH 的浓度为0.6mol·L-1。
3
①在2min末,N 的浓度为
2
②0~2min内,用H 的浓度变化表示反应的平均速率
2
529.(10分)某种石头块的有效成分为碳酸钙,测得其中碳酸钙含量的操作加下(设该岩石
中的其他成分不与盐酸或氢氧化钠反应):
①将一粒研碎过后的石头块(0.10g)放置烧杯中;
②配制0.10mol·L-1稀盐酸和0.10mol·L-1NaOH溶液;
③用0.10mol·L-1NaOH溶液中和过量的稀盐酸,记录所消耗氢氧化钠溶液的体积;
④加入25mL0.10mol·L-1稀盐酸,使石头完全溶解。
请回答:
(1) 配制100mL 0.10mol·L-1NaOH溶液,用托盘天平需称NaOH固体 g。
(2)正确的操作顺序为①→ → → (填序号)。
(3)在“配制0.10mol·L-1稀盐酸”时,下列实验仪器不需要用到的的是
A. B. C. D.
(4) 该测定实验共进行了3次。实验室现有50mL、100mL、250mL、500mL4种规格容
量瓶,则配制盐酸选用的容量瓶规格为 mL。
(5)某同学用容量瓶配制盐酸,其他操作均正确,仅定容时仰视容量瓶上的刻度线,会导致
最终测得岩石中碳酸钙的质量分数 (填“偏大”“偏小”或“不变”)。
30.(6分)化合物A仅
.
含碳、硫两种元素。为测定化合物A中碳、硫元素的含量,某化学
兴趣小组进行了如下实验:
步骤Ⅰ:取10.00g化合物A固体,充分加热至完全分解,得到混合气体X,X由SO 和CO
2
组成;
步骤Ⅱ:为除去混合气体X中的SO ,将混合气体X通入足量酸性高锰酸钾溶液充分反应;
2
步骤Ⅲ:再将剩
.
余
.
气体通入足量Ca(OH)
2
溶液充分反应,测得沉淀质量为30g。
已知SO 与Mn 的反应如下:
2
−
O4 5SO
2
+2Mn +2H
2
O=5SO
4
2-+2Mn2++4H+
−
请计算: O4
(1)混合气体中CO 的物质的量为 mol。
2
(2)物质A中硫元素的质量分数为 。
(3)有兴趣小组设计的其他实验方案,也能测定化合物A中硫的质量的是 。
A.将混合气体通入足量Ba(OH) 溶液充分反应,过滤、洗涤、干燥,得ag固体
2
B.将混合气体通入H O 和BaCl 混合溶液充分反应,过滤、洗涤、干燥,得bg固体
2 2 2
C.将混合气体通入酸性KMnO 溶液充分反应,共消耗cmol的酸性KMnO
4 4
67