文档内容
2015年上海市徐汇区中考化学二模试卷
一、选择题(共20分,每题1分)
1.(1分)下列物质变化,属于化学变化的是( )
A.玻璃破碎 B.冰块融化 C.干冰升华 D.蜡烛燃烧
2.(1分)稀土中提取的氧化铕(化学式为Eu O )用于荧光粉、光学滤光、夜光材
2 3
料等,则Eu O 中铕元素的化合价为( )
2 3
A.+2 B.+3 C.+5 D.+6
3.(1分)空气是一种宝贵的自然资源,从分离空气的成分中不能得到的气体是(
)
A.用作医疗急救的氧气
B.用作霓虹灯中填充气的稀有气体
C.用作食品防腐剂的氮气
D.用作清洁燃料的氢气
4.(1分)物质的化学式书写正确的是( )
A.氯化铵﹣NH Cl B.氧化铁﹣FeO
3
C.甲烷﹣CH D.纯碱﹣Na0H
4
5.(1分)下列化学方程式书写正确的是( )
A.S+O →SO ↑ B.Cu+2HCl→CuCl +H ↑
2 2 2 2
C.Fe+CuSO →FeSO +Cu D.Ca(OH) +2HCl→CaCl +H O
4 4 2 2 2
6.(1分)下图实验操作中正确的是( )
A. 吸取液体药品 B. 量取液体的读数
C. 固体药品的取用D. 熄灭酒精灯
第1页(共35页)7.(1分)对分子和原子两种微粒的叙述正确的是( )
A.原子构成分子,物质只能由分子构成
B.同种原子可能构成不同的分子
C.化学变化中分子数目一定发生变化
D.分子质量一定大于原子质量
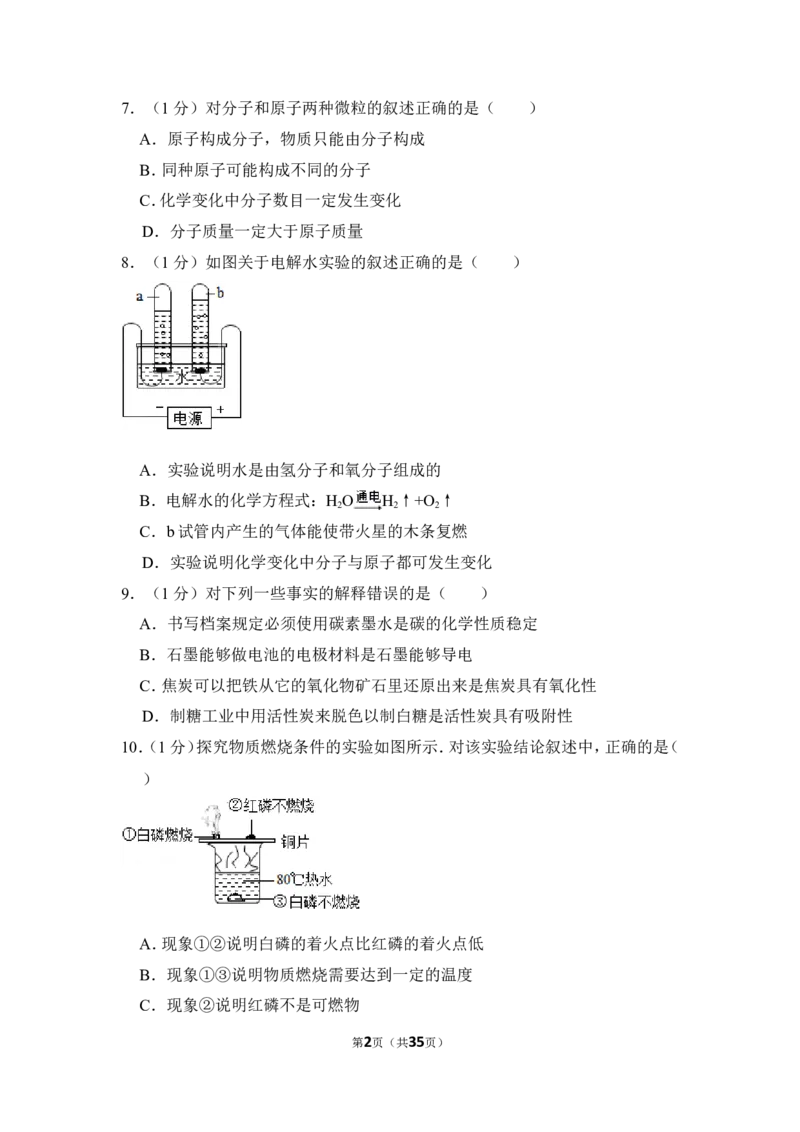
8.(1分)如图关于电解水实验的叙述正确的是( )
A.实验说明水是由氢分子和氧分子组成的
B.电解水的化学方程式:H O H ↑+O ↑
2 2 2
C.b试管内产生的气体能使带火星的木条复燃
D.实验说明化学变化中分子与原子都可发生变化
9.(1分)对下列一些事实的解释错误的是( )
A.书写档案规定必须使用碳素墨水是碳的化学性质稳定
B.石墨能够做电池的电极材料是石墨能够导电
C.焦炭可以把铁从它的氧化物矿石里还原出来是焦炭具有氧化性
D.制糖工业中用活性炭来脱色以制白糖是活性炭具有吸附性
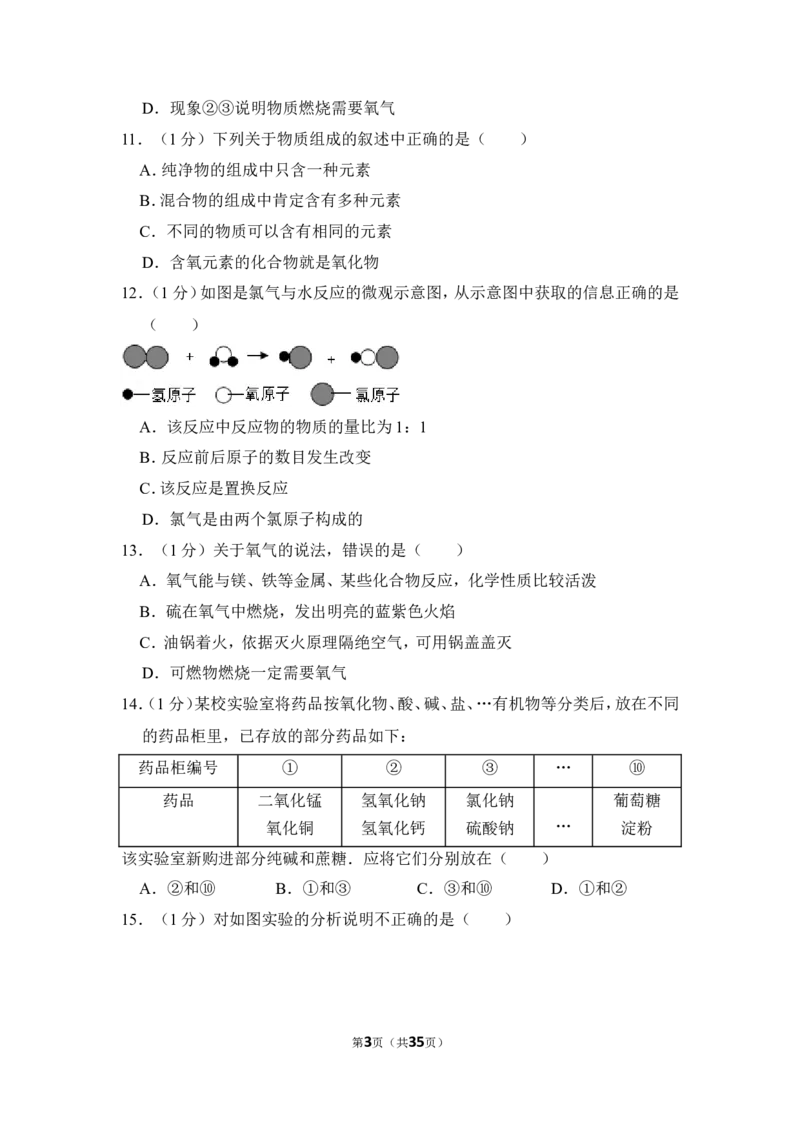
10.(1分)探究物质燃烧条件的实验如图所示.对该实验结论叙述中,正确的是(
)
A.现象①②说明白磷的着火点比红磷的着火点低
B.现象①③说明物质燃烧需要达到一定的温度
C.现象②说明红磷不是可燃物
第2页(共35页)D.现象②③说明物质燃烧需要氧气
11.(1分)下列关于物质组成的叙述中正确的是( )
A.纯净物的组成中只含一种元素
B.混合物的组成中肯定含有多种元素
C.不同的物质可以含有相同的元素
D.含氧元素的化合物就是氧化物
12.(1分)如图是氯气与水反应的微观示意图,从示意图中获取的信息正确的是
( )
A.该反应中反应物的物质的量比为1:1
B.反应前后原子的数目发生改变
C.该反应是置换反应
D.氯气是由两个氯原子构成的
13.(1分)关于氧气的说法,错误的是( )
A.氧气能与镁、铁等金属、某些化合物反应,化学性质比较活泼
B.硫在氧气中燃烧,发出明亮的蓝紫色火焰
C.油锅着火,依据灭火原理隔绝空气,可用锅盖盖灭
D.可燃物燃烧一定需要氧气
14.(1分)某校实验室将药品按氧化物、酸、碱、盐、…有机物等分类后,放在不同
的药品柜里,已存放的部分药品如下:
药品柜编号 ① ② ③ … ⑩
药品 二氧化锰 氢氧化钠 氯化钠 葡萄糖
氧化铜 氢氧化钙 硫酸钠 … 淀粉
该实验室新购进部分纯碱和蔗糖.应将它们分别放在( )
A.②和⑩ B.①和③ C.③和⑩ D.①和②
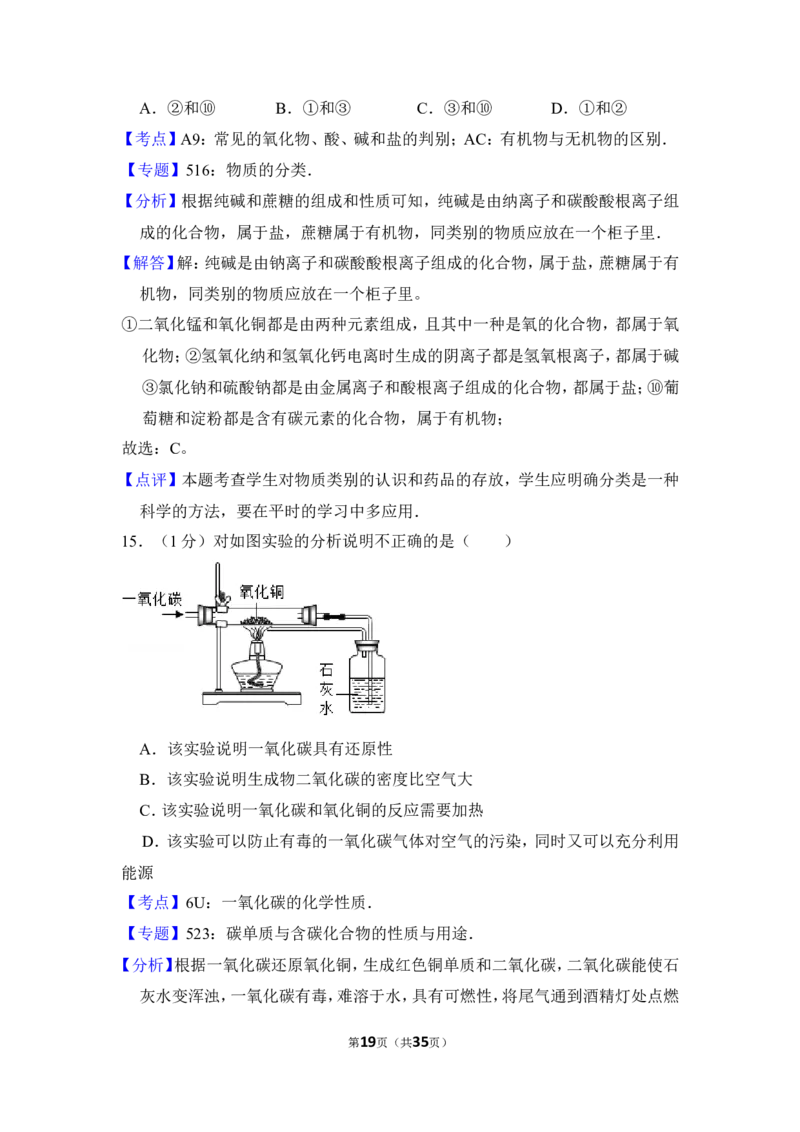
15.(1分)对如图实验的分析说明不正确的是( )
第3页(共35页)A.该实验说明一氧化碳具有还原性
B.该实验说明生成物二氧化碳的密度比空气大
C.该实验说明一氧化碳和氧化铜的反应需要加热
D.该实验可以防止有毒的一氧化碳气体对空气的污染,同时又可以充分利用
能源
16.(1分)仅用下列各组试剂无法完成验证Zn、Cu、Ag三种金属活动性顺序的是
( )
A.Zn、Ag、CuSO 溶液 B.Cu、ZnSO 溶液、AgNO 溶液
4 4 3
C.Zn、Cu、Ag、稀硫酸D.Zn、Cu、稀硫酸、AgNO 溶液
3
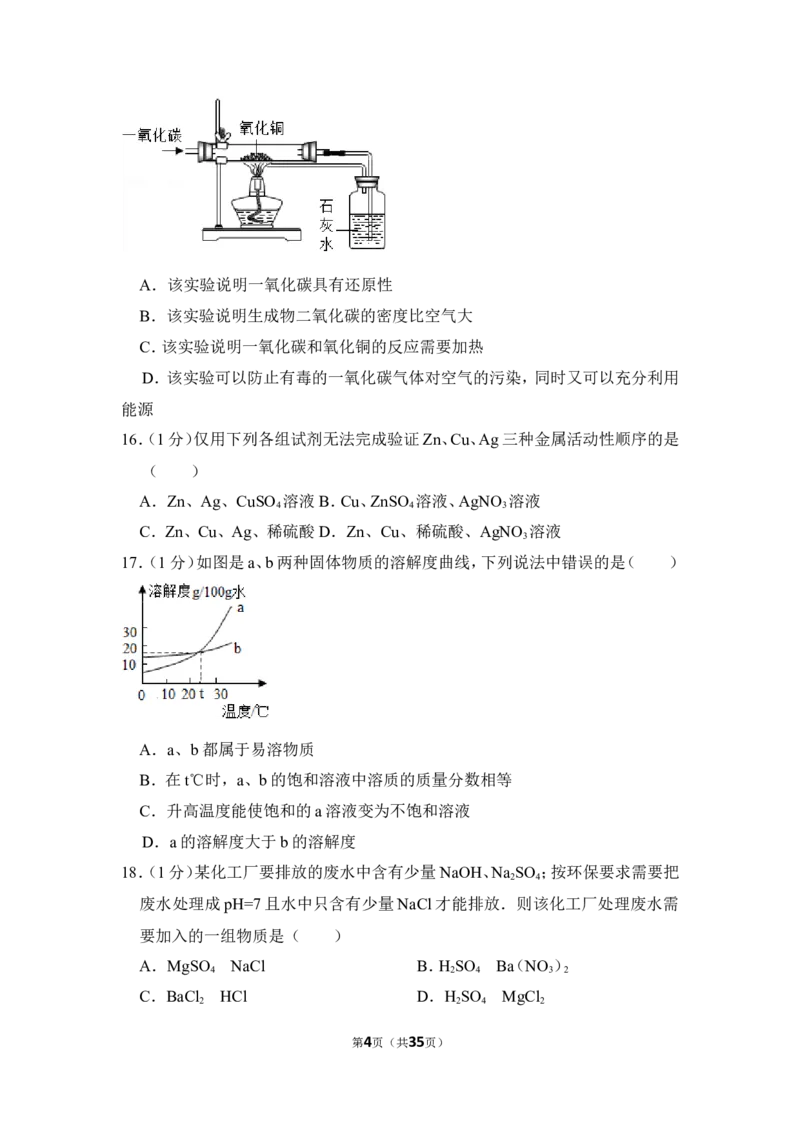
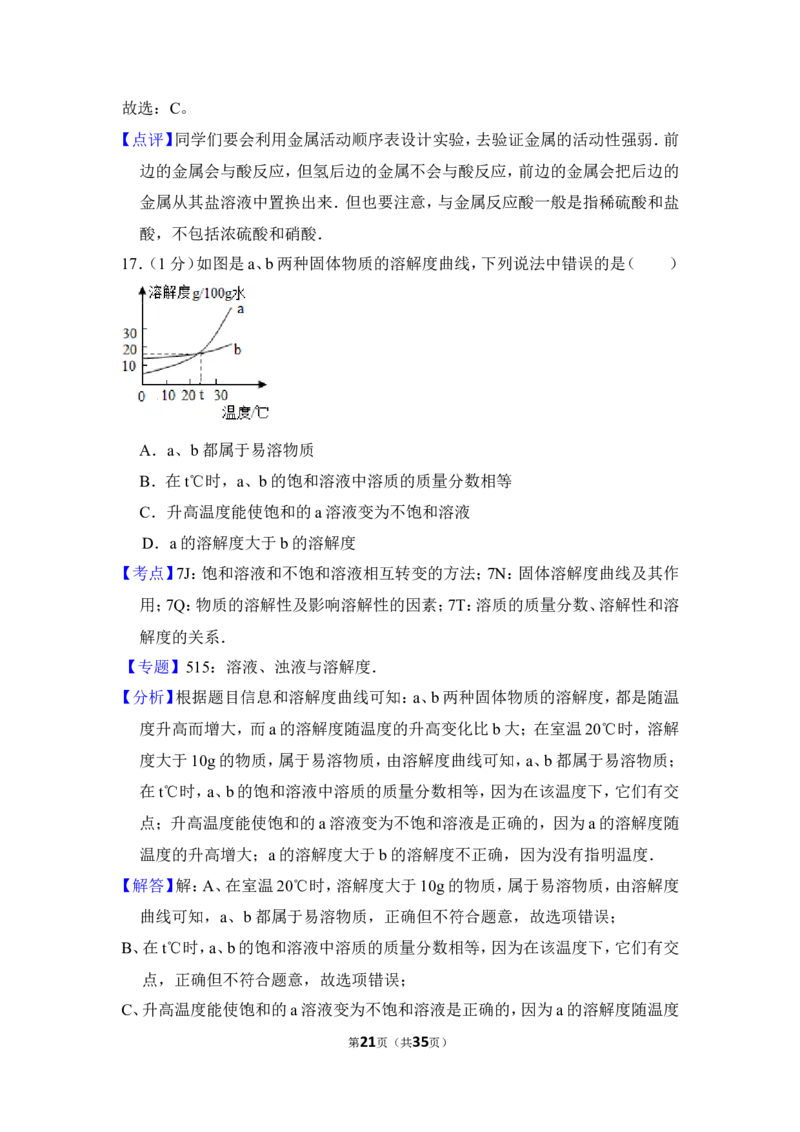
17.(1分)如图是a、b两种固体物质的溶解度曲线,下列说法中错误的是( )
A.a、b都属于易溶物质
B.在t℃时,a、b的饱和溶液中溶质的质量分数相等
C.升高温度能使饱和的a溶液变为不饱和溶液
D.a的溶解度大于b的溶解度
18.(1分)某化工厂要排放的废水中含有少量NaOH、Na SO ;按环保要求需要把
2 4
废水处理成pH=7且水中只含有少量NaCl才能排放.则该化工厂处理废水需
要加入的一组物质是( )
A.MgSO NaCl B.H SO Ba(NO )
4 2 4 3 2
C.BaCl HCl D.H SO MgCl
2 2 4 2
第4页(共35页)19.(1分)1个铅(Pb)原子质量是34.419×10﹣26Kg,一个碳﹣12原子质量是
1.993×10﹣26Kg,则铅原子的相对原子质量是( )
A.68.6 B.207.2 C.413.0 D.823.2
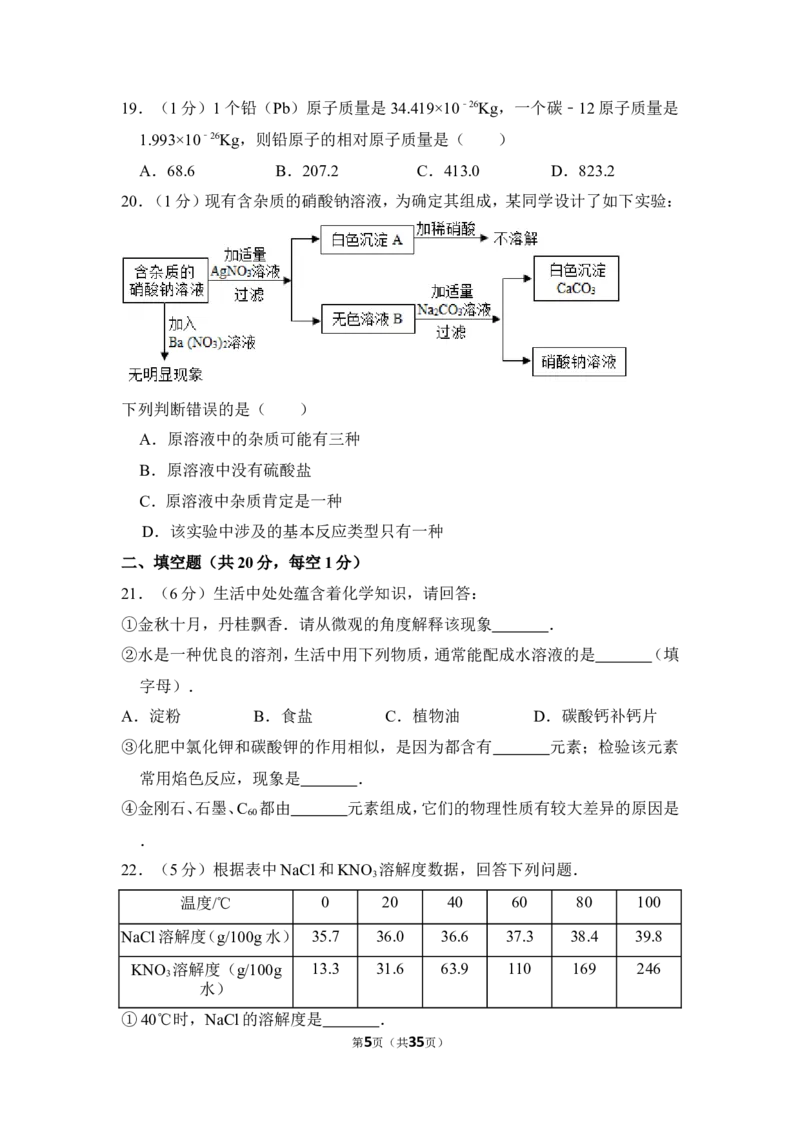
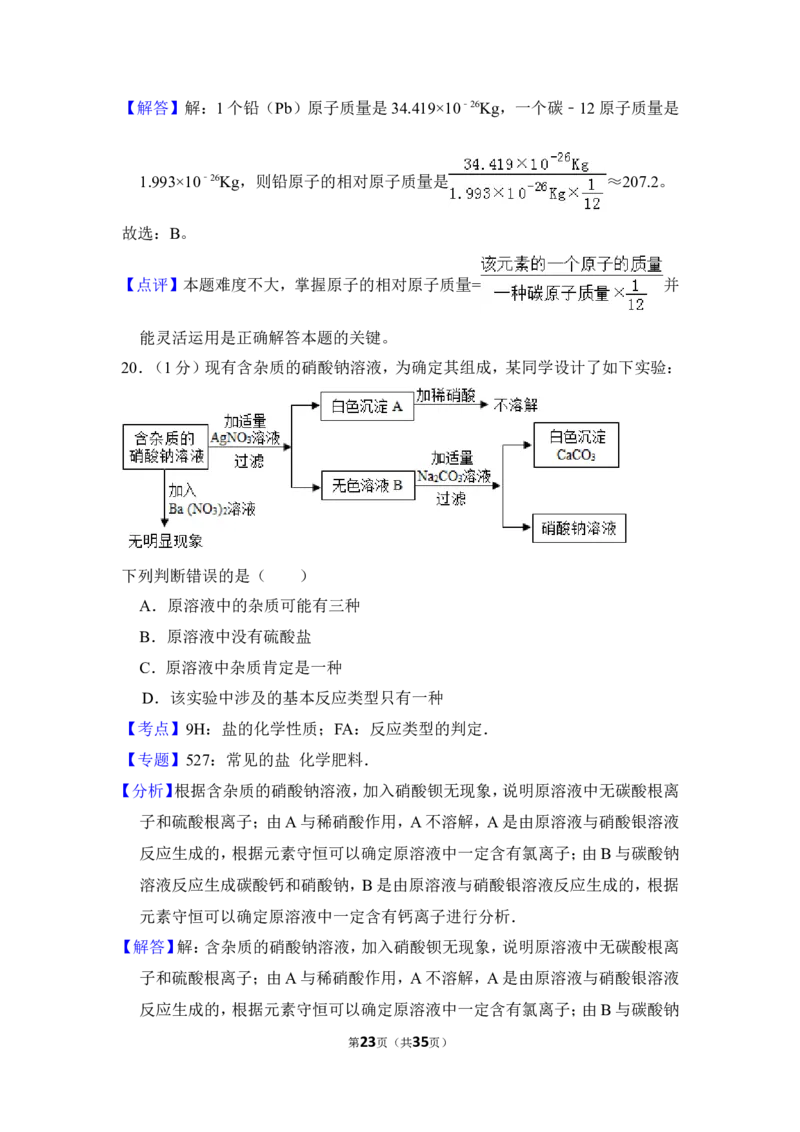
20.(1分)现有含杂质的硝酸钠溶液,为确定其组成,某同学设计了如下实验:
下列判断错误的是( )
A.原溶液中的杂质可能有三种
B.原溶液中没有硫酸盐
C.原溶液中杂质肯定是一种
D.该实验中涉及的基本反应类型只有一种
二、填空题(共20分,每空1分)
21.(6分)生活中处处蕴含着化学知识,请回答:
①金秋十月,丹桂飘香.请从微观的角度解释该现象 .
②水是一种优良的溶剂,生活中用下列物质,通常能配成水溶液的是 (填
字母).
A.淀粉 B.食盐 C.植物油 D.碳酸钙补钙片
③化肥中氯化钾和碳酸钾的作用相似,是因为都含有 元素;检验该元素
常用焰色反应,现象是 .
④金刚石、石墨、C 都由 元素组成,它们的物理性质有较大差异的原因是
60
.
22.(5分)根据表中NaCl和KNO 溶解度数据,回答下列问题.
3
温度/℃ 0 20 40 60 80 100
NaCl溶解度(g/100g水) 35.7 36.0 36.6 37.3 38.4 39.8
KNO 溶解度(g/100g 13.3 31.6 63.9 110 169 246
3
水)
①40℃时,NaCl的溶解度是 .
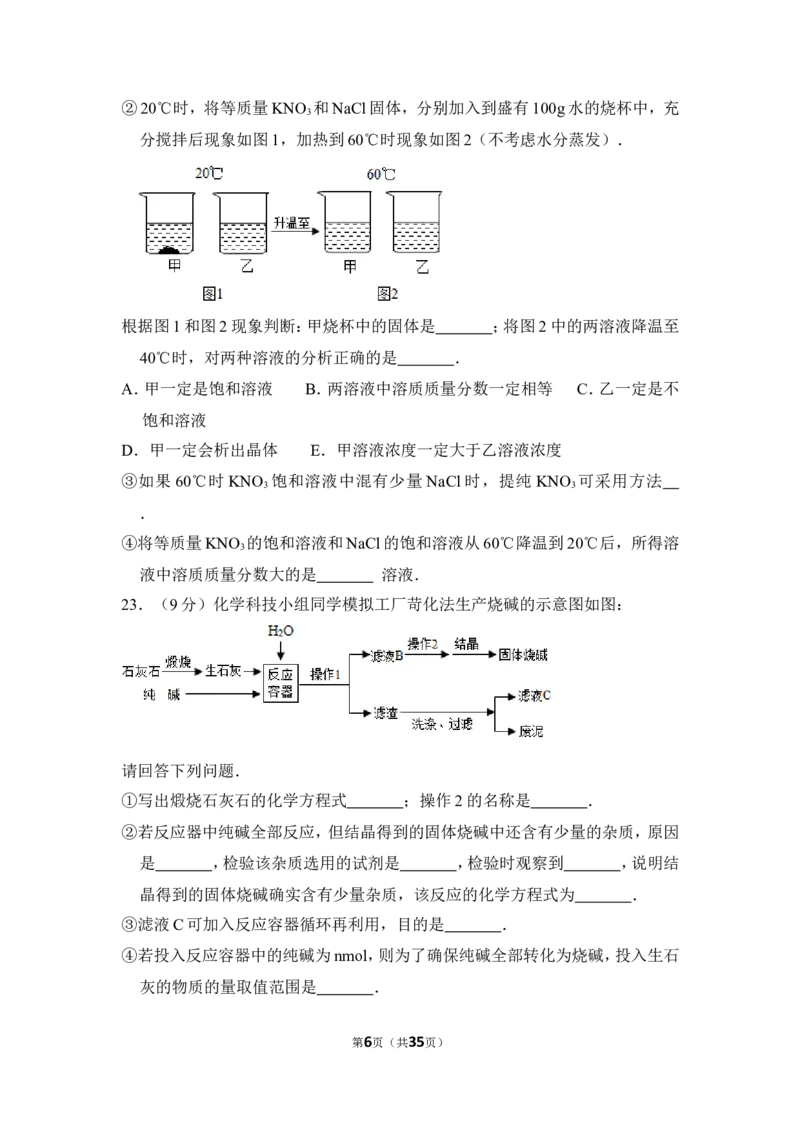
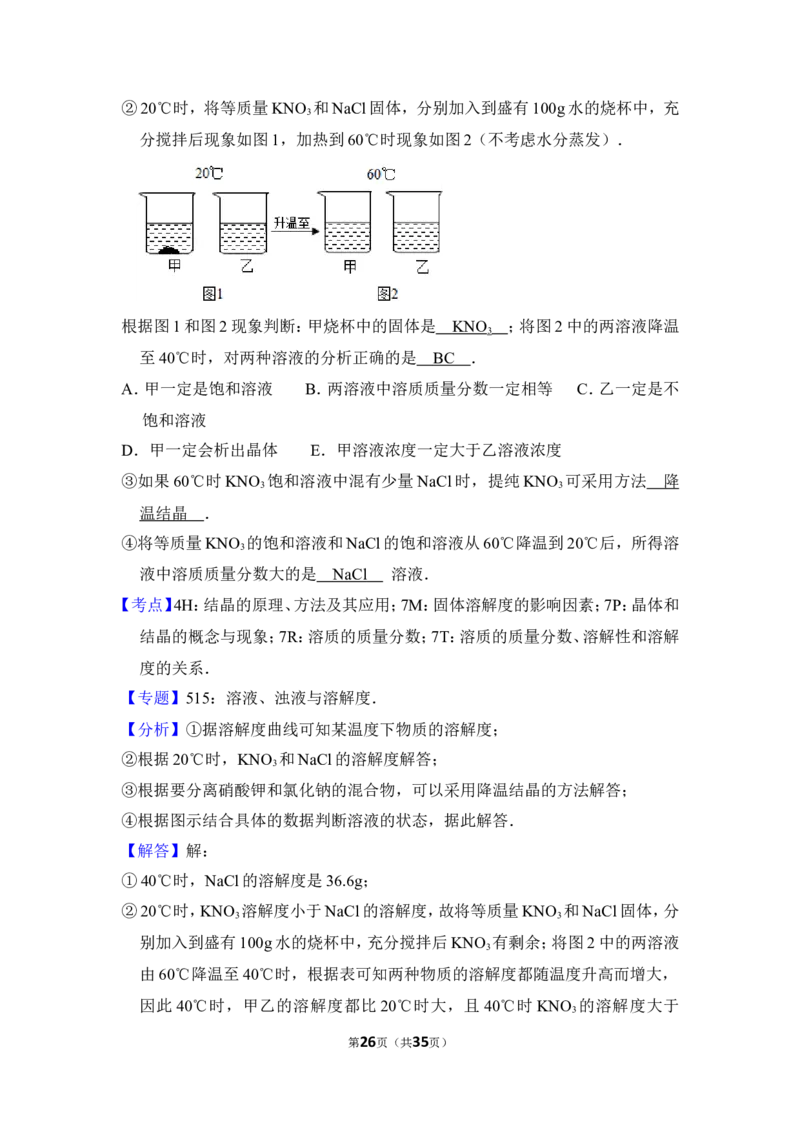
第5页(共35页)②20℃时,将等质量KNO 和NaCl固体,分别加入到盛有100g水的烧杯中,充
3
分搅拌后现象如图1,加热到60℃时现象如图2(不考虑水分蒸发).
根据图1和图2现象判断:甲烧杯中的固体是 ;将图2中的两溶液降温至
40℃时,对两种溶液的分析正确的是 .
A.甲一定是饱和溶液 B.两溶液中溶质质量分数一定相等 C.乙一定是不
饱和溶液
D.甲一定会析出晶体 E.甲溶液浓度一定大于乙溶液浓度
③如果 60℃时 KNO 饱和溶液中混有少量 NaCl 时,提纯 KNO 可采用方法
3 3
.
④将等质量KNO 的饱和溶液和NaCl的饱和溶液从60℃降温到20℃后,所得溶
3
液中溶质质量分数大的是 溶液.
23.(9分)化学科技小组同学模拟工厂苛化法生产烧碱的示意图如图:
请回答下列问题.
①写出煅烧石灰石的化学方程式 ;操作2的名称是 .
②若反应器中纯碱全部反应,但结晶得到的固体烧碱中还含有少量的杂质,原因
是 ,检验该杂质选用的试剂是 ,检验时观察到 ,说明结
晶得到的固体烧碱确实含有少量杂质,该反应的化学方程式为 .
③滤液C可加入反应容器循环再利用,目的是 .
④若投入反应容器中的纯碱为nmol,则为了确保纯碱全部转化为烧碱,投入生石
灰的物质的量取值范围是 .
第6页(共35页)三、简答题(共20分,每空1分)
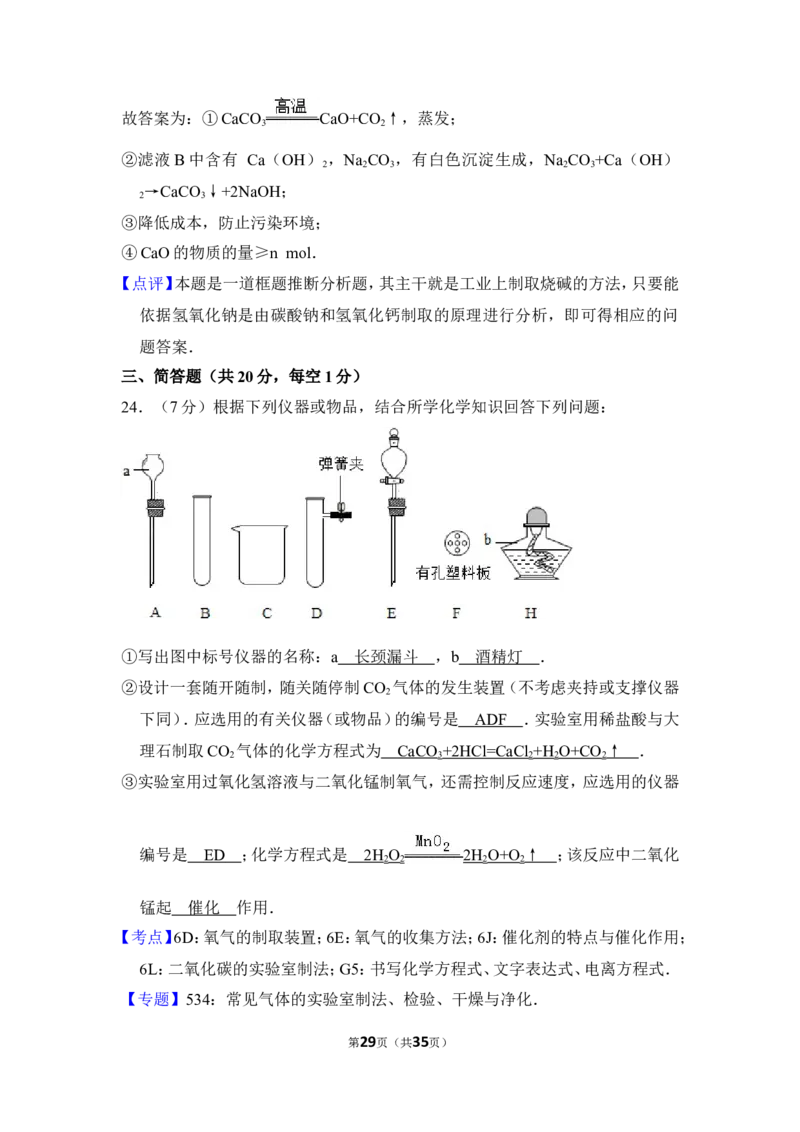
24.(7分)根据下列仪器或物品,结合所学化学知识回答下列问题:
①写出图中标号仪器的名称:a ,b .
②设计一套随开随制,随关随停制CO 气体的发生装置(不考虑夹持或支撑仪器
2
下同).应选用的有关仪器(或物品)的编号是 .实验室用稀盐酸与大理
石制取CO 气体的化学方程式为 .
2
③实验室用过氧化氢溶液与二氧化锰制氧气,还需控制反应速度,应选用的仪器
编号是 ;化学方程式是 ;该反应中二氧化锰起 作用.
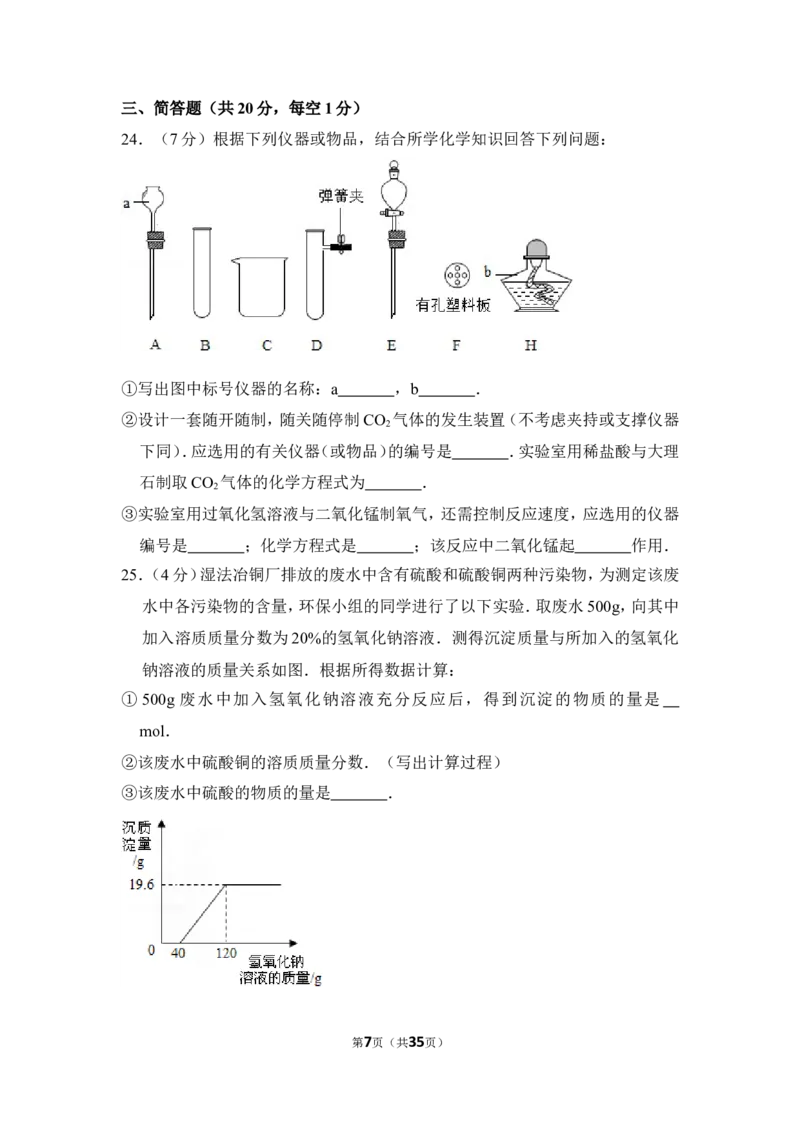
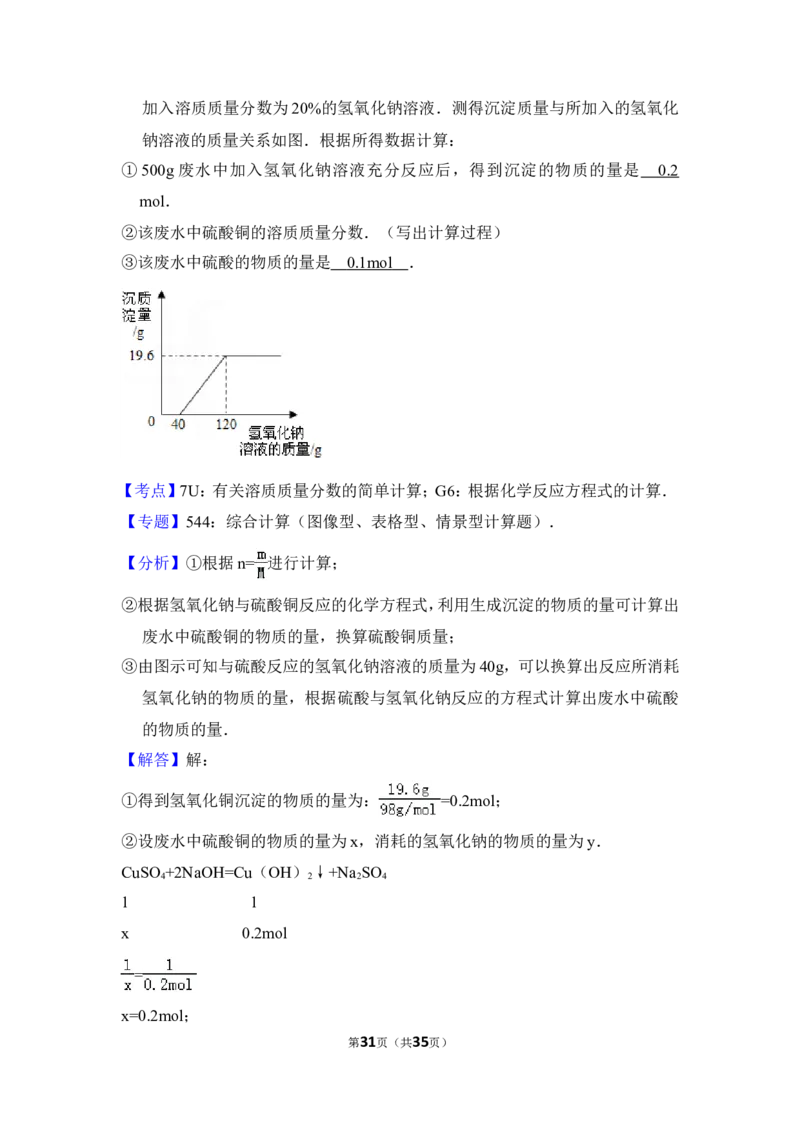
25.(4分)湿法冶铜厂排放的废水中含有硫酸和硫酸铜两种污染物,为测定该废
水中各污染物的含量,环保小组的同学进行了以下实验.取废水500g,向其中
加入溶质质量分数为20%的氢氧化钠溶液.测得沉淀质量与所加入的氢氧化
钠溶液的质量关系如图.根据所得数据计算:
① 500g 废水中加入氢氧化钠溶液充分反应后,得到沉淀的物质的量是
mol.
②该废水中硫酸铜的溶质质量分数.(写出计算过程)
③该废水中硫酸的物质的量是 .
第7页(共35页)26.(9分)氯碱工业用电解饱和食盐水制取氯气、烧碱.电解饱和食盐水的化学
方程式:
2NaCl+2H O 2NaOH+H ↑+Cl ↑
2 2 2
化学兴趣小组同学认为用上述方法制备的烧碱不纯,进行如下探究,请回答有关
问题.
①甲同学认为该烧碱可能含有少量食盐,为了检验食盐是否存在,进行了如下实
验:
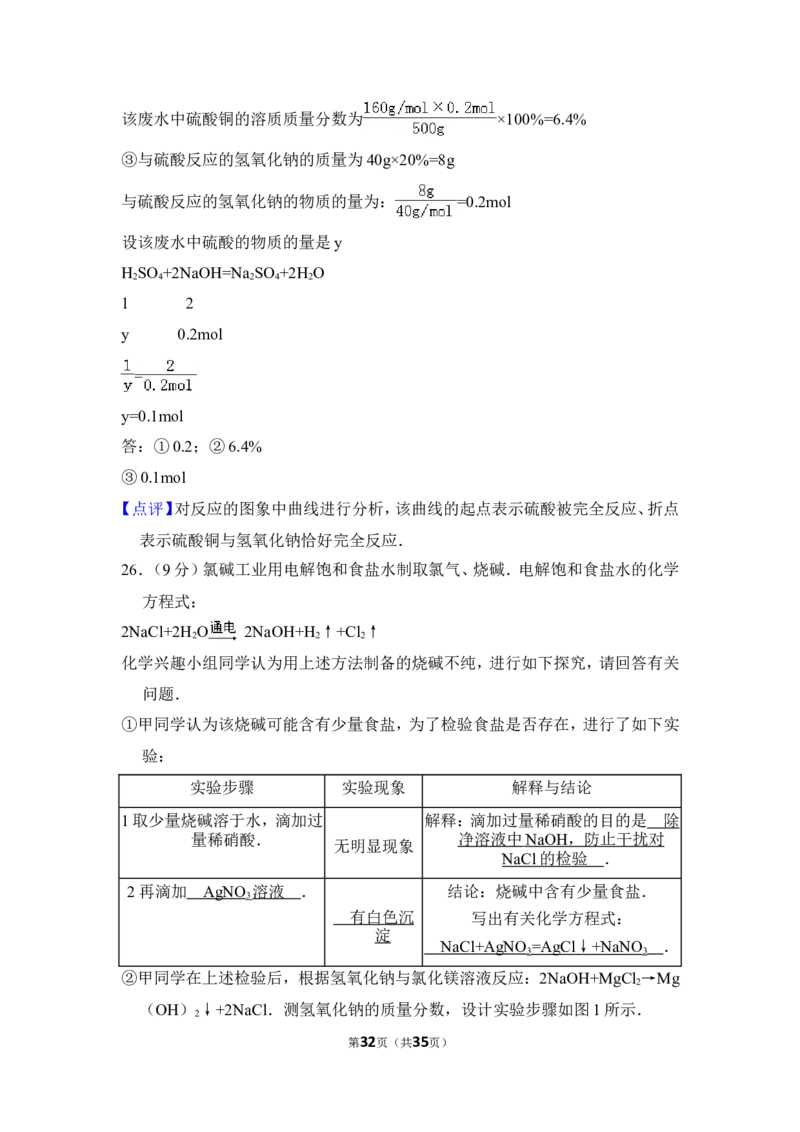
实验步骤 实验现象 解释与结论
1取少量烧碱溶于水,滴加过量 解释:滴加过量稀硝酸的目的是
稀硝酸. .
无明显现象
2再滴加 . 结论:烧碱中含有少量食盐.
写出有关化学方程式:
.
②甲同学在上述检验后,根据氢氧化钠与氯化镁溶液反应:2NaOH+MgCl →Mg
2
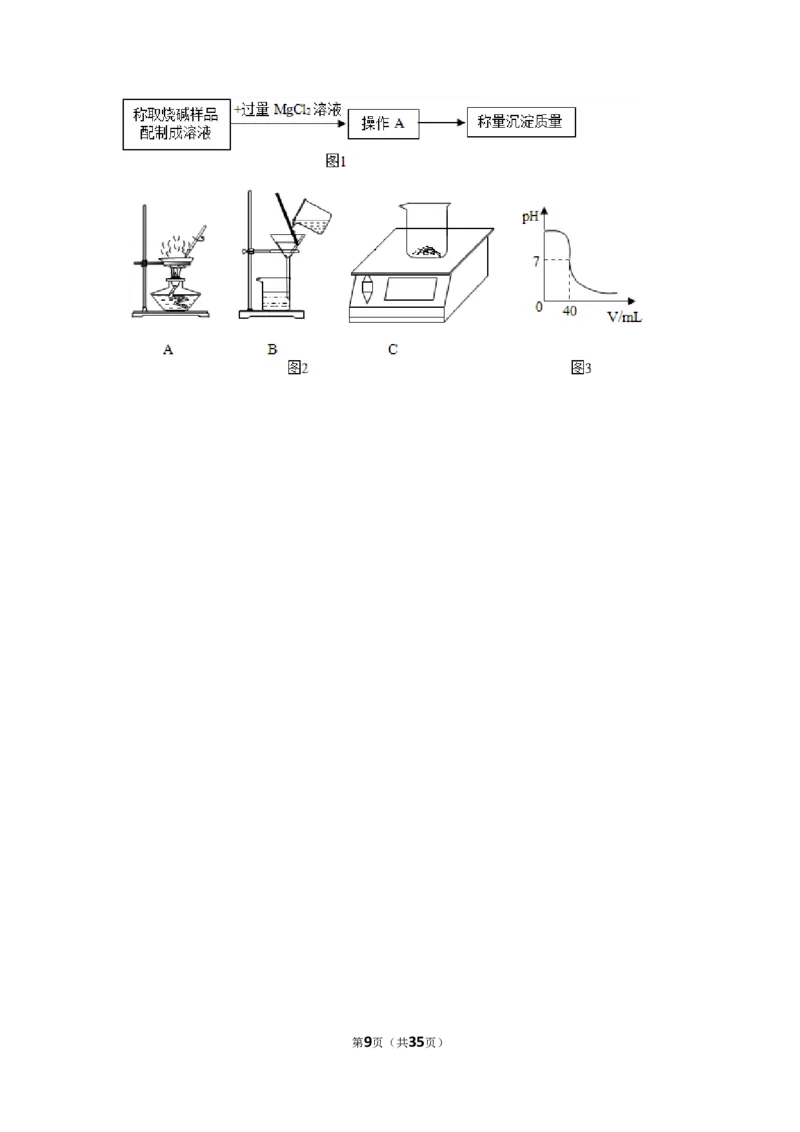
(OH) ↓+2NaCl.测氢氧化钠的质量分数,设计实验步骤如图1所示.
2
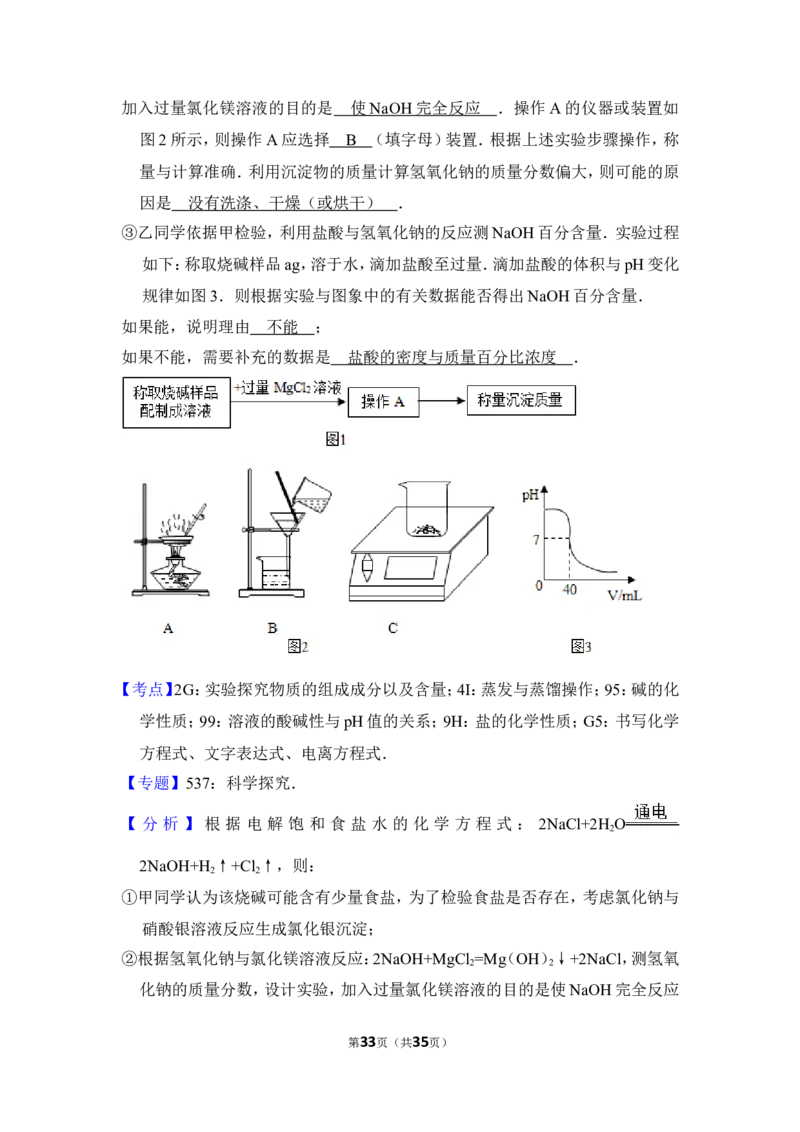
加入过量氯化镁溶液的目的是 .操作A的仪器或装置如图2所示,则操
作A应选择 (填字母)装置.根据上述实验步骤操作,称量与计算准确
利用沉淀物的质量计算氢氧化钠的质量分数偏大,则可能的原因是 .
③乙同学依据甲检验,利用盐酸与氢氧化钠的反应测NaOH百分含量.实验过程
如下:称取烧碱样品ag,溶于水,滴加盐酸至过量.滴加盐酸的体积与pH变化
规律如图3.则根据实验与图象中的有关数据能否得出NaOH百分含量.
如果能,说明理由 ;
如果不能,需要补充的数据是 .
第8页(共35页)第9页(共35页)2015 年上海市徐汇区中考化学二模试卷
参考答案与试题解析
一、选择题(共20分,每题1分)
1.(1分)下列物质变化,属于化学变化的是( )
A.玻璃破碎 B.冰块融化 C.干冰升华 D.蜡烛燃烧
【考点】E3:化学变化和物理变化的判别.
菁优网版权所有
【专题】512:物质的变化与性质.
【分析】有新物质生成的变化叫化学变化,没有新物质生成的变化叫物理变化.化
学变化的特征是:有新物质生成.判断物理变化和化学变化的依据是:是否有
新物质生成.
【解答】解:A、玻璃破碎,没有新物质生成,属于物理变化,故选项错误;
B、冰块融化只是水的状态的变化,没有新物质生成,属于物理变化,故选项错误;
C、干冰升华只是二氧化碳状态的变化,没有新物质生成,属于物理变化,故选项
错误;
D、蜡烛燃烧的过程中有新物质二氧化碳等生成,属于化学变化,故选项正确;
故选:D。
【点评】本考点考查了物理变化和化学变化的区别,基础性比较强,只要抓住关键
点:是否有新物质生成,问题就很容易解决.本考点主要出现在选择题和填空
题中.
2.(1分)稀土中提取的氧化铕(化学式为Eu O )用于荧光粉、光学滤光、夜光材
2 3
料等,则Eu O 中铕元素的化合价为( )
2 3
A.+2 B.+3 C.+5 D.+6
【考点】D6:有关元素化合价的计算.
菁优网版权所有
【专题】191:化学式的计算.
【分析】根据在化合物中正负化合价代数和为零,结合氧化铕(化学式为Eu O )的
2 3
化学式进行解答即可.
【解答】解:氧元素显﹣2价,设铕元素的化合价是x,根据在化合物中正负化合价
代数和为零,可得:2x+(﹣2)×3=0,则x=+3价。
第10页(共35页)故选:B。
【点评】本题难度不大,掌握利用化合价的原则(化合物中正负化合价代数和为
零)计算指定元素的化合价的方法即可正确解答此类题.
3.(1分)空气是一种宝贵的自然资源,从分离空气的成分中不能得到的气体是(
)
A.用作医疗急救的氧气
B.用作霓虹灯中填充气的稀有气体
C.用作食品防腐剂的氮气
D.用作清洁燃料的氢气
【考点】61:空气的成分及各成分的体积分数.
菁优网版权所有
【专题】521:空气与水.
【分析】空气中各成分的体积分数分别是:氮气大约占78%、氧气大约占21%、稀
有气体大约占0.94%、二氧化碳大约占0.03%、水蒸气和其它气体和杂质大约
占0.03%;可以利用分离液态空气法得到各种气体.
【解答】解:A、氧气大约占21%,可以直接从空气中分离出来,故选项不符合题意;
B、稀有气体大约占0.94%,可以直接从空气中分离出来,故选项不符合题意;
C、氮气大约占78%,可以直接从空气中分离出来,故选项不符合题意;
D、空气中没有氢气,因此不可直接从空气中分离,故选项符合题意。
故选:D。
【点评】本考点考查了空气中各种气体的含量,同学们要加强记忆有关的知识点,
在理解的基础上加以应用,本考点基础性比较强,主要出现在选择题和填空题
中.
4.(1分)物质的化学式书写正确的是( )
A.氯化铵﹣NH Cl B.氧化铁﹣FeO
3
C.甲烷﹣CH D.纯碱﹣Na0H
4
【考点】D1:化学式的书写及意义.
菁优网版权所有
【专题】513:化学用语和质量守恒定律.
【分析】化合物化学式的书写一般规律:先读后写,后读先写;金属在前,非金属在
后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零.
【解答】解:A.铵根离子写错了,氯化铵的化学式为NH Cl,故错误;
4
第11页(共35页)B.在氧化铁中,铁元素显+3价,氧元素显﹣2价,故化学式为Fe O ,故错误;
2 3
C.甲烷的化学式为CH ,故正确;
4
D.纯碱是碳酸钠的俗称,化学式为Na CO ,故错误。
2 3
故选:C。
【点评】本题难度不大,考查化合物化学式的书写方法,掌握化合物化学式的书写
方法是正确解答此类题的关键.
5.(1分)下列化学方程式书写正确的是( )
A.S+O →SO ↑
2 2
B.Cu+2HCl→CuCl +H ↑
2 2
C.Fe+CuSO →FeSO +Cu
4 4
D.Ca(OH) +2HCl→CaCl +H O
2 2 2
【考点】G5:书写化学方程式、文字表达式、电离方程式.
菁优网版权所有
【专题】513:化学用语和质量守恒定律.
【分析】根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书
写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.
【解答】解:A、该化学方程式缺少反应条件,反应物中氧气是气体,二氧化碳后面
不需要标注↑,正确的化学方程式应为:S+O SO 。
2 2
B、铜的金属活动性不氢弱,不能与稀盐酸反应,故选项错误。
C、该化学方程式书写完全正确。
D 、 该 化 学 方 程 式 配 平 错 误 , 正 确 的 化 学 方 程 式 应 为 Ca ( OH )
+2HCl→CaCl +2H O。
2 2 2
故选:C。
【点评】本题难度不大,在解此类题时,首先分析应用的原理是否正确,然后再根
据方程式的书写规则进行判断;化学方程式正误判断方法是:先看化学式是否
正确,再看配平,再看反应条件,再看气体和沉淀
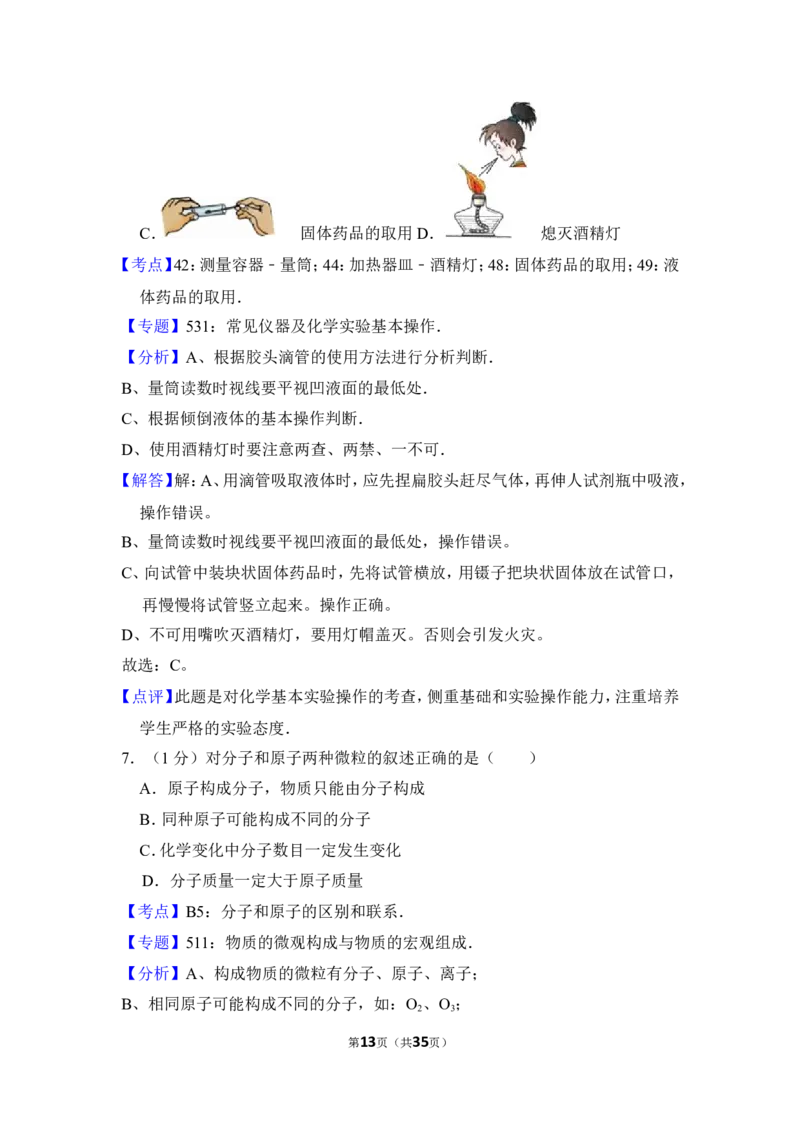
6.(1分)下图实验操作中正确的是( )
A. 吸取液体药品 B. 量取液体的读数
第12页(共35页)C. 固体药品的取用D. 熄灭酒精灯
【考点】42:测量容器﹣量筒;44:加热器皿﹣酒精灯;48:固体药品的取用;49:液
体药品的取用.
菁优网版权所有
【专题】531:常见仪器及化学实验基本操作.
【分析】A、根据胶头滴管的使用方法进行分析判断.
B、量筒读数时视线要平视凹液面的最低处.
C、根据倾倒液体的基本操作判断.
D、使用酒精灯时要注意两查、两禁、一不可.
【解答】解:A、用滴管吸取液体时,应先捏扁胶头赶尽气体,再伸人试剂瓶中吸液,
操作错误。
B、量筒读数时视线要平视凹液面的最低处,操作错误。
C、向试管中装块状固体药品时,先将试管横放,用镊子把块状固体放在试管口,
再慢慢将试管竖立起来。操作正确。
D、不可用嘴吹灭酒精灯,要用灯帽盖灭。否则会引发火灾。
故选:C。
【点评】此题是对化学基本实验操作的考查,侧重基础和实验操作能力,注重培养
学生严格的实验态度.
7.(1分)对分子和原子两种微粒的叙述正确的是( )
A.原子构成分子,物质只能由分子构成
B.同种原子可能构成不同的分子
C.化学变化中分子数目一定发生变化
D.分子质量一定大于原子质量
【考点】B5:分子和原子的区别和联系.
菁优网版权所有
【专题】511:物质的微观构成与物质的宏观组成.
【分析】A、构成物质的微粒有分子、原子、离子;
B、相同原子可能构成不同的分子,如:O 、O ;
2 3
第13页(共35页)C、化学变化中分子数目可能发生变化;
D、分子比构成它的原子的质量大,但不同的分子、原子无法比较大小;
【解答】解:A、构成物质的微粒有分子、原子、离子,故错误;
B、相同原子可能构成不同的分子,如:O 、O ,正确;
2 3
C、化学变化中分子数目可能发生变化,如:改变:2H +O 2H 0,改变:
2 2 2
H +Cl 2HCl,分子数目不改变,故错误;
2 2
D、分子比构成它的原子的质量大,但不同的分子、原子无法比较大小,故错误;
故选:B。
【点评】了解构成物质的微粒、分子、原子的相关知识即可正确解答该题,属基础
知识考查题.
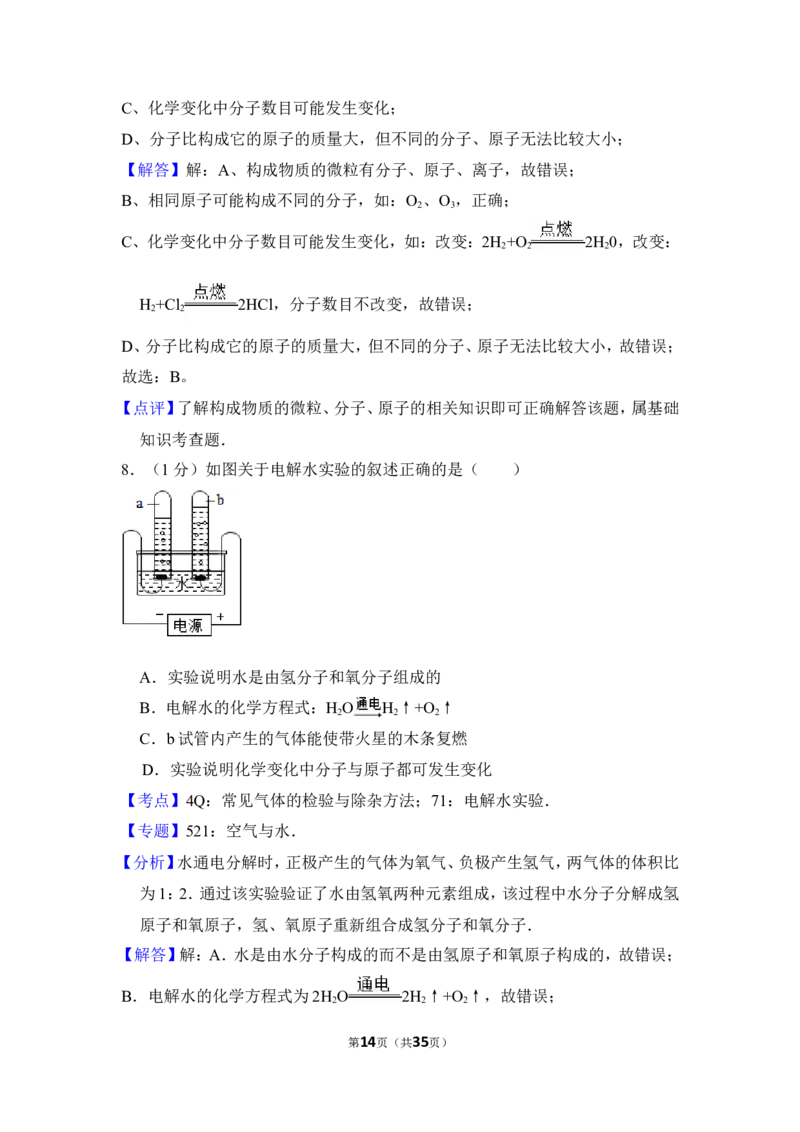
8.(1分)如图关于电解水实验的叙述正确的是( )
A.实验说明水是由氢分子和氧分子组成的
B.电解水的化学方程式:H O H ↑+O ↑
2 2 2
C.b试管内产生的气体能使带火星的木条复燃
D.实验说明化学变化中分子与原子都可发生变化
【考点】4Q:常见气体的检验与除杂方法;71:电解水实验.
菁优网版权所有
【专题】521:空气与水.
【分析】水通电分解时,正极产生的气体为氧气、负极产生氢气,两气体的体积比
为1:2.通过该实验验证了水由氢氧两种元素组成,该过程中水分子分解成氢
原子和氧原子,氢、氧原子重新组合成氢分子和氧分子.
【解答】解:A.水是由水分子构成的而不是由氢原子和氧原子构成的,故错误;
B.电解水的化学方程式为2H O 2H ↑+O ↑,故错误;
2 2 2
第14页(共35页)C.b中气体体积较小,是氧气,能使带火星的木条复燃,故正确;
D.在化学变化中,分子可以再分,而原子不能再分,故错误。
故选:C。
【点评】明确该实验的现象、化学变化的实质及由该实验所得到的结论,此为该问
题的考查目标.
9.(1分)对下列一些事实的解释错误的是( )
A.书写档案规定必须使用碳素墨水是碳的化学性质稳定
B.石墨能够做电池的电极材料是石墨能够导电
C.焦炭可以把铁从它的氧化物矿石里还原出来是焦炭具有氧化性
D.制糖工业中用活性炭来脱色以制白糖是活性炭具有吸附性
【考点】C6:碳单质的物理性质及用途;C7:碳的化学性质.
菁优网版权所有
【专题】523:碳单质与含碳化合物的性质与用途.
【分析】A、碳的化学性质稳定,使用碳素墨水书写档案,字迹长时间不会变化;
B、石墨能够导电所以能够做电池的电极材料;
C、焦炭可以把铁从它的氧化物矿石里还原出来是焦炭具有还原性;
D、活性炭具有吸附性,能够吸附有色素;
【解答】解:A、碳的化学性质稳定,使用碳素墨水书写档案,字迹长时间不会变化,
所以书写档案规定必须使用碳素墨水是碳的化学性质稳定,故A正确;
B、石墨能够导电所以能够做电池的电极材料,故B正确;
C、焦炭可以把铁从它的氧化物矿石里还原出来是焦炭具有还原性,故C错误;
D、活性炭具有吸附性,能够吸附有色素,所以制糖工业中用活性炭来脱色以制白
糖,故D正确;
故选:C。
【点评】此题主要考查了物质的性质决定物质的用途,知识强,较易回答.
10.(1分)探究物质燃烧条件的实验如图所示.对该实验结论叙述中,正确的是(
)
第15页(共35页)A.现象①②说明白磷的着火点比红磷的着火点低
B.现象①③说明物质燃烧需要达到一定的温度
C.现象②说明红磷不是可燃物
D.现象②③说明物质燃烧需要氧气
【考点】H1:燃烧与燃烧的条件.
菁优网版权所有
【专题】537:科学探究.
【分析】A、现象①②说明白磷燃烧所需温度不高于80℃,红磷高于80℃;
B、现象①③不同是因为与氧气(或空气)的接触不同;
C、红磷是可燃物;
D、现象②是因为没有达到着火点,现象③是因为不与氧气接触;
【解答】解:A、温水是80℃,铜片上的白磷燃烧,说明它的燃烧所需温度不高于
80℃,而红磷不能燃烧则说明红磷的着火点高于80℃,说明白磷的着火点比红
磷的着火点低,故正确;
B、现象①③不同是因为铜片上的白磷满足了物质燃烧的三个条件;水中的白磷
不能燃烧是因为不与氧气接触,故错误;
C、水中的白磷不燃烧,是因为没有与氧气接触,不能说明红磷不是可燃物,故错
误;
D、现象③是因为不与氧气接触,说明物质燃烧需要氧气,现象②是因为没有达到
着火点,不能说明需要氧气,故错误;
故选:A。
【点评】本题主要检测学生对“燃烧需要同时满足三个条件”这一知识点的掌握
情况.
11.(1分)下列关于物质组成的叙述中正确的是( )
A.纯净物的组成中只含一种元素
B.混合物的组成中肯定含有多种元素
C.不同的物质可以含有相同的元素
D.含氧元素的化合物就是氧化物
【考点】A3:从组成上识别氧化物;A4:纯净物和混合物的概念.
菁优网版权所有
【专题】516:物质的分类.
【分析】根据已有的概念进行分析,纯净物只含有一种物质,混合物含有多种物质,
第16页(共35页)氧化物是由两种元素组成且其中一种是氧元素的化合物,据此解答.
【解答】解:A、纯净物只含有一种物质,这种物质可能是由两种元素组成的,例如
H O,故A错误;
2
B、混合物含有多种物质,这些物质可能只由一种元素组成,例如O 和O ,故B错
2 3
误;
C、不同的物质可以含有相同的元素,例如H O和H O ,故C正确;
2 2 2
D、含氧元素的化合物不一定是氧化物,例如KMnO ,故D错误;
4
故选:C。
【点评】本题考查了有关物质的类别的判断,完成此题,可以依据已有的概念进行.
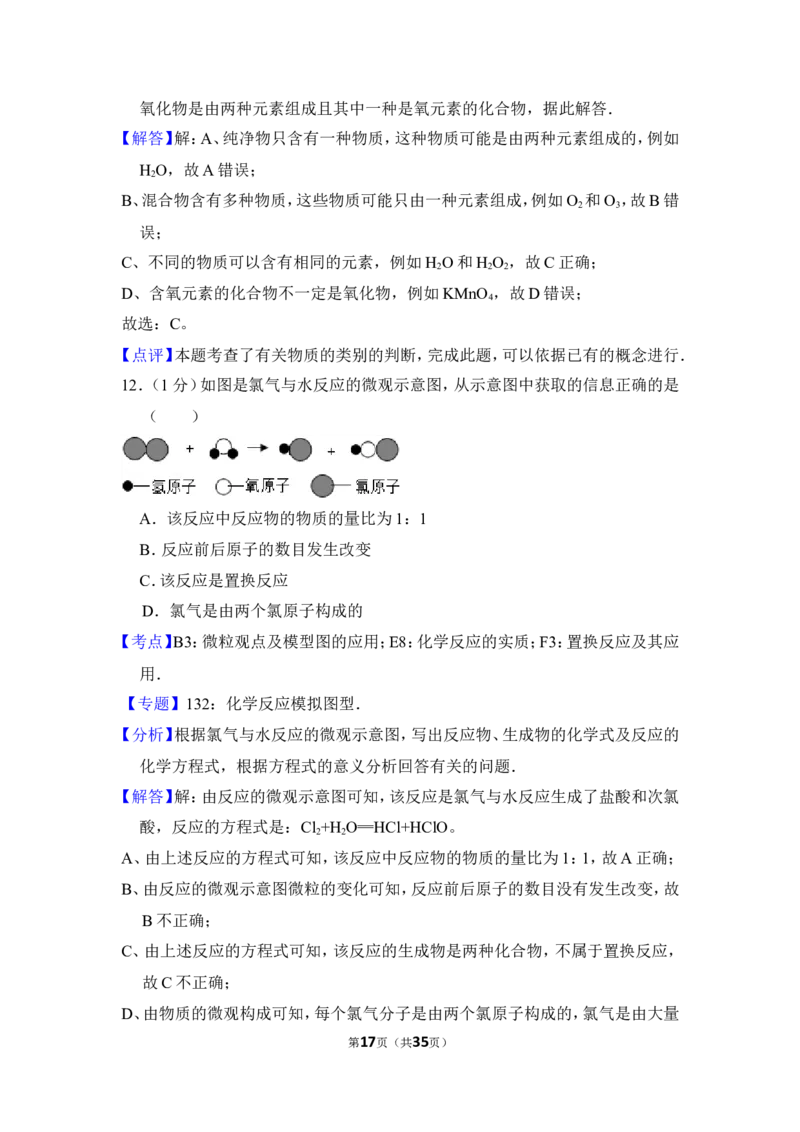
12.(1分)如图是氯气与水反应的微观示意图,从示意图中获取的信息正确的是
( )
A.该反应中反应物的物质的量比为1:1
B.反应前后原子的数目发生改变
C.该反应是置换反应
D.氯气是由两个氯原子构成的
【考点】B3:微粒观点及模型图的应用;E8:化学反应的实质;F3:置换反应及其应
用.
菁优网版权所有
【专题】132:化学反应模拟图型.
【分析】根据氯气与水反应的微观示意图,写出反应物、生成物的化学式及反应的
化学方程式,根据方程式的意义分析回答有关的问题.
【解答】解:由反应的微观示意图可知,该反应是氯气与水反应生成了盐酸和次氯
酸,反应的方程式是:Cl +H O═HCl+HClO。
2 2
A、由上述反应的方程式可知,该反应中反应物的物质的量比为1:1,故A正确;
B、由反应的微观示意图微粒的变化可知,反应前后原子的数目没有发生改变,故
B不正确;
C、由上述反应的方程式可知,该反应的生成物是两种化合物,不属于置换反应,
故C不正确;
D、由物质的微观构成可知,每个氯气分子是由两个氯原子构成的,氯气是由大量
第17页(共35页)的氯气分子聚集而成的,故D不正确。
故选:A。
【点评】解答本题的关键是要充分理解图中提供的信息,充分理解“一种小球代
表一种原子”,只有这样才能对问题做出正确的判断.
13.(1分)关于氧气的说法,错误的是( )
A.氧气能与镁、铁等金属、某些化合物反应,化学性质比较活泼
B.硫在氧气中燃烧,发出明亮的蓝紫色火焰
C.油锅着火,依据灭火原理隔绝空气,可用锅盖盖灭
D.可燃物燃烧一定需要氧气
【考点】68:氧气的化学性质;H1:燃烧与燃烧的条件;H4:灭火的原理和方法.
菁优网版权所有
【专题】522:氧气、氢气的性质与用途.
【分析】A、根据氧气的化学性质比较活泼,能与大多数的金属、某些化合物反应
解答;
B、根据硫在氧气中燃烧的现象和结论进行分析;
C、根据灭火的原理解答;
D、根据可燃物燃烧不一定需要氧气解答.
【解答】解:
A、氧气的化学性质比较活泼,能与大多数的金属、某些化合物反应,故说法正确
B、硫在氧气里燃烧,发出蓝紫色火焰,生成有刺激性气味的气体,故说法正确;
C、油锅着火,可用锅盖盖灭,依据的灭火原理是隔绝空气,故说法正确;
D、可燃物燃烧不一定需要氧气,如氯气在氧气中燃烧,故说法错误。
故选:D。
【点评】解答本题要掌握灭火的原理以及可燃物燃烧时的实验现象、结论等方面
的内容,只有这样才能对实验现象方面的问题做出正确的判断.
14.(1分)某校实验室将药品按氧化物、酸、碱、盐、…有机物等分类后,放在不同
的药品柜里,已存放的部分药品如下:
药品柜编号 ① ② ③ … ⑩
药品 二氧化锰 氢氧化钠 氯化钠 葡萄糖
氧化铜 氢氧化钙 硫酸钠 … 淀粉
该实验室新购进部分纯碱和蔗糖.应将它们分别放在( )
第18页(共35页)A.②和⑩ B.①和③ C.③和⑩ D.①和②
【考点】A9:常见的氧化物、酸、碱和盐的判别;AC:有机物与无机物的区别.
菁优网版权所有
【专题】516:物质的分类.
【分析】根据纯碱和蔗糖的组成和性质可知,纯碱是由纳离子和碳酸酸根离子组
成的化合物,属于盐,蔗糖属于有机物,同类别的物质应放在一个柜子里.
【解答】解:纯碱是由钠离子和碳酸酸根离子组成的化合物,属于盐,蔗糖属于有
机物,同类别的物质应放在一个柜子里。
①二氧化锰和氧化铜都是由两种元素组成,且其中一种是氧的化合物,都属于氧
化物;②氢氧化纳和氢氧化钙电离时生成的阴离子都是氢氧根离子,都属于碱
③氯化钠和硫酸钠都是由金属离子和酸根离子组成的化合物,都属于盐;⑩葡
萄糖和淀粉都是含有碳元素的化合物,属于有机物;
故选:C。
【点评】本题考查学生对物质类别的认识和药品的存放,学生应明确分类是一种
科学的方法,要在平时的学习中多应用.
15.(1分)对如图实验的分析说明不正确的是( )
A.该实验说明一氧化碳具有还原性
B.该实验说明生成物二氧化碳的密度比空气大
C.该实验说明一氧化碳和氧化铜的反应需要加热
D.该实验可以防止有毒的一氧化碳气体对空气的污染,同时又可以充分利用
能源
【考点】6U:一氧化碳的化学性质.
菁优网版权所有
【专题】523:碳单质与含碳化合物的性质与用途.
【分析】根据一氧化碳还原氧化铜,生成红色铜单质和二氧化碳,二氧化碳能使石
灰水变浑浊,一氧化碳有毒,难溶于水,具有可燃性,将尾气通到酒精灯处点燃
第19页(共35页)据此进行分析判断.
【解答】解:A、一氧化碳在加热条件下与氧化铜反应生成铜,说明一氧化碳具有
还原性,故选项说法正确。
B、该实验无法证明生成物二氧化碳的密度比空气大,故选项说法错误。
C、装置中酒精灯加热,说明反应条件为加热,故选项说法正确。
D、尾气通到酒精灯处点燃,可防止有毒的一氧化碳气体对空气的污染,同时燃烧
产生的热量充分利用,故选项说法正确。
故选:B。
【点评】本题难度不大,掌握一氧化碳还原氧化铜的实验原理、一氧化碳具有还原
性与可燃性等并能灵活运用是正确解答本题的关键.
16.(1分)仅用下列各组试剂无法完成验证Zn、Cu、Ag三种金属活动性顺序的是
( )
A.Zn、Ag、CuSO 溶液
4
B.Cu、ZnSO 溶液、AgNO 溶液
4 3
C.Zn、Cu、Ag、稀硫酸
D.Zn、Cu、稀硫酸、AgNO 溶液
3
【考点】86:金属活动性顺序及其应用.
菁优网版权所有
【专题】524:金属与金属材料.
【分析】根据金属活动性顺序,验证金属的活动性顺序是否合理,可根据金属与酸、
盐溶液“反应则活泼,不反应则不活泼”进行分析判断,通过分析方案所能得
到的结论,确定是否能得出Zn、Cu、Ag三种金属的活动性顺序.
【解答】解:A、锌可以置换CuSO 溶液中的铜而出现红色固体,证明锌的活动性
4
比铜强;银和CuSO 溶液不反应,证明铜比银的活动性强。可以证明三种金属
4
的活动性强弱,此方案可行;
B、铜与ZnSO 溶液液不反应,证明锌的活动性比铜强;铜与AgNO 溶液能反应,
4 3
证明铜比银的活动性强,可以证明三种金属的活动性强弱,此方案可行;
C、由于Cu、Ag都不与稀硫酸反应,无法比较Cu、Ag的活泼性的大小,此方案不
可行;
D、锌能与稀硫酸反应,铜不能与稀硫酸反应,证明锌比铜活泼;铜能与硝酸银反
应说明了铜比银活泼。因可以证明三种金属的活动性强弱,此方案可行。
第20页(共35页)故选:C。
【点评】同学们要会利用金属活动顺序表设计实验,去验证金属的活动性强弱.前
边的金属会与酸反应,但氢后边的金属不会与酸反应,前边的金属会把后边的
金属从其盐溶液中置换出来.但也要注意,与金属反应酸一般是指稀硫酸和盐
酸,不包括浓硫酸和硝酸.
17.(1分)如图是a、b两种固体物质的溶解度曲线,下列说法中错误的是( )
A.a、b都属于易溶物质
B.在t℃时,a、b的饱和溶液中溶质的质量分数相等
C.升高温度能使饱和的a溶液变为不饱和溶液
D.a的溶解度大于b的溶解度
【考点】7J:饱和溶液和不饱和溶液相互转变的方法;7N:固体溶解度曲线及其作
用;7Q:物质的溶解性及影响溶解性的因素;7T:溶质的质量分数、溶解性和溶
解度的关系.
菁优网版权所有
【专题】515:溶液、浊液与溶解度.
【分析】根据题目信息和溶解度曲线可知:a、b两种固体物质的溶解度,都是随温
度升高而增大,而a的溶解度随温度的升高变化比b大;在室温20℃时,溶解
度大于10g的物质,属于易溶物质,由溶解度曲线可知,a、b都属于易溶物质;
在t℃时,a、b的饱和溶液中溶质的质量分数相等,因为在该温度下,它们有交
点;升高温度能使饱和的a溶液变为不饱和溶液是正确的,因为a的溶解度随
温度的升高增大;a的溶解度大于b的溶解度不正确,因为没有指明温度.
【解答】解:A、在室温20℃时,溶解度大于10g的物质,属于易溶物质,由溶解度
曲线可知,a、b都属于易溶物质,正确但不符合题意,故选项错误;
B、在t℃时,a、b的饱和溶液中溶质的质量分数相等,因为在该温度下,它们有交
点,正确但不符合题意,故选项错误;
C、升高温度能使饱和的a溶液变为不饱和溶液是正确的,因为a的溶解度随温度
第21页(共35页)的升高增大,正确但不符合题意,故选项错误;
D、a的溶解度大于b的溶解度不正确,因为没有指明温度,故选项正确;
故选:D。
【点评】本考点考查了溶解度曲线及其应用、饱和溶液与不饱和溶液的转化等,通
过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的
计算,有关的计算要准确,本考点主要出现在选择题和填空题中.
18.(1分)某化工厂要排放的废水中含有少量NaOH、Na SO ;按环保要求需要把
2 4
废水处理成pH=7且水中只含有少量NaCl才能排放.则该化工厂处理废水需
要加入的一组物质是( )
A.MgSO NaCl B.H SO Ba(NO )
4 2 4 3 2
C.BaCl HCl D.H SO MgCl
2 2 4 2
【考点】95:碱的化学性质;9H:盐的化学性质;F8:酸、碱性废水的处理.
菁优网版权所有
【专题】212:化学与环境保护.
【分析】根据由离子和物质的共存进行分析得出结论.
【解答】解:
A、镁离子只会将氢氧根离子除去,而不会除去硫酸根离子,故A错误,
B、虽然会将氢氧根离子除去,但是还会引入硝酸根离子,故B错误,
C、钡离子会将硫酸根离子沉淀,氢离子会中和氢氧根离子,同时阴离子为氯离子。
故C正确,
D、镁离子会将氢氧根离子除去,不能将硫酸根离子除去,故D错误,
故选:C。
【点评】本题主要考查了常见的离子的共存问题,以及酸碱度的调节.
19.(1分)1个铅(Pb)原子质量是34.419×10﹣26Kg,一个碳﹣12原子质量是
1.993×10﹣26Kg,则铅原子的相对原子质量是( )
A.68.6 B.207.2 C.413.0 D.823.2
【考点】D7:相对原子质量的概念及其计算方法.
菁优网版权所有
【专题】511:物质的微观构成与物质的宏观组成.
【分析】根据某原子的相对原子质量= ,结合题意进行
分析解答即可。
第22页(共35页)【解答】解:1个铅(Pb)原子质量是34.419×10﹣26Kg,一个碳﹣12原子质量是
1.993×10﹣26Kg,则铅原子的相对原子质量是 ≈207.2。
故选:B。
【点评】本题难度不大,掌握原子的相对原子质量= 并
能灵活运用是正确解答本题的关键。
20.(1分)现有含杂质的硝酸钠溶液,为确定其组成,某同学设计了如下实验:
下列判断错误的是( )
A.原溶液中的杂质可能有三种
B.原溶液中没有硫酸盐
C.原溶液中杂质肯定是一种
D.该实验中涉及的基本反应类型只有一种
【考点】9H:盐的化学性质;FA:反应类型的判定.
菁优网版权所有
【专题】527:常见的盐 化学肥料.
【分析】根据含杂质的硝酸钠溶液,加入硝酸钡无现象,说明原溶液中无碳酸根离
子和硫酸根离子;由A与稀硝酸作用,A不溶解,A是由原溶液与硝酸银溶液
反应生成的,根据元素守恒可以确定原溶液中一定含有氯离子;由B与碳酸钠
溶液反应生成碳酸钙和硝酸钠,B是由原溶液与硝酸银溶液反应生成的,根据
元素守恒可以确定原溶液中一定含有钙离子进行分析.
【解答】解:含杂质的硝酸钠溶液,加入硝酸钡无现象,说明原溶液中无碳酸根离
子和硫酸根离子;由A与稀硝酸作用,A不溶解,A是由原溶液与硝酸银溶液
反应生成的,根据元素守恒可以确定原溶液中一定含有氯离子;由B与碳酸钠
第23页(共35页)溶液反应生成碳酸钙和硝酸钠,B是由原溶液与硝酸银溶液反应生成的,根据
元素守恒可以确定原溶液中一定含有钙离子。
通过上述分析可知原溶液中一定含有钙离子和氯离子,因此杂质可能有三种,即
CaCl 、Ca(NO )、NaCl.根据题设条件和这一推论,结合新的要求,可以得出
2 3 2
如下答案:
A、通过上述分析可知原溶液中一定含有钙离子和氯离子,因此杂质可能有三种,
即:CaCl 、Ca(NO ) 、NaCl,故A正确;
2 3 2
B、硝酸钠溶液加入硝酸钡没有明显现象,所以原溶液中没有硫酸盐,故B正确;
C、通过上述分析可知原溶液中一定含有钙离子和氯离子,因此杂质可能有三种,
即:CaCl 、Ca(NO ) 、NaCl,不一定是一种,故C错误;
2 3 2
D、该实验中都是两种化合物相互交换成分生成另外两种两种化合物,都是复分
解反应,故D正确。
故选:C。
【点评】本题主要考查盐的溶解性、酸碱盐之间的反应规律、氯离子的鉴定、钙离
子的确定和物质的组成和构成等方面的知识.
二、填空题(共20分,每空1分)
21.(6分)生活中处处蕴含着化学知识,请回答:
①金秋十月,丹桂飘香.请从微观的角度解释该现象 桂花花香中含有的分子是
在不断的运动的,向四周扩散,使人们闻到桂花花香 .
②水是一种优良的溶剂,生活中用下列物质,通常能配成水溶液的是 B (填字
母).
A.淀粉 B.食盐 C.植物油 D.碳酸钙补钙片
③化肥中氯化钾和碳酸钾的作用相似,是因为都含有 钾 元素;检验该元素常
用焰色反应,现象是 透过蓝色钴玻璃火焰显紫色 .
④金刚石、石墨、C 都由 碳 元素组成,它们的物理性质有较大差异的原因是
60
碳原子排列方式不同 .
【考点】7C:溶液的概念、组成及其特点;9H:盐的化学性质;B9:利用分子与原子
的性质分析和解决问题;CA:碳元素组成的单质.
菁优网版权所有
【专题】511:物质的微观构成与物质的宏观组成;515:溶液、浊液与溶解度;523:
碳单质与含碳化合物的性质与用途;527:常见的盐 化学肥料.
第24页(共35页)【分析】①根据分子的基本特征:分子质量和体积都很小;分子之间有间隔;分子
是在不断运动的;同种物质的分子性质相同,不同物质的分子性质不同,结合
事实进行分析解答即可.
②根据溶液的特点进行分析:溶液是均一、稳定的混合物.
③根据含有钾元素的肥料称为钾肥分析.
④根据物质的组成及构成解答.物质是由元素组成的,结构决定性质.
【解答】解:①金秋十月,丹桂飘香,是因为桂花花香中含有的分子是在不断的运
动的,向四周扩散,使人们闻到桂花花香.故填:桂花花香中含有的分子是在不
断的运动的,向四周扩散,使人们闻到桂花花香.
②A、淀粉不溶于水,不能和水形成均一、稳定的混合物,即不能和水形成溶液,
故错误;
B、食盐溶于水,能和水形成均一、稳定的混合物,即能和水形成溶液,故正确.
C、植物油不溶于水,不能和水形成均一、稳定的混合物,即不能和水形成溶液,植
物油和水形成的混合物属于乳浊液,故错误;
D、碳酸钙不溶于水,不能和水形成均一、稳定的混合物,即不能和水形成溶液,
故错误;
故选B.
③化肥中氯化钾和碳酸钾都含有钾元素,都属于钾肥,因此作用相似,检验钾元
素常用焰色反应,现象是透过蓝色钴玻璃火焰显紫色,故填:钾;透过蓝色钴
玻璃火焰显紫色;
④金刚石、石墨和C 等都是由碳元素组成的,碳原子排列方式不同,决定了物理
60
性质不同.故答案为:碳;碳原子排列方式不同.
【点评】本题难度不大,掌握利用分子的基本性质、溶液的概念、物质的组成和结
构等分析和解决问题的方法是正确解答本题的关键.
22.(5分)根据表中NaCl和KNO 溶解度数据,回答下列问题.
3
温度/℃ 0 20 40 60 80 100
NaCl溶解度(g/100g水) 35.7 36.0 36.6 37.3 38.4 39.8
KNO 溶解度(g/100g 13.3 31.6 63.9 110 169 246
3
水)
①40℃时,NaCl的溶解度是 36.6 g .
第25页(共35页)②20℃时,将等质量KNO 和NaCl固体,分别加入到盛有100g水的烧杯中,充
3
分搅拌后现象如图1,加热到60℃时现象如图2(不考虑水分蒸发).
根据图1和图2现象判断:甲烧杯中的固体是 KNO ;将图2中的两溶液降温
3
至40℃时,对两种溶液的分析正确的是 BC .
A.甲一定是饱和溶液 B.两溶液中溶质质量分数一定相等 C.乙一定是不
饱和溶液
D.甲一定会析出晶体 E.甲溶液浓度一定大于乙溶液浓度
③如果60℃时KNO 饱和溶液中混有少量NaCl时,提纯KNO 可采用方法 降
3 3
温结晶 .
④将等质量KNO 的饱和溶液和NaCl的饱和溶液从60℃降温到20℃后,所得溶
3
液中溶质质量分数大的是 NaC l 溶液.
【考点】4H:结晶的原理、方法及其应用;7M:固体溶解度的影响因素;7P:晶体和
结晶的概念与现象;7R:溶质的质量分数;7T:溶质的质量分数、溶解性和溶解
度的关系.
菁优网版权所有
【专题】515:溶液、浊液与溶解度.
【分析】①据溶解度曲线可知某温度下物质的溶解度;
②根据20℃时,KNO 和NaCl的溶解度解答;
3
③根据要分离硝酸钾和氯化钠的混合物,可以采用降温结晶的方法解答;
④根据图示结合具体的数据判断溶液的状态,据此解答.
【解答】解:
①40℃时,NaCl的溶解度是36.6g;
②20℃时,KNO 溶解度小于NaCl的溶解度,故将等质量KNO 和NaCl固体,分
3 3
别加入到盛有100g水的烧杯中,充分搅拌后KNO 有剩余;将图2中的两溶液
3
由60℃降温至40℃时,根据表可知两种物质的溶解度都随温度升高而增大,
因此40℃时,甲乙的溶解度都比 20℃时大,且40℃时KNO 的溶解度大于
3
第26页(共35页)NaCl的溶解度;再根据图1中信息可以知道20℃时乙中没有晶体析出,因此
40℃时乙中一定也无晶体析出,因此图2中两溶液降温至40℃一定都不会析
出晶体;
由于溶解的溶质相等,溶剂相等,故两溶液中溶质质量分数一定相等,甲乙一定
是不饱和溶液
③由于硝酸钾的溶解度随温度的升高而明显增大,而氯化钠的溶解度受温度影响
很小,因此提纯混有少量氯化钠的硝酸钾应采用降温结晶的方法,故答案为:
降温结晶;
④60℃时,NaCl和KNO 的溶解的分别是37.3g和110g,因此等质量的饱和溶液,
3
KNO 溶液中的溶剂质量较小,将等质量的两物质的饱和溶液分别降温至
3
20℃,都是饱和溶液,20℃时,KNO 的溶解度小于NaCl的溶解度,所以两种物
3
质的饱和溶液溶质质量分数硝酸钾的小于氯化钠的
答案:
①36.6g
②KNO B C
3
③冷却结晶
④NaCl
【点评】本题考查溶解度知识的具体应用,对学生深入理解溶解度的概念有一定
帮助,同时也考查了学生对知识的运用能力.
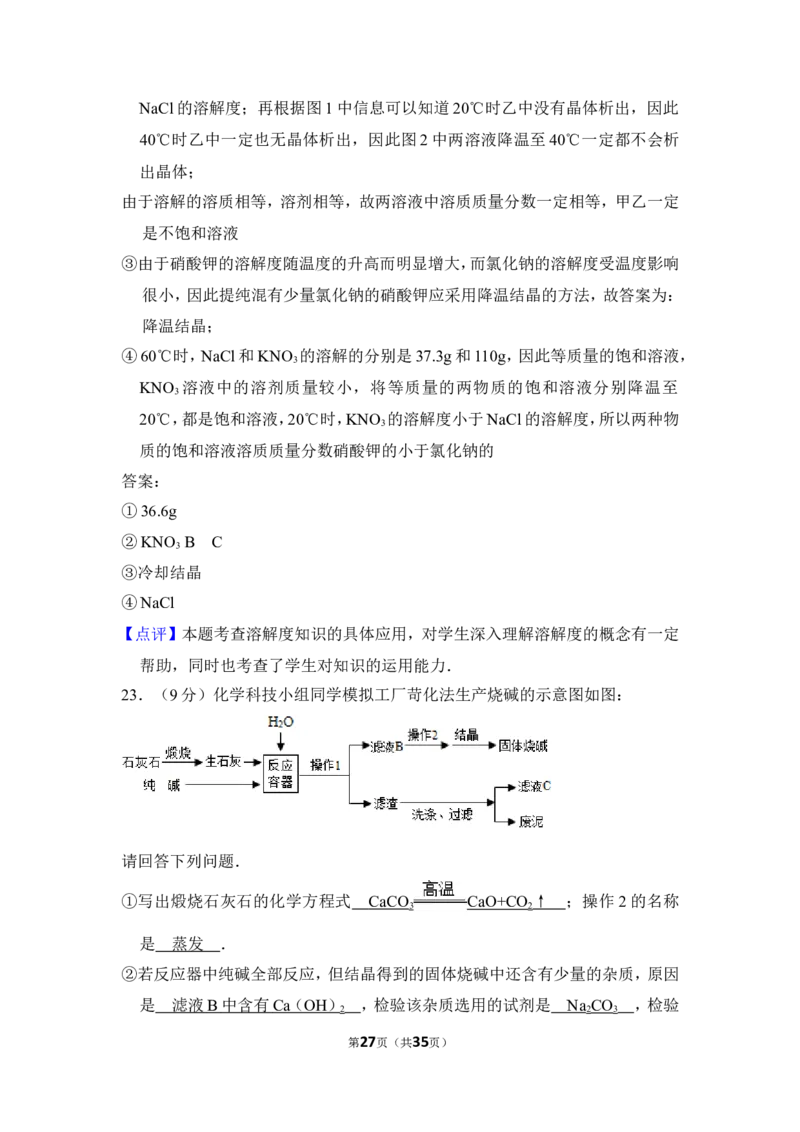
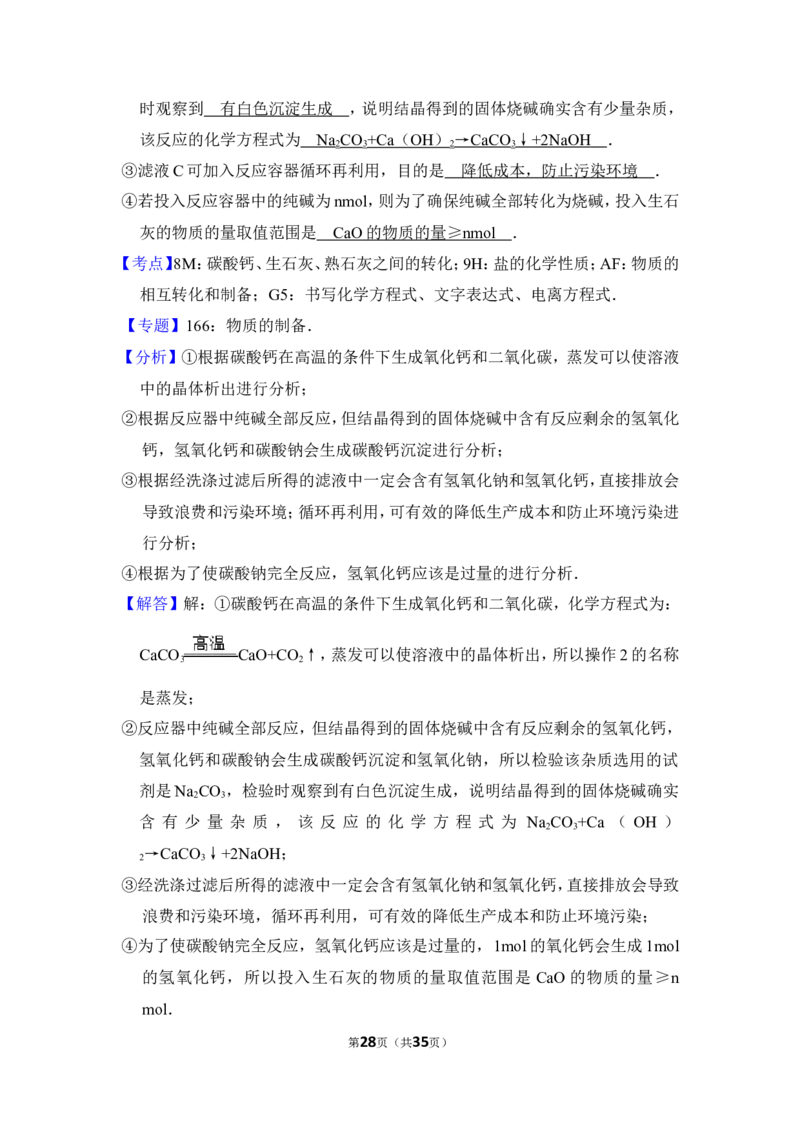
23.(9分)化学科技小组同学模拟工厂苛化法生产烧碱的示意图如图:
请回答下列问题.
①写出煅烧石灰石的化学方程式 CaCO CaO+CO ↑ ;操作2的名称
3 2
是 蒸发 .
②若反应器中纯碱全部反应,但结晶得到的固体烧碱中还含有少量的杂质,原因
是 滤液 B 中含有 C a( OH ) ,检验该杂质选用的试剂是 N a CO ,检验
2 2 3
第27页(共35页)时观察到 有白色沉淀生成 ,说明结晶得到的固体烧碱确实含有少量杂质,
该反应的化学方程式为 N a CO +Ca ( OH ) → CaCO ↓ +2NaOH .
2 3 2 3
③滤液C可加入反应容器循环再利用,目的是 降低成本,防止污染环境 .
④若投入反应容器中的纯碱为nmol,则为了确保纯碱全部转化为烧碱,投入生石
灰的物质的量取值范围是 CaO 的物质的量≥ nmo l .
【考点】8M:碳酸钙、生石灰、熟石灰之间的转化;9H:盐的化学性质;AF:物质的
相互转化和制备;G5:书写化学方程式、文字表达式、电离方程式.
菁优网版权所有
【专题】166:物质的制备.
【分析】①根据碳酸钙在高温的条件下生成氧化钙和二氧化碳,蒸发可以使溶液
中的晶体析出进行分析;
②根据反应器中纯碱全部反应,但结晶得到的固体烧碱中含有反应剩余的氢氧化
钙,氢氧化钙和碳酸钠会生成碳酸钙沉淀进行分析;
③根据经洗涤过滤后所得的滤液中一定会含有氢氧化钠和氢氧化钙,直接排放会
导致浪费和污染环境;循环再利用,可有效的降低生产成本和防止环境污染进
行分析;
④根据为了使碳酸钠完全反应,氢氧化钙应该是过量的进行分析.
【解答】解:①碳酸钙在高温的条件下生成氧化钙和二氧化碳,化学方程式为:
CaCO CaO+CO ↑,蒸发可以使溶液中的晶体析出,所以操作2的名称
3 2
是蒸发;
②反应器中纯碱全部反应,但结晶得到的固体烧碱中含有反应剩余的氢氧化钙,
氢氧化钙和碳酸钠会生成碳酸钙沉淀和氢氧化钠,所以检验该杂质选用的试
剂是Na CO ,检验时观察到有白色沉淀生成,说明结晶得到的固体烧碱确实
2 3
含 有 少 量 杂 质 , 该 反 应 的 化 学 方 程 式 为 Na CO +Ca ( OH )
2 3
→CaCO ↓+2NaOH;
2 3
③经洗涤过滤后所得的滤液中一定会含有氢氧化钠和氢氧化钙,直接排放会导致
浪费和污染环境,循环再利用,可有效的降低生产成本和防止环境污染;
④为了使碳酸钠完全反应,氢氧化钙应该是过量的,1mol的氧化钙会生成1mol
的氢氧化钙,所以投入生石灰的物质的量取值范围是 CaO的物质的量≥n
mol.
第28页(共35页)故答案为:①CaCO CaO+CO ↑,蒸发;
3 2
②滤液B中含有 Ca(OH) ,Na CO ,有白色沉淀生成,Na CO +Ca(OH)
2 2 3 2 3
→CaCO ↓+2NaOH;
2 3
③降低成本,防止污染环境;
④CaO的物质的量≥n mol.
【点评】本题是一道框题推断分析题,其主干就是工业上制取烧碱的方法,只要能
依据氢氧化钠是由碳酸钠和氢氧化钙制取的原理进行分析,即可得相应的问
题答案.
三、简答题(共20分,每空1分)
24.(7分)根据下列仪器或物品,结合所学化学知识回答下列问题:
①写出图中标号仪器的名称:a 长颈漏斗 ,b 酒精灯 .
②设计一套随开随制,随关随停制CO 气体的发生装置(不考虑夹持或支撑仪器
2
下同).应选用的有关仪器(或物品)的编号是 ADF .实验室用稀盐酸与大
理石制取CO 气体的化学方程式为 CaCO +2HCl=CaCl +H O+CO ↑ .
2 3 2 2 2
③实验室用过氧化氢溶液与二氧化锰制氧气,还需控制反应速度,应选用的仪器
编号是 ED ;化学方程式是 2H O 2H O+O ↑ ;该反应中二氧化
2 2 2 2
锰起 催化 作用.
【考点】6D:氧气的制取装置;6E:氧气的收集方法;6J:催化剂的特点与催化作用;
6L:二氧化碳的实验室制法;G5:书写化学方程式、文字表达式、电离方程式.
菁优网版权所有
【专题】534:常见气体的实验室制法、检验、干燥与净化.
第29页(共35页)【分析】(1)要熟悉各种仪器的名称、用途和使用方法;
(2)根据启普发生器的原理分析即可,打开止水夹,球形干燥管内气体逸出,压强
减小,液体与固体反应;关闭止水夹,球形干燥管内压强增大,将液体压出,反
应停止.实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需
要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、
水和二氧化碳;
(3)根据反应物的状态和反应条件确定发生装置,根据反应写出反应的方程式;
【解答】解:(1)a是长颈漏斗;b是酒精灯.故填:酒精灯;长颈漏斗.
(2)因为要装配一套“随开随用、随关随停”的气体发生装置,而启普发生器的
特点为“随开随用、随关随停”,根据启普发生器的原理并结合图中所给仪器
可以选出ADF进行连接,它的工作原理是:打开止水夹,球形干燥管内气体逸
出,压强减小,液体与固体反应;关闭止水夹,球形干燥管内压强增大,将液体
压出,反应停止;实验室制取二氧化碳常用大理石或石灰石和稀盐酸反应制取
二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐
酸反应生成氯化钙、水和二氧化碳;
故填:ADF;CaCO +2HCl=CaCl +H O+CO ↑;
3 2 2 2
(3)实验室用过氧化氢溶液与二氧化锰制取氧气,属于固液在常温下反应制取气
体,可选用装置ED作发生装置,反应的方程式是:2H O 2H O+O ↑,
2 2 2 2
其中二氧化锰起催化作用;
故 答 案 为 : ( 1 ) 长 颈 漏 斗 ; 酒 精 灯 ; ( 2 ) A D F ;
CaCO +2HCl=CaCl +H O+CO ↑
3 2 2 2
(3)E D;2H O 2H O+O ↑;催化
2 2 2 2
【点评】题重点考查实验室制取气体的发生装置和收集装置,以及实验中的注意
事项,需要同学们对常见实验做到了然于心.
25.(4分)湿法冶铜厂排放的废水中含有硫酸和硫酸铜两种污染物,为测定该废
水中各污染物的含量,环保小组的同学进行了以下实验.取废水500g,向其中
第30页(共35页)加入溶质质量分数为20%的氢氧化钠溶液.测得沉淀质量与所加入的氢氧化
钠溶液的质量关系如图.根据所得数据计算:
① 500g 废水中加入氢氧化钠溶液充分反应后,得到沉淀的物质的量是 0.2
mol.
②该废水中硫酸铜的溶质质量分数.(写出计算过程)
③该废水中硫酸的物质的量是 0.1mo l .
【考点】7U:有关溶质质量分数的简单计算;G6:根据化学反应方程式的计算.
菁优网版权所有
【专题】544:综合计算(图像型、表格型、情景型计算题).
【分析】①根据n= 进行计算;
②根据氢氧化钠与硫酸铜反应的化学方程式,利用生成沉淀的物质的量可计算出
废水中硫酸铜的物质的量,换算硫酸铜质量;
③由图示可知与硫酸反应的氢氧化钠溶液的质量为40g,可以换算出反应所消耗
氢氧化钠的物质的量,根据硫酸与氢氧化钠反应的方程式计算出废水中硫酸
的物质的量.
【解答】解:
①得到氢氧化铜沉淀的物质的量为: =0.2mol;
②设废水中硫酸铜的物质的量为x,消耗的氢氧化钠的物质的量为y.
CuSO +2NaOH=Cu(OH) ↓+Na SO
4 2 2 4
1 1
x 0.2mol
=
x=0.2mol;
第31页(共35页)该废水中硫酸铜的溶质质量分数为 ×100%=6.4%
③与硫酸反应的氢氧化钠的质量为40g×20%=8g
与硫酸反应的氢氧化钠的物质的量为: =0.2mol
设该废水中硫酸的物质的量是y
H SO +2NaOH=Na SO +2H O
2 4 2 4 2
1 2
y 0.2mol
=
y=0.1mol
答:①0.2;②6.4%
③0.1mol
【点评】对反应的图象中曲线进行分析,该曲线的起点表示硫酸被完全反应、折点
表示硫酸铜与氢氧化钠恰好完全反应.
26.(9分)氯碱工业用电解饱和食盐水制取氯气、烧碱.电解饱和食盐水的化学
方程式:
2NaCl+2H O 2NaOH+H ↑+Cl ↑
2 2 2
化学兴趣小组同学认为用上述方法制备的烧碱不纯,进行如下探究,请回答有关
问题.
①甲同学认为该烧碱可能含有少量食盐,为了检验食盐是否存在,进行了如下实
验:
实验步骤 实验现象 解释与结论
1取少量烧碱溶于水,滴加过 解释:滴加过量稀硝酸的目的是 除
量稀硝酸. 净溶液中 NaOH ,防止干扰对
无明显现象
NaCl 的检验 .
2再滴加 AgNO 溶液 . 结论:烧碱中含有少量食盐.
3
有白色沉 写出有关化学方程式:
淀
NaCl+AgNO =AgCl ↓ +NaNO .
3 3
②甲同学在上述检验后,根据氢氧化钠与氯化镁溶液反应:2NaOH+MgCl →Mg
2
(OH) ↓+2NaCl.测氢氧化钠的质量分数,设计实验步骤如图1所示.
2
第32页(共35页)加入过量氯化镁溶液的目的是 使 NaOH 完全反应 .操作A的仪器或装置如
图2所示,则操作A应选择 B (填字母)装置.根据上述实验步骤操作,称
量与计算准确.利用沉淀物的质量计算氢氧化钠的质量分数偏大,则可能的原
因是 没有洗涤、干燥(或烘干) .
③乙同学依据甲检验,利用盐酸与氢氧化钠的反应测NaOH百分含量.实验过程
如下:称取烧碱样品ag,溶于水,滴加盐酸至过量.滴加盐酸的体积与pH变化
规律如图3.则根据实验与图象中的有关数据能否得出NaOH百分含量.
如果能,说明理由 不能 ;
如果不能,需要补充的数据是 盐酸的密度与质量百分比浓度 .
【考点】2G:实验探究物质的组成成分以及含量;4I:蒸发与蒸馏操作;95:碱的化
学性质;99:溶液的酸碱性与pH值的关系;9H:盐的化学性质;G5:书写化学
方程式、文字表达式、电离方程式.
菁优网版权所有
【专题】537:科学探究.
【 分 析 】 根 据 电 解 饱 和 食 盐 水 的 化 学 方 程 式 : 2NaCl+2H O
2
2NaOH+H ↑+Cl ↑,则:
2 2
①甲同学认为该烧碱可能含有少量食盐,为了检验食盐是否存在,考虑氯化钠与
硝酸银溶液反应生成氯化银沉淀;
②根据氢氧化钠与氯化镁溶液反应:2NaOH+MgCl =Mg(OH)↓+2NaCl,测氢氧
2 2
化钠的质量分数,设计实验,加入过量氯化镁溶液的目的是使NaOH完全反应
第33页(共35页)经过过滤,称量与计算,考虑误差的原因.
③如果利用盐酸与氢氧化钠的反应测NaOH百分含量,需要补充的数据是 盐酸
的密度与质量百分比浓度.
【解答】解:根据氯碱工业用电解饱和食盐水制取氯气、烧碱,则电解饱和食盐水
的化学方程式:2NaCl+2H O 2NaOH+H ↑+Cl ↑,则:①甲同学认为该
2 2 2
烧碱可能含有少量食盐,为了检验食盐是否存在,进行了如下实验,则:
实验步骤 实验现象 解释与结论
1.取少量烧碱溶于水,滴加 解释:滴加过量稀硝酸的目的是 除
过量稀硝酸. 净溶液中NaOH,防止干扰对NaCl
无明显现象
的检验.
2.再滴加AgNO 溶液 结论:烧碱中含有少量食盐.
3
有白色沉淀 写出有关化学方程式:
NaCl+AgNO =AgCl↓+NaNO .
3 3
②甲同学在上述检验后,根据氢氧化钠与氯化镁溶液反应:2NaOH+MgCl =Mg
2
(OH)↓+2NaCl,测氢氧化钠的质量分数,加入过量氯化镁溶液的目的是使
2
NaOH完全反应.操作A的仪器或装置如图2所示,则操作A应选择B的过滤
装置.根据上述实验步骤操作,称量与计算准确;利用沉淀物的质量计算氢氧
化钠的质量分数偏大,则可能的原因是没有洗涤、干燥(或烘干).
③乙同学依据甲检验,利用盐酸与氢氧化钠的反应测NaOH百分含量:称取烧碱
样品ag,溶于水,滴加盐酸至过量,则根据实验与图象中的有关数据不能得出
NaOH百分含量,因为需要补充的数据是盐酸的密度与质量百分比浓度.
故答案为:
①
实验步骤 实验现象 解释与结论
除净溶液中NaOH,防止干扰对NaCl的检验.
AgNO 溶液. NaCl+AgNO =AgCl↓+NaNO .
3 3 3
有白色沉淀
②使NaOH完全反应. B,没有洗涤、干燥(或烘干).
③不能;盐酸的密度与质量百分比浓度.
【点评】本考点属于实验探究题,根据题目提供的信息,既有质量分数的计算,又
第34页(共35页)有化学方程式的书写、配平,综合性比较强.
声明:试题解析著作权属菁优网所有,未经书面同意,不得复制发布
日期:2018/12/24 23:13:29;用户:初中化学;邮箱:xdjyhx002@xyh.com;学号:25905210
第35页(共35页)