文档内容
2019年上海市松江区中考化学二模试卷
一、选择题(共20分,每题1分)
1.(1分)属于化学变化的是( )
A.酒精挥发 B.蜡烛燃烧 C.干冰升华 D.水结成冰
2.(1分)空气中体积分数约为五分之一的气体是( )
A.O B.N C.He D.CO
2 2 2
3.(1分)“高钙牛奶”中的“钙”应理解为( )
A.单质 B.元素 C.分子 D.原子
4.(1分)属于纯净物的是( )
A.大理石 B.天然气 C.氧化镁 D.石灰水
5.(1分)属于溶液的是( )
A.果酱 B.纯水 C.盐水 D.米糊
6.(1分)氮元素的化合价为+5价的是( )
A.NH B.N C.NO D.HNO
3 2 2 3
7.(1分)家用净水器中活性炭的作用是( )
A.凝聚 B.吸附 C.消毒 D.杀菌
8.(1分)纯碱的化学式是( )
A.NaOH B.Ca(OH) C.Na CO D.CaO
2 2 3
9.(1分)能给农作物增加两种营养元素的化肥是( )
A.KNO B.NH Cl C.K SO D.Ca(H PO )
3 4 2 4 2 4 2
10.(1分)实验现象描述正确的是( )
A.镁条在空气中燃烧,发出白光生成黑色固体
B.铁丝在氧气中燃烧,火星四射生成四氧化三铁
C.铁锈与稀盐酸反应,溶液由无色变成黄色
D.木炭还原氧化铜时,固体由红色变成黑色
11.(1分)物质用途错误的是( )
A.一氧化碳冶炼钢铁 B.氢氧化钠治疗胃酸过多
C.稀有气体制霓虹灯 D.氢气是绿色能源
12.(1分)正确的化学方程式是( )
A.H O H ↑+O ↑ B.2Fe+6HCl═2FeCl +3H ↑
2 2 2 3 2
第1页(共24页)C.2AgCl+Cu═CuCl +2Ag D.CuO+CO Cu+CO
2 2
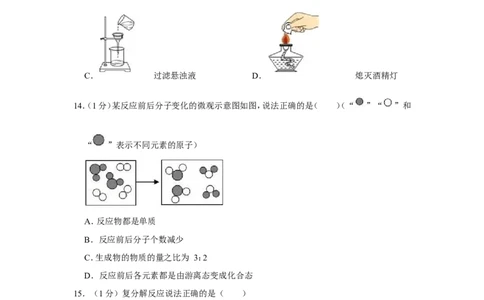
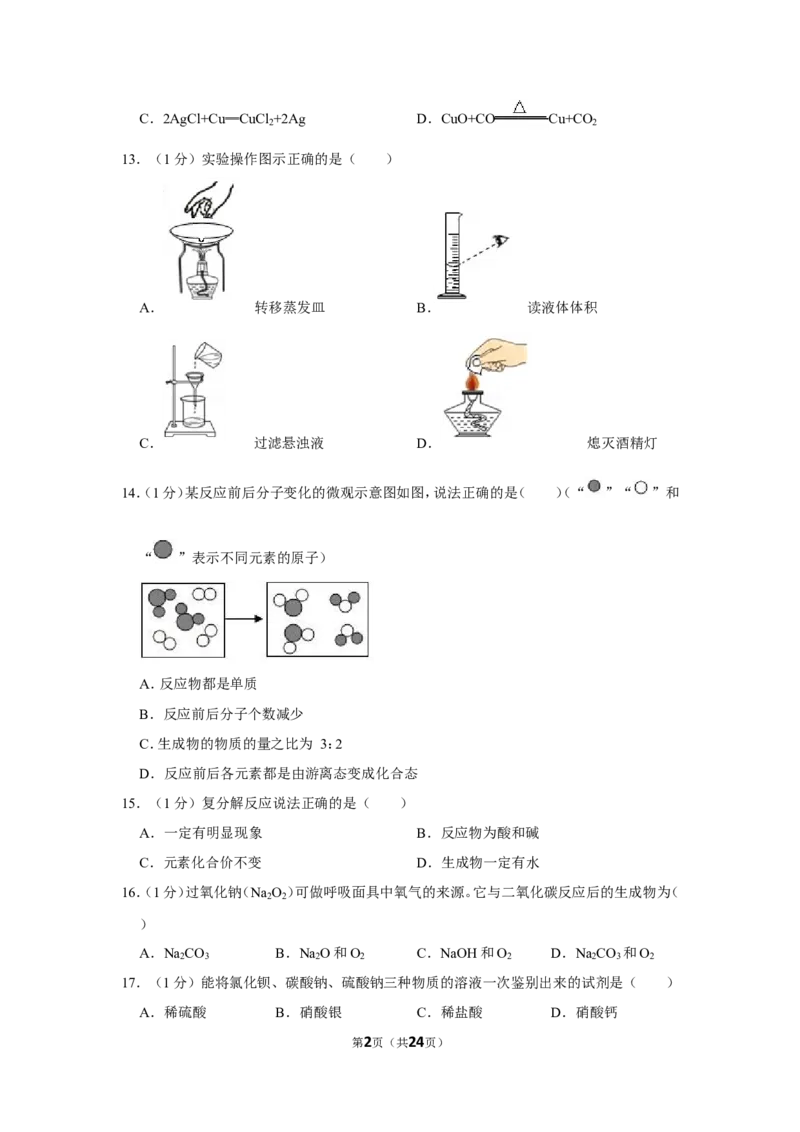
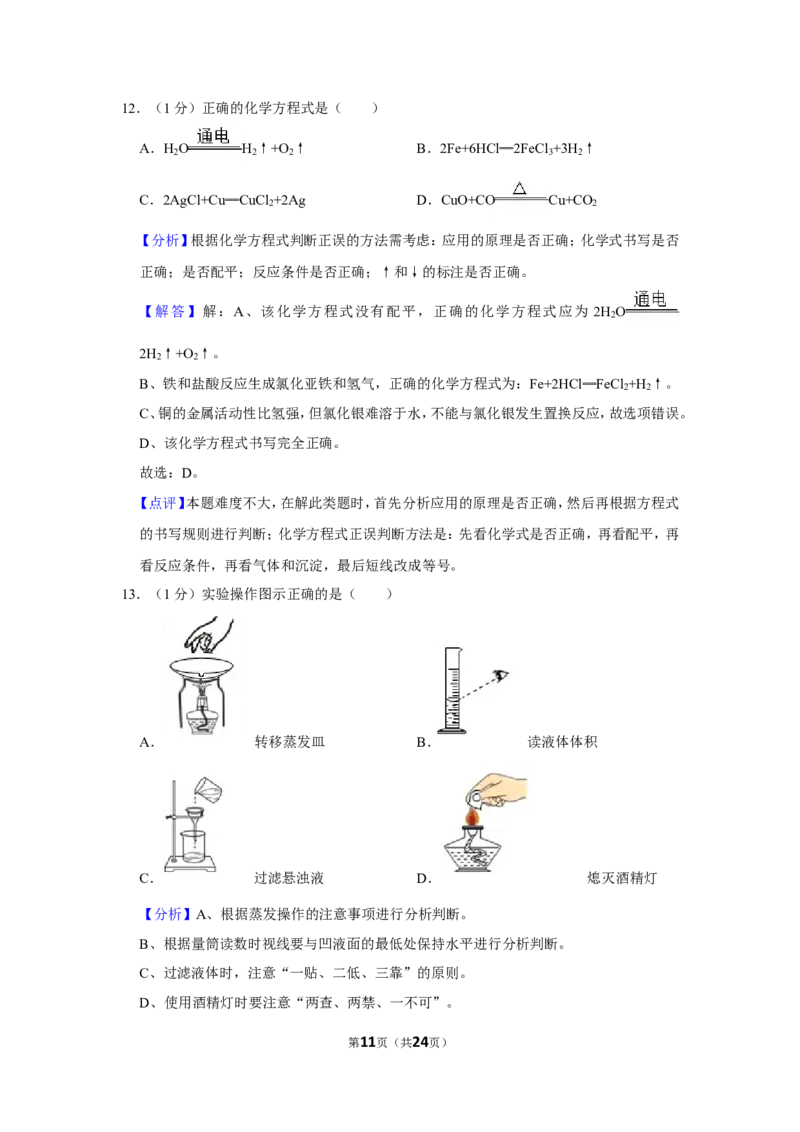
13.(1分)实验操作图示正确的是( )
A. 转移蒸发皿 B. 读液体体积
C. 过滤悬浊液 D. 熄灭酒精灯
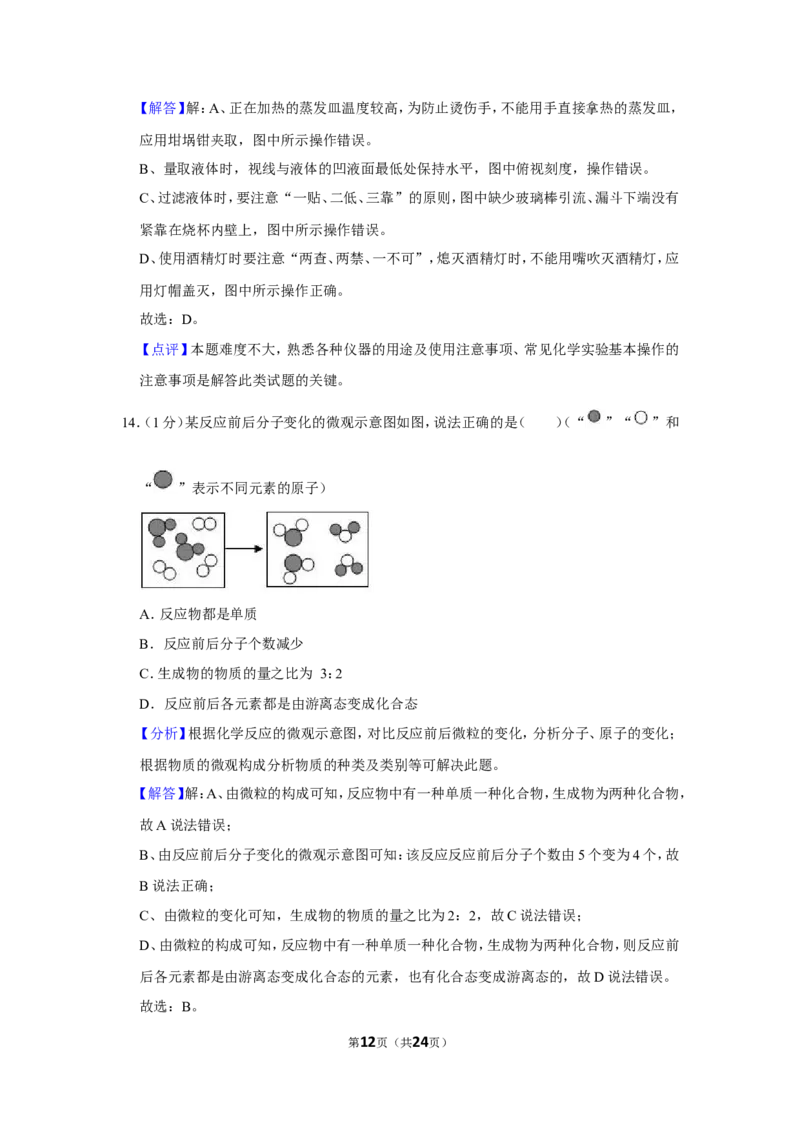
14.(1分)某反应前后分子变化的微观示意图如图,说法正确的是( )(“ ”“ ”和
“ ”表示不同元素的原子)
A.反应物都是单质
B.反应前后分子个数减少
C.生成物的物质的量之比为 3:2
D.反应前后各元素都是由游离态变成化合态
15.(1分)复分解反应说法正确的是( )
A.一定有明显现象 B.反应物为酸和碱
C.元素化合价不变 D.生成物一定有水
16.(1分)过氧化钠(Na O )可做呼吸面具中氧气的来源。它与二氧化碳反应后的生成物为(
2 2
)
A.Na CO B.Na O和O C.NaOH和O D.Na CO 和O
2 3 2 2 2 2 3 2
17.(1分)能将氯化钡、碳酸钠、硫酸钠三种物质的溶液一次鉴别出来的试剂是( )
A.稀硫酸 B.硝酸银 C.稀盐酸 D.硝酸钙
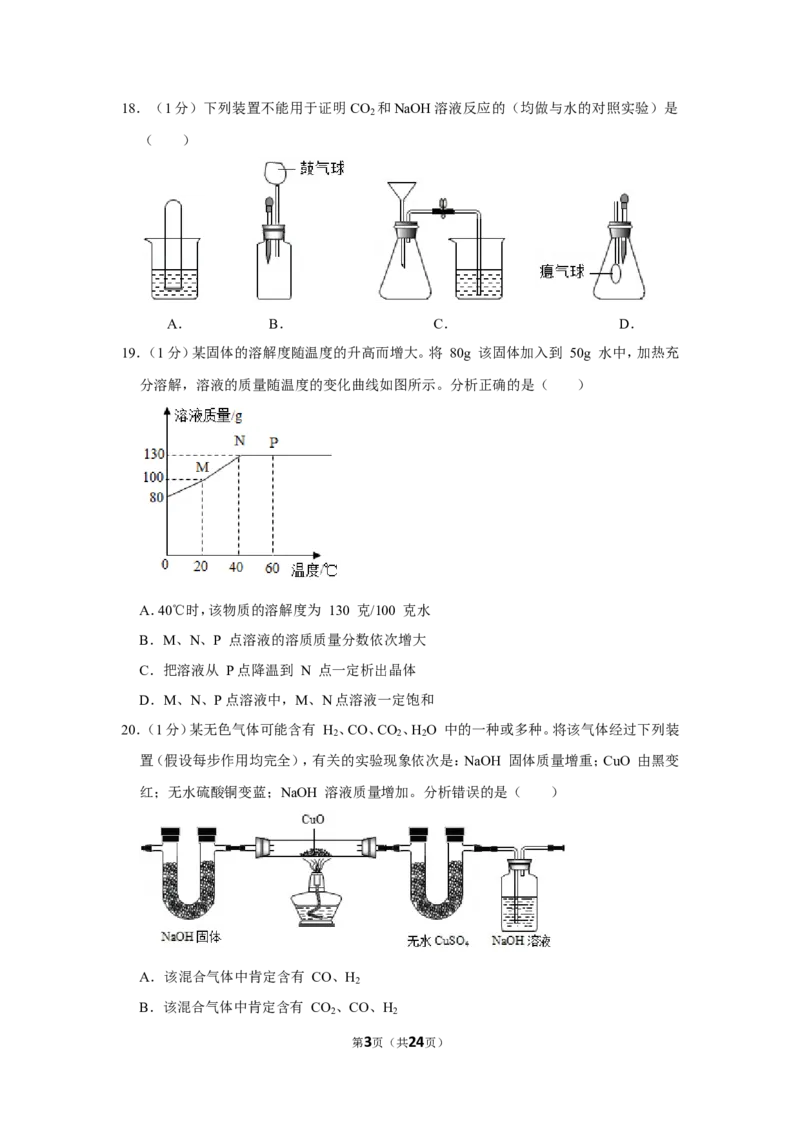
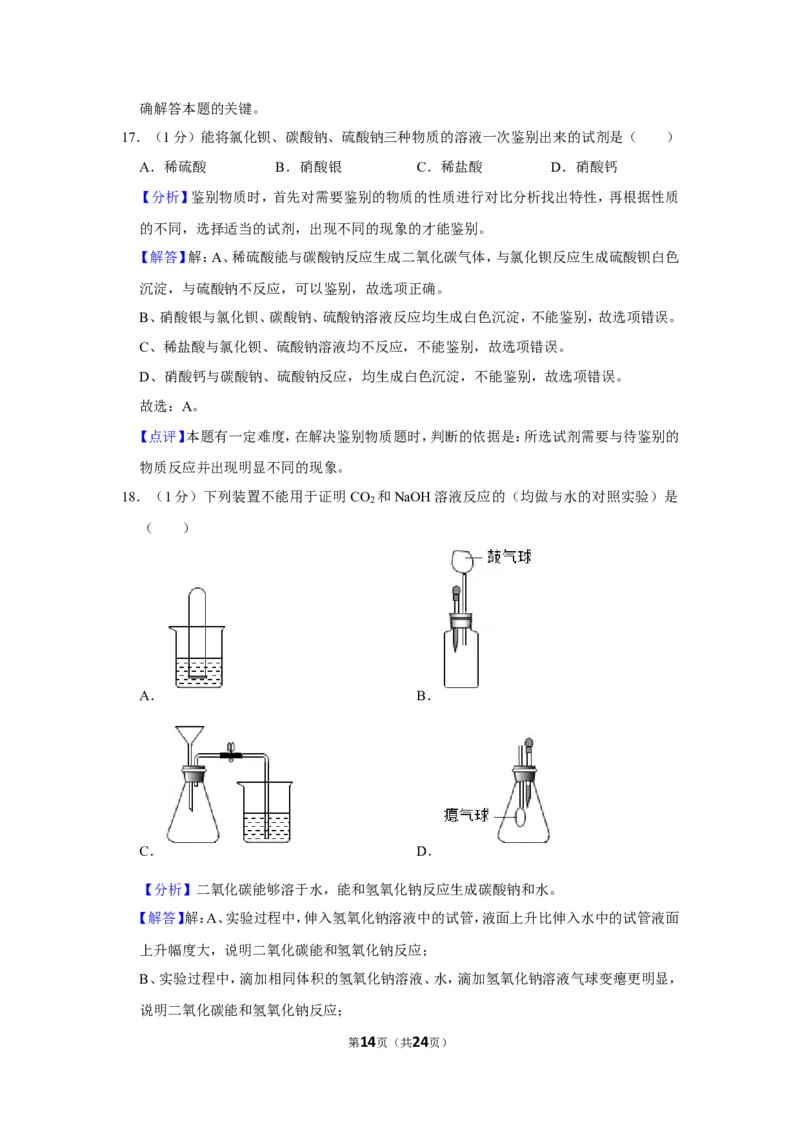
第2页(共24页)18.(1分)下列装置不能用于证明CO 和NaOH溶液反应的(均做与水的对照实验)是
2
( )
A. B. C. D.
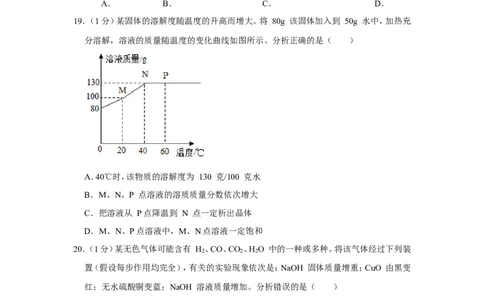
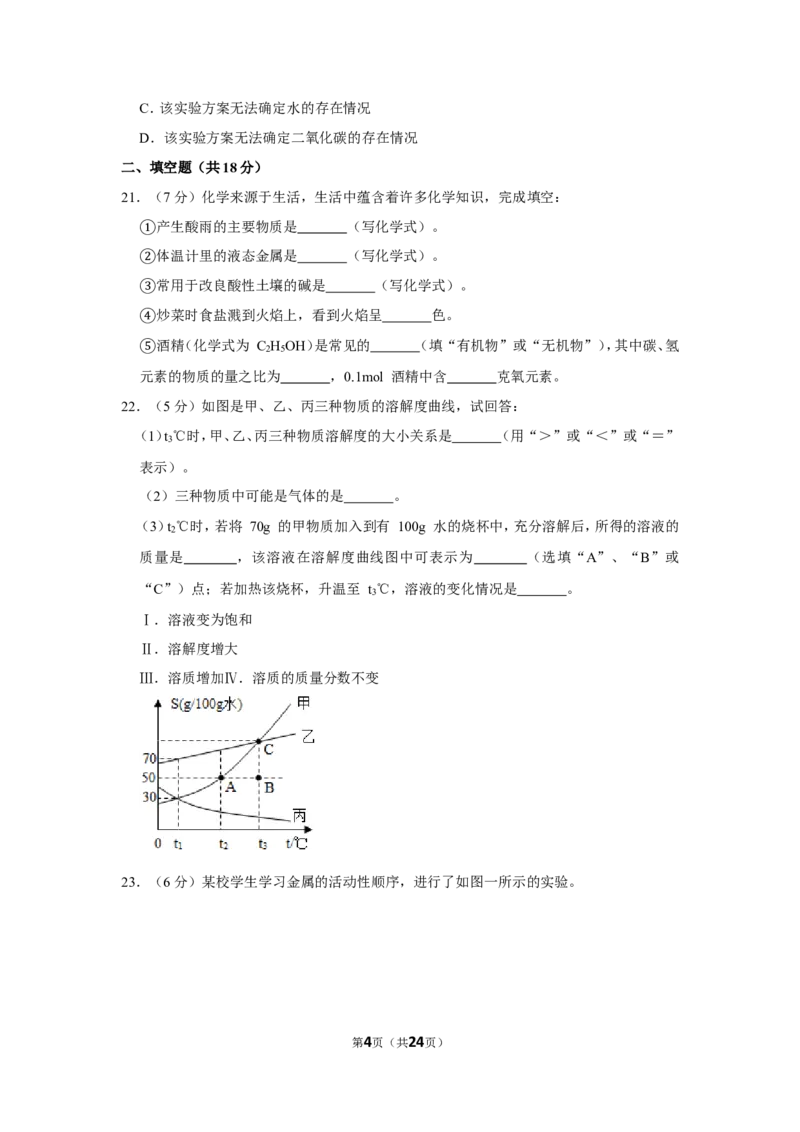
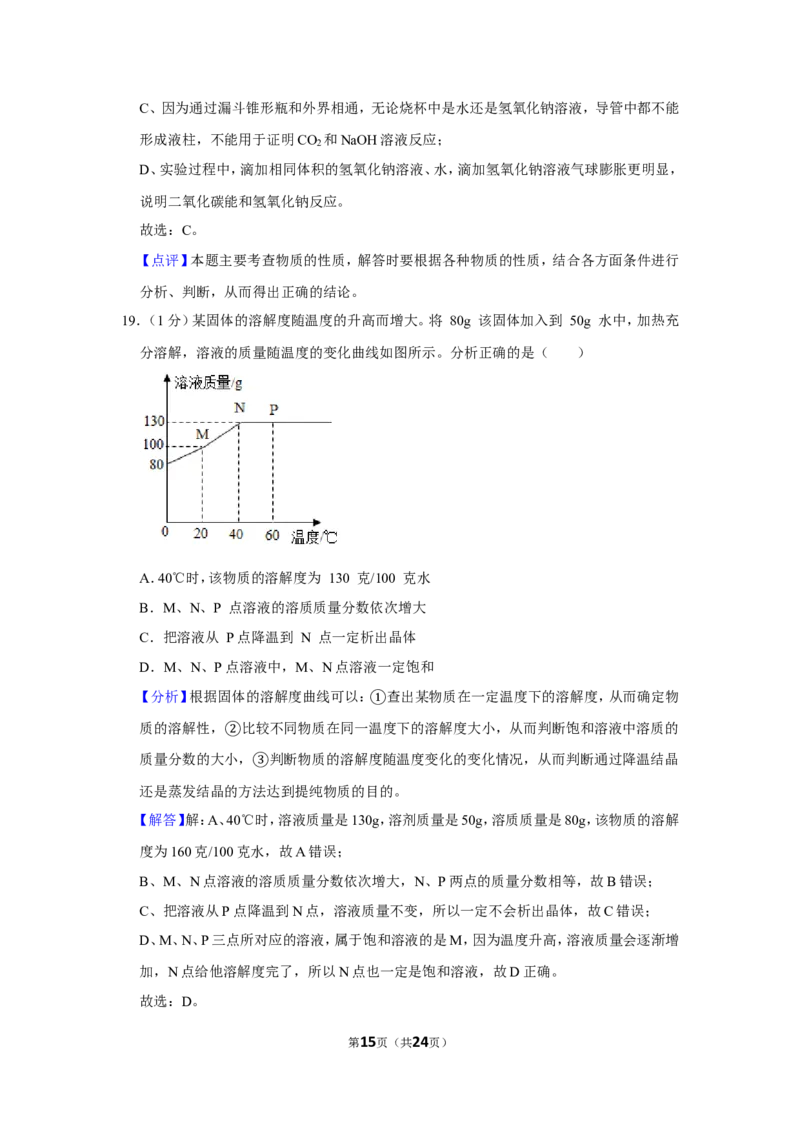
19.(1分)某固体的溶解度随温度的升高而增大。将 80g 该固体加入到 50g 水中,加热充
分溶解,溶液的质量随温度的变化曲线如图所示。分析正确的是( )
A.40℃时,该物质的溶解度为 130 克/100 克水
B.M、N、P 点溶液的溶质质量分数依次增大
C.把溶液从 P点降温到 N 点一定析出晶体
D.M、N、P点溶液中,M、N点溶液一定饱和
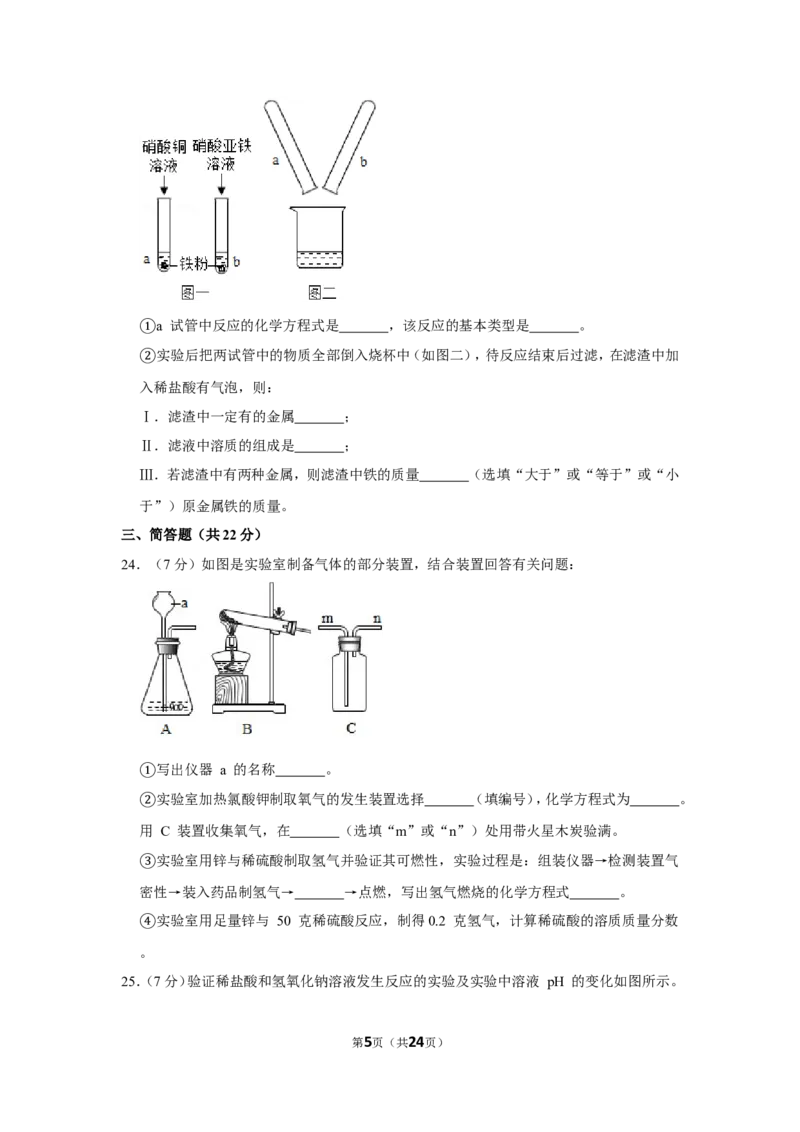
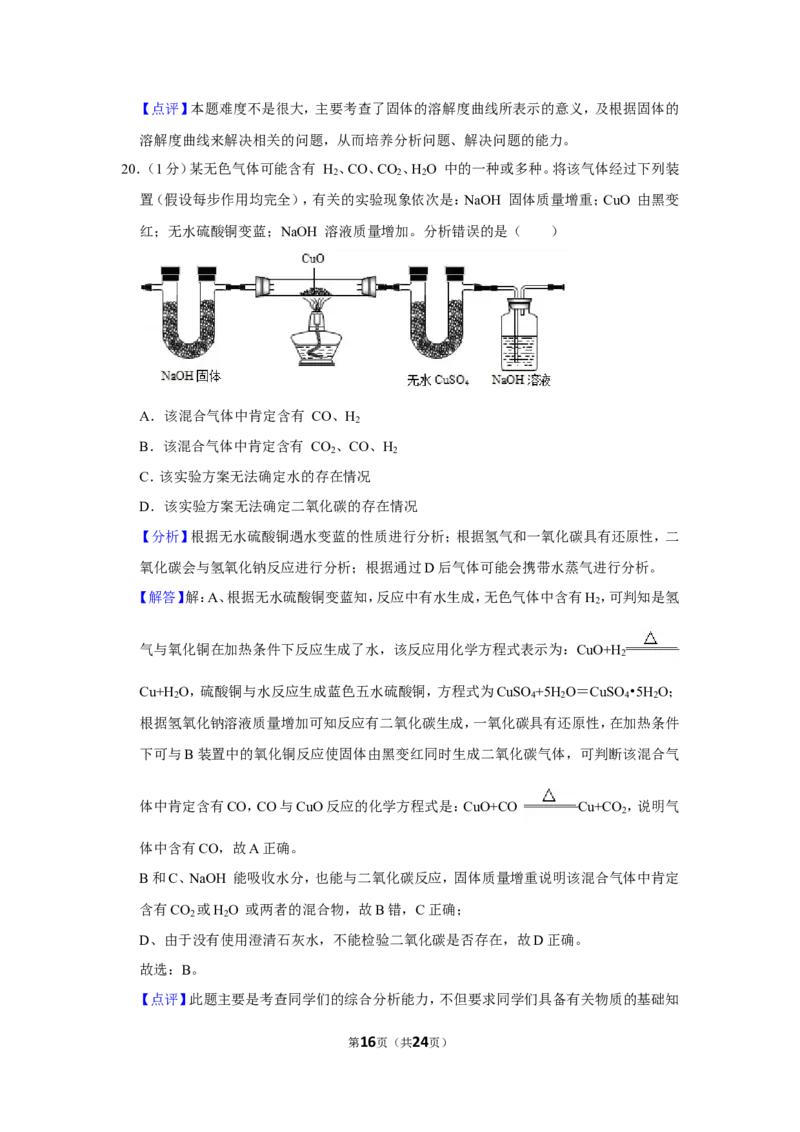
20.(1分)某无色气体可能含有 H 、CO、CO 、H O 中的一种或多种。将该气体经过下列装
2 2 2
置(假设每步作用均完全),有关的实验现象依次是:NaOH 固体质量增重;CuO 由黑变
红;无水硫酸铜变蓝;NaOH 溶液质量增加。分析错误的是( )
A.该混合气体中肯定含有 CO、H
2
B.该混合气体中肯定含有 CO 、CO、H
2 2
第3页(共24页)C.该实验方案无法确定水的存在情况
D.该实验方案无法确定二氧化碳的存在情况
二、填空题(共18分)
21.(7分)化学来源于生活,生活中蕴含着许多化学知识,完成填空:
产生酸雨的主要物质是 (写化学式)。
①体温计里的液态金属是 (写化学式)。
②常用于改良酸性土壤的碱是 (写化学式)。
③炒菜时食盐溅到火焰上,看到火焰呈 色。
④酒精(化学式为 C
2
H
5
OH)是常见的 (填“有机物”或“无机物”),其中碳、氢
⑤元素的物质的量之比为 ,0.1mol 酒精中含 克氧元素。
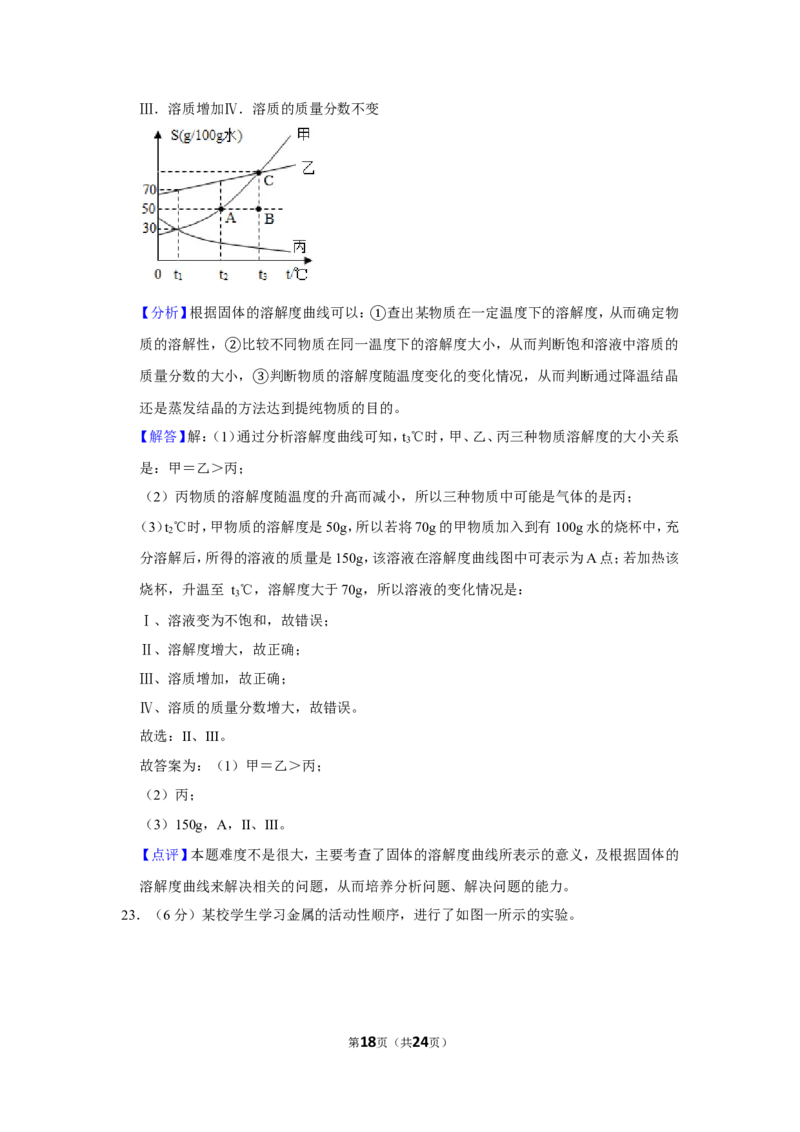
22.(5分)如图是甲、乙、丙三种物质的溶解度曲线,试回答:
(1)t ℃时,甲、乙、丙三种物质溶解度的大小关系是 (用“>”或“<”或“=”
3
表示)。
(2)三种物质中可能是气体的是 。
(3)t ℃时,若将 70g 的甲物质加入到有 100g 水的烧杯中,充分溶解后,所得的溶液的
2
质量是 ,该溶液在溶解度曲线图中可表示为 (选填“A”、“B”或
“C”)点;若加热该烧杯,升温至 t ℃,溶液的变化情况是 。
3
Ⅰ.溶液变为饱和
Ⅱ.溶解度增大
Ⅲ.溶质增加Ⅳ.溶质的质量分数不变
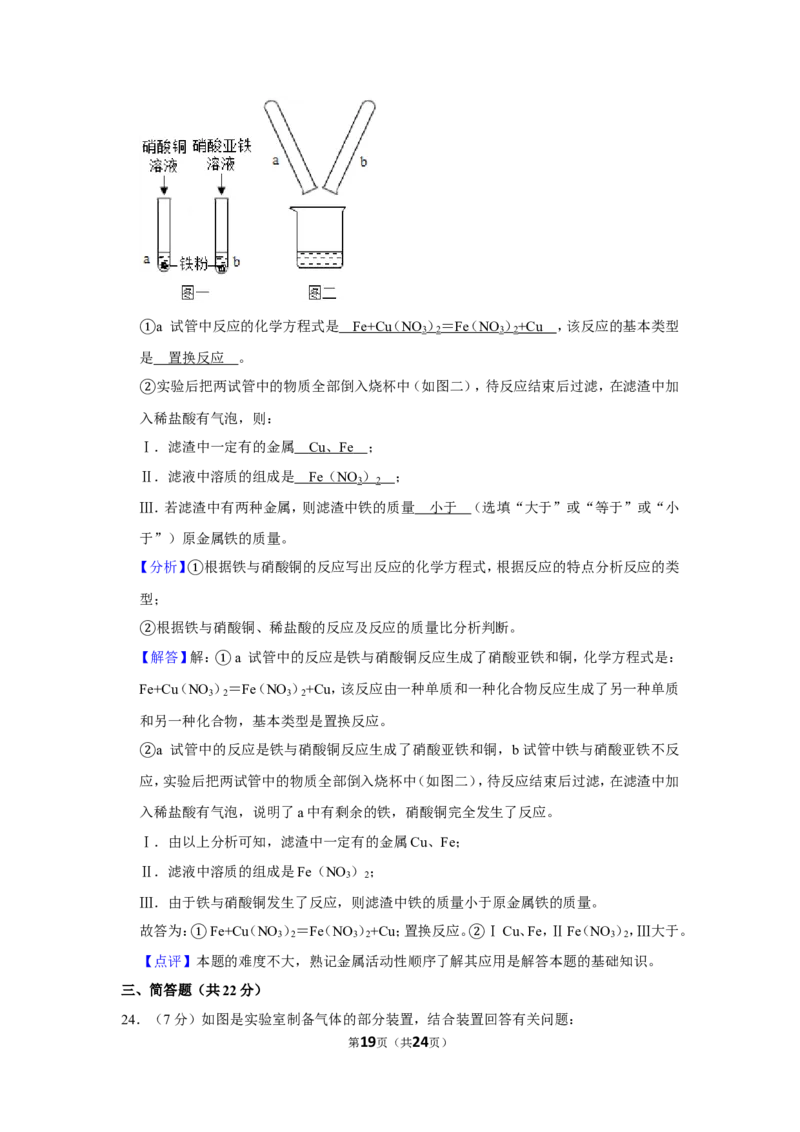
23.(6分)某校学生学习金属的活动性顺序,进行了如图一所示的实验。
第4页(共24页)a 试管中反应的化学方程式是 ,该反应的基本类型是 。
①实验后把两试管中的物质全部倒入烧杯中(如图二),待反应结束后过滤,在滤渣中加
②入稀盐酸有气泡,则:
Ⅰ.滤渣中一定有的金属 ;
Ⅱ.滤液中溶质的组成是 ;
Ⅲ.若滤渣中有两种金属,则滤渣中铁的质量 (选填“大于”或“等于”或“小
于”)原金属铁的质量。
三、简答题(共22分)
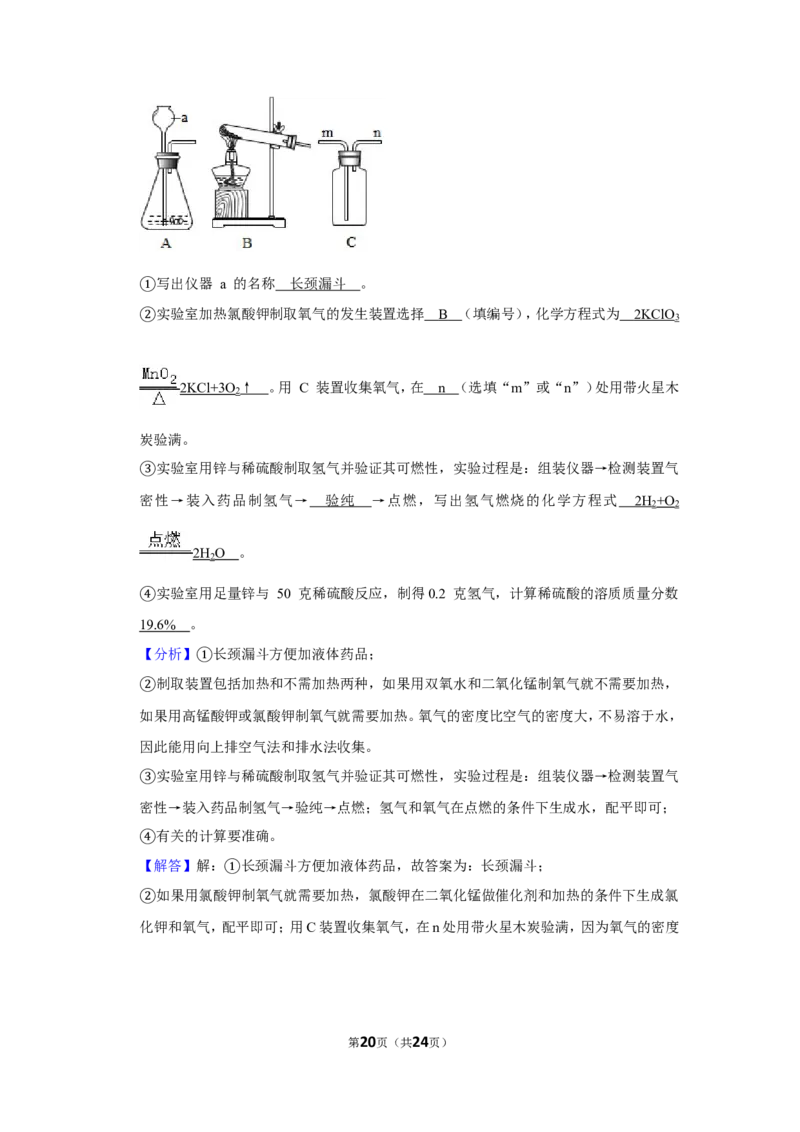
24.(7分)如图是实验室制备气体的部分装置,结合装置回答有关问题:
写出仪器 a 的名称 。
①实验室加热氯酸钾制取氧气的发生装置选择 (填编号),化学方程式为 。
②用 C 装置收集氧气,在 (选填“m”或“n”)处用带火星木炭验满。
实验室用锌与稀硫酸制取氢气并验证其可燃性,实验过程是:组装仪器→检测装置气
③密性→装入药品制氢气→ →点燃,写出氢气燃烧的化学方程式 。
实验室用足量锌与 50 克稀硫酸反应,制得0.2 克氢气,计算稀硫酸的溶质质量分数
④。
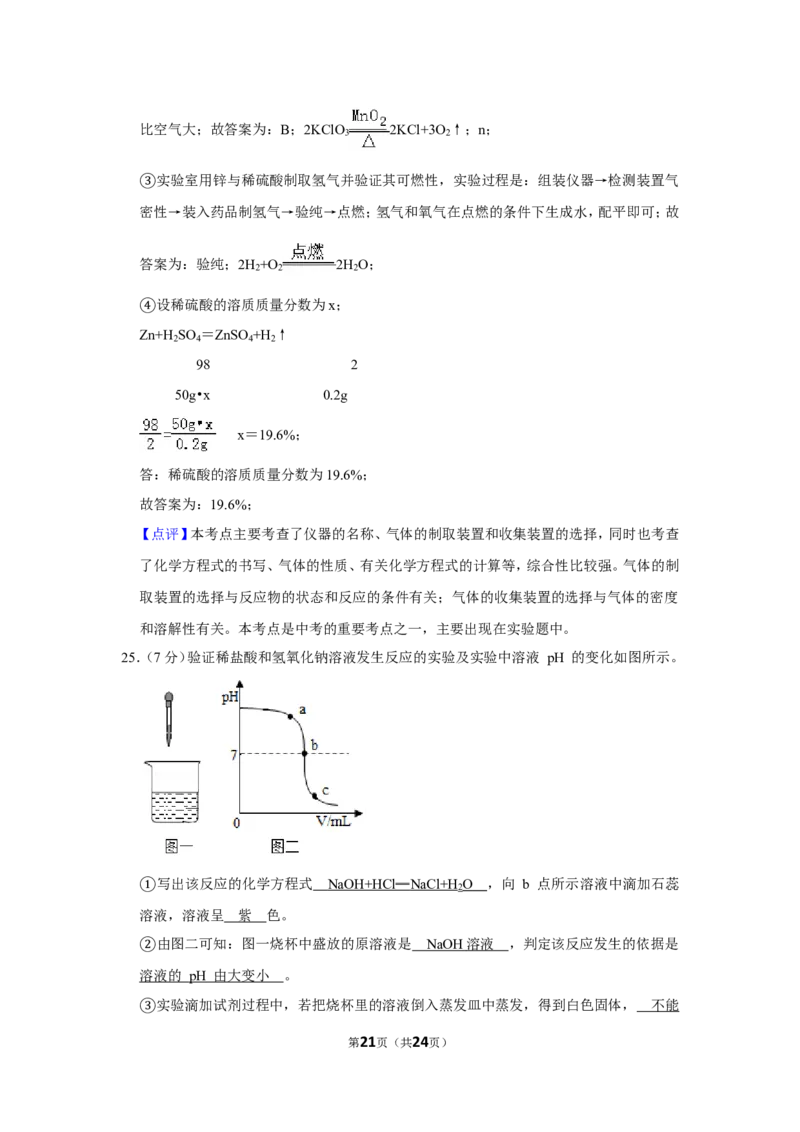
25.(7分)验证稀盐酸和氢氧化钠溶液发生反应的实验及实验中溶液 pH 的变化如图所示。
第5页(共24页)写出该反应的化学方程式 ,向 b 点所示溶液中滴加石蕊溶液,溶液呈
①色。
由图二可知:图一烧杯中盛放的原溶液是 ,判定该反应发生的依据是 。
②实验滴加试剂过程中,若把烧杯里的溶液倒入蒸发皿中蒸发,得到白色固体,
(③选填“能”或“不能”)证明该反应发生;若往烧杯里的溶液中滴加硫酸铜溶液,观察
到 ,能证明该反应发生。
a、b、c 三处对应溶液所含 NaCl 的质量大小关系是 。
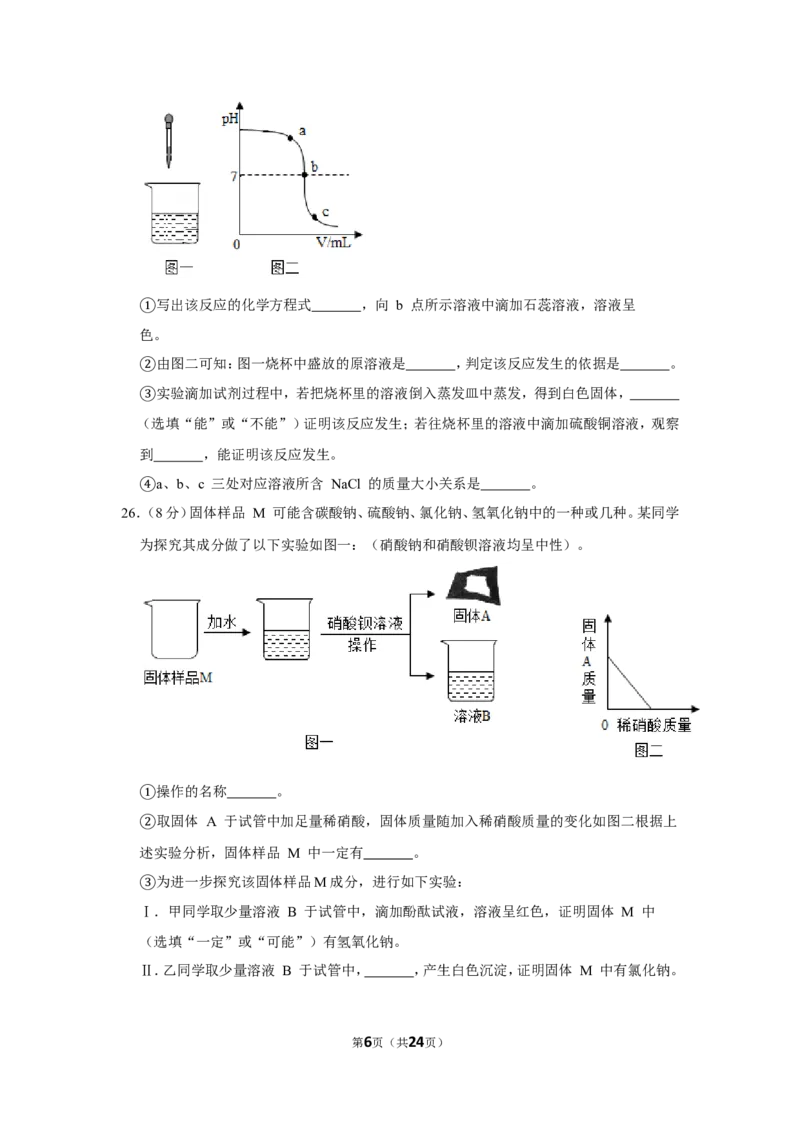
26.④(8分)固体样品 M 可能含碳酸钠、硫酸钠、氯化钠、氢氧化钠中的一种或几种。某同学
为探究其成分做了以下实验如图一:(硝酸钠和硝酸钡溶液均呈中性)。
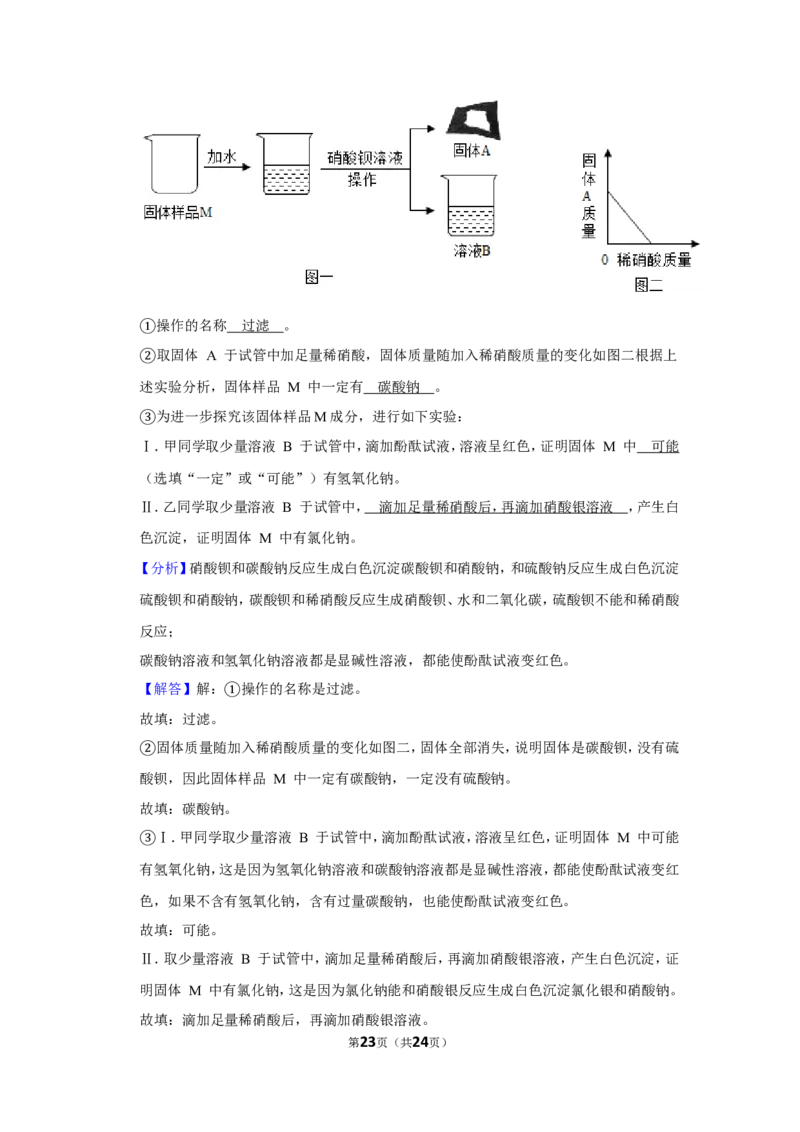
操作的名称 。
①取固体 A 于试管中加足量稀硝酸,固体质量随加入稀硝酸质量的变化如图二根据上
②述实验分析,固体样品 M 中一定有 。
为进一步探究该固体样品M成分,进行如下实验:
③Ⅰ.甲同学取少量溶液 B 于试管中,滴加酚酞试液,溶液呈红色,证明固体 M 中
(选填“一定”或“可能”)有氢氧化钠。
Ⅱ.乙同学取少量溶液 B 于试管中, ,产生白色沉淀,证明固体 M 中有氯化钠。
第6页(共24页)2019年上海市松江区中考化学二模试卷
参考答案与试题解析
一、选择题(共20分,每题1分)
1.(1分)属于化学变化的是( )
A.酒精挥发 B.蜡烛燃烧 C.干冰升华 D.水结成冰
【分析】化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,化学
变化和物理变化的本质区别是否有新物质生成;据此分析判断。
【解答】解:A、酒精挥发的过程中没有新物质生成,属于物理变化。
B、蜡烛燃烧的过程中有新物质二氧化碳等生成,属于化学变化。
C、干冰升华的过程中没有新物质生成,属于物理变化。
D、水结成冰的过程中只是状态发生改变,没有新物质生成,属于物理变化;
故选:B。
【点评】本题难度不大,解答时要分析变化过程中是否有新物质生成,若没有新物质生成
就属于物理变化,若有新物质生成就属于化学变化。
2.(1分)空气中体积分数约为五分之一的气体是( )
A.O B.N C.He D.CO
2 2 2
【分析】空气中各成分的体积分数分别是:氮气大约占空气体积的78%、氧气大约占空气
体积的21%、稀有气体大约占空气体积的0.94%、二氧化碳大约占空气体积的0.03%、水
蒸气和其它气体和杂质大约占0.03%;空气的成分主要以氮气和氧气为主,氧气约占空气
体积的五分之一,氮气约占空气体积的五分之四。
【解答】解:A、氧气约占空气体积的五分之一,故选项正确;
B、氮气约占空气体积的五分之四,故选项错误;
C、He属于稀有气体,含量比较少,故选项错误;
D、二氧化碳大约占空气体积的0.03%,故选项错误;
故选:A。
【点评】本考点考查了空气中各种气体的含量,同学们要加强记忆有关的知识点,在理解
的基础上加以应用,本考点基础性比较强,主要出现在选择题和填空题中。
3.(1分)“高钙牛奶”中的“钙”应理解为( )
A.单质 B.元素 C.分子 D.原子
第7页(共24页)【分析】食品、药品、营养品、矿泉水等物质中的“钙”等不是以单质、分子、原子等形式存
在,而是指元素,通常用元素及其所占质量(质量分数)来描述.
【解答】解:“高钙奶粉”中的“钙”不是以单质、分子、原子等形式存在,这里所指的
“钙”是强调存在的元素,与具体形态无关。
故选:B。
【点评】本题难度不大,主要考查元素与微观粒子及物质的区别,加深对元素概念的理解
是正确解答此类试题的关键.
4.(1分)属于纯净物的是( )
A.大理石 B.天然气 C.氧化镁 D.石灰水
【分析】纯净物由一种物质组成,混合物由两种或两种以上的物质组成。
【解答】解:A、大理石主要成分是碳酸钙,还含有一些杂质,是混合物;
B、天然气主要成分是甲烷,还含有一些杂质,是混合物;
C、氧化镁是由一种物质组成的,是纯净物;
D、石灰水中含有水和氢氧化钙,是混合物。
故选:C。
【点评】由一种物质组成的物质属于纯净物,混合物中至少含有两种物质,根据物质的组
成种类可以判断物质属于纯净物,还是属于混合物。
5.(1分)属于溶液的是( )
A.果酱 B.纯水 C.盐水 D.米糊
【分析】溶液是均一、稳定的混合物;溶液的本质特征是均一性、稳定性,属于混合物;据此
结合物质的组成进行分析判断。
【解答】解:A、果酱是果肉分散到水中形成的,不均一、不稳定,不属于溶液。
B、纯水是纯净物,不属于混合物,故不是溶液。
C、盐水是一种均一稳定的混合物,属于溶液。
D、油水是油是分散到水中形成的,不均一、不稳定,不属于溶液。
故选:C。
【点评】本题难度不大,掌握溶液的本质特征(均一性、稳定性、混合物)是解答本题的关键。
6.(1分)氮元素的化合价为+5价的是( )
A.NH B.N C.NO D.HNO
3 2 2 3
【分析】根据单质中元素的化合价为0、在化合物中正负化合价代数和为零,结合各选项中
的化学式进行解答本题。
第8页(共24页)【解答】解:A、氢元素显+1价,设氮元素的化合价是x,根据在化合物中正负化合价代数和
为零,可得:x+(﹣1)×3=0,则x=+3价。
B、根据单质中元素的化合价为0,N 属于单质,故氮元素的化合价为0,故选项错误。
2
C、氧元素显﹣2价,设氮元素的化合价是y,根据在化合物中正负化合价代数和为零,可
得:y+(﹣2)×2=0,则y=+4价。
D、氢元素显+1价,氧元素显﹣2价,设氮元素的化合价是z,根据在化合物中正负化合价
代数和为零,可得:(+1)+x+(﹣2)×3=0,则z=+5价。
故选:D。
【点评】本题难度不大,掌握单质中元素的化合价为0、在化合物中正负化合价代数和为零
并能灵活运用是正确解答本题的关键。
7.(1分)家用净水器中活性炭的作用是( )
A.凝聚 B.吸附 C.消毒 D.杀菌
【分析】根据活性炭具有吸附性分析;
【解答】解:活性炭具有疏松多孔的结构,可以吸附异味、颜色等一些不溶性物质;
故选:B。
【点评】物质的性质决定物质的用途。
8.(1分)纯碱的化学式是( )
A.NaOH B.Ca(OH) C.Na CO D.CaO
2 2 3
【分析】根据物质的名称、俗称及其化学式来分析解答。
【解答】解:纯碱是碳酸钠的俗称,其中钠元素显+1价,碳酸根显﹣2价,所以其化学式为
Na CO 。
2 3
故选:C。
【点评】本题考查了物质的名称、俗称、化学式的写法,难度不大。
9.(1分)能给农作物增加两种营养元素的化肥是( )
A.KNO B.NH Cl C.K SO D.Ca(H PO )
3 4 2 4 2 4 2
【分析】含有氮元素的肥料称为氮肥。含有磷元素的肥料称为磷肥。含有钾元素的肥料称
为钾肥。同时含有氮、磷、钾三种元素中的两种或两种以上的肥料称为复合肥。
【解答】解:A、KNO 中含有钾元素和氮元素两种营养元素。故选项正确;
3
B、NH Cl中含有一种营养元素氮元素。故选项错误;
4
C、K SO 中含有一种营养元素钾元素。故选项错误;
2 4
D、Ca(H PO ) 中含有一种营养元素磷元素。故选项错误。
2 4 2
第9页(共24页)故选:A。
【点评】解答本题要掌握化肥的分类方法方面的知识,只有这样才能对各种化肥进行正确
的分类。
10.(1分)实验现象描述正确的是( )
A.镁条在空气中燃烧,发出白光生成黑色固体
B.铁丝在氧气中燃烧,火星四射生成四氧化三铁
C.铁锈与稀盐酸反应,溶液由无色变成黄色
D.木炭还原氧化铜时,固体由红色变成黑色
【分析】镁燃烧生成氧化镁;
铁在氧气中燃烧生成四氧化三铁;
铁锈主要成分是氧化铁,和盐酸反应生成氯化铁和水;
高温条件下氧化铜和碳反应生成铜和二氧化碳。
【解答】解:A、镁条在空气中燃烧,发出白光生成白色固体,该选项说法不正确;
B、铁丝在氧气中燃烧,火星四射,放热,生成黑色固体,生成四氧化三铁是实验结论,该选
项说法不正确;
C、铁锈与稀盐酸反应生成氯化铁和水,溶液由无色变成黄色,该选项说法正确;
D、木炭还原氧化铜时,氧化铜和碳反应生成铜和二氧化碳,观察到固体由黑色变成红色,
该选项说法不正确。
故选:C。
【点评】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行
分析、判断,从而得出正确的结论。
11.(1分)物质用途错误的是( )
A.一氧化碳冶炼钢铁 B.氢氧化钠治疗胃酸过多
C.稀有气体制霓虹灯 D.氢气是绿色能源
【分析】物质的性质决定了物质的用途,解题时根据物质的性质来分析解答即可。
【解答】解:A.一氧化碳具有还原性,也用于冶炼金属,故正确;
B.氢氧化钠具有强烈的腐蚀性,不能用来治疗胃酸过多,故错误;
C.稀有气体通电时会发出有色光,所以可用于制霓虹灯,故正确;
D.氢气的热值高,燃烧产物只有水,是最绿色能源,故正确。
故选:B。
【点评】本题考查了常见物质的用途,同学们需在平常的生活中注意知识的积累。
第10页(共24页)12.(1分)正确的化学方程式是( )
A.H O H ↑+O ↑ B.2Fe+6HCl═2FeCl +3H ↑
2 2 2 3 2
C.2AgCl+Cu═CuCl +2Ag D.CuO+CO Cu+CO
2 2
【分析】根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否
正确;是否配平;反应条件是否正确;↑和↓的标注是否正确。
【解答】解:A、该化学方程式没有配平,正确的化学方程式应为 2H O
2
2H ↑+O ↑。
2 2
B、铁和盐酸反应生成氯化亚铁和氢气,正确的化学方程式为:Fe+2HCl═FeCl +H ↑。
2 2
C、铜的金属活动性比氢强,但氯化银难溶于水,不能与氯化银发生置换反应,故选项错误。
D、该化学方程式书写完全正确。
故选:D。
【点评】本题难度不大,在解此类题时,首先分析应用的原理是否正确,然后再根据方程式
的书写规则进行判断;化学方程式正误判断方法是:先看化学式是否正确,再看配平,再
看反应条件,再看气体和沉淀,最后短线改成等号。
13.(1分)实验操作图示正确的是( )
A. 转移蒸发皿 B. 读液体体积
C. 过滤悬浊液 D. 熄灭酒精灯
【分析】A、根据蒸发操作的注意事项进行分析判断。
B、根据量筒读数时视线要与凹液面的最低处保持水平进行分析判断。
C、过滤液体时,注意“一贴、二低、三靠”的原则。
D、使用酒精灯时要注意“两查、两禁、一不可”。
第11页(共24页)【解答】解:A、正在加热的蒸发皿温度较高,为防止烫伤手,不能用手直接拿热的蒸发皿,
应用坩埚钳夹取,图中所示操作错误。
B、量取液体时,视线与液体的凹液面最低处保持水平,图中俯视刻度,操作错误。
C、过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流、漏斗下端没有
紧靠在烧杯内壁上,图中所示操作错误。
D、使用酒精灯时要注意“两查、两禁、一不可”,熄灭酒精灯时,不能用嘴吹灭酒精灯,应
用灯帽盖灭,图中所示操作正确。
故选:D。
【点评】本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的
注意事项是解答此类试题的关键。
14.(1分)某反应前后分子变化的微观示意图如图,说法正确的是( )(“ ”“ ”和
“ ”表示不同元素的原子)
A.反应物都是单质
B.反应前后分子个数减少
C.生成物的物质的量之比为 3:2
D.反应前后各元素都是由游离态变成化合态
【分析】根据化学反应的微观示意图,对比反应前后微粒的变化,分析分子、原子的变化;
根据物质的微观构成分析物质的种类及类别等可解决此题。
【解答】解:A、由微粒的构成可知,反应物中有一种单质一种化合物,生成物为两种化合物,
故A说法错误;
B、由反应前后分子变化的微观示意图可知:该反应反应前后分子个数由5个变为4个,故
B说法正确;
C、由微粒的变化可知,生成物的物质的量之比为2:2,故C说法错误;
D、由微粒的构成可知,反应物中有一种单质一种化合物,生成物为两种化合物,则反应前
后各元素都是由游离态变成化合态的元素,也有化合态变成游离态的,故D说法错误。
故选:B。
第12页(共24页)【点评】本题是有关微观示意图的考查,学会利用微观的观点及微观示意图的意义对反应
基本类型判断及化学变化的微观信息的获取等是解题的关键,难度不大。
15.(1分)复分解反应说法正确的是( )
A.一定有明显现象 B.反应物为酸和碱
C.元素化合价不变 D.生成物一定有水
【分析】复分解反应是两种化合物相互交换成分生成两种新的化合物的反应,进行分析判
断。
【解答】解:A、复分解反应不一定有明显现象,如氢氧化钠与稀盐酸反应,无明显变化,故
选项说法错误。
B、复分解反的反应物不一定是为酸和碱,如氢氧化钙与碳酸钠溶液反应,故选项说法错
误。
C、复分解反应是两种化合物相互交换成分生成两种新的化合物的反应,特征是换成分、
价不变,故选项说法正确。
D、复分解反的生成物不一定有水,如氢氧化钙与碳酸钠溶液反应生成碳酸钙沉淀和氢氧
化钠,故选项说法错误。
故选:C。
【点评】本题难度不大,掌握复分解反应的特征(换成分、价不变)是正确解答本题的关键。
16.(1分)过氧化钠(Na O )可做呼吸面具中氧气的来源。它与二氧化碳反应后的生成物为(
2 2
)
A.Na CO B.Na O和O C.NaOH和O D.Na CO 和O
2 3 2 2 2 2 3 2
【分析】根据质量守恒定律,反应前后元素种类不变,结合题意进行分析解答。
【解答】解:A、过氧化钠(Na O )可做呼吸面具中氧气的来源,则与二氧化碳反应后的生
2 2
成物为碳酸钠和氧气,不只是碳酸钠,故选项错误。
B、过氧化钠(Na O )可做呼吸面具中氧气的来源,由质量守恒定律,反应前后元素种类不
2 2
变,则与二氧化碳反应后的生成物不可能为Na O和O ,故选项错误。
2 2
C、过氧化钠(Na O )可做呼吸面具中氧气的来源,由质量守恒定律,反应前后元素种类不
2 2
变,则与二氧化碳反应后的生成物不可能为氢氧化钠和氧气,故选项错误。
D、过氧化钠(Na O )可做呼吸面具中氧气的来源,则与二氧化碳反应后的生成物为碳酸
2 2
钠和氧气,故选项正确。
故选:D。
【点评】本题难度不大,掌握质量守恒定律(反应前后,元素种类不变)并能灵活运用是正
第13页(共24页)确解答本题的关键。
17.(1分)能将氯化钡、碳酸钠、硫酸钠三种物质的溶液一次鉴别出来的试剂是( )
A.稀硫酸 B.硝酸银 C.稀盐酸 D.硝酸钙
【分析】鉴别物质时,首先对需要鉴别的物质的性质进行对比分析找出特性,再根据性质
的不同,选择适当的试剂,出现不同的现象的才能鉴别。
【解答】解:A、稀硫酸能与碳酸钠反应生成二氧化碳气体,与氯化钡反应生成硫酸钡白色
沉淀,与硫酸钠不反应,可以鉴别,故选项正确。
B、硝酸银与氯化钡、碳酸钠、硫酸钠溶液反应均生成白色沉淀,不能鉴别,故选项错误。
C、稀盐酸与氯化钡、硫酸钠溶液均不反应,不能鉴别,故选项错误。
D、硝酸钙与碳酸钠、硫酸钠反应,均生成白色沉淀,不能鉴别,故选项错误。
故选:A。
【点评】本题有一定难度,在解决鉴别物质题时,判断的依据是:所选试剂需要与待鉴别的
物质反应并出现明显不同的现象。
18.(1分)下列装置不能用于证明CO 和NaOH溶液反应的(均做与水的对照实验)是
2
( )
A. B.
C. D.
【分析】二氧化碳能够溶于水,能和氢氧化钠反应生成碳酸钠和水。
【解答】解:A、实验过程中,伸入氢氧化钠溶液中的试管,液面上升比伸入水中的试管液面
上升幅度大,说明二氧化碳能和氢氧化钠反应;
B、实验过程中,滴加相同体积的氢氧化钠溶液、水,滴加氢氧化钠溶液气球变瘪更明显,
说明二氧化碳能和氢氧化钠反应;
第14页(共24页)C、因为通过漏斗锥形瓶和外界相通,无论烧杯中是水还是氢氧化钠溶液,导管中都不能
形成液柱,不能用于证明CO 和NaOH溶液反应;
2
D、实验过程中,滴加相同体积的氢氧化钠溶液、水,滴加氢氧化钠溶液气球膨胀更明显,
说明二氧化碳能和氢氧化钠反应。
故选:C。
【点评】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行
分析、判断,从而得出正确的结论。
19.(1分)某固体的溶解度随温度的升高而增大。将 80g 该固体加入到 50g 水中,加热充
分溶解,溶液的质量随温度的变化曲线如图所示。分析正确的是( )
A.40℃时,该物质的溶解度为 130 克/100 克水
B.M、N、P 点溶液的溶质质量分数依次增大
C.把溶液从 P点降温到 N 点一定析出晶体
D.M、N、P点溶液中,M、N点溶液一定饱和
【分析】根据固体的溶解度曲线可以: 查出某物质在一定温度下的溶解度,从而确定物
质的溶解性, 比较不同物质在同一温①度下的溶解度大小,从而判断饱和溶液中溶质的
质量分数的大小②, 判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶
还是蒸发结晶的方法③达到提纯物质的目的。
【解答】解:A、40℃时,溶液质量是130g,溶剂质量是50g,溶质质量是80g,该物质的溶解
度为160克/100克水,故A错误;
B、M、N点溶液的溶质质量分数依次增大,N、P两点的质量分数相等,故B错误;
C、把溶液从P点降温到N点,溶液质量不变,所以一定不会析出晶体,故C错误;
D、M、N、P三点所对应的溶液,属于饱和溶液的是M,因为温度升高,溶液质量会逐渐增
加,N点给他溶解度完了,所以N点也一定是饱和溶液,故D正确。
故选:D。
第15页(共24页)【点评】本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的
溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
20.(1分)某无色气体可能含有 H 、CO、CO 、H O 中的一种或多种。将该气体经过下列装
2 2 2
置(假设每步作用均完全),有关的实验现象依次是:NaOH 固体质量增重;CuO 由黑变
红;无水硫酸铜变蓝;NaOH 溶液质量增加。分析错误的是( )
A.该混合气体中肯定含有 CO、H
2
B.该混合气体中肯定含有 CO 、CO、H
2 2
C.该实验方案无法确定水的存在情况
D.该实验方案无法确定二氧化碳的存在情况
【分析】根据无水硫酸铜遇水变蓝的性质进行分析;根据氢气和一氧化碳具有还原性,二
氧化碳会与氢氧化钠反应进行分析;根据通过D后气体可能会携带水蒸气进行分析。
【解答】解:A、根据无水硫酸铜变蓝知,反应中有水生成,无色气体中含有H ,可判知是氢
2
气与氧化铜在加热条件下反应生成了水,该反应用化学方程式表示为:CuO+H
2
Cu+H O,硫酸铜与水反应生成蓝色五水硫酸铜,方程式为CuSO +5H O=CuSO •5H O;
2 4 2 4 2
根据氢氧化钠溶液质量增加可知反应有二氧化碳生成,一氧化碳具有还原性,在加热条件
下可与B装置中的氧化铜反应使固体由黑变红同时生成二氧化碳气体,可判断该混合气
体中肯定含有CO,CO与CuO反应的化学方程式是:CuO+CO Cu+CO ,说明气
2
体中含有CO,故A正确。
B和C、NaOH 能吸收水分,也能与二氧化碳反应,固体质量增重说明该混合气体中肯定
含有CO 或H O 或两者的混合物,故B错,C正确;
2 2
D、由于没有使用澄清石灰水,不能检验二氧化碳是否存在,故D正确。
故选:B。
【点评】此题主要是考查同学们的综合分析能力,不但要求同学们具备有关物质的基础知
第16页(共24页)识,而且要有实验操作的经历和分析、解决化学实验问题的能力。解题时需要认真分析题
目给出的条件,联系实际,逐一分析推断。
二、填空题(共18分)
21.(7分)化学来源于生活,生活中蕴含着许多化学知识,完成填空:
产生酸雨的主要物质是 SO (写化学式)。
2
①体温计里的液态金属是 H g (写化学式)。
②常用于改良酸性土壤的碱是 C a ( OH )
2
(写化学式)。
③炒菜时食盐溅到火焰上,看到火焰呈 黄 色。
④酒精(化学式为 C
2
H
5
OH)是常见的 有机物 (填“有机物”或“无机物”),其中碳、
⑤氢元素的物质的量之比为 1 : 3 ,0.1mol 酒精中含 1. 6 克氧元素。
【分析】首先根据题意确定物质的化学名称,然后根据书写化学式的方法和步骤写出物质
的化学式即可。
【解答】解: 二氧化硫是造成酸雨的主要气体之一;故填:SO ;
2
医用体温计①里的物质通常是常温下为液态的金属汞;故填:Hg;
②常用于改良酸性土壤的碱是氢氧化钙,故填Ca(OH)
2
;
③含钠的化合物的火焰反应的颜色呈黄色,故填黄;
④由酒精(化学式为C
2
H
5
OH)可知酒精属于含碳元素的化合物,属于有机物,其中其中碳、
⑤氢元素的物质的量之比为1:3;酒精的摩尔质量是46g/mol,所以0.1mol酒精的质量:
46g/mol×0.1mol=4.6g;氧元素的质量为:4.6g× ×100%=1.6g,故填:有机物;1:3;1.6。
答案为: SO ; Hg; Ca(OH) ; 黄; 有机物;1:3;1.6。
2 2
【点评】本①题难度不②大,熟练③掌握常见物质的④性质、用⑤途、组成及化学式的书写是正确解答
此类题的关键所在。
22.(5分)如图是甲、乙、丙三种物质的溶解度曲线,试回答:
(1)t ℃时,甲、乙、丙三种物质溶解度的大小关系是 甲=乙>丙 (用“>”或“<”
3
或“=”表示)。
(2)三种物质中可能是气体的是 丙 。
(3)t ℃时,若将 70g 的甲物质加入到有 100g 水的烧杯中,充分溶解后,所得的溶液的
2
质量是 150 g ,该溶液在溶解度曲线图中可表示为 A (选填“A”、“B”或“C”)
点;若加热该烧杯,升温至 t ℃,溶液的变化情况是 I I 、 II I 。
3
Ⅰ.溶液变为饱和Ⅱ.溶解度增大
第17页(共24页)Ⅲ.溶质增加Ⅳ.溶质的质量分数不变
【分析】根据固体的溶解度曲线可以: 查出某物质在一定温度下的溶解度,从而确定物
质的溶解性, 比较不同物质在同一温①度下的溶解度大小,从而判断饱和溶液中溶质的
质量分数的大小②, 判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶
还是蒸发结晶的方法③达到提纯物质的目的。
【解答】解:(1)通过分析溶解度曲线可知,t ℃时,甲、乙、丙三种物质溶解度的大小关系
3
是:甲=乙>丙;
(2)丙物质的溶解度随温度的升高而减小,所以三种物质中可能是气体的是丙;
(3)t ℃时,甲物质的溶解度是50g,所以若将70g的甲物质加入到有100g水的烧杯中,充
2
分溶解后,所得的溶液的质量是150g,该溶液在溶解度曲线图中可表示为A点;若加热该
烧杯,升温至 t ℃,溶解度大于70g,所以溶液的变化情况是:
3
Ⅰ、溶液变为不饱和,故错误;
Ⅱ、溶解度增大,故正确;
Ⅲ、溶质增加,故正确;
Ⅳ、溶质的质量分数增大,故错误。
故选:II、III。
故答案为:(1)甲=乙>丙;
(2)丙;
(3)150g,A,II、III。
【点评】本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的
溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
23.(6分)某校学生学习金属的活动性顺序,进行了如图一所示的实验。
第18页(共24页)a 试管中反应的化学方程式是 Fe+C u( NO ) = F e( NO ) +Cu ,该反应的基本类型
3 2 3 2
①是 置换反应 。
实验后把两试管中的物质全部倒入烧杯中(如图二),待反应结束后过滤,在滤渣中加
②入稀盐酸有气泡,则:
Ⅰ.滤渣中一定有的金属 C u 、 F e ;
Ⅱ.滤液中溶质的组成是 F e ( NO ) ;
3 2
Ⅲ.若滤渣中有两种金属,则滤渣中铁的质量 小于 (选填“大于”或“等于”或“小
于”)原金属铁的质量。
【分析】 根据铁与硝酸铜的反应写出反应的化学方程式,根据反应的特点分析反应的类
型; ①
根据铁与硝酸铜、稀盐酸的反应及反应的质量比分析判断。
【②解答】解: a 试管中的反应是铁与硝酸铜反应生成了硝酸亚铁和铜,化学方程式是:
Fe+Cu(NO )①=Fe(NO )+Cu,该反应由一种单质和一种化合物反应生成了另一种单质
3 2 3 2
和另一种化合物,基本类型是置换反应。
a 试管中的反应是铁与硝酸铜反应生成了硝酸亚铁和铜,b试管中铁与硝酸亚铁不反
②应,实验后把两试管中的物质全部倒入烧杯中(如图二),待反应结束后过滤,在滤渣中加
入稀盐酸有气泡,说明了a中有剩余的铁,硝酸铜完全发生了反应。
Ⅰ.由以上分析可知,滤渣中一定有的金属Cu、Fe;
Ⅱ.滤液中溶质的组成是Fe(NO ) ;
3 2
Ⅲ.由于铁与硝酸铜发生了反应,则滤渣中铁的质量小于原金属铁的质量。
故答为: Fe+Cu(NO )=Fe(NO )+Cu;置换反应。 ⅠCu、Fe,ⅡFe(NO ),Ⅲ大于。
3 2 3 2 3 2
【点评】①本题的难度不大,熟记金属活动性顺序了解其②应用是解答本题的基础知识。
三、简答题(共22分)
24.(7分)如图是实验室制备气体的部分装置,结合装置回答有关问题:
第19页(共24页)写出仪器 a 的名称 长颈漏斗 。
①实验室加热氯酸钾制取氧气的发生装置选择 B (填编号),化学方程式为 2KClO
3
②
2KCl+3O ↑ 。用 C 装置收集氧气,在 n (选填“m”或“n”)处用带火星木
2
炭验满。
实验室用锌与稀硫酸制取氢气并验证其可燃性,实验过程是:组装仪器→检测装置气
③密性→装入药品制氢气→ 验纯 →点燃,写出氢气燃烧的化学方程式 2H +O
2 2
2H O 。
2
实验室用足量锌与 50 克稀硫酸反应,制得0.2 克氢气,计算稀硫酸的溶质质量分数
④19.6% 。
【分析】 长颈漏斗方便加液体药品;
制取装①置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,
②如果用高锰酸钾或氯酸钾制氧气就需要加热。氧气的密度比空气的密度大,不易溶于水,
因此能用向上排空气法和排水法收集。
实验室用锌与稀硫酸制取氢气并验证其可燃性,实验过程是:组装仪器→检测装置气
③密性→装入药品制氢气→验纯→点燃;氢气和氧气在点燃的条件下生成水,配平即可;
有关的计算要准确。
④【解答】解: 长颈漏斗方便加液体药品,故答案为:长颈漏斗;
如果用氯酸①钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯
②化钾和氧气,配平即可;用C装置收集氧气,在n处用带火星木炭验满,因为氧气的密度
第20页(共24页)比空气大;故答案为:B;2KClO 2KCl+3O ↑;n;
3 2
实验室用锌与稀硫酸制取氢气并验证其可燃性,实验过程是:组装仪器→检测装置气
③密性→装入药品制氢气→验纯→点燃;氢气和氧气在点燃的条件下生成水,配平即可;故
答案为:验纯;2H +O 2H O;
2 2 2
设稀硫酸的溶质质量分数为x;
④Zn+H
2
SO
4
=ZnSO
4
+H
2
↑
98 2
50g•x 0.2g
x=19.6%;
答:稀硫酸的溶质质量分数为19.6%;
故答案为:19.6%;
【点评】本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查
了化学方程式的书写、气体的性质、有关化学方程式的计算等,综合性比较强。气体的制
取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度
和溶解性有关。本考点是中考的重要考点之一,主要出现在实验题中。
25.(7分)验证稀盐酸和氢氧化钠溶液发生反应的实验及实验中溶液 pH 的变化如图所示。
写出该反应的化学方程式 NaOH+HC l ═ NaCl+H O ,向 b 点所示溶液中滴加石蕊
2
①溶液,溶液呈 紫 色。
由图二可知:图一烧杯中盛放的原溶液是 NaOH 溶液 ,判定该反应发生的依据是
②溶液的 pH 由大变小 。
实验滴加试剂过程中,若把烧杯里的溶液倒入蒸发皿中蒸发,得到白色固体, 不能
③
第21页(共24页)(选填“能”或“不能”)证明该反应发生;若往烧杯里的溶液中滴加硫酸铜溶液,观察
到 无蓝色沉淀生成 ,能证明该反应发生。
a、b、c 三处对应溶液所含 NaCl 的质量大小关系是 c = b > a 。
【④分析】 稀盐酸和氢氧化钠溶液反应生成氯化钠和水,b 点所示溶液的pH等于7,溶液
显中性,①进行分析解答。
根据图象中pH值的变化是从大于7逐渐的减小到小于7,进行分析解答。
②根据氢氧化钠溶液蒸发也会得到白色固体,氢氧化钠能与硫酸铜溶液反应生成氢氧化
③铜蓝色沉淀,进行分析解答。
根据a点时,氢氧化钠还有剩余,b点时完全反应,进行分析解答。
④【解答】解: 稀盐酸和氢氧化钠溶液反应生成氯化钠和水,反应的化学方程式为:
NaOH+HCl═N①aCl+H O。
2
b 点所示溶液的pH等于7,溶液显中性,向 b 点所示溶液中滴加石蕊溶液,溶液呈紫色。
由图象可知,pH值是开始时大于7逐渐的减小到7然后小于7,可知原溶液显碱性,然
②后不断的加入酸性溶液,使pH减小,说明是把稀盐酸滴加到氢氧化钠溶液中。
实验滴加试剂过程中,若把烧杯里的溶液倒入蒸发皿中蒸发,得到白色固体,不能证明
③该反应发生,因为氢氧化钠溶液蒸发也会得到白色固体;氢氧化钠能与硫酸铜溶液反应生
成氢氧化铜蓝色沉淀,若往烧杯里的溶液中滴加硫酸铜溶液,观察到无蓝色沉淀生成,能
证明该反应发生。
a、b、c三点,在a点时,氢氧化钠还有剩余,此时生成了氯化钠,随着盐酸的继续加入,
④氯化钠质量继续加大,到b点时完全反应的、质量达到最大,随后由于无氢氧化钠,所以加
入盐酸不再生成氯化钠,所以氯化钠的质量保持不变了,则三点处对应溶液所含溶质
NaCl的质量大小关系是c=b>a。
故答案为:
NaOH+HCl═NaCl+H O;紫;
2
①NaOH溶液;溶液的 pH 由大变小;
②不能;无蓝色沉淀生成;
③c=b>a。
【④点评】本题难度不是很大,主要考查了中和反应及其应用,掌握溶液的酸碱性和溶液pH
大小之间的关系、从数形结合的角度理解中和反应是正确解答本题的关键。
26.(8分)固体样品 M 可能含碳酸钠、硫酸钠、氯化钠、氢氧化钠中的一种或几种。某同学
为探究其成分做了以下实验如图一:(硝酸钠和硝酸钡溶液均呈中性)。
第22页(共24页)操作的名称 过滤 。
①取固体 A 于试管中加足量稀硝酸,固体质量随加入稀硝酸质量的变化如图二根据上
②述实验分析,固体样品 M 中一定有 碳酸钠 。
为进一步探究该固体样品M成分,进行如下实验:
③Ⅰ.甲同学取少量溶液 B 于试管中,滴加酚酞试液,溶液呈红色,证明固体 M 中 可能
(选填“一定”或“可能”)有氢氧化钠。
Ⅱ.乙同学取少量溶液 B 于试管中, 滴加足量稀硝酸后,再滴加硝酸银溶液 ,产生白
色沉淀,证明固体 M 中有氯化钠。
【分析】硝酸钡和碳酸钠反应生成白色沉淀碳酸钡和硝酸钠,和硫酸钠反应生成白色沉淀
硫酸钡和硝酸钠,碳酸钡和稀硝酸反应生成硝酸钡、水和二氧化碳,硫酸钡不能和稀硝酸
反应;
碳酸钠溶液和氢氧化钠溶液都是显碱性溶液,都能使酚酞试液变红色。
【解答】解: 操作的名称是过滤。
故填:过滤。①
固体质量随加入稀硝酸质量的变化如图二,固体全部消失,说明固体是碳酸钡,没有硫
②酸钡,因此固体样品 M 中一定有碳酸钠,一定没有硫酸钠。
故填:碳酸钠。
Ⅰ.甲同学取少量溶液 B 于试管中,滴加酚酞试液,溶液呈红色,证明固体 M 中可能
③有氢氧化钠,这是因为氢氧化钠溶液和碳酸钠溶液都是显碱性溶液,都能使酚酞试液变红
色,如果不含有氢氧化钠,含有过量碳酸钠,也能使酚酞试液变红色。
故填:可能。
Ⅱ.取少量溶液 B 于试管中,滴加足量稀硝酸后,再滴加硝酸银溶液,产生白色沉淀,证
明固体 M 中有氯化钠,这是因为氯化钠能和硝酸银反应生成白色沉淀氯化银和硝酸钠。
故填:滴加足量稀硝酸后,再滴加硝酸银溶液。
第23页(共24页)【点评】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行
分析、判断,从而得出正确的结论。
第24页(共24页)