文档内容
2021-2022 学年上海市静安区第二学期初三二模
化学部分
可能用到的相对原子质量:H-1 C-12 O-16
一、选择题(共20分)
1. 能使带火星的木条复燃的气体是
A. 空气 B. 氧气 C. 氮气 D. 二氧化碳
2. 钙是构成人体的重要组分。这里的“钙”是指
A. 单质 B. 元素 C. 分子 D. 原子
3. 与温室效应形成有关的物质是
.
A 氮气 B. 氧气 C. 二氧化硫 D. 二氧化碳
4. 下列物质属于钾肥的是
A. KSO B. NH NO C. MgCl D. Ca (PO )
2 4 4 3 2 3 4 2
5. 下列物质中,放入水里不能形成溶液的是( )
A. 蔗糖 B. 植物油 C. 食盐 D. 酒精
6. 如果用“ ”表示氧原子,用“ ”示硫原子,则下列模型可以表示二氧化硫分子
的
(SO ) 是
2
A. B. C. D.
7. 和金刚石互为同素异形体的是
A. 碳酸 B. 碳酸钙 C. 石墨 D. 一氧化碳
8. “84消毒液”是预防“新冠肺炎”的消毒剂之一、其主要成分次氯酸钠(NaClO)中氯元素的化合价为
A. -2 B. -1 C. +1 D. +2
9. 下列物质在氧气中燃烧,火星四射,生成黑色固体的是
A. 红磷 B. 氢气 C. 酒精 D. 铁丝
10. 属于纯净物的是
A. 盐酸 B. 空气 C. 自来水 D. 氧化铁
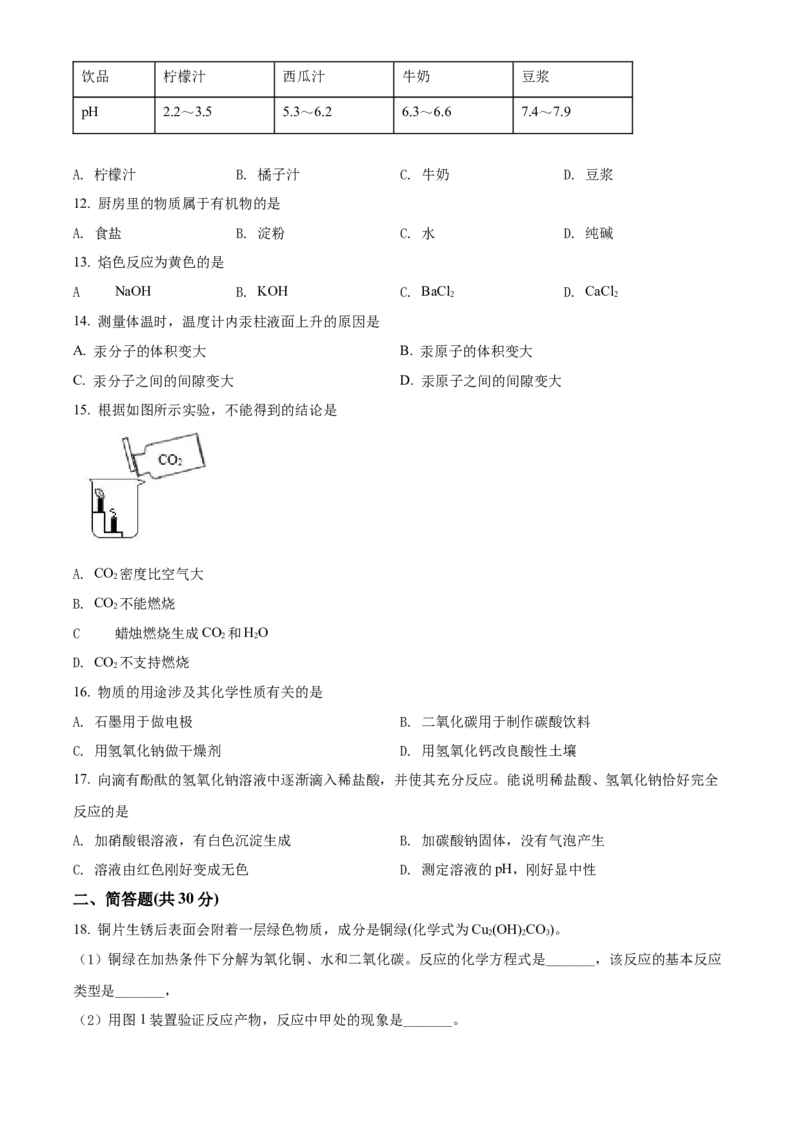
11. 下列饮品酸性最强的是饮品 柠檬汁 西瓜汁 牛奶 豆浆
pH 2.2~3.5 5.3~6.2 6.3~6.6 7.4~7.9
A. 柠檬汁 B. 橘子汁 C. 牛奶 D. 豆浆
12. 厨房里的物质属于有机物的是
A. 食盐 B. 淀粉 C. 水 D. 纯碱
13. 焰色反应为黄色的是
.
A NaOH B. KOH C. BaCl D. CaCl
2 2
14. 测量体温时,温度计内汞柱液面上升的原因是
A. 汞分子的体积变大 B. 汞原子的体积变大
C. 汞分子之间的间隙变大 D. 汞原子之间的间隙变大
15. 根据如图所示实验,不能得到的结论是
A. CO 密度比空气大
2
B. CO 不能燃烧
2
.
C 蜡烛燃烧生成CO 和HO
2 2
D. CO 不支持燃烧
2
16. 物质的用途涉及其化学性质有关的是
A. 石墨用于做电极 B. 二氧化碳用于制作碳酸饮料
C. 用氢氧化钠做干燥剂 D. 用氢氧化钙改良酸性土壤
17. 向滴有酚酞的氢氧化钠溶液中逐渐滴入稀盐酸,并使其充分反应。能说明稀盐酸、氢氧化钠恰好完全
反应的是
A. 加硝酸银溶液,有白色沉淀生成 B. 加碳酸钠固体,没有气泡产生
C. 溶液由红色刚好变成无色 D. 测定溶液的pH,刚好显中性
二、简答题(共30分)
18. 铜片生锈后表面会附着一层绿色物质,成分是铜绿(化学式为Cu (OH) CO)。
2 2 3
(1)铜绿在加热条件下分解为氧化铜、水和二氧化碳。反应的化学方程式是_______,该反应的基本反应
类型是_______,
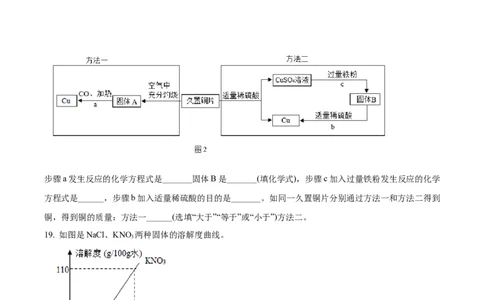
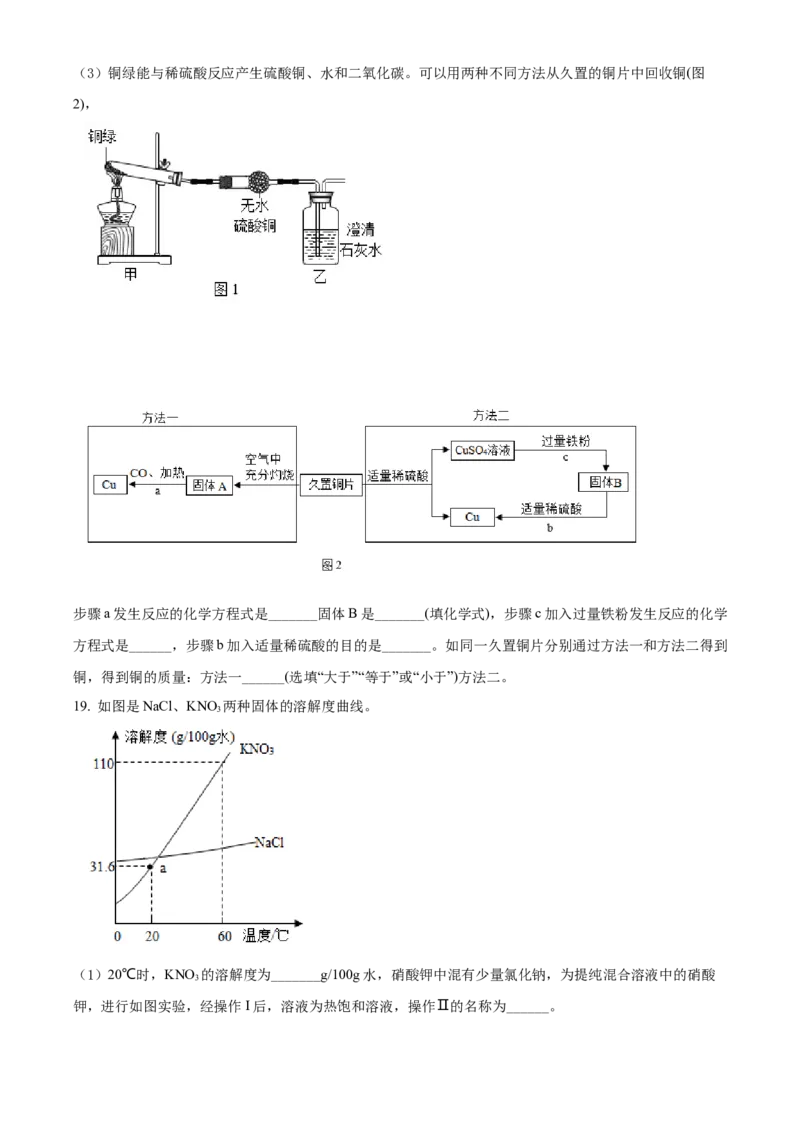
(2)用图1装置验证反应产物,反应中甲处的现象是_______。(3)铜绿能与稀硫酸反应产生硫酸铜、水和二氧化碳。可以用两种不同方法从久置的铜片中回收铜(图
2),
步骤a发生反应的化学方程式是_______固体B是_______(填化学式),步骤c加入过量铁粉发生反应的化学
方程式是______,步骤b加入适量稀硫酸的目的是_______。如同一久置铜片分别通过方法一和方法二得到
铜,得到铜的质量:方法一______(选填“大于”“等于”或“小于”)方法二。
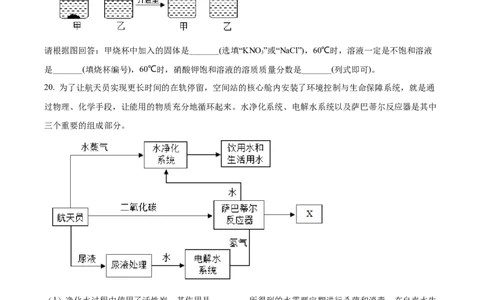
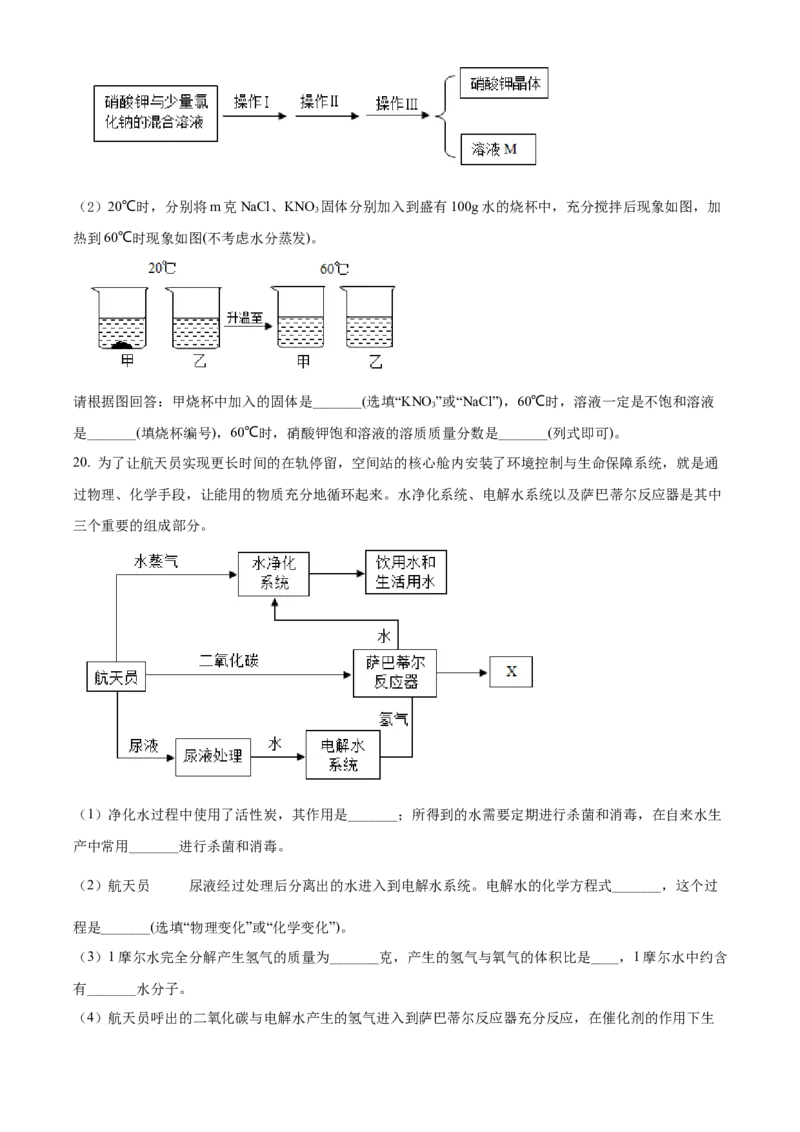
19. 如图是NaCl、KNO 两种固体的溶解度曲线。
3
(1)20℃时,KNO 的溶解度为_______g/100g水,硝酸钾中混有少量氯化钠,为提纯混合溶液中的硝酸
3
钾,进行如图实验,经操作I后,溶液为热饱和溶液,操作Ⅱ的名称为______。(2)20℃时,分别将m克NaCl、KNO 固体分别加入到盛有100g水的烧杯中,充分搅拌后现象如图,加
3
热到60℃时现象如图(不考虑水分蒸发)。
请根据图回答:甲烧杯中加入的固体是_______(选填“KNO”或“NaCl”),60℃时,溶液一定是不饱和溶液
3
是_______(填烧杯编号),60℃时,硝酸钾饱和溶液的溶质质量分数是_______(列式即可)。
20. 为了让航天员实现更长时间的在轨停留,空间站的核心舱内安装了环境控制与生命保障系统,就是通
过物理、化学手段,让能用的物质充分地循环起来。水净化系统、电解水系统以及萨巴蒂尔反应器是其中
三个重要的组成部分。
(1)净化水过程中使用了活性炭,其作用是_______;所得到的水需要定期进行杀菌和消毒,在自来水生
产中常用_______进行杀菌和消毒。
的
(2)航天员 尿液经过处理后分离出的水进入到电解水系统。电解水的化学方程式_______,这个过
程是_______(选填“物理变化”或“化学变化”)。
(3)1摩尔水完全分解产生氢气的质量为_______克,产生的氢气与氧气的体积比是____,1摩尔水中约含
有_______水分子。
(4)航天员呼出的二氧化碳与电解水产生的氢气进入到萨巴蒂尔反应器充分反应,在催化剂的作用下生成水和气体X。用氢氧化钠吸收过量的二氧化碳,为探究物质X的化学式,实验室进行如下探究:
回答下列问题:
A装置中看到的现象是_______;B中发生的化学方程式是_______。已知A装置增重36g, B 装置增重
56g,那么X的化学式可能是_______。
21. 实验室有以下四组未贴标签溶液,需要对每组内两种溶液加以区分。
I.碳酸钠、氢氧化钠 II.氢氧化钙、氢氧化钠
III.氢氧化钙、氯化钙 IV.稀盐酸、稀硫酸
提供的试剂:a.氯化钡溶液 b.碳酸钠溶液 c.二氧化碳 d.稀盐酸
在提供的试剂中(每种试剂只能使用一次),能鉴别I、II、III三组溶液的试剂,依次是____、_____、
______(用字母“a”“b”“c”“d”表示)。写出第IV组鉴别时发生反应的化学方程式_______。