文档内容
2022 学年第二学期初三年级化学学业质量调研
相对原子质量:H-1 C-12 O-16 Na-23 S-32 C1-35.5 Ag-108
一、填空题(1-14每题只有1个正确选项,每题1分,共14分,15-17每题有1-2个正确选项,
每题2分,共6分。)
1. 空气中含量最多的气体是
A. 氮气
B. 氧气
C. 氦气
D. 二氧化碳
【答案】A
【解析】
【详解】空气是由多种气体组成的混合物,主要成分是氮气和氧气,其中氮气约占五分之四,氧气约为五
分之一,所以含量最多的为氮气。二氧化碳约为0.03%,氦气为稀有气体含量也很少。故选A。
2. 属于化学性质的是
A. 挥发性 B. 溶解性 C. 助燃性 D. 导电性
【答案】C
【解析】
【详解】A 、挥发性,是不需要通过化学变化表现出来的性质,属于物理性质,故A错误;
B 、溶解性是不需要通过化学变化表现出来的性质,属于物质的物理性质,故B错误;
C、助燃性,是需要通过化学变化表现出来的性质,属于化学性质,故C正确;
D 、导电性,是不需要通过化学变化表现出来的性质,属于物理性质,故D错误;
故选:C。
3. 与石墨互为同素异形体的是
A. 金刚石 B. 木炭 C. 炭黑 D. 一氧化碳
【答案】A
【解析】
【分析】同素异形体是同种元素形成的不同单质。
【详解】A、金刚石俗称金刚钻,它是一种由碳元素组成的矿物,与石墨互为同素异形体,符合题意。
B、木灰是由石墨的微小晶体和少量杂质构成的混合物,不符合题意;
C、炭黑主要成分是碳,同时含有少量氢、氧、氮等元素,这些杂质元素主要以羟基、羰基、氨基或氰基等
形式存在,它是含碳物质(煤、天然气、重油、燃料油等)在空气不足的条件下经不完全燃烧或受热分解而
得的产物,是混合物,不符合题意;
第1页/共14页
学科网(北京)股份有限公司D、一氧化碳是由碳元素和氧元素组成的氧化物,不符合题意。
故选A
4. 不属于有机物的是
.
A 甲烷 B. 碳酸 C. 酒精 D. 葡萄糖
【答案】B
【解析】
【详解】A、甲烷是含有碳元素的化合物,属于有机物,故选项不符合题意;
B、碳酸是含有碳元素的化合物,但是它的性质和无机物相似,属于无机物,故选项符合题意;
C、酒精是含有碳元素的化合物,属于有机物,故选项不符合题意;
D、葡萄糖是含有碳元素的化合物,属于有机物,故选项不符合题意。
故选B。
5. 赤铁矿(主要成分是Fe O)用于工业炼铁。Fe O 中铁元素的化合价为
2 3 2 3
A. -3 B. -2 C. +2 D. +3
【答案】D
【解析】
【详解】根据化合物中正负化合价代数和为零,Fe O 中氧元素的化合价为-2价,则设铁元素的化合价为
2 3
x, ,解得x=+3,故选D。
6. 加入水中能形成蓝色溶液的是
A. 粉笔灰 B. 食用油 C. 硫酸铜 D. 氯化钠
【答案】C
【解析】
【详解】A、粉笔灰不溶于水,与水混合生成的是悬浊液,不符合题意;
B、食用油不溶于水,与水混合形成的是乳浊液,不符合题意;
C、硫酸铜溶于水形成的是蓝色溶液,符合题意;
D、氯化钠溶于水形成的是无色溶液,不符合题意;
故选C。
7. 实验室制取氧气的反应: ,该反应属于
A. 分解反应 B. 化合反应 C. 复分解反应 D. 置换反应
【答案】A
【解析】
第2页/共14页
学科网(北京)股份有限公司【详解】由一种物质生成两种或两种以上物质的反应叫做分解反应,根据化学方程式可知,反应物有1种,
生成物有2种,符合“一变多”,属于分解反应,故选A。
8. 在氧气中燃烧,产生白色固体的是
A. 硫 B. 铁丝 C. 红磷 D. 氢气
【答案】C
【解析】
【详解】A、硫在氧气中燃烧生成二氧化硫气体,没有固体生成,故选项不符合题意;
B、铁丝在氧气中剧烈燃烧,生成黑色固体,故选项不符合题意;
C、红磷在氧气中燃烧,产生大量白烟,生成白色固体,故选项符合题意;
D、氢气在氧气中燃烧生成水,没有固体生成,故选项不符合题意;
故选C。
9. 氢元素以游离态存在的物质是
A. H B. HO C. HCl D. NaOH
2 2
【答案】A
【解析】
【详解】A、 为单质,则氢元素以游离态形式存在,A选项符合题意;
B、 为化合物,则氢元素以化合态形式存在,B选项不符合题意;
C、 为化合物,则氢元素以化合态形式存在,C选项不符合题意;
D、 为化合物,则氢元素以化合态形式存在,D选项不符合题意。
故选:A。
10. 物质的用途错误的是
A. 氖气:填充霓虹灯 B. 氢氧化钠:治疗胃酸过多
C. 盐酸:除铁锈 D. 一氧化碳:冶炼金属
【答案】B
【解析】
【详解】A、氖气是稀有气体,稀有气体通电能发出有色光,且性质稳定,常用于填充霓虹灯,用途正确;
B、氢氧化钠具有强腐蚀性,不可用于治疗胃酸过多,用途错误;
C、铁锈的主要成分是氧化铁,盐酸可以与氧化铁发生反应,所以盐酸可以用于除铁锈,用途正确;
D、一氧化碳具有还原性,可以与金属氧化物发生反应冶炼金属,用途正确。
故选B。
第3页/共14页
学科网(北京)股份有限公司11. 关于KNO 的叙述错误的是
3
A. 属于盐 B. 含有原子团
C. 可作复合肥料 D. 灼烧时火焰呈黄色
【答案】D
【解析】
【详解】A、硝酸钾能电离出钾离子和硝酸根离子,属于盐;
B、硝酸钾中含有硝酸根离子是原子团,选项正确;
C、硝酸钾含有钾元素和氮元素,含两种营养元素属于复合肥,选项正确;
D、硝酸钾的燃烧会产生紫色的火焰(透过蓝色钴玻璃),选项错误;
故选:D。
12. 将洁净的铁丝浸入含硝酸铜和硝酸锌的混合溶液中,一段时间后取出,铁丝表面覆盖了一层物质,这
层物质是
A. 锌 B. 铜 C. 铜和锌 D. 铁和锌
【答案】B
【解析】
【详解】金属活动性顺序中,排在前面的金属能将排在后面的金属从其化合物的水溶液中置换出来,根据
金属活动性顺序:锌>铁>氢>铜,将洁净的铁丝浸入含硝酸铜和硝酸锌的混合溶液中,铁不能与硝酸锌
反应,铁可以与硝酸铜反应生成铜和硝酸亚铁,故一段时间后取出,铁丝表面覆盖了一层物质,这层物质
是铜,
故选B。
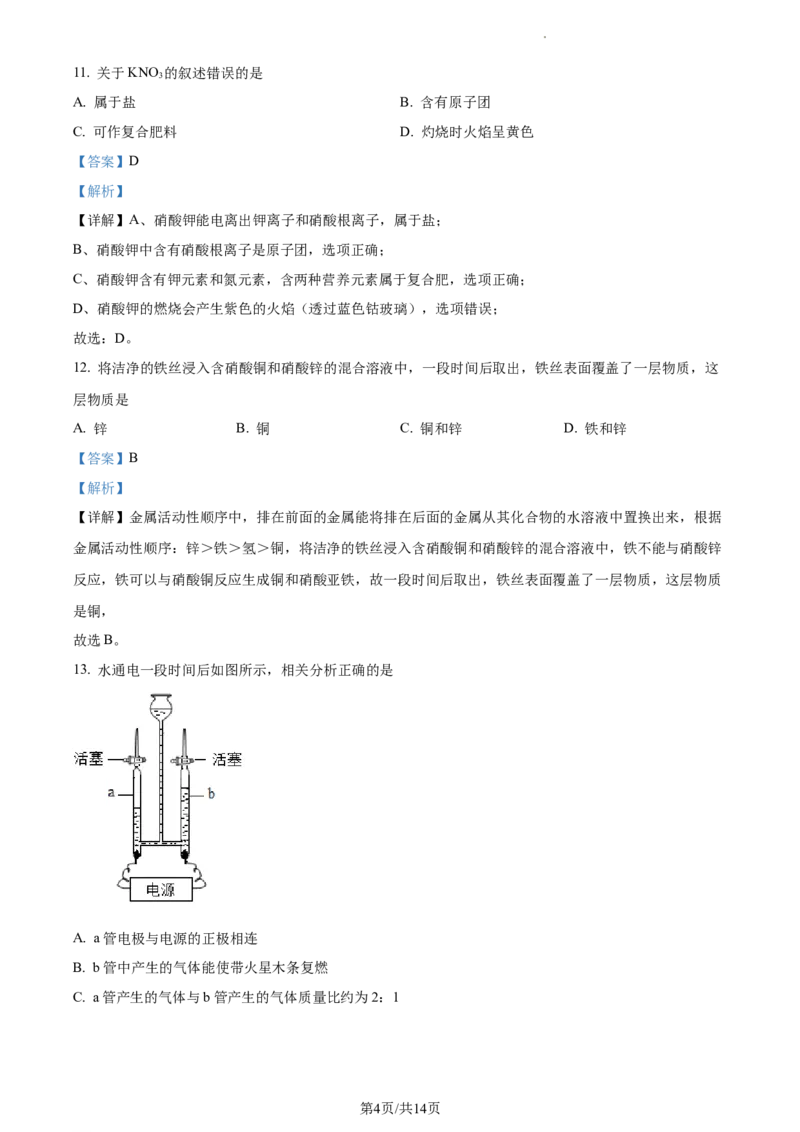
13. 水通电一段时间后如图所示,相关分析正确的是
A. a管电极与电源的正极相连
B. b管中产生的气体能使带火星木条复燃
C. a管产生的气体与b管产生的气体质量比约为2:1
第4页/共14页
学科网(北京)股份有限公司D. 该实验证明每个水分子是由2个氢原子和1个氧原子构成
【答案】B
【解析】
【详解】A、电解水时,负极产生氢气,正极产生氧气,体积比约为2:1。a管产生气体较多,电极与电源
的负极相连,错误;
B、b玻璃管中产生的气体体积少,是氧气,氧气 具有助燃性,能使带火星木条复燃,正确;
C、a、b两玻璃管中产生的气体分别是氢气、氧气,体积比约为2:1,不是质量比,错误;
D、电解水时,负极产生氢气,正极产生氧气,氢气是由氢元素组成,氧气是由氧元素组成,化学变化中
元素的种类不变,该实验证明水是由氢元素和氧元素组成,不能证明每个水分子是由2个氢原子和1个氧
原子构成,错误。
故选B。
14. 对应的实验操作能达到实验目的的是
选项 实验目的 实验操作
A 鉴别稀盐酸和稀硫酸 取样,分别滴加AgNO 溶液
3
B 证明中和反应放出热量 将NaOH固体放入稀盐酸中
C 检验CO 中是否混有HCl 将气体通入紫色石蕊试液中
2
D 除去Cu粉中混有的少量CuO 加入过量的稀HSO ,过滤
2 4
A. A B. B C. C D. D
【答案】D
【解析】
【详解】A、硝酸银和盐酸反应生成氯化银沉淀和硝酸,硝酸银和硫酸生成微溶于水的硫酸银沉淀和硝酸,
因此都会出现浑浊现象,无法鉴别,选项错误;;
B、氢氧化钠固体溶于水时也会放热,因此氢氧化钠固体放入盐酸中无法判断是否为中和反应放出的热,
选项错误;
C、二氧化碳与水反应生成碳酸,碳酸显酸性能使石蕊变红,而氯化氢溶于水形成盐酸显酸性能使石蕊变
红,因此无法检验二氧化碳中是否含有氯化氢,选项错误;
D、氧化铜可以和过量的稀硫酸反应生成硫酸铜和水,因此过滤后可以除去铜中的氧化铜,选项正确;
故选:D。
15. 干垃圾焚烧可用于发电,焚烧前一般需粉碎处理。粉碎的目的是
A. 降低可燃物的着火点 B. 使可燃物分子变小
第5页/共14页
学科网(北京)股份有限公司C. 增大与氧气的接触面积 D. 减少消耗氧气的质量
【答案】C
【解析】
【详解】干垃圾焚烧可用于发电,焚烧前一般需粉碎处理,粉碎可以增大可燃物与氧气的接触面积,其目
的是使燃料充分燃烧。
故选C。
16. 氢气还原氧化铜的实验装置如图所示,说法错误的是
A. 导气管伸入试管底部的原因是氢气的密度比空气小
B. 反应开始后通入0.1mol氢气可生成0.1mol铜
C. 实验中固体减少的质量小于生成水的质量
D. 实验结束后试管内的固体可能是暗红色
【答案】AB
【解析】
【详解】A、导气管伸入试管底部的原因是为了排尽装置中的空气,防止加热时发生爆炸,故选项说法不
正确;
B、氢气与氧化铜在加热时生成铜和水,反应的化学方程式为H+CuO Cu+H O,该反应前后都要通入氢
2 2
气,因此反应开始后通入0.1mol氢气不可能生成0.1mol铜,故选项说法不正确;
C、由反应的化学方程式H+CuO Cu+H O可知,实验中固体减少的质量为氧化铜中氧元素的质量,因此
2 2
小于生成水的质量,故选项说法正确;
D、实验中生成的铜是红色的,若生成的铜部分被氧化,则试管内的固体可能是暗红色,故选项说法正确。
故选AB。
17. 对有关化学概念的理解与认识正确的是
A. 由同种原子构成的物质是纯净物 B. 1molH 和1molO 所含的原子数相同
2 2
C. 溶质的质量分数越大所含溶质的质量也越大 D. 1g硫与1g氧气充分反应可生成2g二氧化硫
第6页/共14页
学科网(北京)股份有限公司【答案】BD
【解析】
【详解】A、由同种原子构成的物质不一定是纯净物,如臭氧和氧气组成的混合物,都是由氧原子构成,
错误;
B、由 ,得1molH 所含原子的个数= , 1molO 所含的原子数
2 2
= ,所含的原子数相同,正确;
C、没有指明溶液的质量,故溶质的质量分数越大所含溶质的质量不一定越大,错误;
D、根据化学反应方程式 ,得硫和氧气反应的质量比为1:1,故1g硫与1g氧气充分反应
可生成2g二氧化硫,正确。
故选BD。
二、简答题(共30分)
18. 化学与人类的生产、生活密切相关。
(1)自来水生产中加入活性炭,利用其_______性除去水中的异味,属于_______变化(填“物理”或“化
学”);可加入二氧化氯(C1O)杀菌消毒,其制取的一种原理是: ,则X的
2
化学式是_______。
(2)化石燃料燃烧产生过多的二氧化碳,导致的环境问题是_______。中国计划在2060年实现“碳中和”,
彰显大国担当。科学家利用新型催化剂,将二氧化碳转化为甲醇,反应的微观示意图如下:
甲醇(CHOH)的摩尔质量是_______,1molCH OH中约含_______个碳原子(用科学计数法表示);上述反应
3 3
中甲与乙的分子个数比是_______。
【答案】(1) ①. 吸附 ②. 物理 ③. NaCl
(2) ①. 温室效应
②. 32g/mol ③. 6.02×1023 ④. 1:3
【解析】
第7页/共14页
学科网(北京)股份有限公司【小问1详解】
自来水生产中加入活性炭,利用其吸附性除去水中的异味,此过程中没有新物质生成,属于物理变化;
根据化学方程式可知,参加反应的一共有4个氯原子、2个钠原子、4个氧原子,而生成物中有4个氧原子、
2个氯原子,化学变化中原子的种类和数目不变,所以X中应有一个氯原子和一个钠原子,故其化学式为
NaCl;
【小问2详解】
化石燃料燃烧产生过多的二氧化碳,导致的环境问题是温室效应;甲醇相对分子质量=12+1×4+16=32,
(CHOH)的摩尔质量是32g/mol,1molCH OH中含有1mol 碳原子,约含6.02×1023个碳原子(用科学计数法
3 3
表示);由反应的微观示意图可知,该反应的化学方程式为:CO+3H CHOH+H O,反应中甲与乙
2 2 3 2
的分子个数比是1:3。
19. 氯化钠和硝酸钾在不同温度时的溶解度见下表:
温度(℃) 20 30 40 60 80 100
氯化钠 36.0 36.3 36.6 37.3 38.4 39.8
溶解度(g/100g水)
硝酸钾 31.6 45.8 63.9 110 169 246
(1)40℃时,氯化钠的溶解度是_______g。
(2)两物质中溶解度受温度影响较大的是_______。
(3)60℃时,100g硝酸钾饱和溶液中溶质与溶剂的质量比是_______。
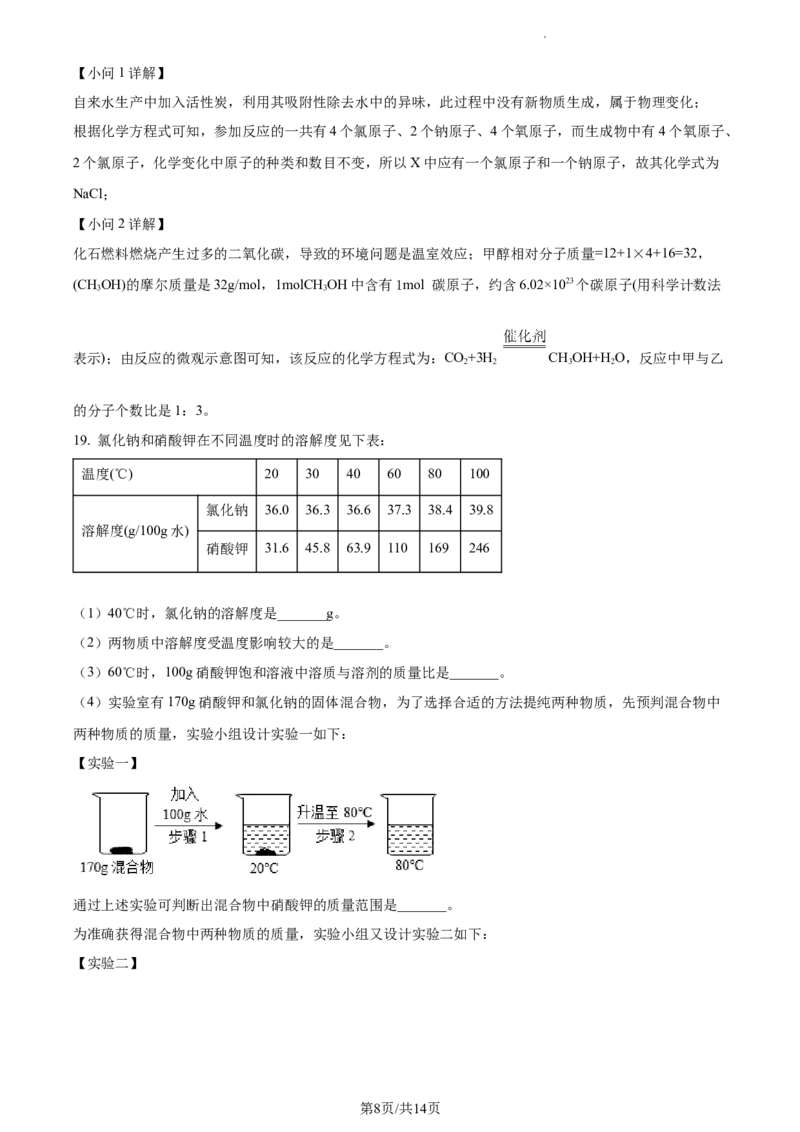
(4)实验室有170g硝酸钾和氯化钠的固体混合物,为了选择合适的方法提纯两种物质,先预判混合物中
两种物质的质量,实验小组设计实验一如下:
【实验一】
通过上述实验可判断出混合物中硝酸钾的质量范围是_______。
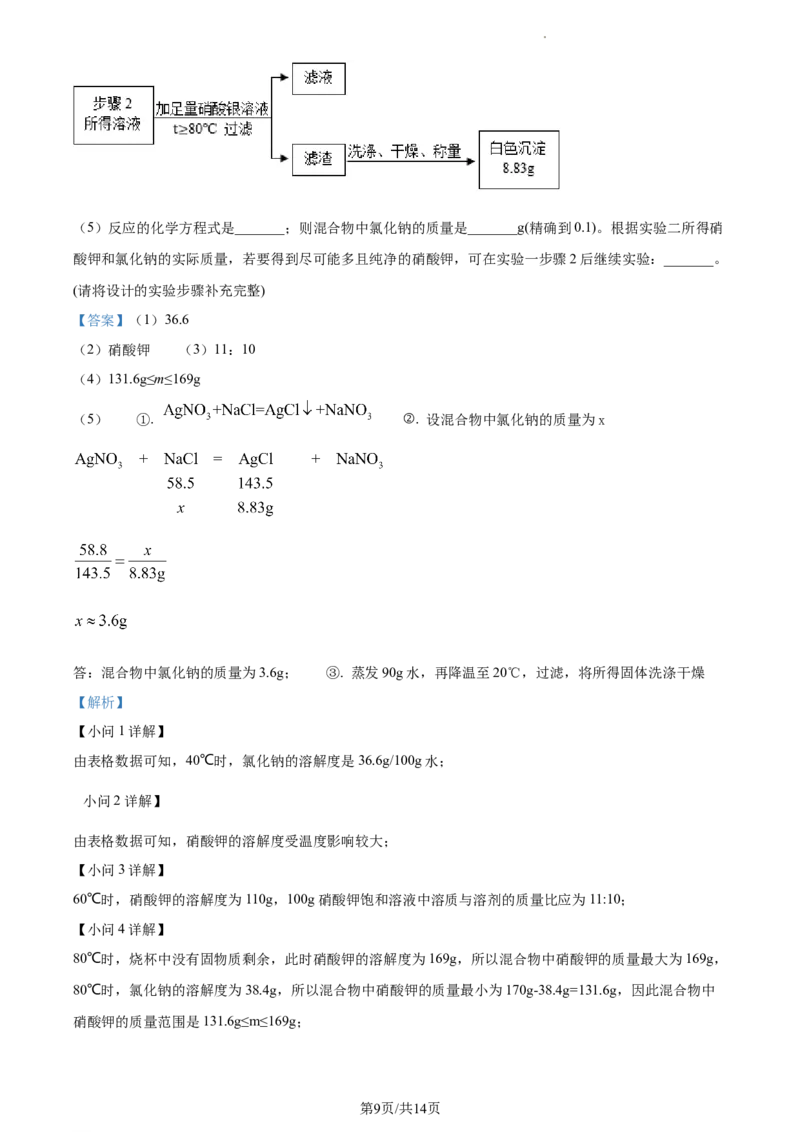
为准确获得混合物中两种物质的质量,实验小组又设计实验二如下:
【实验二】
第8页/共14页
学科网(北京)股份有限公司(5)反应的化学方程式是_______;则混合物中氯化钠的质量是_______g(精确到0.1)。根据实验二所得硝
酸钾和氯化钠的实际质量,若要得到尽可能多且纯净的硝酸钾,可在实验一步骤2后继续实验:_______。
(请将设计的实验步骤补充完整)
【答案】(1)36.6
(2)硝酸钾 (3)11:10
(4)131.6g≤m≤169g
(5) ①. ②. 设混合物中氯化钠的质量为x
答:混合物中氯化钠的质量为3.6g; ③. 蒸发90g水,再降温至20℃,过滤,将所得固体洗涤干燥
【解析】
【小问1详解】
由表格数据可知,40℃时,氯化钠的溶解度是36.6g/100g水;
【
小问2详解】
由表格数据可知,硝酸钾的溶解度受温度影响较大;
【小问3详解】
60℃时,硝酸钾的溶解度为110g,100g硝酸钾饱和溶液中溶质与溶剂的质量比应为11:10;
【小问4详解】
80℃时,烧杯中没有固物质剩余,此时硝酸钾的溶解度为169g,所以混合物中硝酸钾的质量最大为169g,
80℃时,氯化钠的溶解度为38.4g,所以混合物中硝酸钾的质量最小为170g-38.4g=131.6g,因此混合物中
硝酸钾的质量范围是131.6g≤m≤169g;
第9页/共14页
学科网(北京)股份有限公司【小问5详解】
硝酸银和氯化钠反应生成氯化银和硝酸钠,反应的化学方程式为:AgNO+NaCl=AgCl↓+NaNO ,混合物
3 3
中氯化钠的质量见解析;根据实验二所得硝酸钾和氯化钠的实际质量,若要得到尽可能多且纯净的硝酸钾,
混合物中氯化钠3.6g,只需要20℃的10g水就可以完全溶解,可在实验一步骤2后继续实验:蒸发90g水,
再降温至20℃,过滤,将所得固体洗涤干燥。
20. 二氧化碳是碳循环中的重要物质。
的
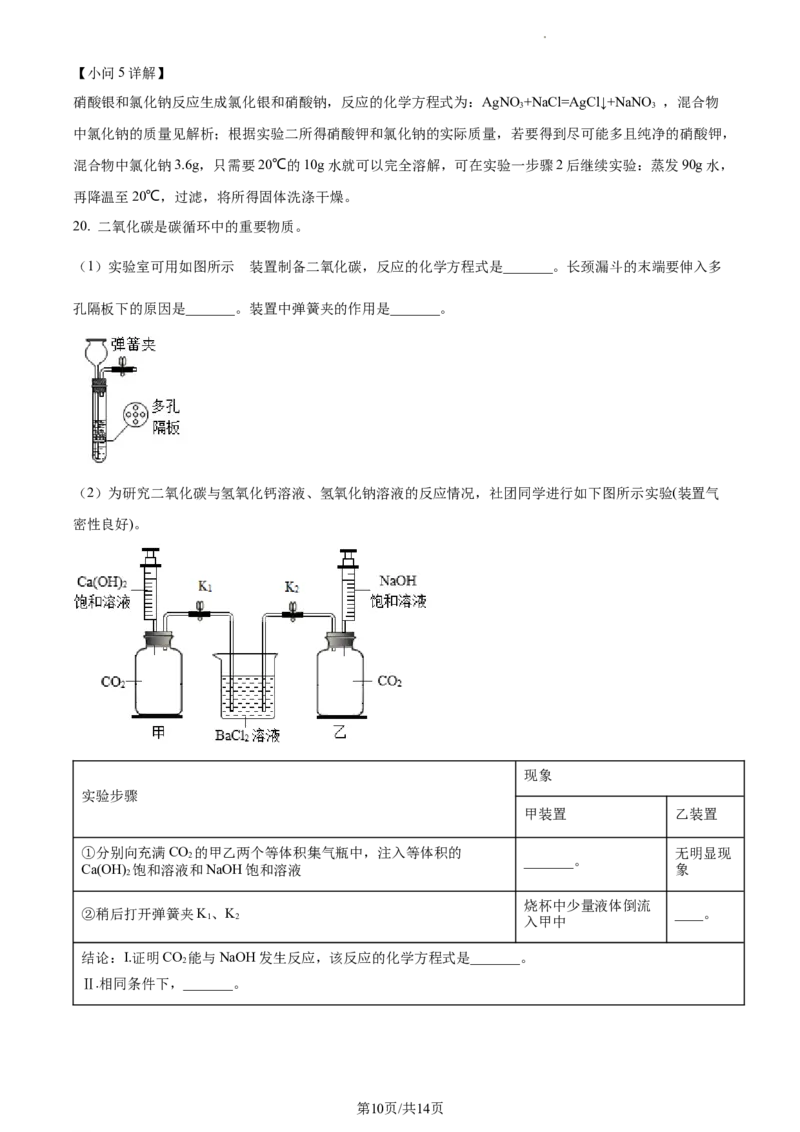
(1)实验室可用如图所示 装置制备二氧化碳,反应的化学方程式是_______。长颈漏斗的末端要伸入多
孔隔板下的原因是_______。装置中弹簧夹的作用是_______。
(2)为研究二氧化碳与氢氧化钙溶液、氢氧化钠溶液的反应情况,社团同学进行如下图所示实验(装置气
密性良好)。
现象
实验步骤
甲装置 乙装置
①分别向充满CO 的甲乙两个等体积集气瓶中,注入等体积的 无明显现
2 _______。
Ca(OH) 饱和溶液和NaOH饱和溶液 象
2
烧杯中少量液体倒流
②稍后打开弹簧夹K、K ____。
1 2 入甲中
结论:I.证明CO 能与NaOH发生反应,该反应的化学方程式是_______。
2
Ⅱ.相同条件下,_______。
第10页/共14页
学科网(北京)股份有限公司(3)社团同学最后对制取二氧化碳后的废液中是否含有盐酸进行了检验,其中可选择的试剂是_______。
A. Zn粒 B. AgNO 溶液 C. 酚酞 D. NaCO 固体
3 2 3
【答案】(1) ①. CaCO +2HCl=CaCl +H O+CO↑ ②. 便于在实现液封的同时,关闭弹簧夹时实现
3 2 2 2
固液分离 ③. 控制反应的发生与停止
(2) ①. 产生白色沉淀 ②. 烧杯中大量液体倒流入乙中,且生成白色沉淀 ③.
2NaOH+CO =Na CO+H O ④. 氢氧化钠溶液吸收二氧化碳效果比氢氧化钙溶液好 (3)AD
2 2 3 2
【解析】
【小问1详解】
实验室用大理石、稀盐酸制取二氧化碳,反应的化学方程式是:CaCO +2HCl=CaCl +H O+CO↑。
3 2 2 2
长颈漏斗 的末端要伸入多孔隔板下的原因是便于在实现液封的同时,关闭弹簧夹时实现固液分离。关闭装
置中的弹簧夹,二氧化碳气体不能排出,试管内压强变大,稀盐酸被压进长颈漏斗中与大理石脱离,反应
停止,打开弹簧夹,二氧化碳气体排出,试管内压强变小,稀盐酸进入试管内与大理石接触,反应发生,
所以装置中弹簧夹的作用是控制反应的发生与停止。
【小问2详解】
①分别向充满CO 的甲、乙两个等体积集气瓶中,注入等体积的Ca(OH) 饱和溶液和NaOH饱和溶液。因
2 2
为二氧化碳与澄清石灰水反应生成碳酸钙白色沉淀、水,二氧化碳与氢氧化钠溶液反应无明显现象,所以
观察到甲装置中产生白色沉淀。②稍后打开弹簧夹K、K,因为乙装置中气体减少,压强变小,所以有大
1 2
量液体倒流入乙中,生成的碳酸钠溶液能与氯化钡溶液反应生成白色碳酸钡沉淀。所以观察到乙装置的烧
杯中有大量液体倒流入乙中,且生成白色沉淀。
结论:I.证明CO 能与NaOH发生反应生成碳酸钠、水,该反应的化学方程式是:
2
2NaOH+CO =Na CO+H O。
2 2 3 2
Ⅱ. 因为氢氧化钠易溶于水、氢氧化钙微溶于水,所以相同条件下,氢氧化钠溶液吸收二氧化碳效果比氢
氧化钙溶液好。
【小问3详解】
制取二氧化碳后的废液中含有氯化钙,可能含有盐酸。
A. Zn粒能与盐酸反应生成气体,不与氯化钙溶液反应,所以用锌粒可检验废液中是否含有盐酸,此选项
符合题意;
B. 氯化钙、盐酸都能与AgNO 溶液发生反应生成白色沉淀,所以用AgNO 溶液不能检验废液中 否是含有
3 3
盐酸,此选项不符合题意;
C. 酚酞试液遇中性溶液、酸性溶液都不变色,用酚酞试液不能检验废液中是否含有盐酸,此选项不符合
题意;
D. Na CO 固体能与稀盐酸反应生成二氧化碳气体而冒气泡,能与氯化钙溶液反应生成白色沉淀,所以可
2 3
第11页/共14页
学科网(北京)股份有限公司用NaCO 固体检验废液中是否含有盐酸,此选项符合题意。
2 3
故选AD。
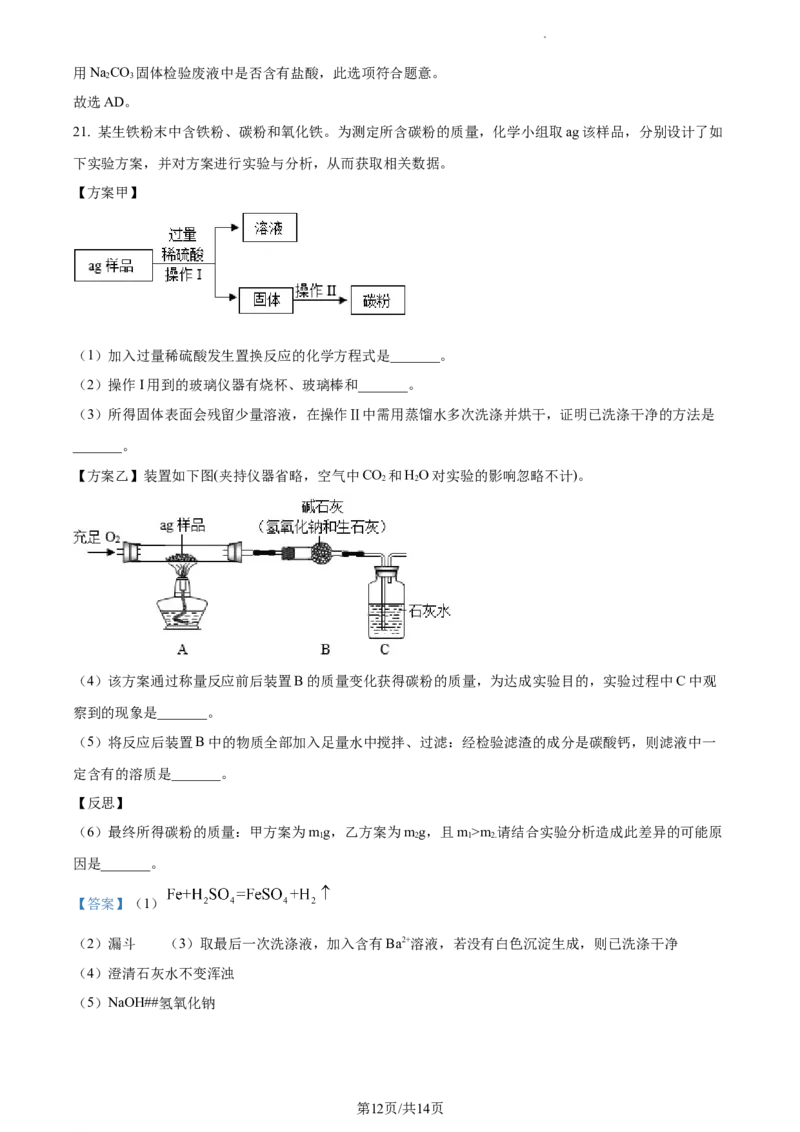
21. 某生铁粉末中含铁粉、碳粉和氧化铁。为测定所含碳粉的质量,化学小组取ag该样品,分别设计了如
下实验方案,并对方案进行实验与分析,从而获取相关数据。
【方案甲】
(1)加入过量稀硫酸发生置换反应的化学方程式是_______。
(2)操作I用到的玻璃仪器有烧杯、玻璃棒和_______。
(3)所得固体表面会残留少量溶液,在操作Ⅱ中需用蒸馏水多次洗涤并烘干,证明已洗涤干净的方法是
_______。
【方案乙】装置如下图(夹持仪器省略,空气中CO 和HO对实验的影响忽略不计)。
2 2
(4)该方案通过称量反应前后装置B的质量变化获得碳粉的质量,为达成实验目的,实验过程中C中观
察到的现象是_______。
(5)将反应后装置B中的物质全部加入足量水中搅拌、过滤:经检验滤渣的成分是碳酸钙,则滤液中一
定含有的溶质是_______。
【反思】
(6)最终所得碳粉的质量:甲方案为mg,乙方案为mg,且m>m 请结合实验分析造成此差异的可能原
1 2 1 2.
因是_______。
【答案】(1)
(2)漏斗 (3)取最后一次洗涤液,加入含有Ba2+溶液,若没有白色沉淀生成,则已洗涤干净
(4)澄清石灰水不变浑浊
(5)NaOH##氢氧化钠
第12页/共14页
学科网(北京)股份有限公司(6)方案乙里A中生成的CO 没有全部进入装置B中吸收
2
【解析】
【小问1详解】
由题干可知,某生铁粉末中含铁粉、碳粉和氧化铁,加入稀硫酸后,碳粉不与硫酸反应,氧化铁与硫酸反
应,发生的是复分解反应,只有铁与硫酸反应发生的是置换反应,生成硫酸亚铁和氢气,化学方程式为:
,故填写: 。
【小问2详解】
操作I将固体和溶液分离,所以,操作为过滤,需要的玻璃仪器有烧杯、玻璃棒和漏斗,故填写:漏斗。
【小问3详解】
ag样品中加入过量的稀硫酸,所以,固体表面残留少量溶液中含有硫酸,铁与硫酸反应生成了硫酸亚铁,
因此,残留溶液中还会有硫酸亚铁,硫酸和硫酸亚铁中都含有 ,所以,检验固体表面是否洗涤干净,
就是检验固体表面是否含有 ,检验硫酸根离子,可以滴加含有钡离子的溶液,因为钡离子与硫酸根离
子结合生成不溶于酸的白色沉淀硫酸钡,因此,证明已洗涤干净的方法是取最后一次洗涤液,加入含有
Ba2+溶液,若没有白色沉淀生成,则已洗涤干净,故填写:取最后一次洗涤液,加入含有Ba2+溶液,若没
有白色沉淀生成,则已洗涤干净。
【小问4详解】
装置B中含有的物质是氢氧化钠和氧化钙,氢氧化钠能吸收二氧化碳生成碳酸钠和水,当二氧化碳全部被
吸收,实验过程中C中观察到的现象是澄清石灰水不变浑浊,故填写:澄清石灰水不变浑浊。
【小问5详解】
因为氢氧化钠能吸收二氧化碳生成碳酸钠和水,水又和氧化钙反应生成氢氧化钙,氢氧化钙与碳酸钠反应
生成碳酸钙和氢氧化钠,氢氧化钠易溶于水,所以,将反应后装置B中的物质全部加入足量水中搅拌、过
滤:经检验滤渣的成分是碳酸钙,则滤液中一定含有的溶质是氢氧化钠(NaOH),故填写:NaOH或氢氧化
钠。
【小问6详解】
甲方案的实验都可以在敞口容器中做,乙方案的A装置必须气密性良好,如果装置气密性不好的话,会导
致进入B装置中的二氧化碳偏少,使方案甲得到的碳粉质量比乙方案多,故填写:方案乙里A中生成的
CO 没有全部进入装置B中吸收。
2
第13页/共14页
学科网(北京)股份有限公司第14页/共14页
学科网(北京)股份有限公司