文档内容
九年级化学练习
(满分50分,考试时间40分钟)
相对原子质量:H-1 C-12 O-16 Ca-40
五、选择题(共20分)
1. 属于物理变化的是
A. 燃气煮饭 B. 水果榨汁 C. 葡萄酿酒 D. 食醋除垢
【答案】B
【解析】
【详解】A、燃气煮饭涉及到天然气的燃烧,天然气燃烧过程中有新物质生成,属于化学变化,不符合题
意;
B、水果榨汁只是物质的形状发生了变化,没有新物质生成,属于物理变化,符合题意;
C、葡萄酿酒过程中有新物质酒精等生成,属于化学变化,不符合题意;
D、食醋除垢过程中有新物质二氧化碳等生成,属于化学变化,不符合题意。
故选B。
2. 元素符号正确的是
A. 钠Ne B. 镁mg C. 氢N D. 银Ag
【答案】D
【解析】
【详解】A、钠的元素符号是Na,氖的元素符号是Ne,故A错误;
B、镁的元素符号是Mg,第一个字母大写,第二个字母小写,故B错误;
C、氢的元素符号是H,故C错误;
D、银的元素符号是Ag,故D正确。
故选D。
3. 属于溶液的是
A. 酸奶 B. 果粒橙 C. 矿泉水 D. 冰水
【答案】C
【解析】
【详解】A、酸奶属于不均一、不稳定的乳浊液,不属于溶液,故A错误;
B、果粒橙属于不均一、不稳定的悬浊液,不属于溶液,故B错误;
C、矿泉水是均一、稳定的混合物,属于溶液,故C正确;
D、冰是固态的水,冰水是由一种物质组成,属于纯净物,不属于溶液,溶液属于混合物,故D错误;
故选:C。
第1页/共15页
学科网(北京)股份有限公司4. 属于结晶水合物的是
A. 胆矾 B. 干冰 C. 食盐 D. 熟石灰
【答案】A
【解析】
【详解】A、胆矾是 ,属于结晶水合物,故A正确;
B、干冰为固体二氧化碳,不属于结晶水合物,故B错误;
C、食盐是氯化钠,不属于结晶水合物,故C错误;
D、熟石灰是氢氧化钙,不属于结晶水合物,故D错误。
故选A。
5. 含有原子团的物质是
A. Cu B. CuO C. CuCl D. CuSO
2 4
【答案】D
【解析】
【详解】A、Cu中只含有铜元素一种元素,不含原子团,故A错误;
B、CuO中只含有铜元素和氧元素,不含原子团,故B错误;
C、CuCl 中只含有铜元素和氯元素,不含原子团,故C错误;
2
D、CuSO 中含有硫酸根,含有原子团,故D正确。
4
故选D。
6. 《本草纲目》中的四种药物,Hg元素化合价最低的是
A. 水银Hg B. 轻粉Hg Cl C. 朱砂HgS D. 升丹HgO
2 2
【答案】A
【解析】
【分析】水银是金属单质汞的俗称,其中汞元素的化合价为零;在Hg Cl 中,氯元素显-1价,根据化合物
2 2
中,正负化合价代数和为零原则,所以汞元素显+1价;在HgS中,硫元素显-2价,根据化合物中,正负
化合价为零原则,所以汞元素显+2价;在HgO中,氧元素显-2价,根据化合物中,正负化合价代数和为
零原则,所以汞元素显+2价;将每个选项中汞元素进行排序,选出化合价最低。
【详解】A.由分析可知,选项A中汞元素的化合价为零,轻粉中汞元素的化合价为+1价,C、D选项中汞
元素的化合价都为+2价,故选项A符合题意;
B.由分析可知,选项B中汞元素的化合价为+1价,汞单质中汞元素的化合价为零,C、D选项中汞元素的
化合价都为+2价,故选项B不符合题意;
C.由分析可知,选项C中汞元素的化合价为+2价,汞单质中汞元素的化合价为零,轻粉中汞元素的化合价
为+1价,D选项中汞元素的化合价都为+2价,故选项C不符合题意;
第2页/共15页
学科网(北京)股份有限公司D.由分析可知,选项D中汞元素的化合价为+2价,汞单质中汞元素的化合价为零,轻粉中汞元素的化合价
为+1价,C选项中汞元素的化合价都为+2价,故选项D不符合题意,故选A。
7. 互为同素异形体的是
A. 氧气和液氧 B. 石墨和金刚石 C. 水和过氧化氢 D. 水银和银
【答案】B
【解析】
【分析】同素异形体指的是:由同种元素组成的不同种单质互为同素异形体。
【详解】A、氧气和液氧属于同一种物质、只是状态不同、故A选项不符合题意;
B、金刚石和石墨都是由碳元素组成的不同的单质、故B选项符合题意;
C、水和过氧化氢是由同种元素组成的两种化合物、不是单质、故C选项不符合题意;
D、水银是汞元素组成、银是银元素组成的、故D选项不符合体音;
故选:B。
8. 能在氧气中燃烧并产生黑色固体的是
A. 碳 B. 镁 C. 铁 D. 硫
【答案】C
【解析】
【详解】A、碳在氧气中燃烧生成二氧化碳气体,没有生成黑色固体,错误;
B、镁在氧气中燃烧生成白色固体氧化镁,没有生成黑色固体,错误;
C、铁在氧气中燃烧生成了黑色固体四氧化三铁,正确;
D、硫在氧气中燃烧生成二氧化硫气体,没有生成黑色固体,错误。
故选C。
9. 从微观角度解释被动吸烟的原因是
A. 分子很小 B. 分子间有间隔 C. 分子不断运动 D. 分子可分
【答案】C
【解析】
【详解】A、分子很小与被动吸烟无关,故A错误;
B、分子间有间隔与被动吸烟无关,故B错误;
C、分子不断运动,有害分子不断扩散,使人被动吸烟,故C正确;
D、分子可分与被动吸烟无关,故D错误;
故选C。
10. 氢元素以游离态存在的物质是
A. NH B. HO C. HCO D. H
2 4 2 2 2 3 2
【答案】D
第3页/共15页
学科网(北京)股份有限公司【解析】
【详解】A、NH 是一种有机物,属于化合物,其中氢元素以化合态存在,选项错误;
2 4
B、HO 是一种氧化物,属于化合物,其中氢元素以化合态存在,选项错误;
2 2
C、HCO 是一种酸,属于化合物,其中氢元素以化合态存在,选项错误;
2 3
D、H 是一种单质,其中氢元素以游离态存在,选项正确;
2
故选D。
11. 使燃料充分燃烧,不合理的是
A. 粉碎燃料 B. 增加燃料 C. 增加空气 D. 喷成雾状
【答案】B
【解析】
【详解】A、粉碎燃料能够增大燃料与氧气的接触面积,使燃料充分燃烧,选项正确;
B、增加燃料会导致氧气不足,不能使燃料充分燃烧,选项错误;
C、增加空气能够增大氧气的含量,使燃料充分燃烧,选项正确;
D、喷成雾状能够增大燃料与氧气的接触面积,使燃料充分燃烧,选项正确,故选B。
12. 物质的用途主要利用其化学性质的是
A. 碳素墨水书写文件档案 B. 稀有气体作电光源
C. 金刚石切割玻璃 D. 分离液态空气制氧气
【答案】A
【解析】
【详解】A、碳素墨水书写文件档案是因为常温下,碳的化学性质稳定,故A正确;
B、稀有气体作电光源是因为稀有气体通电发出不同颜色的光,不需要通过化学变化就能体现出来,属于
物理性质,故B错误;
C、金刚石切割玻璃是因为金刚石的硬度大,不需要通过化学变化就能体现出来,属于物理性质,故C错
误;
D、分离液态空气制氧气是利用各成分沸点不同分离,不需要通过化学变化就能体现出来,属于物理性质,
故D错误。
故选A。
13. 能达到实验目的的是
A. 燃着木条鉴别N 和CO B. 酚酞试液鉴别石灰水和食盐水
2 2
C. 高温灼烧除去炭粉中少量的氧化铜 D. 溶解过滤除去CaO中少量的CaCO
3
【答案】B
【解析】
【详解】A、氮气与二氧化碳都不燃烧也不支持燃烧,燃着的木条伸进气体中都会熄灭,即燃着木条不能
第4页/共15页
学科网(北京)股份有限公司鉴别N 和CO,选项错误;
2 2
B、石灰水呈碱性 ,能够使酚酞试液变红,食盐水呈中性,不能使酚酞试液变红,即酚酞试液能够鉴别石
灰水和食盐水,选项正确;
C、高温灼烧时,炭粉与空气中的氧气反应生成二氧化碳,会将欲保留的物质反应掉,不符合除杂原则,
选项错误;
D、溶解时,CaO与水反应生成氢氧化钙,会将欲保留的物质反应掉,不符合除杂原则,选项错误,故选
B。
14. 比较1g氢气和1g氧气,说法正确的是
A. 分子数相同 B. 物质的量相同
C. 氢原子数>氧原子数 D. 氧元素质量>氢元素质量
【答案】C
【解析】
【详解】A、1g氢气和1g氧气的物质的量分别为: , ;根据
N=nN 可知,两种气体的分子数不相同,故错误;
A
B、由A可知,1g氢气和1g氧气的物质的量不相同,故错误;
C、1g氢气的物质的量为 =0.5mol,含有氢原子个数为N=0.5N ;1g氧气的物质的量为
A
,含有氧原子个数为 ;因此氢原子数>氧原子数,故正确;
D、1g氢气的物质的量为 ,含有氢元素的质量m=0.5mol×2g/mol=1g;1g氧气的物质的
量为 ,含有氧元素质量m= ;所以氧元素质量=氢元素质量,
故错误;
故选:C。
(35~37每题均有1~2个正确选项)
15. 配制50.0g溶质质量分数为10%的氯化钠溶液,说法错误的是
A. 用电子天平称取5.0g氯化钠
第5页/共15页
学科网(北京)股份有限公司B. 用50mL量筒量取所需的水
C. 溶解时用玻璃棒搅拌,可增大溶解度
D. 装瓶时有少量液体洒出,溶质的质量分数不变
【答案】C
【解析】
【详解】A、配制50g溶质质量分数为10%的氯化钠溶液,氯化钠的质量=50g×10%=5.0g,电子天平可以
称量,A正确;
B、需要水的质量为50g-5g=45g,既45mL,可以用50mL水量取,A正确;
C、溶解时用玻璃棒搅拌,能加快溶解速率,不能增大溶解度,C错误;
D、溶液具有均一性,洒出液体后溶质质量分数不变,D正确。
故选:C。
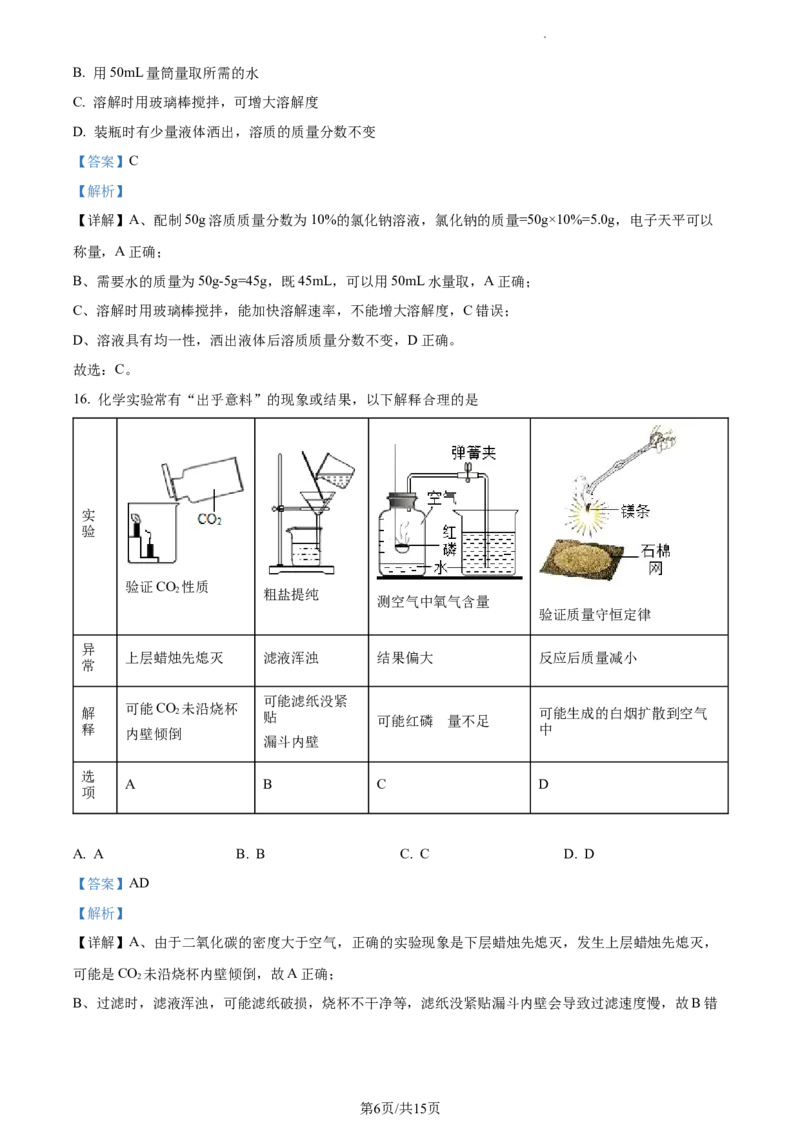
16. 化学实验常有“出乎意料”的现象或结果,以下解释合理的是
实
验
验证CO 性质
2 粗盐提纯
测空气中氧气含量
验证质量守恒定律
异
上层蜡烛先熄灭 滤液浑浊 结果偏大 反应后质量减小
常
可能滤纸没紧
可能CO 未沿烧杯
解 2 贴 可能红磷 的量不足 可能生成的白烟扩散到空气
释 中
内壁倾倒
漏斗内壁
选
A B C D
项
A. A B. B C. C D. D
【答案】AD
【解析】
【详解】A、由于二氧化碳的密度大于空气,正确的实验现象是下层蜡烛先熄灭,发生上层蜡烛先熄灭,
可能是CO 未沿烧杯内壁倾倒,故A正确;
2
B、过滤时,滤液浑浊,可能滤纸破损,烧杯不干净等,滤纸没紧贴漏斗内壁会导致过滤速度慢,故B错
第6页/共15页
学科网(北京)股份有限公司误;
C、测空气中氧气含量,红磷的量不足不能将氧气完全反应,会造成实验结果偏小,故C错误;
D、验证质量守恒定律,由于生成的白烟扩散到空气中,造成反应后质量减小,故D正确;
故选AD。
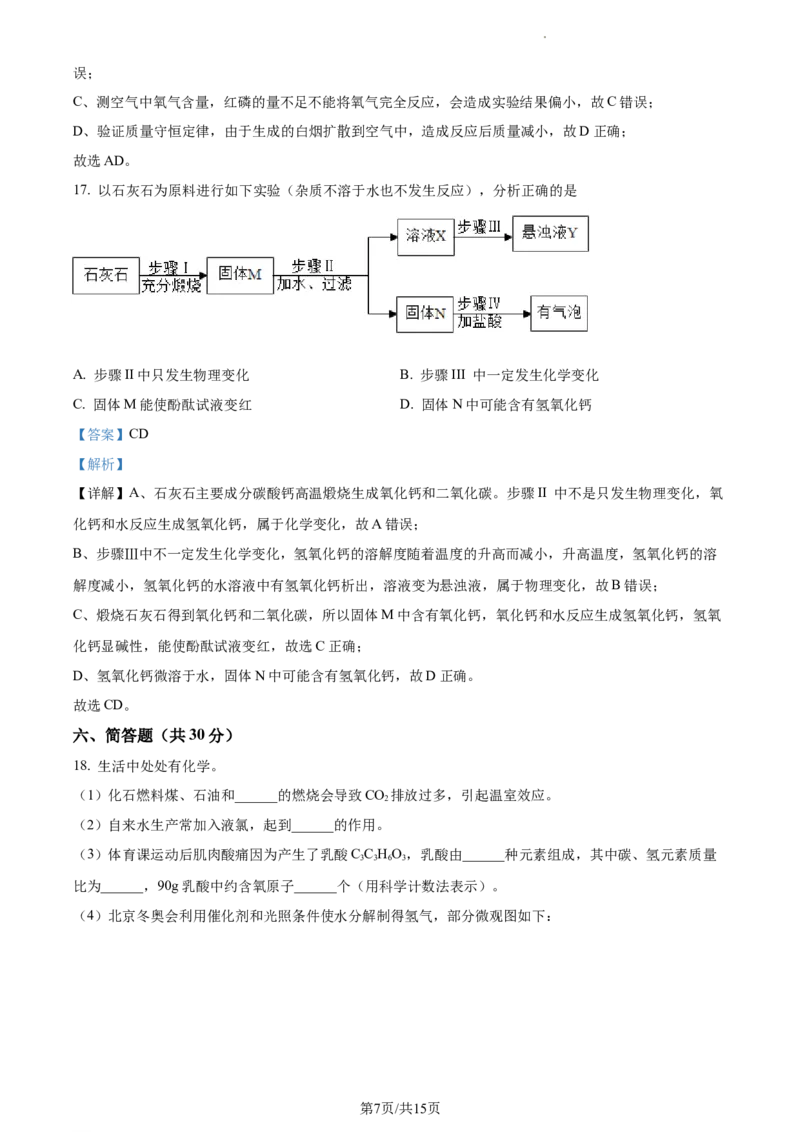
17. 以石灰石为原料进行如下实验(杂质不溶于水也不发生反应),分析正确的是
A. 步骤II中只发生物理变化 B. 步骤III 中一定发生化学变化
C. 固体M能使酚酞试液变红 D. 固体N中可能含有氢氧化钙
【答案】CD
【解析】
【详解】A、石灰石主要成分碳酸钙高温煅烧生成氧化钙和二氧化碳。步骤II 中不是只发生物理变化,氧
化钙和水反应生成氢氧化钙,属于化学变化,故A错误;
B、步骤Ⅲ中不一定发生化学变化,氢氧化钙的溶解度随着温度的升高而减小,升高温度,氢氧化钙的溶
解度减小,氢氧化钙的水溶液中有氢氧化钙析出,溶液变为悬浊液,属于物理变化,故B错误;
C、煅烧石灰石得到氧化钙和二氧化碳,所以固体M中含有氧化钙,氧化钙和水反应生成氢氧化钙,氢氧
化钙显碱性,能使酚酞试液变红,故选C正确;
D、氢氧化钙微溶于水,固体N中可能含有氢氧化钙,故D正确。
故选CD。
六、简答题(共30分)
18. 生活中处处有化学。
(1)化石燃料煤、石油和______的燃烧会导致CO 排放过多,引起温室效应。
2
(2)自来水生产常加入液氯,起到______的作用。
(3)体育课运动后肌肉酸痛因为产生了乳酸C C HO,乳酸由______种元素组成,其中碳、氢元素质量
3 3 6 3
比为______,90g乳酸中约含氧原子______个(用科学计数法表示)。
(4)北京冬奥会利用催化剂和光照条件使水分解制得氢气,部分微观图如下:
第7页/共15页
学科网(北京)股份有限公司反应I的化学方程式______,反应II属于______反应(填基本反应类型)。
【答案】(1)天然气 (2)杀菌消毒
(3) ①. 3 ②. 6:1 ③. 1.806×1024
(4) ①. ②. 分解
【解析】
【小问1详解】
化石燃料煤、石油和天然气的燃烧会导致CO 排放过多,引起温室效应。
2
【小问2详解】
氯气具有消毒杀菌的作用,自来水生产常加入液氯,起到杀灭水中的病菌,从而保证自来水的清洁。
【小问3详解】
乳酸的分子式为C HO,乳酸由碳、氢、氧3种元素组成;其中碳、氢元素质量比为(3×12):(6×1)=6:1;乳
3 6 3
酸的相对分子质量为(3×12)+(6×1)+(3×16) = 90;则乳酸的摩尔质量为90g /mol,由此可知90g乳酸的物
质的量为1mol,氧原子的物质量的量为3mol,则氧原子的个数约为种3×6.02×1023=1.806×1024。
【小问4详解】
根据微观示意图可知,反应Ⅰ为水分解为氢气和过氧化氢,化学方程式为 ;反
应Ⅱ过氧化氢分解为水和氧气,反应物只有一种,生成物有两种,属于分解反应。
19. 水是构成一切生物体的基本成分,是生命之源。
(1)验证水的组成。
第8页/共15页
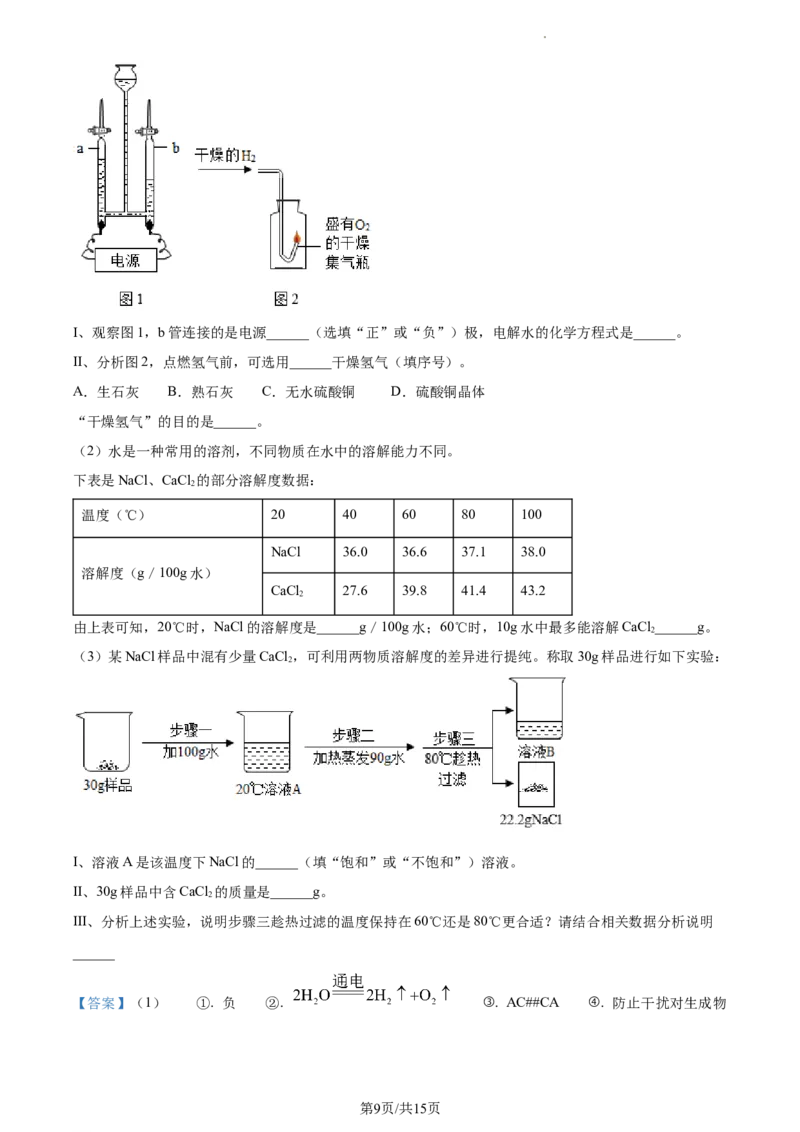
学科网(北京)股份有限公司I、观察图1,b管连接的是电源______(选填“正”或“负”)极,电解水的化学方程式是______。
II、分析图2,点燃氢气前,可选用______干燥氢气(填序号)。
A.生石灰 B.熟石灰 C.无水硫酸铜 D.硫酸铜晶体
“干燥氢气”的目的是______。
(2)水是一种常用的溶剂,不同物质在水中的溶解能力不同。
下表是NaCl、CaCl 的部分溶解度数据:
2
温度(℃) 20 40 60 80 100
NaCl 36.0 36.6 37.1 38.0
溶解度(g/100g水)
CaCl 27.6 39.8 41.4 43.2
2
由上表可知,20℃时,NaCl的溶解度是______g/100g水;60℃时,10g水中最多能溶解CaCl ______g。
2
(3)某NaCl样品中混有少量CaCl ,可利用两物质溶解度的差异进行提纯。称取30g样品进行如下实验:
2
I、溶液A是该温度下NaCl的______(填“饱和”或“不饱和”)溶液。
II、30g样品中含CaCl 的质量是______g。
2
III、分析上述实验,说明步骤三趁热过滤的温度保持在60℃还是80℃更合适?请结合相关数据分析说明
______
【答案】(1) ①. 负 ②. ③. AC##CA ④. 防止干扰对生成物
第9页/共15页
学科网(北京)股份有限公司水的检验
(2) ①. 36.0 ②. 3.98
(3) ①. 不饱和 ②. 4.09 ③. 60℃更合适;因为60℃时过滤,CaCl 不析出,析出NaCl的质
2
量是22.29g,比80℃时析出的NaCl更多(或因为60℃时过滤,CaCl 不析出,析出NaCl的质量比80℃时
2
多0.09g)
【解析】
【分析】b管连接的是电源
【小问1详解】
的
Ⅰ根据“正氧负氢得气体,体积之比1:2”可知b管连接 是电源负极;
电解水的化学方程式是: ;
II、分析图2,点燃氢气前,可选用生石灰(氧化钙的俗称,能和水反应生成氢氧化钙)、无水硫酸铜(无水硫
酸铜能和水反应生成蓝色固体五水硫酸铜)干燥氢气;
“干燥氢气”的目的是除去水蒸气,防止对检验水产生影响;
故答案为: AC;除去水蒸气,防止对检验水产生影响;
【小问2详解】
由如表可知,20°C时,NaCl的溶解度是36.0g/100g水;
60°C时氯化钙的溶解度是39.8g,因此10g水中最多能溶解CaCl 3.98g。
2
故答案为: 36.0;3.98;
【小问3详解】
Ⅰ.20°C时,NaCl的溶解度是36.0g/ 100g水,因为30g<36.0g,所以溶液A是该温度下N aCl的不饱和
溶液;
故答案为:不饱和;
Ⅱ.溶液B是氯化钠的饱和溶液,80° C时,NaCl的溶解度是37.1g/ 100g水,10g水中溶解3.71g氯化钠恰
好饱和,30g样品中氯化钠质量是 ,含CaCl 的质量是 。
2
故答案为: 4.09;
III、60℃更合适;因为60℃时过滤,CaCl 不析出,析出NaCl的质量是22.29g,比80℃时析出的NaCl更
2
多(或因为60℃时过滤,CaCl 不析出,析出NaCl的质量比80℃时多0.09g)。
2
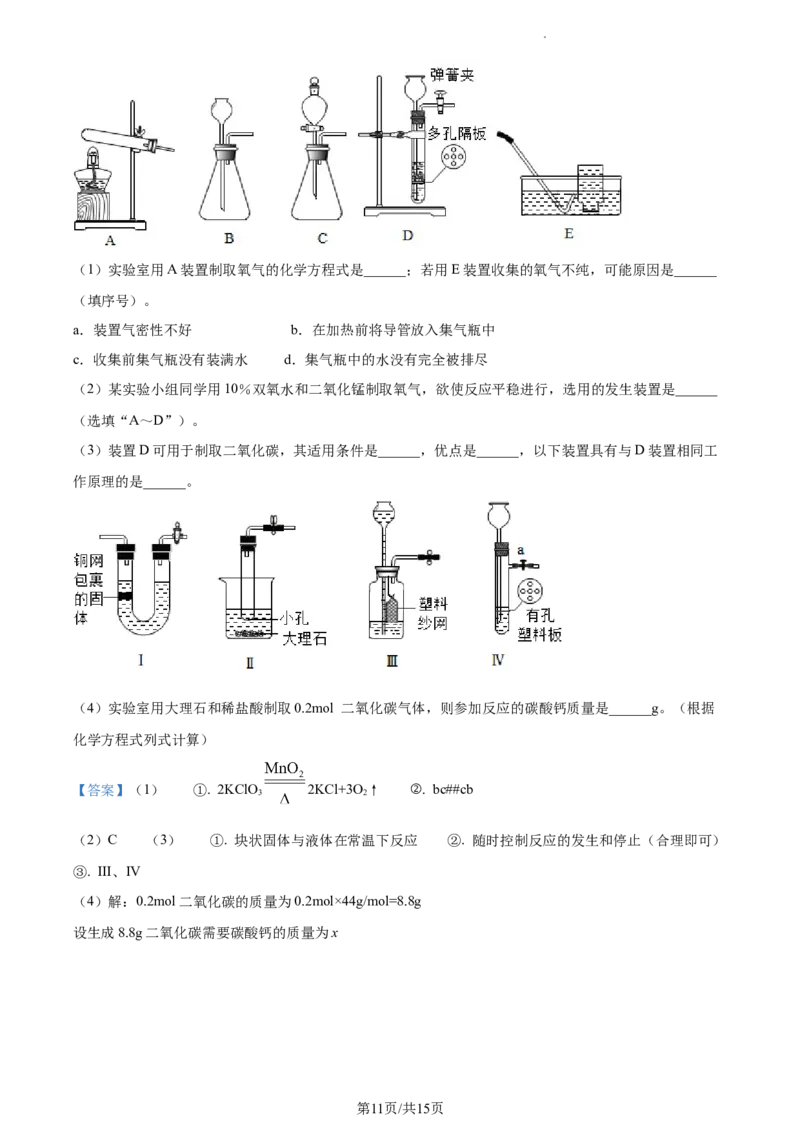
20. 实验室常用下列装置制取气体。
第10页/共15页
学科网(北京)股份有限公司(1)实验室用A装置制取氧气的化学方程式是______;若用E装置收集的氧气不纯,可能原因是______
(填序号)。
a.装置气密性不好 b.在加热前将导管放入集气瓶中
c.收集前集气瓶没有装满水 d.集气瓶中的水没有完全被排尽
(2)某实验小组同学用10%双氧水和二氧化锰制取氧气,欲使反应平稳进行,选用的发生装置是______
(选填“A~D”)。
(3)装置D可用于制取二氧化碳,其适用条件是______,优点是______,以下装置具有与D装置相同工
作原理的是______。
(4)实验室用大理石和稀盐酸制取0.2mol 二氧化碳气体,则参加反应的碳酸钙质量是______g。(根据
化学方程式列式计算)
【答案】(1) ①. 2KClO 2KCl+3O ↑ ②. bc##cb
3 2
(2)C (3) ①. 块状固体与液体在常温下反应 ②. 随时控制反应的发生和停止(合理即可)
③. III、IV
(4)解:0.2mol二氧化碳的质量为0.2mol×44g/mol=8.8g
设生成8.8g二氧化碳需要碳酸钙的质量为x
第11页/共15页
学科网(北京)股份有限公司答:参加反应的碳酸钙质量是20g。
【解析】
【
小问1详解】
A是固体加热型装置,试管口没有棉花,适用于氯酸钾和二氧化锰混合加热制取氧气,化学方程式为
。
E排水法收集氧气不纯:
a.装置气密性不好会导致收集氧气缓慢或无法收集到氧气,但不会导致收集氧气不纯,错误;
b.在加热前将导管放入集气瓶中,收集到开始装置排出的空气,会导致收集氧气不纯,正确;
c.收集前集气瓶没有装满水,收集的氧气会混入残留的空气,会导致收集氧气不纯,正确;
d.集气瓶中的水没有完全被排尽,会导致集气瓶中有水残留,但不会导致收集氧气不纯,错误;
故选bc。
【小问2详解】
双氧水制氧气使用固液不加热型装置,BCD是该类型装置。B使用长颈漏斗便于添加液体药品。C使用分
液漏斗,可以通过活塞控制液体滴加速度,控制反应速率得到平稳气流。D装置有多孔隔板,可以通过止
水夹的开关控制试管内气压,使药品接触或分离从而控制反应的发生和停止。所以欲使反应平稳进行,选
用的发生装置是C。
【小问3详解】
装置D可用于制取二氧化碳,其适用条件是块状固体与液体在常温下反应,如是粉末状固体会从多孔隔板
漏下,装置的优点是块状固体与液体在常温下反应。
Ⅰ、固体药品和液体药品生成气体直接在左侧排出,无法控制反应的发生和停止。
Ⅱ、大理石直接放入烧杯中,直接和稀盐酸接触无法分离,无法控制反应的发生和停止。
Ⅲ、关闭止水夹,集气瓶中气体无法排出,盐酸被压入长颈漏斗,固液分离反应停止。打开止水夹,盐酸
流入集气瓶中,固液接触反应开始,可以控制反应的发生和停止。
Ⅳ、Ⅳ与给出D装置相同,多孔隔板和有空塑料板作用相同,可以控制反应的发生和停止。
故选Ⅲ、Ⅳ。
第12页/共15页
学科网(北京)股份有限公司【小问4详解】
详见答案。
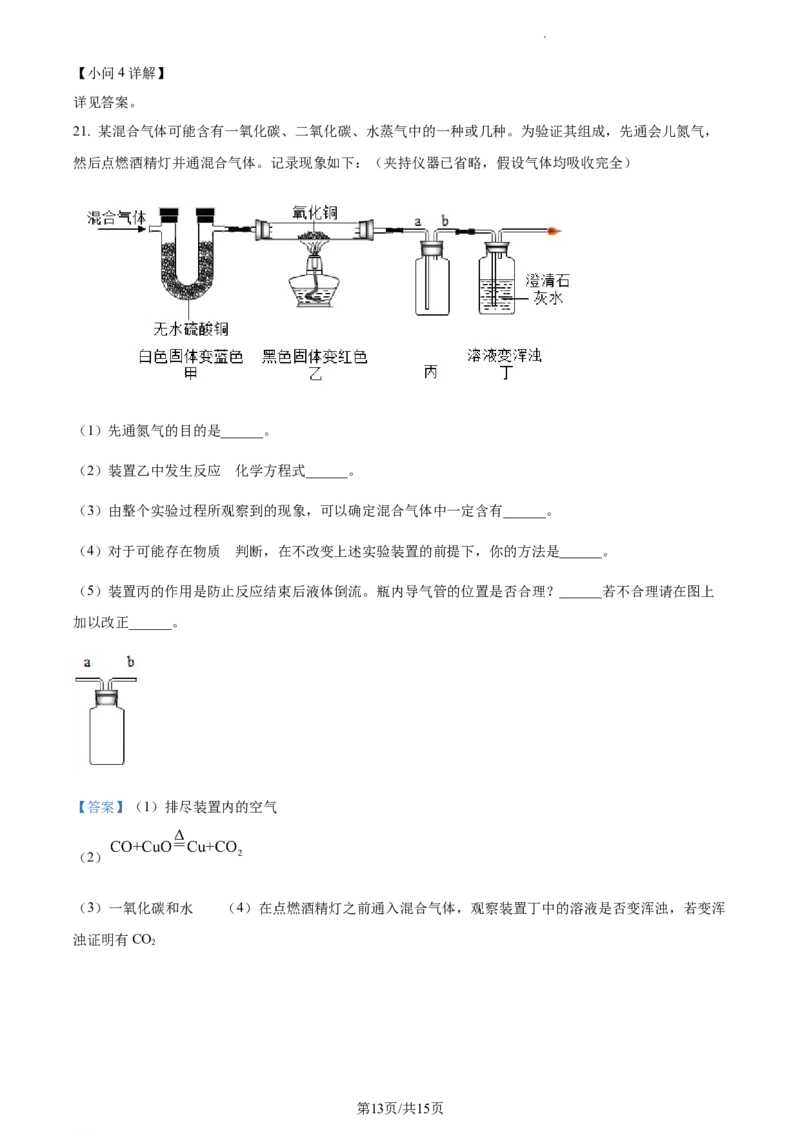
21. 某混合气体可能含有一氧化碳、二氧化碳、水蒸气中的一种或几种。为验证其组成,先通会儿氮气,
然后点燃酒精灯并通混合气体。记录现象如下:(夹持仪器已省略,假设气体均吸收完全)
(1)先通氮气的目的是______。
的
(2)装置乙中发生反应 化学方程式______。
(3)由整个实验过程所观察到的现象,可以确定混合气体中一定含有______。
的
(4)对于可能存在物质 判断,在不改变上述实验装置的前提下,你的方法是______。
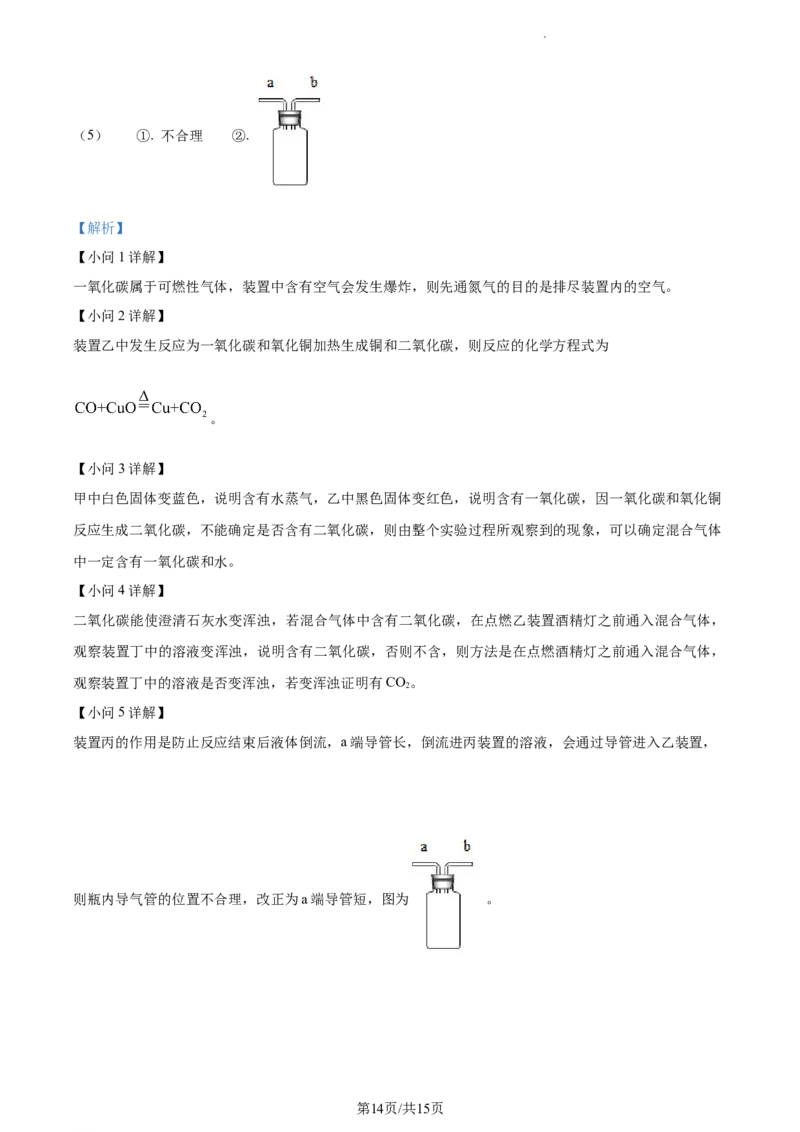
(5)装置丙的作用是防止反应结束后液体倒流。瓶内导气管的位置是否合理?______若不合理请在图上
加以改正______。
【答案】(1)排尽装置内的空气
(2)
(3)一氧化碳和水 (4)在点燃酒精灯之前通入混合气体,观察装置丁中的溶液是否变浑浊,若变浑
浊证明有CO
2
第13页/共15页
学科网(北京)股份有限公司(5) ①. 不合理 ②.
【解析】
【小问1详解】
一氧化碳属于可燃性气体,装置中含有空气会发生爆炸,则先通氮气的目的是排尽装置内的空气。
【小问2详解】
装置乙中发生反应为一氧化碳和氧化铜加热生成铜和二氧化碳,则反应的化学方程式为
。
【小问3详解】
甲中白色固体变蓝色,说明含有水蒸气,乙中黑色固体变红色,说明含有一氧化碳,因一氧化碳和氧化铜
反应生成二氧化碳,不能确定是否含有二氧化碳,则由整个实验过程所观察到的现象,可以确定混合气体
中一定含有一氧化碳和水。
【小问4详解】
二氧化碳能使澄清石灰水变浑浊,若混合气体中含有二氧化碳,在点燃乙装置酒精灯之前通入混合气体,
观察装置丁中的溶液变浑浊,说明含有二氧化碳,否则不含,则方法是在点燃酒精灯之前通入混合气体,
观察装置丁中的溶液是否变浑浊,若变浑浊证明有CO。
2
【小问5详解】
装置丙的作用是防止反应结束后液体倒流,a端导管长,倒流进丙装置的溶液,会通过导管进入乙装置,
则瓶内导气管的位置不合理,改正为a端导管短,图为 。
第14页/共15页
学科网(北京)股份有限公司第15页/共15页
学科网(北京)股份有限公司