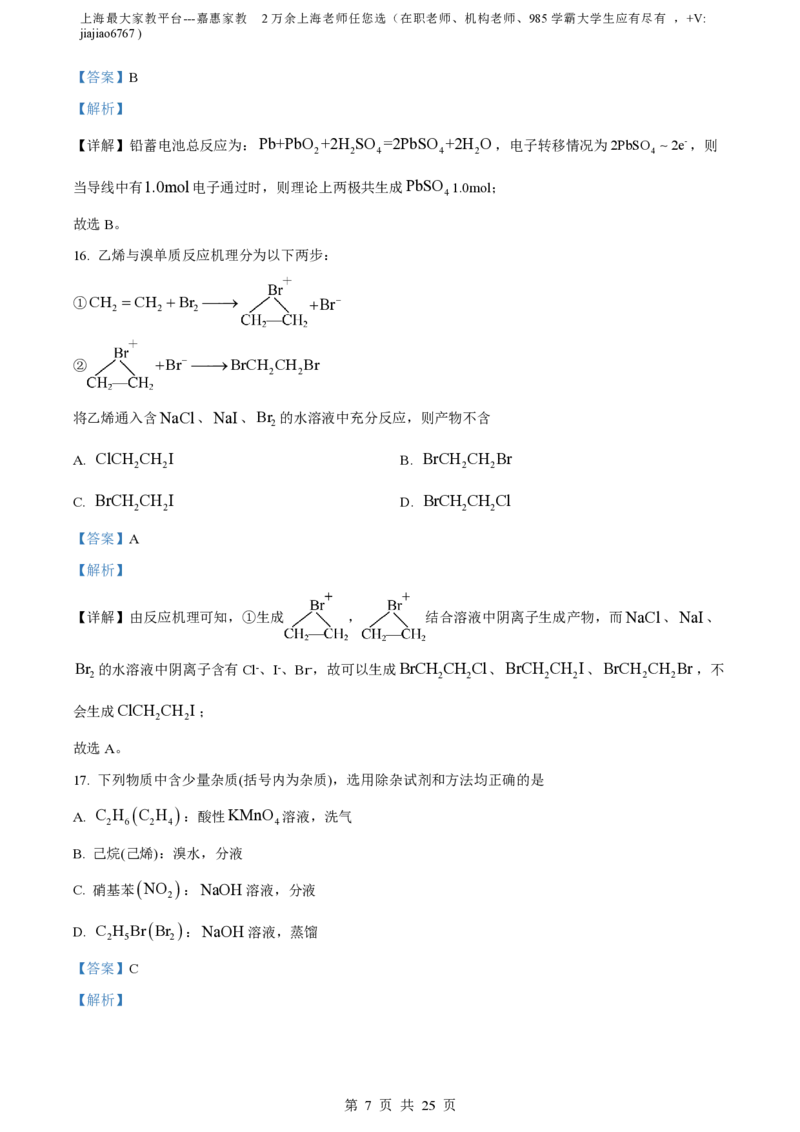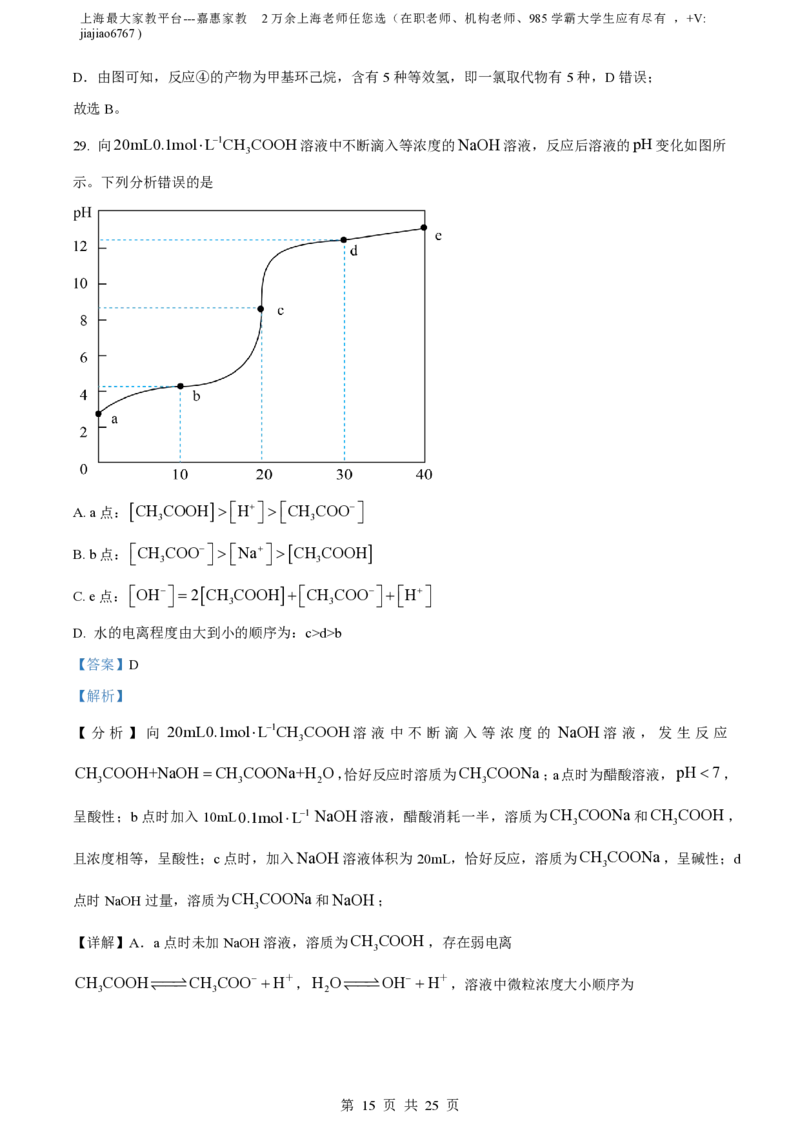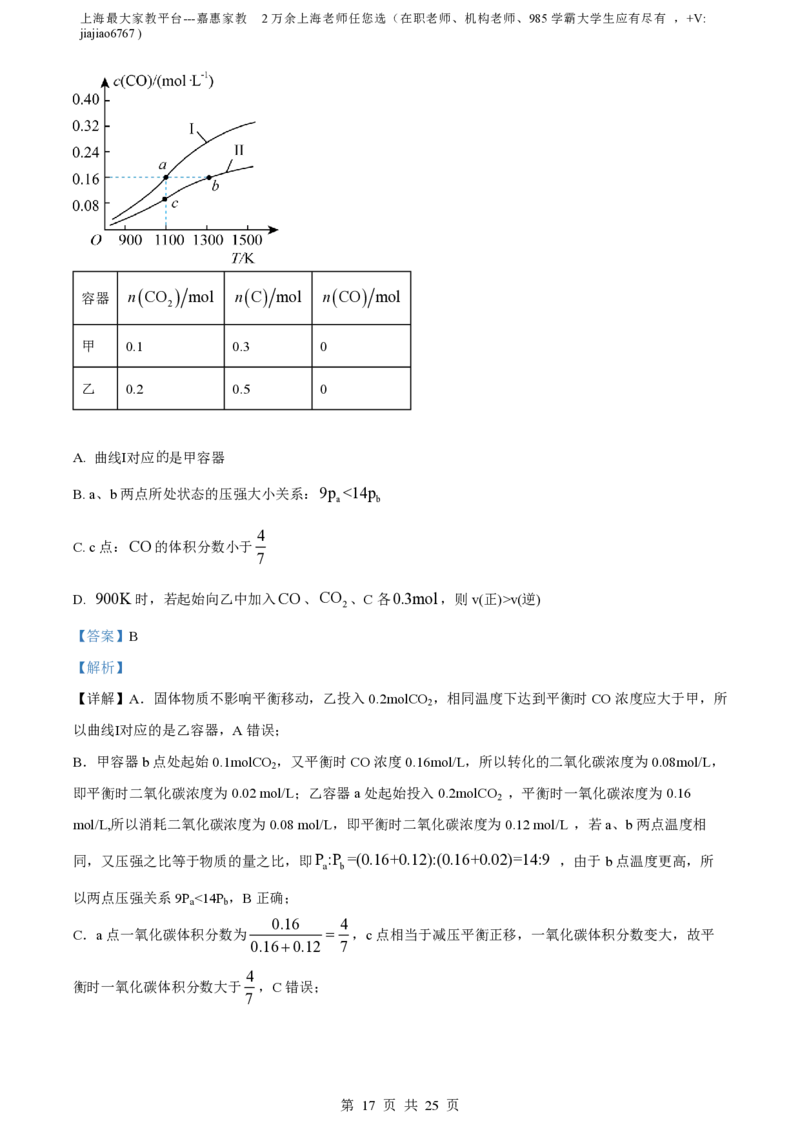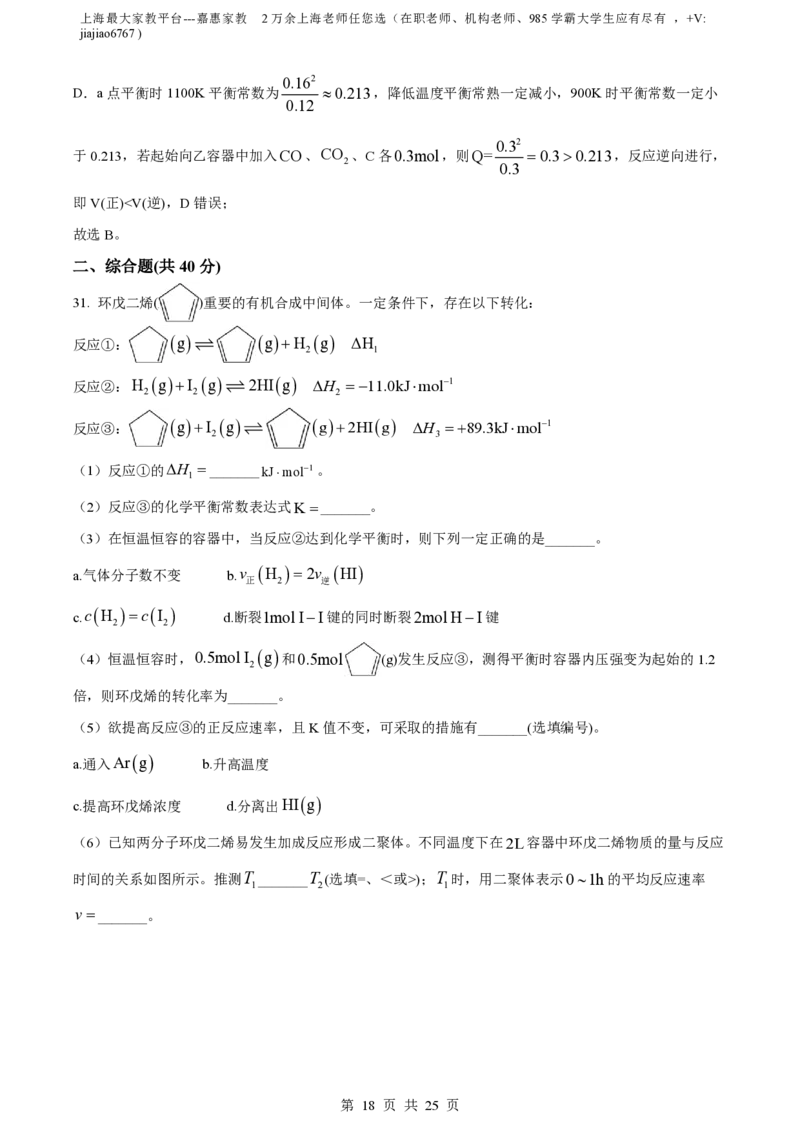文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
上海市七宝中学 2022 学年第一学期
高二化学期末考试
相对原子质量:H1 C12
一、选择题(共 60分,每题只有一个正确答案)
1. 苏轼的《格物粗谈》中记有:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味”。推测文中
的“气”是指
A. 甲烷 B. 乙烯 C. 乙炔 D. 苯
【答案】B
【解析】
【详解】篮中的木瓜释放出气体,与红柿接触后,未熟的红柿成熟,不再有涩味,说明木瓜产生的气体促
进了红柿的成熟,是果实的催熟剂,所以此气体应为乙烯;
答案选B。
2. 酸碱中和滴定是用来测定
A. 溶液酸碱性 B. 溶液pH C. 酸或碱的浓度 D. 电解质电离程度
【答案】C
【解析】
【详解】酸碱中和滴定是用已知浓度的标准液,滴定未知浓度、已知体积的待测液,通过实验现象判断滴
定终点,确定标准的体积,根据c(待测)V(待测)=c(标准)V(标准),计算待测液的浓度,答案
为C。
3. 下列煤化工过程属于物理变化的是
A. 煤的干馏 B. 煤的液化 C. 煤的气化 D. 煤焦油制苯
【答案】D
【解析】
【详解】A.煤的干馏属于化学变化,A错误;
B.煤的液化属于化学变化,B错误;
C.煤的气化属于化学变化,C错误;
D.煤焦油含有苯等,蒸馏可获得苯,属于物理变化,D正确;
故选D。
4. 石油化工在国民经济中占有极其重要的地位。下列关于石油化工说法正确的是
A. 石油分馏塔的顶部获得重馏分
第 1 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
B. 石油分馏时获得各种馏分均为纯净物
C. 石油裂化主要是为提高轻质液体燃料的产量
D. 石油裂解的原理是将长链烃断裂成短链的烷烃
【答案】C
【解析】
【详解】A.石油分馏塔的顶部获得石油气,选项A错误;
B.石油及石油分馏产品均为混合物,不是纯净物,选项B错误;
C.石油裂化的目的是为了提高轻质液体燃料(汽油、煤油、柴油等)的产量,特别是提高汽油的产量,选项
C正确;
D.裂解的目的是为了获得乙烯、丙烯、丁二烯、丁烯、乙炔等,所以石油裂解的主要目的是获得断链不
饱和气态烃,选项D错误;
答案选C。
5. 下列可证明甲烷分子是正四面体结构,而非平面结构的是
A. CH键的键长均相同 B. CH键的键能均相同
C. CH键的键角均相同 D. CH Cl 只有一种结构
2 2
【答案】D
【解析】
【详解】若甲烷分子是正方形的平面结构,其二氯代物CH Cl 有两种结构:相邻或者对角线上的氢被Cl
2 2
取代;若甲烷分子是正四面体结构,则其二氯代物CH Cl 只有一种结构;无论甲烷分子是正方形的平面
2 2
结构还是正四面体结构,其C−H 键的键长、键能、键角均相同;由此可知,选项D符合题意,故选D。
6. 硫酸铵溶液中,离子浓度最大的是
A. NH B. SO2 C. H D. OH
4 4
【答案】A
【解析】
【详解】硫酸铵溶液中溶质为 NH SO ,铵根离子水解,但水解的程度总是很弱的,离子浓度最大的
4 2 4
是NH,故选A。
4
7. 下列过程或现象与盐类水解无关的是
A. 钢铁在潮湿的环境下易生锈 B. 氯化铵溶液加入镁粉有气泡产生
C. 加热氯化铁溶液颜色变深 D. 硫化钠浓溶液有臭味
第 2 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【答案】A
【解析】
【详解】A.钢铁在潮湿的环境下生锈,发生电化学腐蚀,与盐类的水解无关,A符合题意;
B.氯化铵溶液因水解呈酸性,当加入镁粉,与溶液中的氢离子反应生成氢气,与水解有关,B不符合题
意;
C.氯化铁溶液呈黄色,铁离子水解为吸热反应,加热会促进水解生成红褐色氢氧化铁,颜色加深,与水
解有关,C不符合题意;
D.硫化钠溶液中硫离子分步水解生成少量硫化氢气体,硫化氢具有臭味,和水解有关,D不符合题意;
故选A。
8. 下列关于溴乙烷的说法正确的是
A. 电子式为 B. 密度比水小
C. 发生取代反应时CBr键一定会断裂 D. 发生消去反应时CBr键一定会断裂
【答案】D
【解析】
【详解】A.电子式为 ,A错误;
B.溴乙烷密度比水大,B错误;
C.发生取代反应时可能CH断裂,C错误;
D.发生消去反应生成乙烯时CBr键一定会断裂,D正确;
故选D。
9. 加热纯水时,下列叙述正确的是
A. pH变小、呈酸性 B. pH不变、呈中性
C. K 变大、呈中性 D. K 变小、呈碱性
w w
【答案】C
【解析】
【详解】A.加热纯水时,水的电离程度变大,但是氢离子浓度等于氢氧根离子浓度,为中性,A错误;
B.水的电离程度变大,氢离子浓度变大,pH减小,B错误;
C.水的电离程度变大,氢离子、氢氧根离子浓度变大,则K 变大,为中性,C正确;
w
第 3 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
D.由C分析可知,D错误;
故选C。
10. 下列分子式一定表示纯净物的是
A. C H B. C H C. C H Cl D. C H O
3 6 3 8 3 7 3 8
【答案】B
【解析】
【详解】A.C H 可能为丙烯,也可能为环丙烷,A不符合题意;
3 6
B.C H 只能为丙烷,一定表示纯净物,B符合题意;
3 8
C.C H Cl可以表示CH CH CH Cl,也可以表示(CH ) CHCl,C不符合题意;
3 7 3 2 2 3 2
D.C H O可能为醇也可能为醚,D不符合题意;
3 8
故选B。
11. 异辛烷( )含量是汽油抗爆性能的重要指标,下列关于异辛烷说法正确的
是
A. 系统名称为2,4,4-三甲基戊烷 B. 一氯代物有5种
C. 可由2种烯烃催化加氢制取 D. 可由2种炔烃催化加氢制取
【答案】C
【解析】
【详解】A.系统名称应为2,2,4-三甲基戊烷,A错误;
B. 存在4种氢原子,故一氯代物有4种,B错误;
C.可由 加氢获得,C正确;
D.不可由炔烃催化加氢制取,D错误;
故选C。
第 4 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
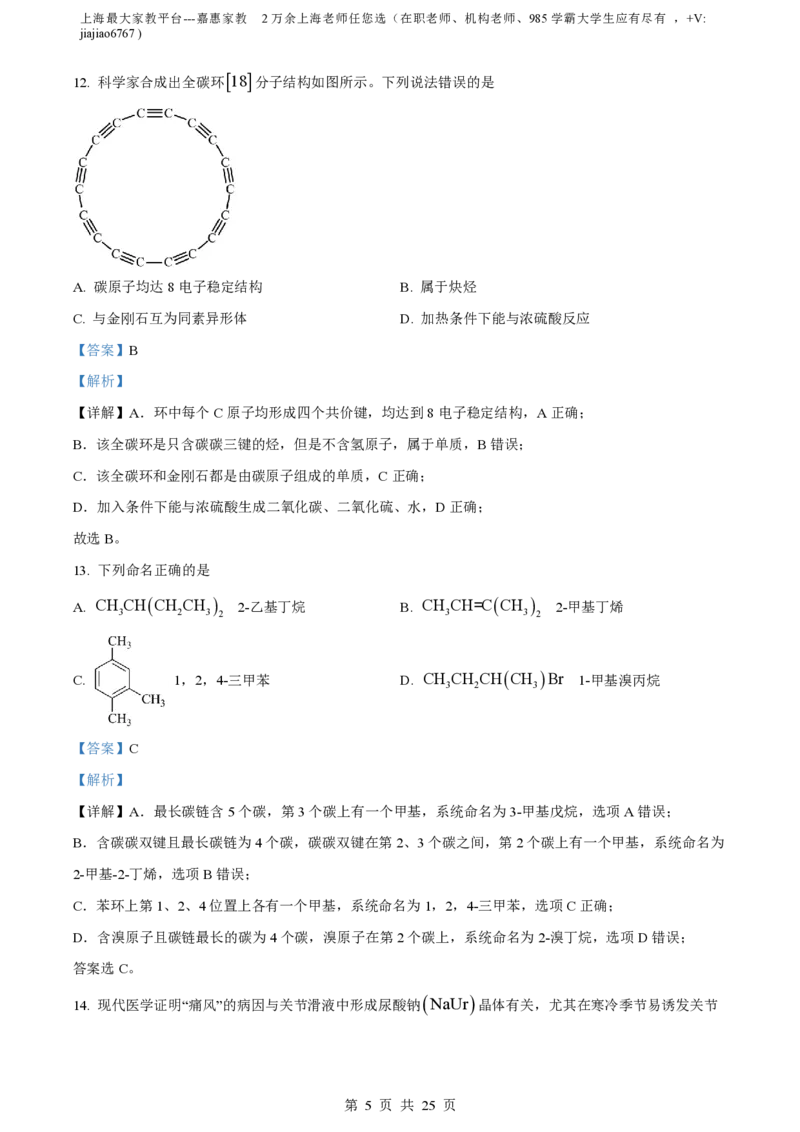
12. 科学家合成出全碳环
18
分子结构如图所示。下列说法错误的是
A. 碳原子均达8电子稳定结构 B. 属于炔烃
C. 与金刚石互为同素异形体 D. 加热条件下能与浓硫酸反应
【答案】B
【解析】
【详解】A.环中每个C原子均形成四个共价键,均达到8电子稳定结构,A正确;
B.该全碳环是只含碳碳三键的烃,但是不含氢原子,属于单质,B错误;
C.该全碳环和金刚石都是由碳原子组成的单质,C正确;
D.加入条件下能与浓硫酸生成二氧化碳、二氧化硫、水,D正确;
故选B。
13. 下列命名正确的是
A. CH CHCH CH 2-乙基丁烷 B. CH CH=CCH 2-甲基丁烯
3 2 3 2 3 3 2
C. 1,2,4-三甲苯 D. CH CH CHCH Br 1-甲基溴丙烷
3 2 3
【答案】C
【解析】
【详解】A.最长碳链含5个碳,第3个碳上有一个甲基,系统命名为3-甲基戊烷,选项A错误;
B.含碳碳双键且最长碳链为4个碳,碳碳双键在第2、3个碳之间,第2个碳上有一个甲基,系统命名为
2-甲基-2-丁烯,选项B错误;
C.苯环上第1、2、4位置上各有一个甲基,系统命名为1,2,4-三甲苯,选项C正确;
D.含溴原子且碳链最长的碳为4个碳,溴原子在第2个碳上,系统命名为2-溴丁烷,选项D错误;
答案选C。
14. 现代医学证明“痛风”的病因与关节滑液中形成尿酸钠
NaUr
晶体有关,尤其在寒冷季节易诱发关节
第 5 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
疼痛。主要原理为:
①HUr(尿酸)H
2
O
Ur(尿酸离子)H
3
O
②UraqNaaq
NaUrs
下列叙述错误的是
A. ①是尿酸的电离方程式
B. 反应②的H 0,因此热敷能减轻关节疼痛
C. 饮食中摄入过多食盐,容易诱发痛风
D. “痛风”患者应控制摄入产生较多尿酸的食物
【答案】B
【解析】
【详解】A.尿酸为弱酸,存在电离平衡,则HUr(尿酸)H
2
O
Ur(尿酸离子)H
3
O为尿酸的电离方
程式,选项A正确;
B.寒冷的季节诱发关节疼痛,说明反应②的ΔH<0,选项B错误;
C.饮食中摄入过多食盐,会增大Na+的浓度,使得平衡正向移动,人体中NaUr含量增多,病情加重,选
项C正确;
D.若患痛风病的人应多吃能代谢产生更多尿酸的食物,会增大尿酸的浓度,使得平衡正向移动,人体中
NaUr含量增多,病情加重,故患痛风病的人应控制摄入产生较多尿酸的食物,选项D正确;
答案选B。
15. 铅蓄电池构造如图所示,放电时正极和负极均会生成PbSO 。当导线中有1.0mol电子通过时,则理
4
论上两极共生成PbSO
4
A. 0.5mol B. 1.0mol C. 1.5mol D. 2.0mol
第 6 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【答案】B
【解析】
【详解】铅蓄电池总反应为:Pb+PbO +2H SO =2PbSO +2H O,电子转移情况为2PbSO 2e-,则
2 2 4 4 2 4
当导线中有1.0mol电子通过时,则理论上两极共生成PbSO 1.0mol;
4
故选B。
16. 乙烯与溴单质反应机理分为以下两步:
①CH CH Br Br
2 2 2
② Br BrCH CH Br
2 2
将乙烯通入含NaCl、NaI、Br 的水溶液中充分反应,则产物不含
2
A. ClCH CH I B. BrCH CH Br
2 2 2 2
C. BrCH CH I D. BrCH CH Cl
2 2 2 2
【答案】A
【解析】
【详解】由反应机理可知,①生成 , 结合溶液中阴离子生成产物,而NaCl、NaI、
Br 的水溶液中阴离子含有Cl-、I-、Br-,故可以生成BrCH CH Cl、BrCH CH I、BrCH CH Br,不
2 2 2 2 2 2 2
会生成ClCH CH I;
2 2
故选A。
17. 下列物质中含少量杂质(括号内为杂质),选用除杂试剂和方法均正确的是
A. C H C H :酸性KMnO 溶液,洗气
2 6 2 4 4
B. 己烷(己烯):溴水,分液
C. 硝基苯 NO :NaOH溶液,分液
2
D. C H BrBr :NaOH溶液,蒸馏
2 5 2
【答案】C
【解析】
第 7 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【详解】A.乙烯含有碳碳双键能和酸性高锰酸钾反应生成二氧化碳气体,引入新杂质气体,A错误;
B.己烯和溴加成的生成物和己烷互溶,不能分液分离,B错误;
C.氢氧化钠和二氧化氮反应生成盐溶液,盐溶液与硝基苯互不相溶,可以分液分离,C正确;
D.C H Br和氢氧化钠溶液加热会发生取代反应生成乙醇,D错误;
2 5
故选C。
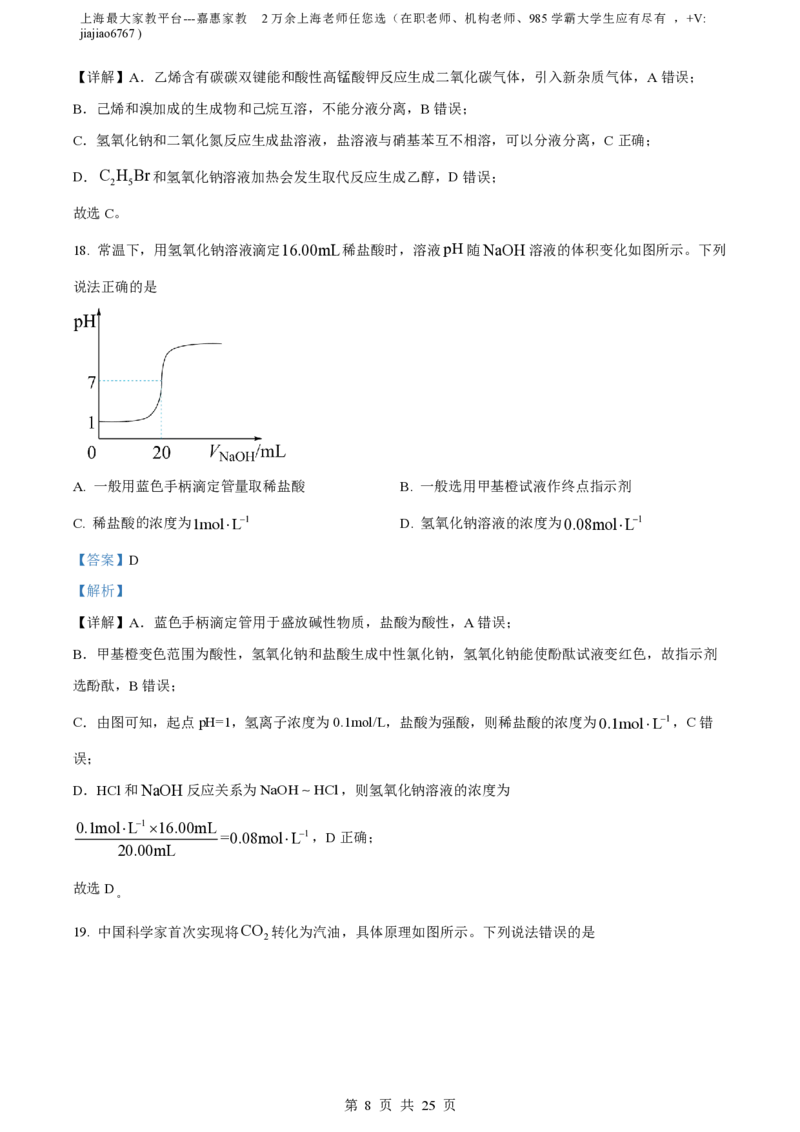
18. 常温下,用氢氧化钠溶液滴定16.00mL稀盐酸时,溶液pH随NaOH溶液的体积变化如图所示。下列
说法正确的是
A. 一般用蓝色手柄滴定管量取稀盐酸 B. 一般选用甲基橙试液作终点指示剂
C. 稀盐酸的浓度为1molL1 D. 氢氧化钠溶液的浓度为0.08molL1
【答案】D
【解析】
【详解】A.蓝色手柄滴定管用于盛放碱性物质,盐酸为酸性,A错误;
B.甲基橙变色范围为酸性,氢氧化钠和盐酸生成中性氯化钠,氢氧化钠能使酚酞试液变红色,故指示剂
选酚酞,B错误;
C.由图可知,起点pH=1,氢离子浓度为0.1mol/L,盐酸为强酸,则稀盐酸的浓度为0.1molL1,C错
误;
D.HCl和NaOH反应关系为NaOH HCl,则氢氧化钠溶液的浓度为
0.1molL116.00mL
=0.08molL1,D正确;
20.00mL
故选D
。
19. 中国科学家首次实现将CO 转化为汽油,具体原理如图所示。下列说法错误的是
2
第 8 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. 该技术有助于实现碳中和 B. a与异戊烷互为同分异构体
C. 反应②形成碳氢键和碳碳键 D. 汽油主要是C C 的烃类混合物
5 12
【答案】B
【解析】
【详解】A.该技术将二氧化碳转化为燃料,能充分利于二氧化碳,利于碳中和,A正确;
B.同分异构体是分子式相同、结构不同的化合物;a与异戊烷是同一种物质,B错误;
C.由图可知,反应②由CO和氢气生成(CH )n,故反应中形成碳氢键和碳碳键,C正确;
2
D.只由碳氢两种元素组成的有机化合物叫作烃;由图可知,生成的汽油主要是C C 的烃类混合物,
5 12
D正确;
故选B。
20. 一种气态烷烃和一种气态单烯烃组成的混合物共10g,混合气体的密度是相同状况下氢气密度的12.5
倍,该混合气体通过溴水时,溴水的质量增加8.4g,则该混合气体可能是( )
A. 甲烷、乙烯 B. 丙烷、乙烯 C. 乙烷、丙烯 D. 甲烷、丙烯
【答案】A
【解析】
【详解】混合气体的平均相对分子质量M 12.5225,由此可确定混合气体中的烷烃必定为CH (相
r 4
对分子质量小于25 的烃类只有甲烷);设单烯烃为C H ,由题意知混合物中该烯烃的质量为 8.4g,则
n 2n
10g
=25g/mol
mCH =10g-8.4g=1.6g,又有 1.6g 8.4g ,解得该烯烃的相对分子质量为28,其为
4 +
16g/mol M C H
n 2n
C H ,故答案为A。
2 4
21. 化工生产中常用MnS作为沉淀剂除去工业废水中的Cu2:
Cu2aqMnSs
CuSsMn2aq
,下列说法正确的是
A. MnS的K 比CuS的K 小
sp sp
第 9 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
B. 该反应达平衡时c
Mn2+
>c
Cu2+
c
Mn2+
c Cu2+ ,B错误;
c(Cu2+) K CuS
sp
c(Mn2+) K MnS
C.该反应的平衡常数K= sp ,C正确;
c(Cu2+) K CuS
sp
D.若平衡后再加入少量CuSO s ,则c Cu2+ 变大,D错误;
4
故选C。
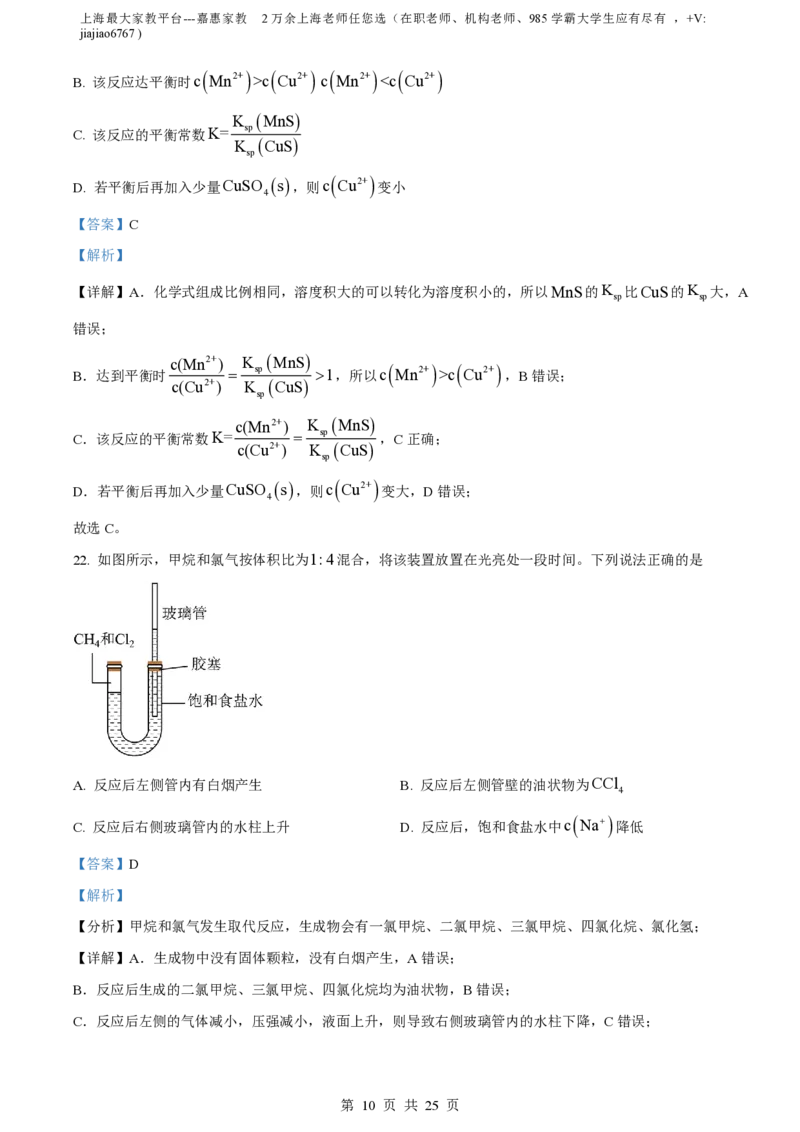
22. 如图所示,甲烷和氯气按体积比为1:4混合,将该装置放置在光亮处一段时间。下列说法正确的是
A. 反应后左侧管内有白烟产生 B. 反应后左侧管壁的油状物为CCl
4
C. 反应后右侧玻璃管内的水柱上升 D. 反应后,饱和食盐水中c
Na
降低
【答案】D
【解析】
【分析】甲烷和氯气发生取代反应,生成物会有一氯甲烷、二氯甲烷、三氯甲烷、四氯化烷、氯化氢;
【详解】A.生成物中没有固体颗粒,没有白烟产生,A错误;
B.反应后生成的二氯甲烷、三氯甲烷、四氯化烷均为油状物,B错误;
C.反应后左侧的气体减小,压强减小,液面上升,则导致右侧玻璃管内的水柱下降,C错误;
第 10 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
D.反应后,溶液中溶解了生成的氯化氢,溶液中氯离子浓度增大,会导致氯化钠溶解度减小而析出,故
饱和食盐水中c
Na
降低,D正确;
故选D。
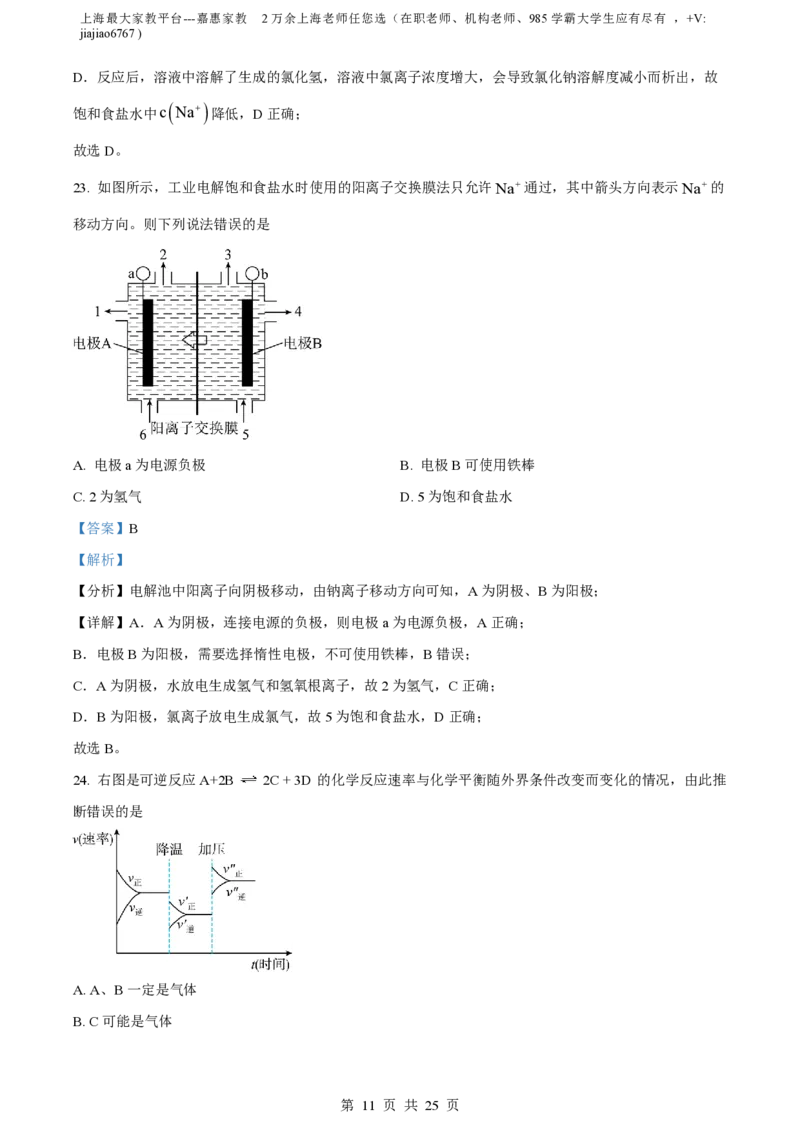
23. 如图所示,工业电解饱和食盐水时使用的阳离子交换膜法只允许Na通过,其中箭头方向表示Na的
移动方向。则下列说法错误的是
A. 电极a为电源负极 B. 电极B可使用铁棒
C. 2为氢气 D. 5为饱和食盐水
【答案】B
【解析】
【分析】电解池中阳离子向阴极移动,由钠离子移动方向可知,A为阴极、B为阳极;
【详解】A.A为阴极,连接电源的负极,则电极a为电源负极,A正确;
B.电极B为阳极,需要选择惰性电极,不可使用铁棒,B错误;
C.A为阴极,水放电生成氢气和氢氧根离子,故2为氢气,C正确;
D.B为阳极,氯离子放电生成氯气,故5为饱和食盐水,D正确;
故选B。
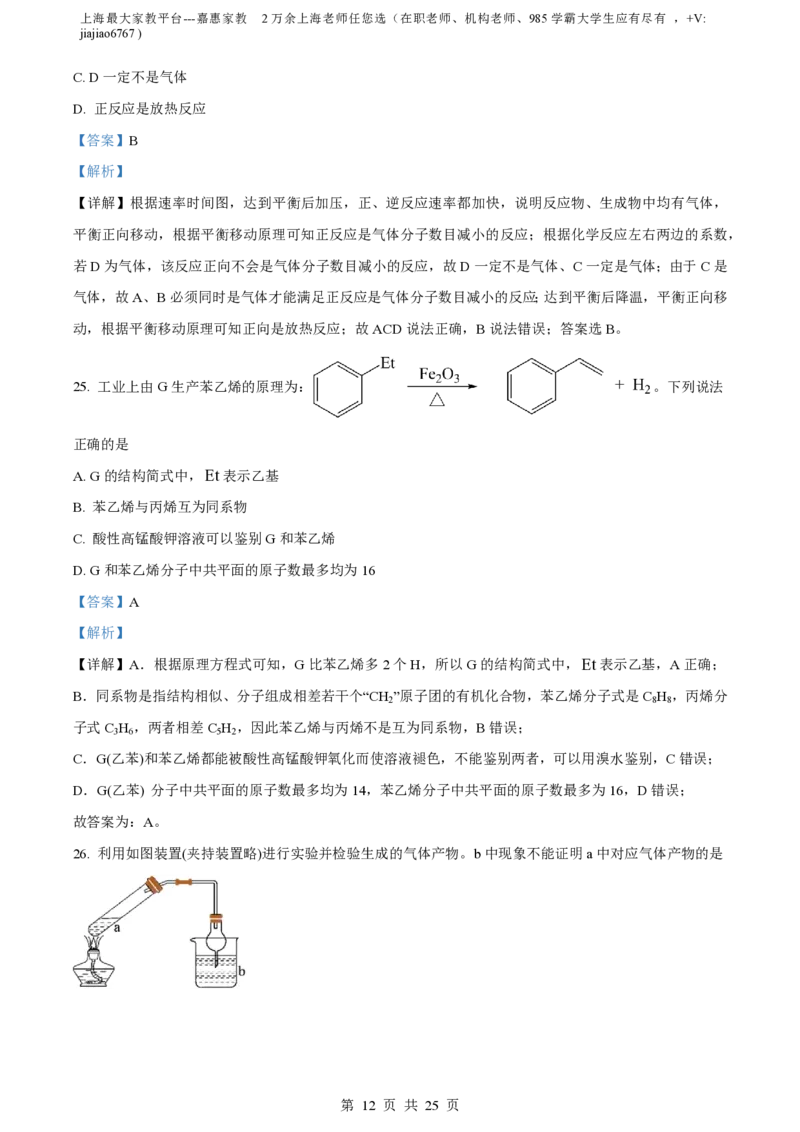
24. 右图是可逆反应A+2B 2C + 3D 的化学反应速率与化学平衡随外界条件改变而变化的情况,由此推
断错误的是
A. A、B一定是气体
B. C可能是气体
第 11 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
C. D一定不是气体
D. 正反应是放热反应
【答案】B
【解析】
【详解】根据速率时间图,达到平衡后加压,正、逆反应速率都加快,说明反应物、生成物中均有气体,
平衡正向移动,根据平衡移动原理可知正反应是气体分子数目减小的反应;根据化学反应左右两边的系数,
若D为气体,该反应正向不会是气体分子数目减小的反应,故D一定不是气体、C一定是气体;由于C是
气体,故A、B必须同时是气体才能满足正反应是气体分子数目减小的反应;达到平衡后降温,平衡正向移
动,根据平衡移动原理可知正向是放热反应;故ACD说法正确,B说法错误;答案选B。
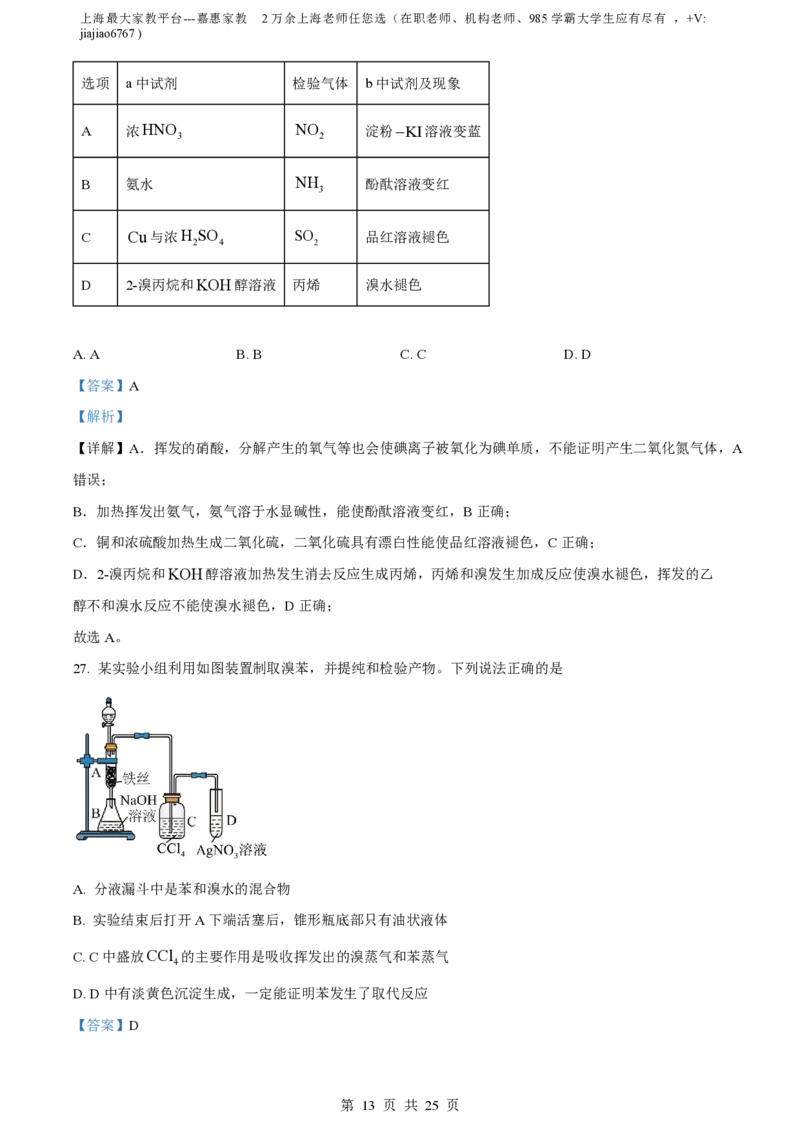
25. 工业上由G生产苯乙烯的原理为: 。下列说法
正确的是
A. G的结构简式中,Et表示乙基
B. 苯乙烯与丙烯互为同系物
C. 酸性高锰酸钾溶液可以鉴别G和苯乙烯
D. G和苯乙烯分子中共平面的原子数最多均为16
【答案】A
【解析】
【详解】A.根据原理方程式可知,G比苯乙烯多2个H,所以G的结构简式中,Et表示乙基,A正确;
B.同系物是指结构相似、分子组成相差若干个“CH ”原子团的有机化合物,苯乙烯分子式是C H ,丙烯分
2 8 8
子式C H ,两者相差C H ,因此苯乙烯与丙烯不是互为同系物,B错误;
3 6 5 2
C.G(乙苯)和苯乙烯都能被酸性高锰酸钾氧化而使溶液褪色,不能鉴别两者,可以用溴水鉴别,C错误;
D.G(乙苯) 分子中共平面的原子数最多均为14,苯乙烯分子中共平面的原子数最多为16,D错误;
故答案为:A。
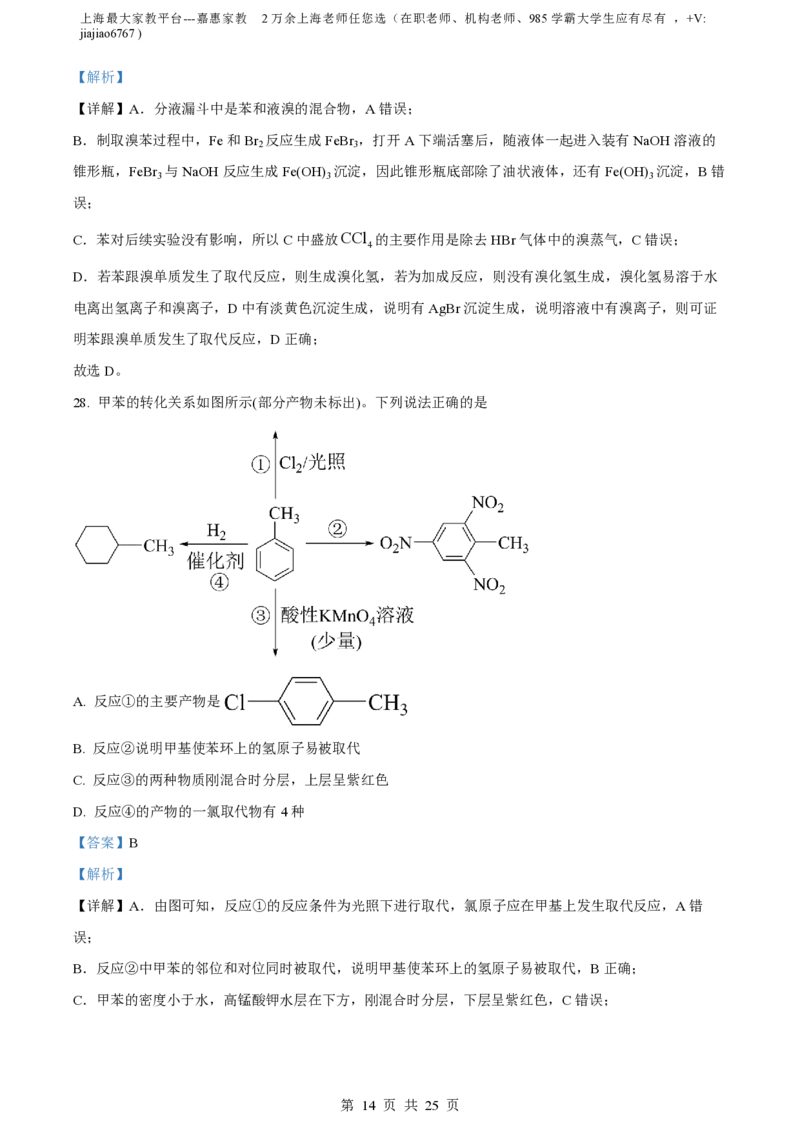
26. 利用如图装置(夹持装置略)进行实验并检验生成的气体产物。b中现象不能证明a中对应气体产物的是
第 12 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
选项 a中试剂 检验气体 b中试剂及现象
A 浓HNO NO 淀粉KI溶液变蓝
3 2
B 氨水 NH 酚酞溶液变红
3
C Cu与浓H SO SO 品红溶液褪色
2 4 2
D 2-溴丙烷和KOH醇溶液 丙烯 溴水褪色
A. A B. B C. C D. D
【答案】A
【解析】
【详解】A.挥发的硝酸,分解产生的氧气等也会使碘离子被氧化为碘单质,不能证明产生二氧化氮气体,A
错误;
B.加热挥发出氨气,氨气溶于水显碱性,能使酚酞溶液变红,B正确;
C.铜和浓硫酸加热生成二氧化硫,二氧化硫具有漂白性能使品红溶液褪色,C正确;
D.2-溴丙烷和KOH醇溶液加热发生消去反应生成丙烯,丙烯和溴发生加成反应使溴水褪色,挥发的乙
醇不和溴水反应不能使溴水褪色,D正确;
故选A。
27. 某实验小组利用如图装置制取溴苯,并提纯和检验产物。下列说法正确的是
A. 分液漏斗中是苯和溴水的混合物
B. 实验结束后打开A下端活塞后,锥形瓶底部只有油状液体
C. C中盛放CCl 的主要作用是吸收挥发出的溴蒸气和苯蒸气
4
D. D中有淡黄色沉淀生成,一定能证明苯发生了取代反应
【答案】D
第 13 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【解析】
【详解】A.分液漏斗中是苯和液溴的混合物,A错误;
B.制取溴苯过程中,Fe和Br 反应生成FeBr ,打开A下端活塞后,随液体一起进入装有NaOH溶液的
2 3
锥形瓶,FeBr 与NaOH反应生成Fe(OH) 沉淀,因此锥形瓶底部除了油状液体,还有Fe(OH) 沉淀,B错
3 3 3
误;
C.苯对后续实验没有影响,所以C中盛放CCl 的主要作用是除去HBr气体中的溴蒸气,C错误;
4
D.若苯跟溴单质发生了取代反应,则生成溴化氢,若为加成反应,则没有溴化氢生成,溴化氢易溶于水
电离出氢离子和溴离子,D中有淡黄色沉淀生成,说明有AgBr沉淀生成,说明溶液中有溴离子,则可证
明苯跟溴单质发生了取代反应,D正确;
故选D。
28. 甲苯的转化关系如图所示(部分产物未标出)。下列说法正确的是
A. 反应①的主要产物是
B. 反应②说明甲基使苯环上的氢原子易被取代
C. 反应③的两种物质刚混合时分层,上层呈紫红色
D. 反应④的产物的一氯取代物有4种
【答案】B
【解析】
【详解】A.由图可知,反应①的反应条件为光照下进行取代,氯原子应在甲基上发生取代反应,A错
误;
B.反应②中甲苯的邻位和对位同时被取代,说明甲基使苯环上的氢原子易被取代,B正确;
C.甲苯的密度小于水,高锰酸钾水层在下方,刚混合时分层,下层呈紫红色,C错误;
第 14 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
D.由图可知,反应④的产物为甲基环己烷,含有5种等效氢,即一氯取代物有5种,D错误;
故选B。
29. 向20mL0.1molL1CH COOH溶液中不断滴入等浓度的NaOH溶液,反应后溶液的pH变化如图所
3
示。下列分析错误的是
A. a点: CH 3 COOH H CH 3 COO
B. b点: CH 3 COO Na CH 3 COOH
C. e点: OH 2CH 3 COOH CH 3 COO H
D. 水的电离程度由大到小的顺序为:c>d>b
【答案】D
【解析】
【 分 析 】 向 20mL0.1molL1CH COOH溶 液 中 不 断 滴 入 等 浓 度 的 NaOH溶 液 , 发 生 反 应
3
CH COOH+NaOHCH COONa+H O,恰好反应时溶质为CH COONa;a点时为醋酸溶液,pH 7,
3 3 2 3
呈酸性;b点时加入10mL0.1molL1 NaOH溶液,醋酸消耗一半,溶质为CH COONa和CH COOH,
3 3
且浓度相等,呈酸性;c点时,加入NaOH溶液体积为20mL,恰好反应,溶质为CH COONa,呈碱性;d
3
点时NaOH过量,溶质为CH COONa和NaOH;
3
【详解】A.a点时未加NaOH溶液,溶质为CH COOH,存在弱电离
3
CH COOHCH COO H+ ,H OOH H+ ,溶液中微粒浓度大小顺序为
3 3 2
第 15 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
CH
3
COOH
H
CH
3
COO
,故A正确;
B.b点时加入10mL0.1molL1 NaOH溶液,醋酸消耗一半,溶质为CH COONa和CH COOH,且
3 3
浓度相等,呈酸性,c(H+)c(OH-),根据据电荷守恒c(H+)c(Na+)c(OH-)c(CH COO),所
3
以c(Na+)c(CH COO);物料守恒为2c(Na+)c(CH COO)c(CH COOH),即
3 3 3
c(Na+)c(CH
3
COOH),综上所述,
CH
3
COO
Na
CH
3
COOH ,故B正确;
C.e点加入40mL等浓度NaOH溶液,醋酸完全反应,溶质为CH COONa和NaOH,且浓度相等,根
3
据电荷守恒c(H+)c(Na+)c(OH-)c(CH COO),物料守恒
3
c(Na+)2[c(CH COO)c(CH COOH)],可得质子守恒
3 3
c(CH COO)2c(CH COOH)c(H+)c(OH-),故C正确;
3 3
D.综上所述,c点时溶质为CH COONa,只存在CH COONa的水解,水的电离程度最大;b点时溶质
3 3
为CH COONa和CH COOH,且浓度相等,其中CH COOH的浓度为
3 3 3
20mL0.1molL110mL0.1molL1 0.1
molL1,d点时溶质为CH COONa和NaOH,其中
20mL10mL 3 3
30mL0.1molL120mL0.1molL1 0.1
NaOH的浓度为 molL1,因为CH COOH为弱酸,
20mL30mL 5 3
0.1 0.1
溶液溶液中c(H+)
molL1,对水的抑制能力弱,NaOH为强碱,c(OH-) molL1,对水的
3 5
0.1
抑制能力大于 molL1 CH COOH,综上所述,水的电离程度由大到小的顺序为:cbd,故D
3 3
错误;
故选D。
30. 在体积均为1.0L的恒容密闭容器甲、乙中,起始投料量如下表,在不同温度下发生反应:
CO
2
gCs
2COg 。CO的平衡浓度随温度的变化如图所示。下列说法正确的是
第 16 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
容器 nCO mol nC mol nCO mol
2
甲 0.1 0.3 0
乙 0.2 0.5 0
A. 曲线Ⅰ对应的是甲容器
B. a、b两点所处状态的压强大小关系:9p <14p
a b
4
C. c点:CO的体积分数小于
7
D. 900K时,若起始向乙中加入CO、CO 、C各0.3mol,则v(正)>v(逆)
2
【答案】B
【解析】
【详解】A.固体物质不影响平衡移动,乙投入0.2molCO ,相同温度下达到平衡时CO浓度应大于甲,所
2
以曲线Ⅰ对应的是乙容器,A错误;
B.甲容器b点处起始0.1molCO ,又平衡时CO浓度0.16mol/L,所以转化的二氧化碳浓度为0.08mol/L,
2
即平衡时二氧化碳浓度为0.02 mol/L;乙容器a处起始投入0.2molCO ,平衡时一氧化碳浓度为0.16
2
mol/L,所以消耗二氧化碳浓度为0.08 mol/L,即平衡时二氧化碳浓度为0.12 mol/L ,若a、b两点温度相
同,又压强之比等于物质的量之比,即P :P =(0.16+0.12):(0.16+0.02)=14:9 ,由于b点温度更高,所
a b
以两点压强关系9P <14P ,B正确;
a b
0.16 4
C.a点一氧化碳体积分数为 ,c点相当于减压平衡正移,一氧化碳体积分数变大,故平
0.160.12 7
4
衡时一氧化碳体积分数大于 ,C错误;
7
第 17 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
0.162
D.a点平衡时1100K平衡常数为 0.213,降低温度平衡常熟一定减小,900K时平衡常数一定小
0.12
0.32
于0.213,若起始向乙容器中加入CO、CO 、C各0.3mol,则Q= 0.30.213,反应逆向进行,
2
0.3
即V(正));T 时,用二聚体表示01h的平均反应速率
1 2 1
v _______。
第 18 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【答案】(1)100.3
c(环戊二烯)c2(HI)
(2)
c(环戊烯)c(I )
2
(3)ad (4)40%
(5)c (6) ①. < ②. 0.225molL-1h-1
【解析】
【小问1详解】
根据盖斯定律可知,①=③-②,则H H H 100.3kJmol1;
1 3 2
【小问2详解】
c(环戊二烯)c2(HI)
反应③的化学平衡常数表达式K ;
c(环戊烯)c(I )
2
【小问3详解】
a.该反应属于反应前后气体分子数不变的反应,则达到化学平衡时气体分子数不变,a正确;
b.2v H v HI 时,反应达到化学平衡状态,b错误;
正 2 逆
c.由于起始投料量未知,则cH cI
时,反应不一定达到平衡状态,c错误;
2 2
d.断裂 II键代表正反应速率,断裂HI键代表逆反应速率,则当断裂1mol II键的同时断裂
2mol HI键,反应达到平衡状态,d正确;
故选ad。
【小问4详解】
设 变化xmol,根据题意列三段式有
第 19 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
环戊烯(g) + I (g) 环戊二烯(g) + 2HI(g)
2
起始/mol 0.5 0.5 0 0
变化/mol x x x 2x
平衡/mol 0.5x 0.5x x 2x
0.50.5 1
恒温恒容下,压强之比等于物质的量之比,则 ,解得x=0.2,环戊烯的转
0.5x0.5xx2x 1.2
0.2mol
化率为 100%40%;
0.5mol
【小问5详解】
a.若是在恒温恒容条件下,通入惰性气体Arg
,各组分浓度不变,正逆反应速率不变,若是在恒温恒
压条件下,通入惰性气体Arg
,相当于增大容器体积,各组分浓度均减小,正逆反应速率均减小,a不
符合题意;
b.升高温度,平衡正向移动,K值增大,b不符合题意;
c.提高环戊烯浓度,即增大反应物浓度,加入反应物这一瞬间,正反应速率突然增大,后逐渐减小,总
的结果正反应速率增大,温度不变,K值不变,c符合题意;
d.分离出HIg
,即减小生成物的浓度,平衡正向移动,正反应速率减小,d不符合题意;
故选c。
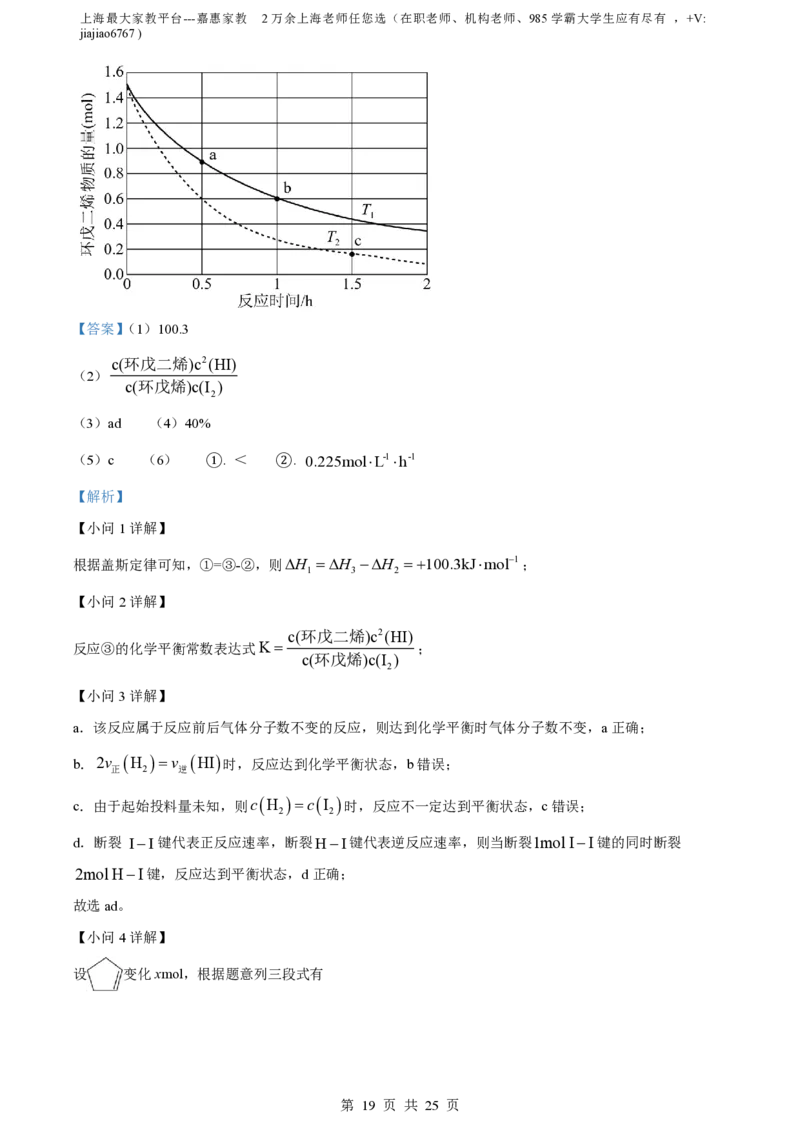
【小问6详解】
环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下2L溶液中环戊二烯物质的量与反应
1.5mol-0.6mol
时间的关系如图所示。b点时,0-1小时内环戊二烯的浓度变化为: =0.45molL1,环戊
2L
1
二烯的二聚体的浓度为环戊二烯浓度变化的 ,则b点时二聚体的浓度为
2
1 0.225molL1
0.45molL1 0.225molL1,二聚体的生成速率v= 0.225molL-1h-1;温度越高
2 1h
反应速率越快,根据图示可知,在温度T (虚线)的反应速率较大,则T <T 。
2 1 2
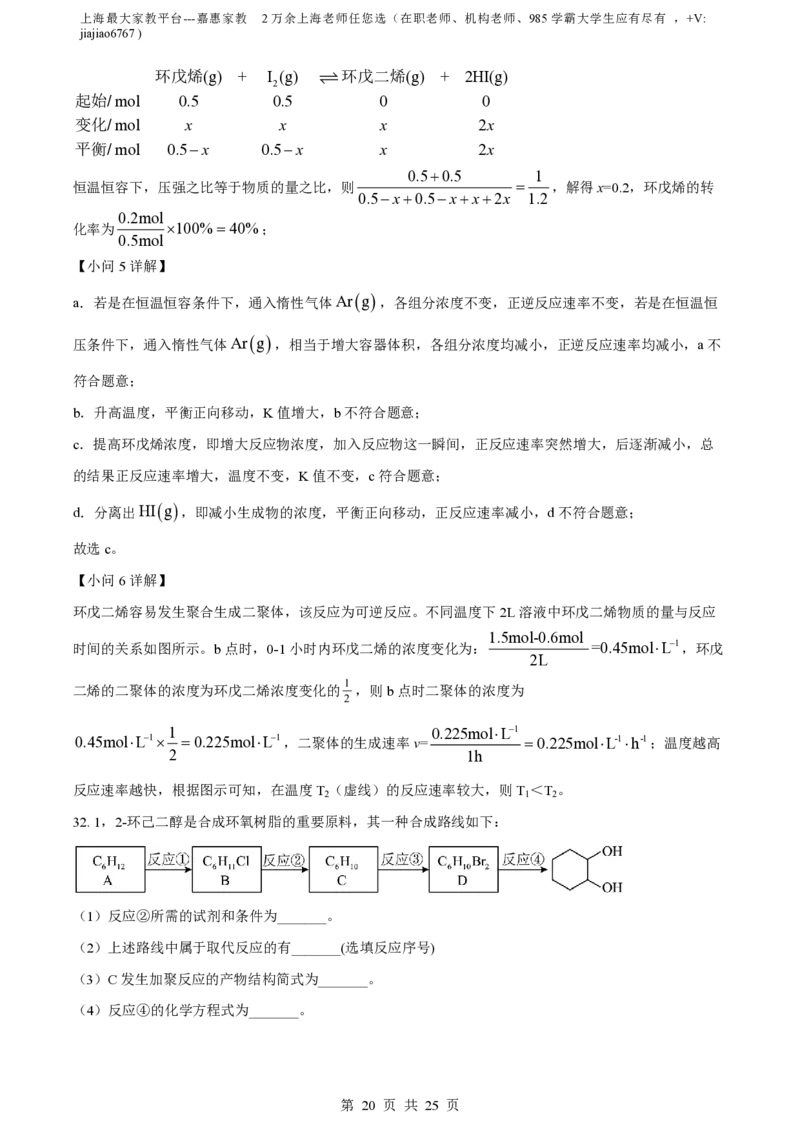
32. 1,2-环己二醇是合成环氧树脂的重要原料,其一种合成路线如下:
(1)反应②所需的试剂和条件为_______。
(2)上述路线中属于取代反应的有_______(选填反应序号)
(3)C发生加聚反应的产物结构简式为_______。
(4)反应④的化学方程式为_______。
第 20 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
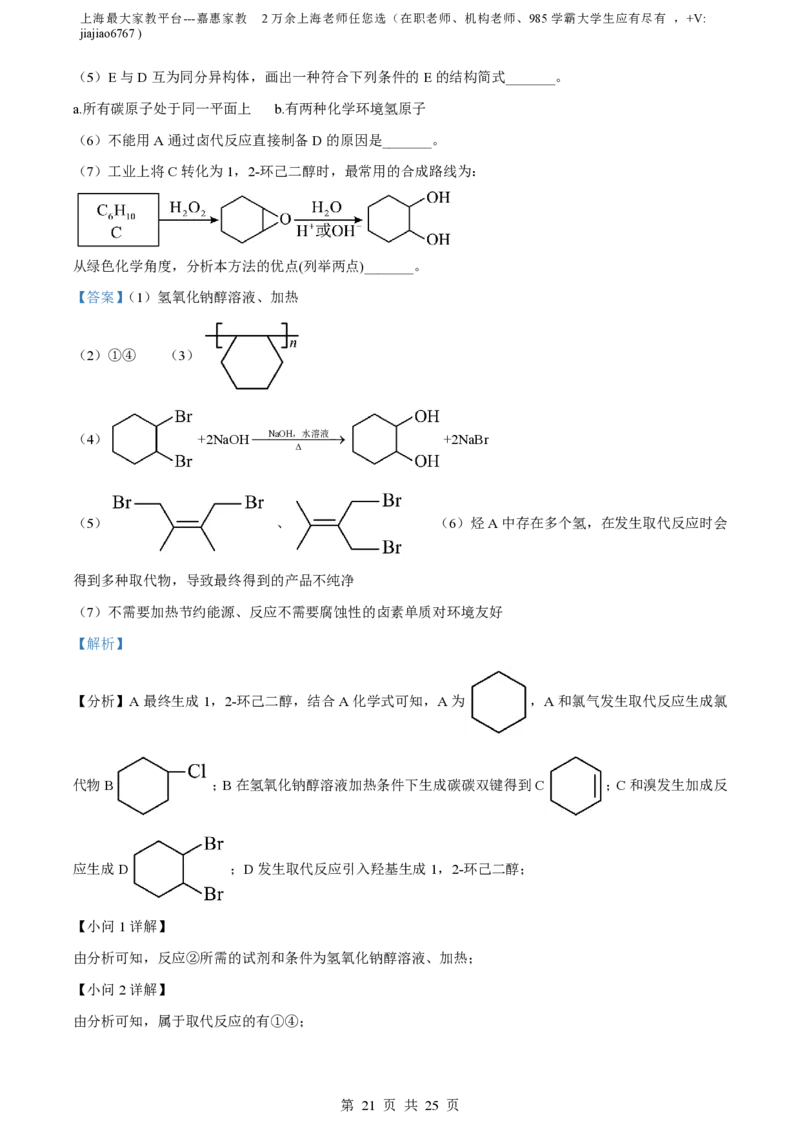
(5)E与D互为同分异构体,画出一种符合下列条件的E的结构简式_______。
a.所有碳原子处于同一平面上 b.有两种化学环境氢原子
(6)不能用A通过卤代反应直接制备D的原因是_______。
(7)工业上将C转化为1,2-环己二醇时,最常用的合成路线为:
从绿色化学角度,分析本方法的优点(列举两点)_______。
【答案】(1)氢氧化钠醇溶液、加热
(2)①④ (3)
(4) +2NaOHNaOH,水溶液 +2NaBr
Δ
(5) 、 (6)烃A中存在多个氢,在发生取代反应时会
得到多种取代物,导致最终得到的产品不纯净
(7)不需要加热节约能源、反应不需要腐蚀性的卤素单质对环境友好
【解析】
【分析】A最终生成1,2-环己二醇,结合A化学式可知,A为 ,A和氯气发生取代反应生成氯
代物B ;B在氢氧化钠醇溶液加热条件下生成碳碳双键得到C ;C和溴发生加成反
应生成D ;D发生取代反应引入羟基生成1,2-环己二醇;
【小问1详解】
由分析可知,反应②所需的试剂和条件为氢氧化钠醇溶液、加热;
【小问2详解】
由分析可知,属于取代反应的有①④;
第 21 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【小问3详解】
C含有碳碳,能发生加聚反应得到 ;
【小问4详解】
D发生取代反应引入羟基生成1,2-环己二醇,反应为: +2NaOHNaOH,水溶液
Δ
+2NaBr;
【小问5详解】
D为 ,不饱和度为1;E与D互为同分异构体,符合下列条件:
a.所有碳原子处于同一平面上,会含有碳碳双键;
b.有两种化学环境氢原子,结构对称性好;
故可以为 、 ;
【小问6详解】
烃A中存在多个氢,在发生取代反应时会得到多种取代物,导致最终得到的产品不纯净,故不能用A通
过卤代反应直接制备D;
【小问7详解】
由图可知,本方法优点有不需要加热节约能源,且反应的不产生无机盐等副产品,反应不需要腐蚀性的卤
素单质对环境友好。
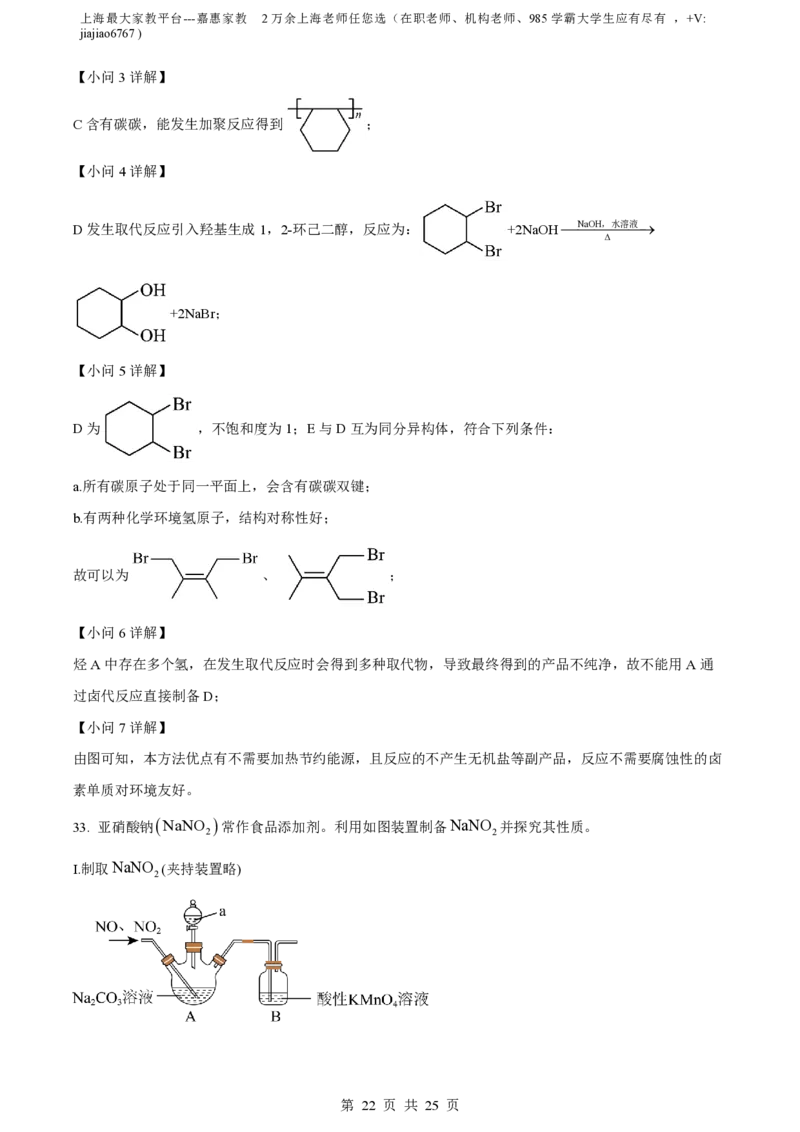
33. 亚硝酸钠 NaNO 常作食品添加剂。利用如图装置制备NaNO 并探究其性质。
2 2
Ⅰ.制取NaNO (夹持装置略)
2
第 22 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
已知:NO NONa CO 2NaNO CO
2 2 3 2 2
2NO Na CO NaNO NaNO CO
2 2 3 2 3 2
(1)仪器a的名称是_______。
(2)已知HNO 为弱酸。判断NaNO 溶液的酸碱性,并结合离子方程式进行解释_______。
2 2
(3)反应前需通入N ,其作用是_______。
2
(4)A中反应后溶液经蒸发浓缩、_______、_______、洗涤干燥等,制得NaNO 晶体。
2
(5)等浓度的NaNO 和NaNO 的混合溶液中,微粒浓度关系正确的是_______(选填编号)。
2 3
a.c Na c NO c NO b.c NO c NO cHNO
3 2 3 2 2
c.c
Na
2c
NO
2c
NO
d.c
NO
c
H
c
NO
c
OH
3 2 3 2
Ⅱ.NaNO 性质探究
2
配制0.1molL1NaNO 溶液进行以下实验:
2
已知:Ag与NO反应,可生成AgNO 白色沉淀或无色络合离子。
2 2
(6)由实验现象得出结论:是否产生白色沉淀与_______有关。
(7)仅用上述实验中的试剂,设计不同实验方案进一步证实上述结论。实验操作及现象是_______。
【答案】(1)分液漏斗
(2)NaNO
2
是强碱弱酸盐,溶液中存在NO
2
的水解平衡:NO
2
H
2
O
HNO
2
+OH,NO
2
的水解
使溶液呈碱性。
(3)把装置内的空气全部排出
(4) ①. 冷却结晶 ②. 过滤
(5)bd (6)络合离子
(7)在试管中加入2mL0.1molL1 AgNO 溶液,向其中缓慢滴加0.1molL1 NaNO 溶液,边滴加边振
3 2
荡试管,可观察到先生成白色沉淀,后沉淀逐渐溶解。
第 23 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【解析】
【分析】NO能与O 反应,通入混合气体前,需要先通N 把装置内的空气排出,根据已知中的反应,要控
2 2
制好NO 与NO的比例,减小或避免副反应的发生,反应后剩余气体含有氮的氧化物,能污染空气,不能
2
直接排放到空气中,用装置B进行吸收处理。
【小问1详解】
仪器a的名称是分液漏斗。
【小问2详解】
NaNO 是强碱弱酸盐,溶液中存在NO的水解平衡:NO H O HNO +OH,NO的水解使溶
2 2 2 2 2 2
液呈碱性。
【小问3详解】
NO能与O 反应生成NO ,影响NaNO 的制取,因此必须把装置内的空气全部排出,故反应前需要通入
2 2 2
N 。
2
【小问4详解】
从溶液中分离出晶体通常要进行以下操作:蒸发浓缩、冷却结晶、过滤、洗涤、干燥。
【小问5详解】
a.等浓度的NaNO 和NaNO 的混合溶液中,由于NO发生水解,因此
2 3 2
c
Na
c
NO
c
NO
,a错误;
3 2
b.根据N元素守恒得c NO c NO cHNO ,b正确;
3 2 2
c.根据Na元素和N元素守恒得c Na 2c NO 或c Na 2c NO 2cHNO ,c错误;
3 2 2
d.根据电荷守恒得:c(Na+)c(H+)c(NO)c(NO)c(OH),结合c Na 2c NO ,得
3 2 3
c
NO
c
H
c
NO
c
OH
,d正确;
3 2
故选bd
【小问6详解】
已知:Ag与NO反应,可生成AgNO 白色沉淀或无色络合离子,当向NaNO 溶液中滴加AgNO 溶
2 2 2 3
液时,NO相对过量,此时Ag+与NO反应生成无色络合离子,继续滴加AgNO 溶液至一定程度后,
2 2 3
络合离子变得不稳定,与Ag+反应生成白色沉淀。根据实验现象,是否生成沉淀与络合离子有关。
【小问7详解】
第 24 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
为验证上述结论,可先在试管中加入2mL0.1molL1 AgNO 溶液,再向其中缓慢滴加0.1molL1
3
NaNO 溶液,边滴加边振荡试管,可观察到先生成白色沉淀,后沉淀逐渐溶解。
2
第 25 页 共 25 页