文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
虹口区 2022 学年度第二学期期中学生学习能力诊断测试
高三化学试卷
考生注意:
1.本试卷满分100分,考试时间60分钟。
2.本考试设试卷和答题纸两部分,试卷包括试题与答题要求,所有答案必须涂(选择题)或写
(非选择题)在答题纸上,做在试卷上一律不得分。
3.答题前,考生务必在答题纸上用水笔清楚填写姓名、准考证号,并将核对后的条形码贴在
指定位置上。
4.答题纸与试卷在试题编号上是一一对应的,答题时应特别注意,不能错位。
相对原子质量:H-1 C-12 N-14 O-16 Al-27 S-32 Cl-35.5 Ba-137
一、选择题(本题共40分,每小题2分,每题只有一个正确选项)
1. 用铜锌合金制成的黄铜制品常被误认为黄金。下列关于黄铜的说法错误的是
A. 有金属光泽 B. 熔点比锌高
C. 硬度比铜大 D. 可用稀盐酸鉴别黄铜与黄金
【答案】B
【解析】
【详解】A.黄铜为铜锌合金,有金属光泽,A正确;
B.合金的熔点通常比成分金属要低,故黄铜的熔点低于锌,B错误;
C.合金的硬度通常大于成分金属,黄铜硬度大于铜,C正确;
D.黄铜中的锌能与HCl反应生成氢气,黄金不与HCl反应,可用稀盐酸鉴别两者,D正确;
故答案选B。
2. 铼( Re)是广泛用于航空发动机涡轮叶片的稀土元素。从此信息中不能确定的是
75
A. 铼原子的质量数 B. 铼元素的原子序数
C. 铼原子核外电子排布 D. 铼元素在元素周期表中位置
【答案】A
【解析】
【详解】A.根据 Re只能知道铼原子的质子数,无法知道中子数,无法确定铼原子的质量数,A正确;
75
B.根据 Re可以确定铼元素的原子序数为75,B错误;
75
C.根据 Re可以确定铼原子的核外电子排布,C错误;
75
D.根据 Re可确定铼原子在元素周期表中的位置,D错误;
75
故答案选A。
第 1 页 共 23 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
3. 下列属于含有非极性键的强电解质的是
A. HBr B. NaO C. KOH D. NH Cl
2 2 4
【答案】B
【解析】
【详解】A.HBr中H-Br键为极性共价键,故A不符合题意;
B.NaO 属于强电解质,由钠离子和过氧根离子组成,过氧根离子中 O-O之间存在非极性共价键,故B
2 2
符合题意;
C.KOH为强碱,属于强电解质,氢氧根离子中存在极性共价键,不含非极性键,故C不符合题意;
D.氯化铵属于盐,是强电解质,铵根离子中N-H键为极性共价键,不含非极性键,故D不符合题意;
故选:B。
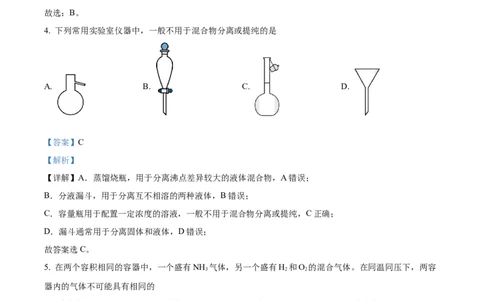
4. 下列常用实验室仪器中,一般不用于混合物分离或提纯的是
A. B. C. D.
【答案】C
【解析】
【详解】A.蒸馏烧瓶,用于分离沸点差异较大的液体混合物,A错误;
B.分液漏斗,用于分离互不相溶的两种液体,B错误;
C.容量瓶用于配置一定浓度的溶液,一般不用于混合物分离或提纯,C正确;
D.漏斗通常用于分离固体和液体,D错误;
故答案选C。
5. 在两个容积相同的容器中,一个盛有NH 气体,另一个盛有H 和O 的混合气体。在同温同压下,两容
3 2 2
器内的气体不可能具有相同的
.
A 原子数 B. 分子数 C. 质量 D. 电子数
【答案】A
【解析】
【分析】同温同压下,气体摩尔体积相等,相同体积的不同气体的物质的量相等、分子数相等,再结合
m=nM、分子构成分析解答。
【详解】同温同压下,气体摩尔体积相等,相同体积的不同气体的物质的量相等、分子数相等,
A. NH 分子中含有4个原子,H 和O 为双原子分子,物质的量相等时含有原子数一定不相等,所以A选
3 2 2
第 2 页 共 23 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
项符合题意;
B.根据N=nN 可以知道,气体物质的量相等时含有分子数一定相等,故B不符合题意;
A
C. NH 的摩尔质量为17g/mol;H 的摩尔质量为2g/mol,O 的摩尔质量为32g/mol,当H 和O 的平均摩尔
3 2 2 2 2
质量为17g/mol时,两个容器中盛有气体的质量相等,故C不符合题意;
D. NH 分子中含有10个电子;H 分子中含有2个电子,O 分子中含有16个电子,当H 和O 的混合气体
3 2 2 2 2
的平均电子数为10时,两个容器中含有电子数相等,故D不符合题意。
答案选A。
6. 将足量SO 气体通入BaCl 溶液中,无明显现象。若要观察到BaSO 沉淀,可再通入
2 2 3
A. Cl B. NO C. HS D. NH
2 2 2 3
【答案】D
【解析】
【详解】A.Cl 与SO 反应生成硫酸,硫酸与氯化钡反应生成硫酸钡沉淀,不能得到 BaSO 沉淀,故A不
2 2 3
符合;
B.NO 与SO 反应生成硫酸,硫酸与氯化钡反应生成硫酸钡沉淀,不能得到BaSO 沉淀,故B不符合;
2 2 3
C.HS与SO 反应生成S单质沉淀,不能得到BaSO 沉淀,故C不符合;
2 2 3
D.NH 与SO 反应生成亚硫酸铵,亚硫酸铵与氯化钡生成BaSO 沉淀,故D符合;
3 2 3
故选:D。
7. 下列有关CH=CH—CH=CH 说法错误的是
2 2
A. 所有原子可能处于同一平面上 B. 与溴的加成产物共有2种
C. 与异戊二烯互为同系物 D. 属于炔烃类的同分异构体有2种
【答案】B
【解析】
【详解】A.碳碳双键为平面结构,两个平面通过单键相连,可以重合,所有原子可处于同一平面上,故
A正确;
B.与溴单质1:1加成时可1,2-加成和1,4-加成得到两种加成产物,另外还可以按照1:2与溴加成生
成四溴丁烷,故B错误;
C.该结构与异戊二烯均含两个碳碳双键,结构相似,组成上相差1个CH,两者互为同系物,故C正确;
2
D.属于炔烃类的同分异构体有1-丁炔,2-丁炔两种,故D正确;
故选:B。
的
8. 下列物质性质 变化规律与化学键强弱无关的是
A. HF、HCl、HBr的热稳定性依次减弱 B. NaF、NaCl、NaBr的熔点依次降低
C. Li、Na、K的熔点逐渐降低 D. SiF、SiCl 、SiBr 的熔、沸点逐渐升高
4 4 4
第 3 页 共 23 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【答案】D
【解析】
【详解】A.F、Cl、Br的非金属性逐渐减弱,HF、HCl、HBr的共价键强度逐渐减弱,热稳定性逐渐减弱,
A正确;
B.NaF、NaCl、NaBr均为离子晶体,离子半径越大,键能越小,故NaF、NaCl、NaBr的熔点依次降低,
B正确;
C.Li、Na、K阳离子所带电荷数相同,但离子半径逐渐增大,金属键逐渐减弱,熔点逐渐降低,C正确;
D.SiF、SiCl 、SiBr 都为分子晶体,相对分子质量逐渐增大,分子间作用力增强,熔、沸点逐渐升高,
4 4 4
与化学键无关,D错误;
故答案选D。
9. 短周期主族元素W、X、Y、Z、Q原子序数依次增大。W与Q同主族,且Q的原子序数是W的2倍;
X的简单离子在同周期元素形成的简单离子中半径最小。下列说法正确的是
A. 元素最高正价:W = Q B. 原子半径:W>X
C. 核外未成对电子数:Y = Q D. 非金属性:Y>Z
【答案】C
【解析】
【分析】短周期主族元素W、X、Y、Z、Q原子序数依次增大,W与Q同主族,且Q的原子序数为W的
2倍,则W为O,Q为S,X的简单离子在同周期元素形成的简单离子中半径最小,X原子序数大于O,X
为Al,Y为Si,Z为P。
【详解】A.O最高正价为+2价,S最高正价为+6价,A错误;
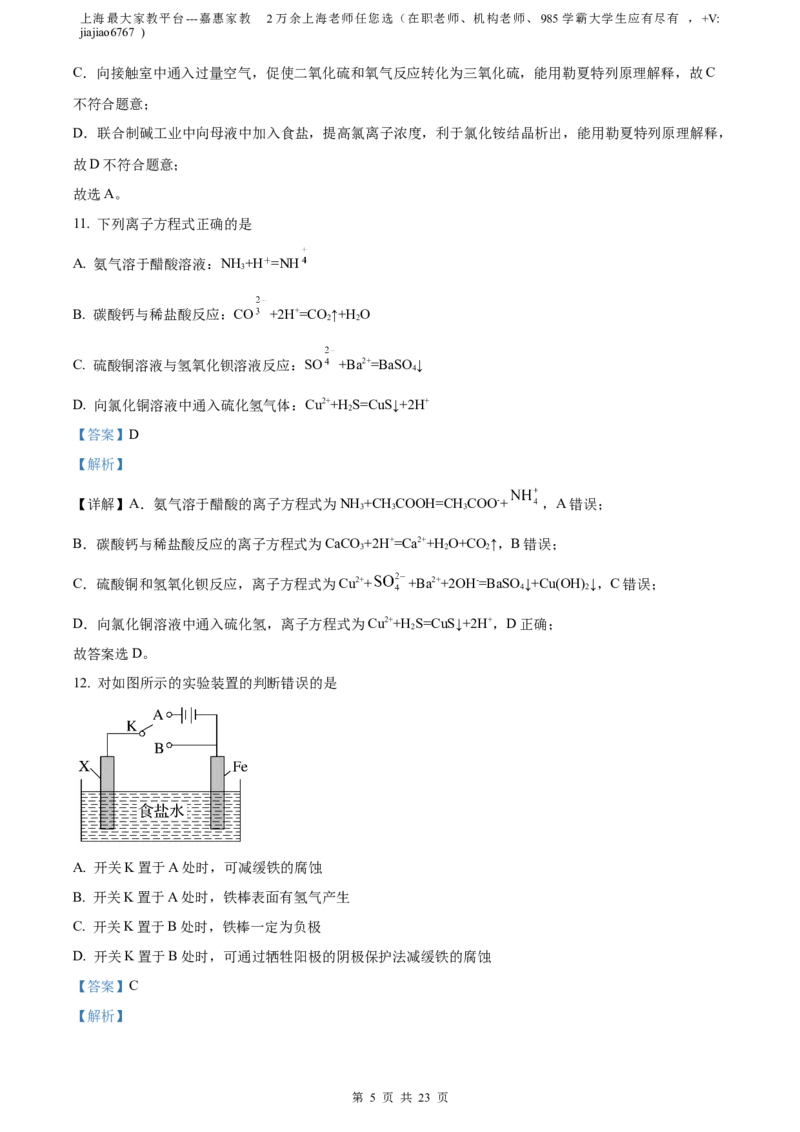
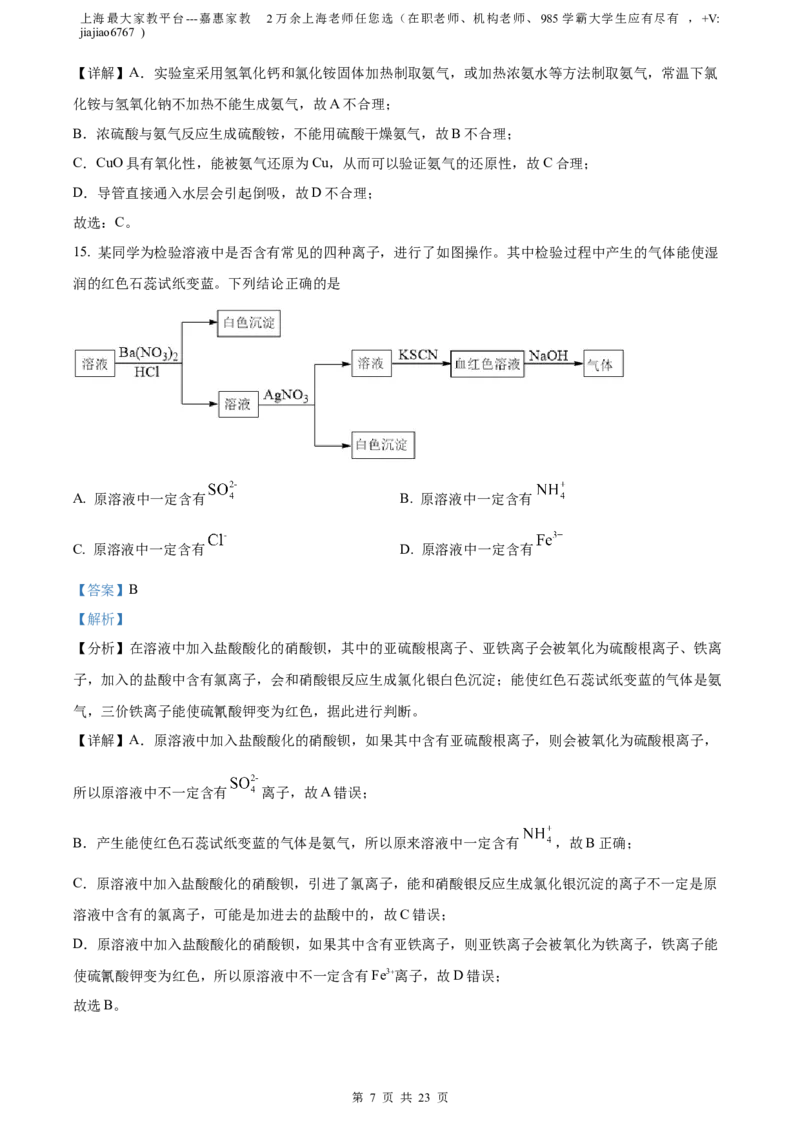
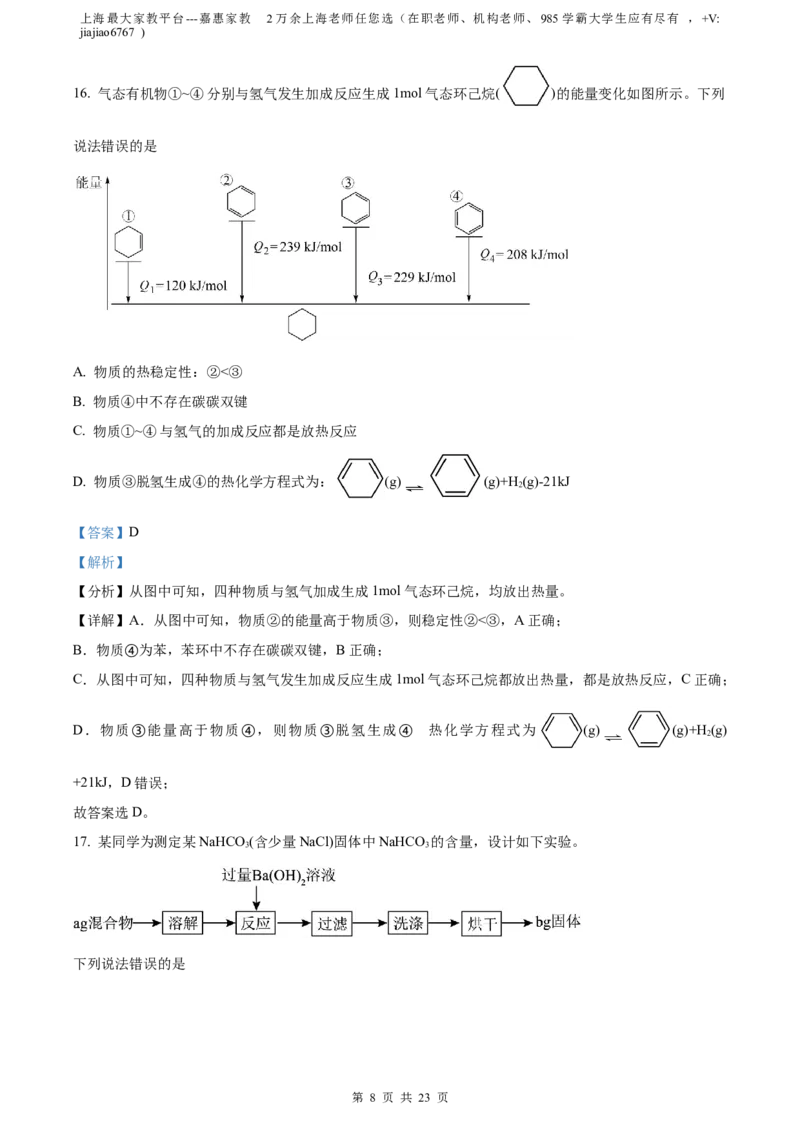
B.Al有3个电子层,O有2个电子层,原子半径Oc(Cl-)
C. ③中溶液又变红的原因:沉淀溶解平衡正向移动
D. ①中存在沉淀溶解平衡:Mg(OH) (s) Mg2+(aq)+2OH-(aq)
2
第 9 页 共 23 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【答案】A
【解析】
【详解】A.①中含有氢氧化镁,③中除了氢氧化镁还有氯化镁,同温度下K [Mg(OH) ]相同,③中镁离
sp 2
子浓度大,则c(OH-):③<①,A错误;
B.③中除了有Mg(OH) 还有MgCl ,则2c(Mg2+)>c(Cl-),B正确;
2 2
C.加入浓盐酸后,Mg(OH) 电离出的氢氧根离子与HCl反应被消耗,促使Mg(OH) 的沉淀溶解平衡正向
2 2
移动,电离出氢氧根离子,溶液又变红,C正确;
D.①为Mg(OH) 的悬浊液,存在沉淀溶解平衡Mg(OH) (s) Mg2+(aq)+2OH-(aq),D正确;
2 2
故答案选A。
19. 一定温度下,向1L密闭容器中充入2molX和1molY,发生反应2X(g)+Y(g) 3Z(?)。达到平衡时,容
器的压强从原来的P 变为0.4P 。下列说法错误的是 ⇌
0 0
A. Z不可能为气体
B. 达到平衡时容器内有1.8molZ
C. 压缩体积,再次达到平衡,X的浓度不变
D. Y的体积分数不变说明反应达到平衡状态
【答案】D
【解析】
【详解】A.若Z为气体,则反应前后气体的压强不变,题目中压强从原来的P 变为0.4P 故Z不可能为气
0 0
体,故A正确;
B.根据向1L密闭容器中充入2molX和1molY,发生反应2X(g)+Y(g) 3Z(?)。达到平衡时,容器的压强
从原来的P 变为0.4P ,则 ⇌
0 0
则 ,则x= 0.6,故达到平衡时容器内有1.8molZ,故B正确;
C.Z为非气体,故压缩体积,再次达到平衡,X的浓度不变,故C正确;
D.反应体系中只有X和Y,Y的体积分数一直为 ,故Y的体积分数不变不能说明反应达到平衡状态,
故D错误;
第 10 页 共 23 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
故选D。
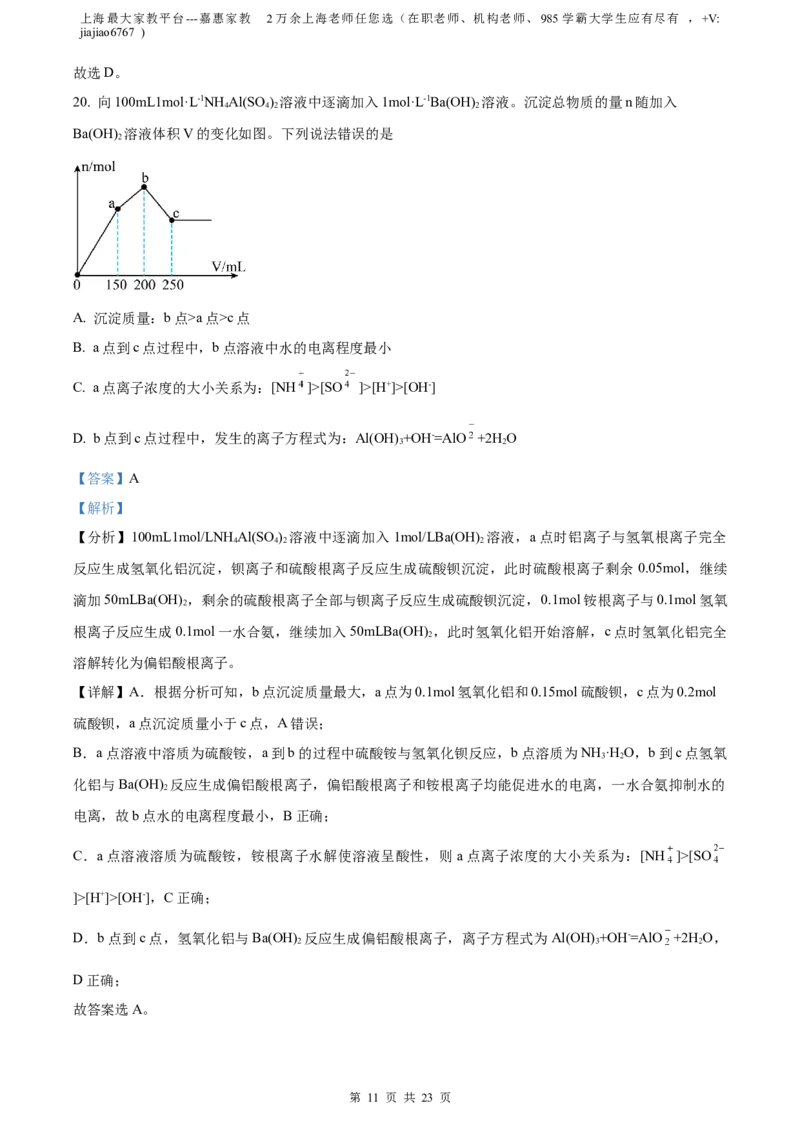
20. 向100mL1mol·L-1NH Al(SO ) 溶液中逐滴加入1mol·L-1Ba(OH) 溶液。沉淀总物质的量n随加入
4 4 2 2
Ba(OH) 溶液体积V的变化如图。下列说法错误的是
2
A. 沉淀质量:b点>a点>c点
B. a点到c点过程中,b点溶液中水的电离程度最小
C. a点离子浓度的大小关系为:[NH ]>[SO ]>[H+]>[OH-]
D. b点到c点过程中,发生的离子方程式为:Al(OH) +OH-=AlO +2H O
3 2
【答案】A
【解析】
【分析】100mL1mol/LNH Al(SO ) 溶液中逐滴加入1mol/LBa(OH) 溶液,a点时铝离子与氢氧根离子完全
4 4 2 2
反应生成氢氧化铝沉淀,钡离子和硫酸根离子反应生成硫酸钡沉淀,此时硫酸根离子剩余 0.05mol,继续
滴加50mLBa(OH) ,剩余的硫酸根离子全部与钡离子反应生成硫酸钡沉淀,0.1mol铵根离子与0.1mol氢氧
2
根离子反应生成0.1mol一水合氨,继续加入50mLBa(OH) ,此时氢氧化铝开始溶解,c点时氢氧化铝完全
2
溶解转化为偏铝酸根离子。
【详解】A.根据分析可知,b点沉淀质量最大,a点为0.1mol氢氧化铝和0.15mol硫酸钡,c点为0.2mol
硫酸钡,a点沉淀质量小于c点,A错误;
B.a点溶液中溶质为硫酸铵,a到b的过程中硫酸铵与氢氧化钡反应,b点溶质为NH ·H O,b到c点氢氧
3 2
化铝与Ba(OH) 反应生成偏铝酸根离子,偏铝酸根离子和铵根离子均能促进水的电离,一水合氨抑制水的
2
电离,故b点水的电离程度最小,B正确;
C.a点溶液溶质为硫酸铵,铵根离子水解使溶液呈酸性,则a点离子浓度的大小关系为:[NH ]>[SO
]>[H+]>[OH-],C正确;
D.b点到c点,氢氧化铝与Ba(OH) 反应生成偏铝酸根离子,离子方程式为Al(OH) +OH-=AlO +2H O,
2 3 2
D正确;
故答案选A。
第 11 页 共 23 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
二、综合题
21. SO 是大气污染物,SO 废气的处理可以先用H 还原成HS后再设法回收S,主要涉及反应:3H+SO
2 2 2 2 2 2
HS+2HO。完成下列填空:
2 2
(1)写出硫化氢的电子式_______,硫原子的核外有_______种不同运动状态的电子。
(2)列举一个硫元素比氧元素非金属性弱的事实:_______。
(3)在一定温度下,向2L反应器中通入含SO 的废气与H,经过10min,有0.4mol水生成,则这段时间
2 2
内v(SO )=_______。
2
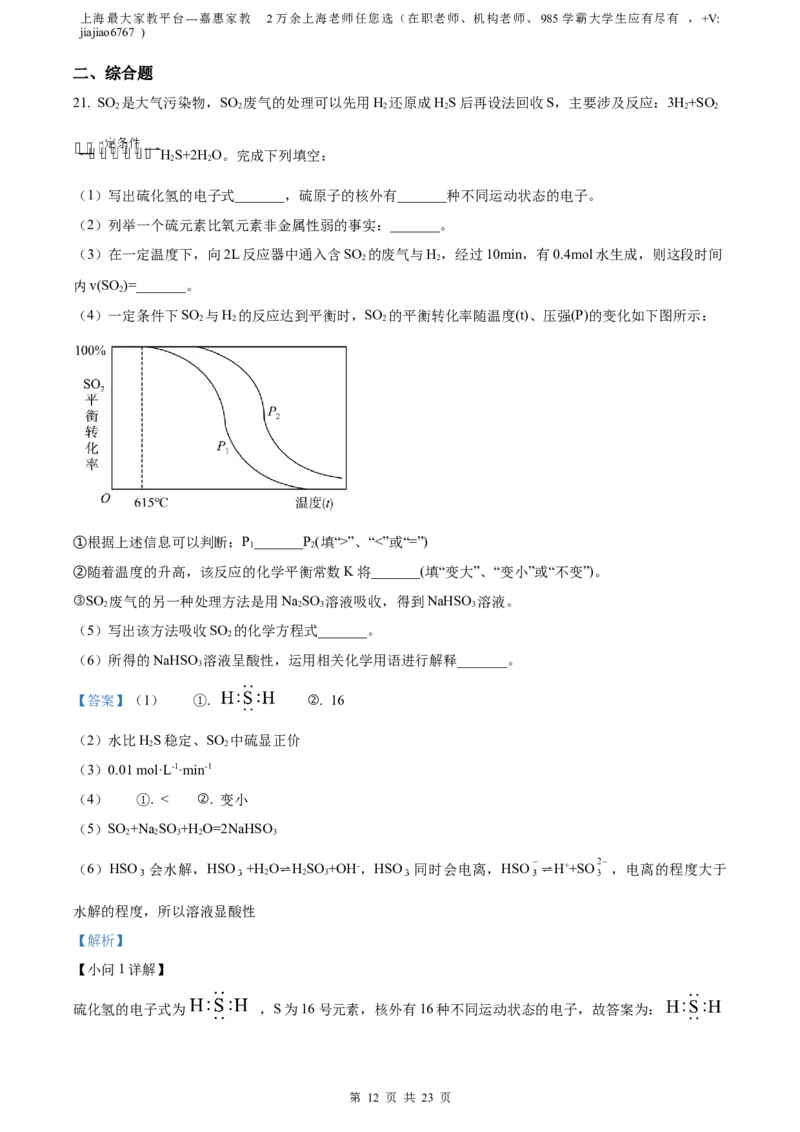
(4)一定条件下SO 与H 的反应达到平衡时,SO 的平衡转化率随温度(t)、压强(P)的变化如下图所示:
2 2 2
①根据上述信息可以判断:P_______P(填“>”、“<”或“=”)
1 2
②随着温度的升高,该反应的化学平衡常数K将_______(填“变大”、“变小”或“不变”)。
③SO 废气的另一种处理方法是用NaSO 溶液吸收,得到NaHSO 溶液。
2 2 3 3
(5)写出该方法吸收SO 的化学方程式_______。
2
(6)所得的NaHSO 溶液呈酸性,运用相关化学用语进行解释_______。
3
【答案】(1) ①. ②. 16
(2)水比HS稳定、SO 中硫显正价
2 2
(3)0.01 mol·L-1·min-1
(4) ①. < ②. 变小
(5)SO +Na SO +H O=2NaHSO
2 2 3 2 3
(6)HSO 会水解,HSO +H
2
O⇌H
2
SO
3
+OH-,HSO 同时会电离,HSO ⇌H++SO ,电离的程度大于
水解的程度,所以溶液显酸性
【解析】
【小问1详解】
硫化氢的电子式为 ,S为16号元素,核外有16种不同运动状态的电子,故答案为:
第 12 页 共 23 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
;16;
【小问2详解】
可通过简单氢化物的稳定性、最高价氧化物的水化物的酸性、氢化物的还原性、单质之间的置换反应或者
在同一化合物中的化合价正负比较S和O的非金属性强弱,如水比HS稳定,氧气能与硫化氢反应生成S
2
单质,或者在二氧化硫中S为+4价,O为-2价,故答案为:水比HS稳定、SO 中硫显正价;
2 2
【小问3详解】
经过10min,有0.4mol水生成,根据反应可知此时消耗的二氧化硫的物质的量为0.2mol,v(SO )=
2
0.01 mol·L-1·min-1,故答案为:0.01 mol·L-1·min-1;
【小问4详解】
①根据上述信息当温度相同时,压强由P 到P 时,二氧化硫的转化率增大,说明平衡正向移动,而该反应
1 2
正向气体分子数减小,压强增大平衡正向移动,则P 大于P,故答案为:<;
2 1
②压强相同时,随温度的升高,二氧化硫的转化率减小,可知平衡逆向移动,则逆向为吸热反应,正向为
放热反应,温度升高K减小,故答案为:变小;
【小问5详解】
NaSO 溶液吸收SO ,得到NaHSO 溶液,反应方程式为:O+Na SO +H O=2NaHSO ,故答案为:
2 3 2 3 2 2 3 2 3
O+Na SO +H O=2NaHSO ;
2 2 3 2 3
【小问6详解】
NaHSO
3
溶液存在一下平衡:HSO +H
2
O⇌H
2
SO
3
+OH-,HSO ⇌H++SO ,NaHSO
3
溶液呈酸性,HSO
可知电离的程度大于水解的程度,所以溶液显酸性;故答案为:HSO 会水解,HSO
+H
2
O⇌H
2
SO
3
+OH-,HSO 同时会电离,HSO ⇌H++SO ,电离的程度大于水解的程度,所以溶液显酸
性;
22. 铁及其化合物在人类生活中有着极其重要的作用。完成下列填空:
(1)铁的原子结构示意图为 。由此可知,铁是第_______周期元素,铁原子核外3d轨道上共填
充了_______个电子。
第 13 页 共 23 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(2)古代中国四大发明之一的司南是由天然的磁石制成的,其主要成分是_______(选填编号)。
a.Fe b.FeO c.Fe O d.Fe O
2 3 3 4
(3)FeSO 可以用来净水、治疗缺铁性贫血等,实验室在配制FeSO 溶液时,为了防止FeSO 变质,经常
4 4 4
向溶液中加入铁粉,其原因是_______(用离子方程式表示)。
(4)向新配制的FeSO 溶液中,加入一定量的稀硝酸,发生如下反应:
4
_______Fe2++_______H++_______NO =_______Fe3++_______NO↑+_______HO
2
①配平上述反应_______。
②每生成0.5molNO气体,转移的电子数为_______。
③要检验该反应后的溶液中是否还含有Fe2+,实验方案是_______。
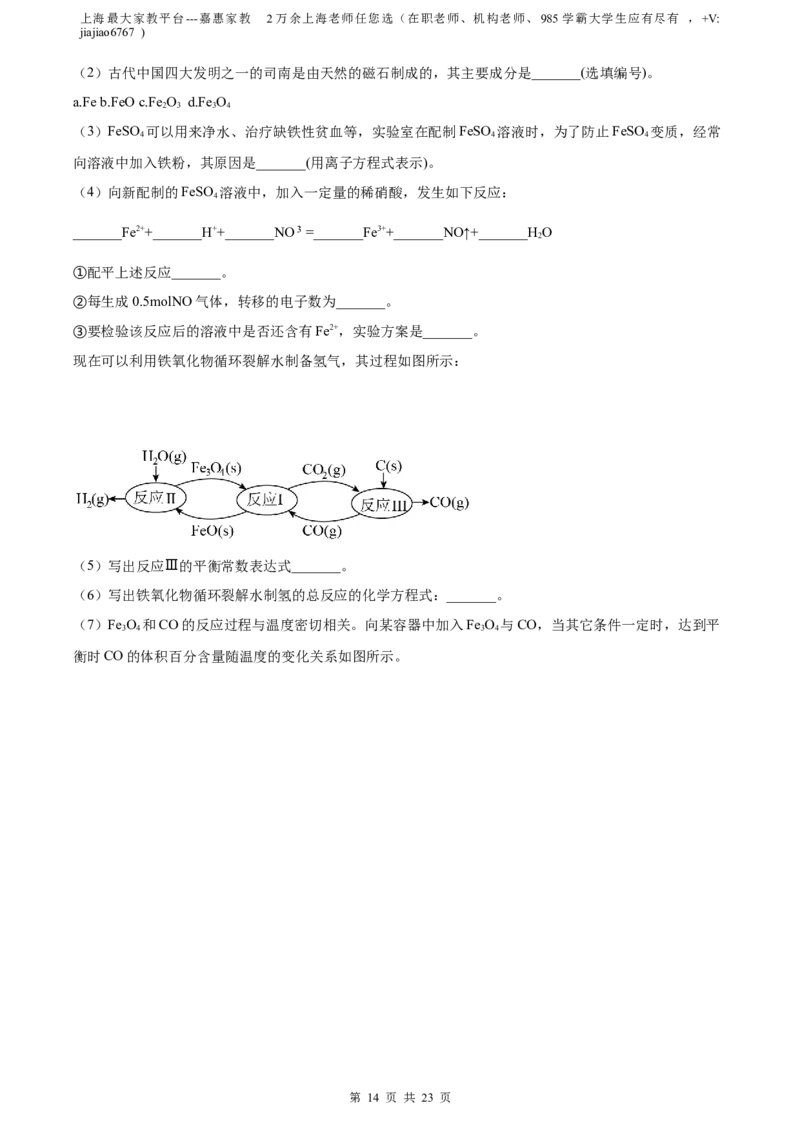
现在可以利用铁氧化物循环裂解水制备氢气,其过程如图所示:
(5)写出反应Ⅲ的平衡常数表达式_______。
(6)写出铁氧化物循环裂解水制氢的总反应的化学方程式:_______。
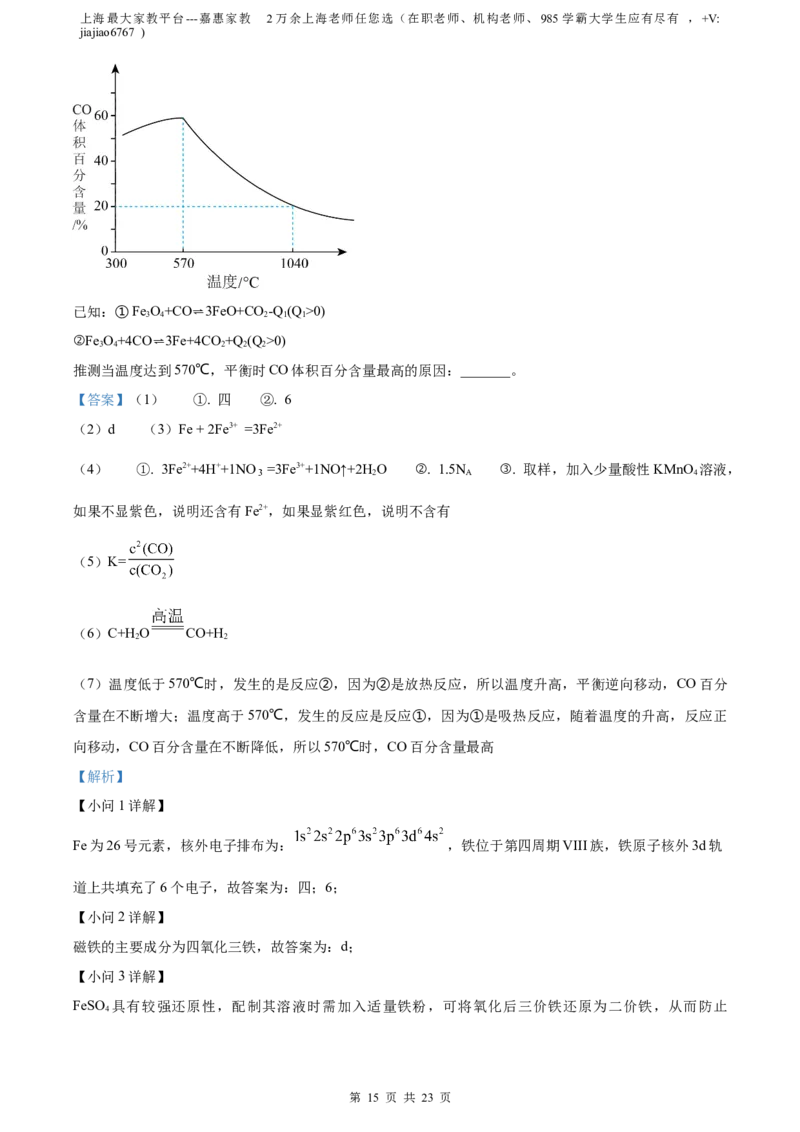
(7)Fe O 和CO的反应过程与温度密切相关。向某容器中加入Fe O 与CO,当其它条件一定时,达到平
3 4 3 4
衡时CO的体积百分含量随温度的变化关系如图所示。
第 14 页 共 23 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
已知:①Fe
3
O
4
+CO⇌3FeO+CO
2
-Q
1
(Q
1
>0)
②Fe
3
O
4
+4CO⇌3Fe+4CO
2
+Q
2
(Q
2
>0)
推测当温度达到570℃,平衡时CO体积百分含量最高的原因:_______。
【答案】(1) ①. 四 ②. 6
(2)d (3)Fe + 2Fe3+ =3Fe2+
(4) ①. 3Fe2++4H++1NO =3Fe3++1NO↑+2HO ②. 1.5N ③. 取样,加入少量酸性KMnO 溶液,
2 A 4
如果不显紫色,说明还含有Fe2+,如果显紫红色,说明不含有
(5)K=
(6)C+H O CO+H
2 2
(7)温度低于570℃时,发生的是反应②,因为②是放热反应,所以温度升高,平衡逆向移动,CO百分
含量在不断增大;温度高于570℃,发生的反应是反应①,因为①是吸热反应,随着温度的升高,反应正
向移动,CO百分含量在不断降低,所以570℃时,CO百分含量最高
【解析】
【小问1详解】
Fe为26号元素,核外电子排布为: ,铁位于第四周期VIII族,铁原子核外3d轨
道上共填充了6个电子,故答案为:四;6;
【小问2详解】
磁铁的主要成分为四氧化三铁,故答案为:d;
【小问3详解】
FeSO 具有较强还原性,配制其溶液时需加入适量铁粉,可将氧化后三价铁还原为二价铁,从而防止
4
第 15 页 共 23 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
FeSO 氧化,发生的离子反应为:Fe + 2Fe3+ =3Fe2+,故答案为:Fe + 2Fe3+ =3Fe2+;
4
【小问4详解】
1mol Fe2+被氧化为Fe3+失去1mol电子,1mol NO 被还原为NO得3mol电子,根据得失电子守恒得到反应
方程式:3Fe2++4H++1NO =3Fe3++1NO↑+2HO;由反应可知每生成1molNO转移3mol电子,则生成
2
0.5molNO气体,转移的电子数为1.5N ;检验反应后溶液中是否存在亚铁离子,可利用其还原性,用高锰
A
酸钾溶液检验,具体的操作为:取样,加入少量酸性KMnO 溶液,如果不显紫色,说明还含有Fe2+,如果
4
显紫红色,说明不含有;故答案为:3Fe2++4H++1NO =3Fe3++1NO↑+2HO;1.5N ;取样,加入少量酸性
2 A
KMnO 溶液,如果不显紫色,说明还含有Fe2+,如果显紫红色,说明不含有;
4
【小问5详解】
由图可知反应III为C与二氧化碳反应生成CO,反应方程式为:C(s)+CO(g) 2CO(g),平衡常数表达式
2
K= ,故答案为:K= ;
【小问6详解】
由图可知总反应为C与水高温生成CO和氢气,反应为:C+H O CO+H,故答案为:C+H O
2 2 2
CO+H;
2
【小问7详解】
温度较低时发生反应②,由题意可知反应②为放热反应,随温度的升高,平衡逆向移动,CO的百分含量
不断增大;当温度较高时发生反应①,反应①为吸热反应,随温度升高,反应正向移动,CO的百分含量
又降低,故答案为:温度低于570℃时,发生的是反应②,因为②是放热反应,所以温度升高,平衡逆向
移动,CO百分含量在不断增大;温度高于570℃,发生的反应是反应①,因为①是吸热反应,随着温度的
升高,反应正向移动,CO百分含量在不断降低,所以570℃时,CO百分含量最高。
23. 某同学查阅资料得知,无水三氯化铝能催化乙醇制备乙烯,为探究适宜的反应温度,设计如下反应装
置:
第 16 页 共 23 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
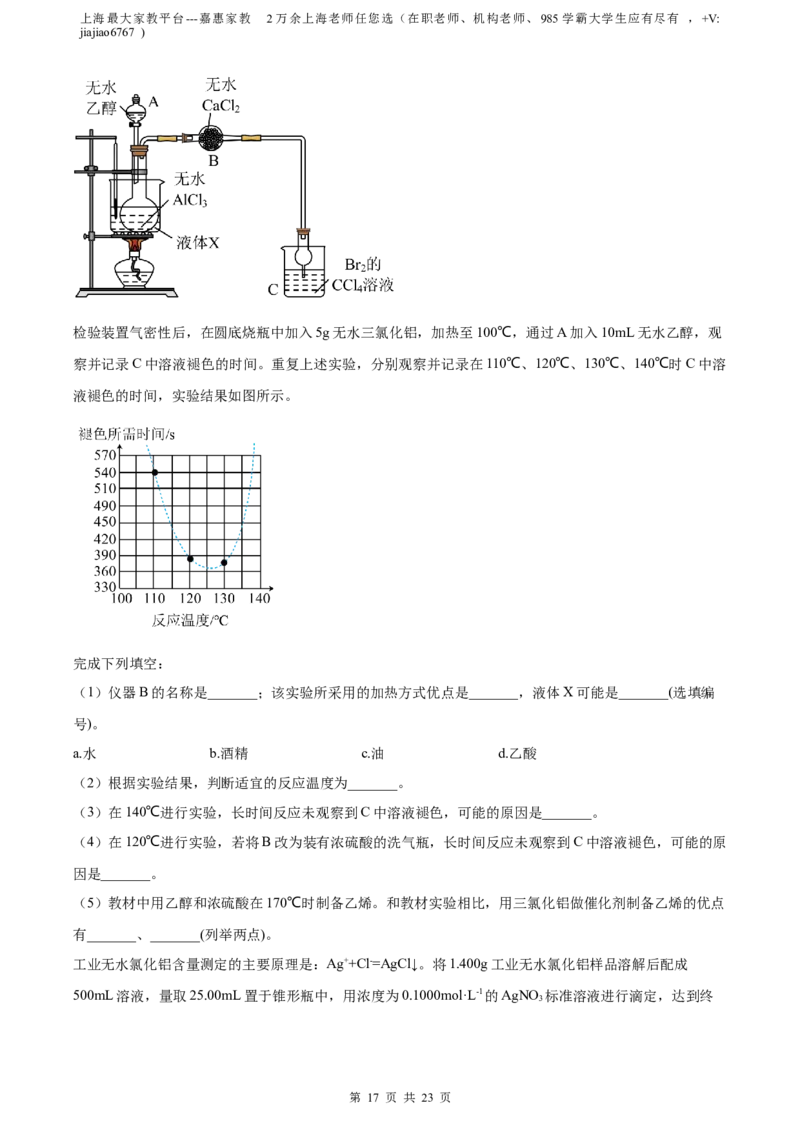
检验装置气密性后,在圆底烧瓶中加入5g无水三氯化铝,加热至100℃,通过A加入10mL无水乙醇,观
察并记录C中溶液褪色的时间。重复上述实验,分别观察并记录在110℃、120℃、130℃、140℃时C中溶
液褪色的时间,实验结果如图所示。
完成下列填空:
(1)仪器B的名称是_______;该实验所采用的加热方式优点是_______,液体X可能是_______(选填编
号)。
a.水 b.酒精 c.油 d.乙酸
(2)根据实验结果,判断适宜的反应温度为_______。
(3)在140℃进行实验,长时间反应未观察到C中溶液褪色,可能的原因是_______。
(4)在120℃进行实验,若将B改为装有浓硫酸的洗气瓶,长时间反应未观察到C中溶液褪色,可能的原
因是_______。
(5)教材中用乙醇和浓硫酸在170℃时制备乙烯。和教材实验相比,用三氯化铝做催化剂制备乙烯的优点
有_______、_______(列举两点)。
工业无水氯化铝含量测定的主要原理是:Ag++Cl-=AgCl↓。将1.400g工业无水氯化铝样品溶解后配成
500mL溶液,量取25.00mL置于锥形瓶中,用浓度为0.1000mol·L-1的AgNO 标准溶液进行滴定,达到终
3
第 17 页 共 23 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
点时消耗标准液15.30mL。
(6)该样品中AlCl 的质量分数为_______(保留3位有效数字)。
3
(7)某次测定结果误差为-2.1%,可能会造成此结果的原因是_______(选填编号)。
a.称量样品时少量吸水潮解 b.配制AlCl 溶液时未洗涤烧杯
3
c.滴定管水洗后未用AgNO 标准溶液润洗 d.样品中含有少量Al(NO ) 杂质
3 3 3
【答案】(1) ①. 干燥管 ②. 受热均匀,便于控制温度 ③. c
(2)125℃(或120~130℃)
(3)温度过高,AlCl 催化活性降低,无法催化乙醇制乙烯
3
(4)乙烯被浓硫酸吸收或乙烯与浓硫酸发生反应
(5) ①. 反应条件温和 ②. 副反应少
(6)0.973 (7)ab
【解析】
【分析】在圆底烧瓶中加入5g无水三氯化铝,加热至100℃,通过A加入100mL无水乙醇,无水三氯化
铝催化乙醇发生消去反应生成乙烯,生成的乙烯进入C中与Br 发生加成反应使溴的四氯化碳溶液褪色。
2
【小问1详解】
仪器B的名称为干燥管。该实验采用水浴加热的方式,优点是受热均匀且便于控制温度。从题中可知,加
热温度最高达到了140℃,水沸点为100℃,酒精加热易挥发且沸点为78℃,乙酸加热易挥发且沸点为
118℃,因此液体X可能为油,答案选c。
【小问2详解】
从图中可知,125℃(120-130℃)时,C中溶液褪色时间最短,反应速率最快,故适宜的反应温度为
125℃(120-130℃)。
【小问3详解】
在140℃时进行实验,长时间反应未观察到C中溶液褪色,可能的原因为温度过高,AlCl 催化活性降低,
3
无法催化乙醇制乙烯。
【
小问4详解】
若将B改为装有浓硫酸的洗气瓶,浓硫酸具有强氧化性,能与乙烯反应,故C中溶液不褪色。
【
小问5详解】
教材中乙醇和浓硫酸在170℃时制备乙烯,用AlCl 做催化剂制备乙烯,反应温度约为125℃,相对而言反
3
应条件温和,且浓硫酸与乙醇反应制乙烯的过程中有副反应发生,会生成二氧化硫等杂质,用AlCl 做催
3
化剂制备乙烯,副反应少,无其他杂质生成。
【小问6详解】
第 18 页 共 23 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
已知消耗AgNO 的物质的量为0.1mol×0.0153L=1.53×10-3mol,则参与反应的Cl-有1.53×10-3mol,1.4g工
3
业无水氯化铝中含有Cl-3.06×10-2mol,AlCl 物质的量为1.02×10-2mol,样品中AlCl 的质量分数为
3 3
【小问7详解】
a.称量样品时少量吸水潮解,则样品中AlCl 的量偏少,消耗的硝酸银偏少,测定结果偏低,a正确;
3
b.配制AlCl 溶液时未洗涤烧杯,使得部分AlCl 溶质损失,测定结果偏低,b正确;
3 3
c.滴定管水洗后未用硝酸银标准液润洗,则硝酸银浓度偏小,消耗的硝酸银偏多,测定结果偏高,c错误;
d.样品中本来就有部分杂质,样品中的少量硝酸铝不与硝酸银反应,只有 AlCl 与硝酸银反应,则得到的
3
计算结果就是AlCl 实际的质量分数,含有的少量Al(NO ) 本就是杂质的一种,不影响测定结果,d错误;
3 3 3
故答案选ab。
24. 贝沙罗汀(分子式C H O)主要用于治疗顽固性早期皮肤T细胞淋巴瘤,其一种合成路线如下:
24 28 2
完成下列填空:
(1)①的反应类型是_______;③所需的无机试剂是_______;④中官能团的转化为:
_______→_______(填官能团名称)。
(2)②的反应式为_______。
(3)已知:1molC与1molD反应生成1molE,同时生成1molHCl。D的结构简式为_______。
(4)写出满足下列条件的A的一种同分异构体的结构简式_______。
i.属于芳香族化合物,能发生银镜反应
ⅱ.只含有2种化学环境不同的氢原子
(5)参考E→F的反应信息,写出以 为原料合成 的路线_______。(无机试剂
第 19 页 共 23 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
与溶剂任选,合成路线常用的表示方式为:A ……B 目标产物)
【答案】(1) ①. 氧化反应 ②. NaHCO 溶液 ③. 酯基 ④. 羧基
3
(2) (3) (4)
(5)
【解析】
【分析】 与酸性高锰酸钾反应生成A为 , 与甲醇发生酯化反应生成B,B与碳
酸氢钠发生反应生成 , 与SOCl 反应生成C,1molC与1molD反应生成1molE的
2
同时生成1molHCl,则D为 ,E一定条件下反应生成F,F发生酯类的水解反应生成贝沙罗
汀。
【小问1详解】
与酸性高锰酸钾反应生成A为 ,反应类型为氧化反应。反应③中羧基与碳酸氢钠反应生
成羧酸钠,从流程图可知,反应④发生的是酯类的水解,官能团转化为酯基→羧基。
【小问2详解】
第 20 页 共 23 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
反应②为1分子 与1分子CHOH反应生成B,化学方程式为
3
。
【小问3详解】
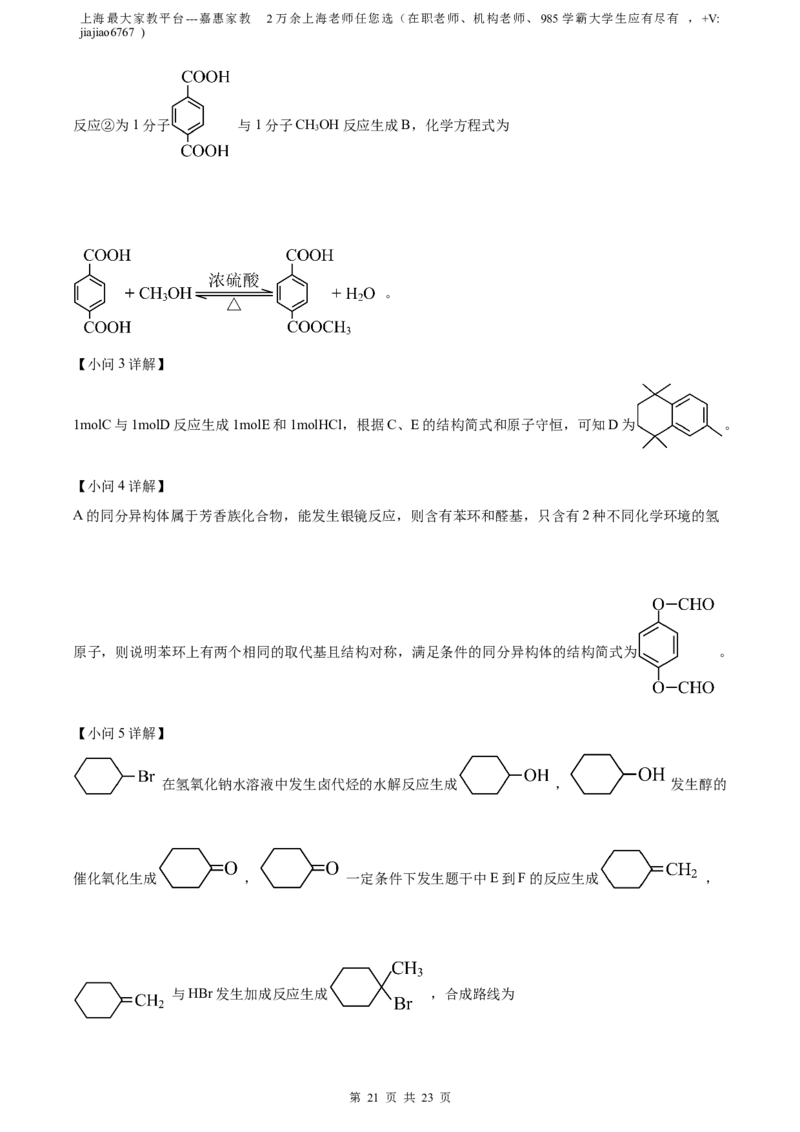
1molC与1molD反应生成1molE和1molHCl,根据C、E的结构简式和原子守恒,可知D为 。
【小问4详解】
A的同分异构体属于芳香族化合物,能发生银镜反应,则含有苯环和醛基,只含有2种不同化学环境的氢
原子,则说明苯环上有两个相同的取代基且结构对称,满足条件的同分异构体的结构简式为 。
【小问5详解】
在氢氧化钠水溶液中发生卤代烃的水解反应生成 , 发生醇的
催化氧化生成 , 一定条件下发生题干中E到F的反应生成 ,
与HBr发生加成反应生成 ,合成路线为
第 21 页 共 23 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
第 22 页 共 23 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
第 23 页 共 23 页