文档内容
专练 17 氯、溴、碘及其化合物
授课提示:对应学生用书33页
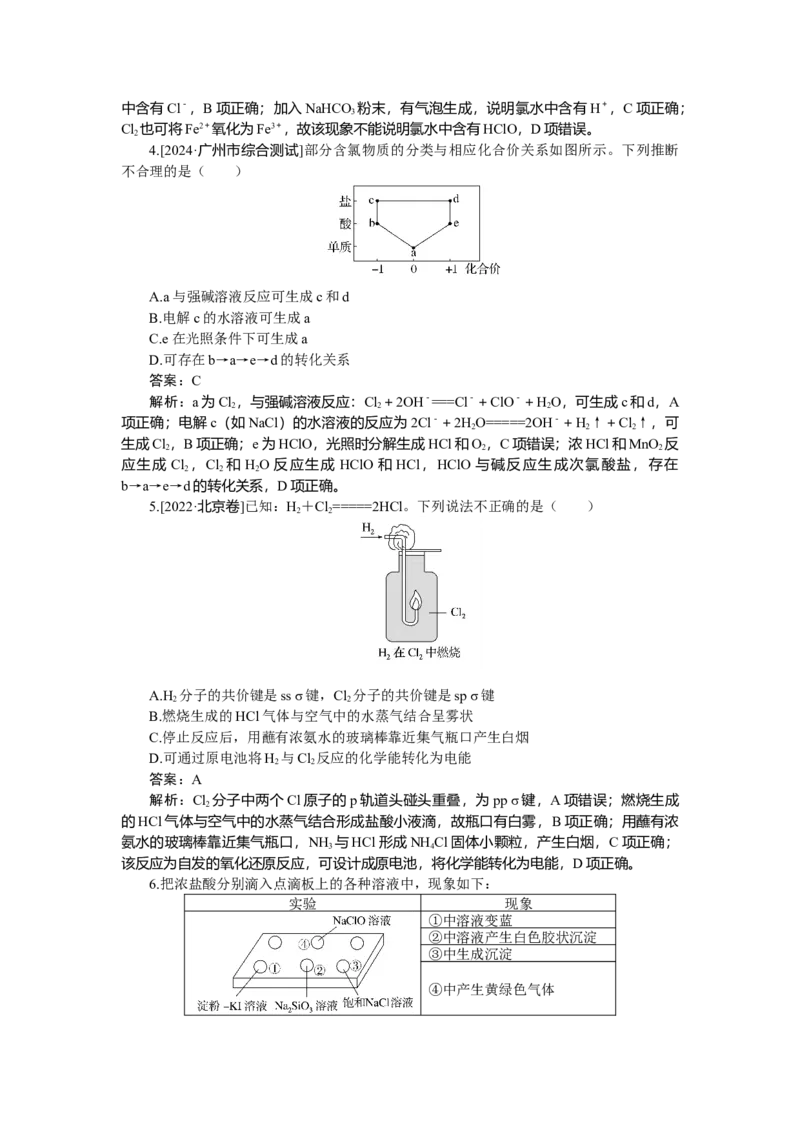
1.[2022·广东卷]实验室用MnO 和浓盐酸反应生成Cl 后,按照净化、收集、性质检验
2 2
及尾气处理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是(
)
答案:D
解析:A项,除杂装置,先除去HCl,后除去水蒸气,正确;B项,集气装置,氯气
密度比空气大,进气管长,出气管短,正确;C项,探究干燥的红布条和湿润的红布条与
氯气的反应,正确;D项,尾气吸收应用碱液,错误。
2.[2023·辽宁卷]某小组进行实验,向10 mL蒸馏水中加入0.4 g I ,充分振荡,溶液呈
2
浅棕色,再加入 0.2 g锌粒,溶液颜色加深;最终紫黑色晶体消失,溶液褪色。已知 I
(aq)为棕色,下列关于颜色变化的解释错误的是( )
选项 颜色变化 解释
A 溶液呈浅棕色 I 在水中溶解度较小
2
B 溶液颜色加深 发生了反应:I
2
+I- ⇌I
I(aq)的消耗使溶解平衡
C 紫黑色晶体消失 2
I
2
(s) ⇌I
2
(aq)右移
D 溶液褪色 Zn与有色物质发生了置换反应
答案:D
解析:向10 mL蒸馏水中加入0.4 g I ,充分振荡,溶液呈浅棕色,说明I 的浓度较小,
2 2
因为I 在水中溶解度较小,A项正确;已知I(aq)为棕色,加入0.2 g锌粒后,Zn与I 反
2 2
应生成ZnI
2
,生成的I-与I
2
发生反应I-+I 2⇌I,生成I使溶液颜色加深,B项正确;I
2
在水
中存在溶解平衡I
2
(s)⇌I
2
(aq),Zn与I
2
反应生成的I-与I
2
(aq)反应生成I,I
2
(aq)
浓度减小,上述溶解平衡向右移动,紫黑色晶体消失,C项正确;最终溶液褪色是Zn与有
色物质发生了化合反应,不是置换反应,D项错误;答案选D。
3.在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是(
)
A.氯水的颜色呈浅黄绿色,说明氯水中含有Cl
2
B.向氯水中滴加硝酸酸化的AgNO 溶液,产生白色沉淀,说明氯水中含有Cl-
3
C.向氯水中加入NaHCO 粉末,有气泡产生,说明氯水中含有H+
3
D.向FeCl 溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO
2
答案:D
解析:新制氯水中含有Cl ,所以呈浅黄绿色,A项正确;生成氯化银沉淀,说明氯水
2中含有Cl-,B项正确;加入NaHCO 粉末,有气泡生成,说明氯水中含有H+,C项正确;
3
Cl 也可将Fe2+氧化为Fe3+,故该现象不能说明氯水中含有HClO,D项错误。
2
4.[2024·广州市综合测试]部分含氯物质的分类与相应化合价关系如图所示。下列推断
不合理的是( )
A.a与强碱溶液反应可生成c和d
B.电解c的水溶液可生成a
C.e在光照条件下可生成a
D.可存在b→a→e→d的转化关系
答案:C
解析:a为Cl ,与强碱溶液反应:Cl +2OH-===Cl-+ClO-+HO,可生成c和d,A
2 2 2
项正确;电解c(如NaCl)的水溶液的反应为2Cl-+2HO=====2OH-+H↑+Cl↑,可
2 2 2
生成Cl,B项正确;e为HClO,光照时分解生成HCl和O,C项错误;浓HCl和MnO 反
2 2 2
应生成 Cl ,Cl 和 HO 反应生成 HClO 和 HCl,HClO 与碱反应生成次氯酸盐,存在
2 2 2
b→a→e→d的转化关系,D项正确。
5.[2022·北京卷]已知:H+Cl=====2HCl。下列说法不正确的是( )
2 2
A.H 分子的共价键是ss σ键,Cl 分子的共价键是sp σ键
2 2
B.燃烧生成的HCl气体与空气中的水蒸气结合呈雾状
C.停止反应后,用蘸有浓氨水的玻璃棒靠近集气瓶口产生白烟
D.可通过原电池将H 与Cl 反应的化学能转化为电能
2 2
答案:A
解析:Cl 分子中两个Cl原子的p轨道头碰头重叠,为pp σ键,A项错误;燃烧生成
2
的HCl气体与空气中的水蒸气结合形成盐酸小液滴,故瓶口有白雾,B项正确;用蘸有浓
氨水的玻璃棒靠近集气瓶口,NH 与HCl形成NH Cl固体小颗粒,产生白烟,C项正确;
3 4
该反应为自发的氧化还原反应,可设计成原电池,将化学能转化为电能,D项正确。
6.把浓盐酸分别滴入点滴板上的各种溶液中,现象如下:
实验 现象
①中溶液变蓝
②中溶液产生白色胶状沉淀
③中生成沉淀
④中产生黄绿色气体下列分析不正确的是( )
A.①中溶液变蓝,体现了浓盐酸的氧化性
B.②中产生白色胶状沉淀:
2H++SiO===H SiO↓
2 3
C.③中产生沉淀的原因可用平衡移动原理解释
D.④中产生黄绿色气体:
ClO-+Cl-+2H+===Cl↑+HO
2 2
答案:A
解析:①HCl遇KI溶液不能发生反应生成I,A项错误;由于酸性HCl>H SiO,所以
2 2 3
浓盐酸遇NaSiO 溶液会发生反应2HCl+NaSiO===H SiO↓+2NaCl,由于硅酸是白色难
2 3 2 3 2 3
溶性的物质,所以会产生白色胶状沉淀,B项正确;在饱和NaCl溶液中存在平衡NaCl
(s)⇌Na+(aq)+Cl-(aq),HCl溶于饱和NaCl溶液,使溶液中Cl-浓度增大,平衡
逆向移动,降低了NaCl的溶解度,因此会析出NaCl固体,即产生白色沉淀,C项正确;
HCl溶于NaClO溶液中,会发生反应2HCl+NaClO===NaCl+Cl↑+HO,离子方程式是
2 2
ClO-+Cl-+2H+===Cl↑+HO,因此有黄绿色气体产生,D项正确。
2 2
7.[2024·河北石家庄外国语学校月考]下列实验操作对应的实验现象、实验结论均正确
且有逻辑关系的是( )
选项 实验操作 实验现象 实验结论
常温下,用pH计测定0.1
A mol·L-1 NaHRO 溶液的 溶液的pH=3.71 HRO 为二元酸
3 2 3
pH
将过量干燥的氯气通入装
B 红色鲜花颜色无变化 干燥的氯气不具有漂白性
有红色鲜花的集气瓶中
分别将乙烯和SO 通入溴 两种气体使溴水褪色的原
C 2 溴水均褪色
水中 理完全相同
向湿润的KI-淀粉试纸上 该黄色溶液中一定含有
D KI-淀粉试纸变蓝
滴2滴某黄色溶液 Fe3+
答案:A
解析:常温下,用pH计测定0.1 mol·L-1 NaHRO 溶液的pH=3.71,说明HRO可以电
3
离出H+,则HRO 为二元酸,A项正确;将过量干燥的氯气通入装有红色鲜花的集气瓶中,
2 3
因为鲜花中有水,Cl 与水生成HClO,则红色鲜花颜色褪去,B项错误;乙烯使溴水褪色,
2
是因为发生加成反应,SO 使溴水褪色,是因为发生氧化还原反应,两种气体使溴水褪色
2
的原理不相同,C项错误;向湿润的KI-淀粉试纸上滴2滴某黄色溶液,试纸变蓝,说明
生成了碘单质,则黄色溶液具有氧化性,也可能含CrO,D项错误。
8.[2024·重庆七中四模]实验小组同学制备KClO 并探究其性质,过程如图:
3
下列说法不正确的是( )
A.可用饱和NaCl溶液净化氯气
B.生成KClO 的离子方程式为
3
3Cl+6OH-=====ClO+5Cl-+3HO
2 2
C.若取少量无色溶液a于试管中,滴加稀HSO 后,溶液仍为无色
2 4
D.上述实验说明碱性条件下氧化性:Cl>KCl ,酸性条件下氧化性:Cl<KClO
2 3 2 3答案:C
解析:用浓盐酸和MnO 制取Cl 的反应为MnO +4HCl(浓)=====MnCl +Cl↑+
2 2 2 2 2
2HO,氯气中含有挥发出的HCl,可用饱和NaCl溶液吸收挥发出的HCl,达到净化氯气的
2
目的,A正确;Cl 和KOH在加热条件下反应生成KClO ,其离子方程式为3Cl +6OH-
2 3 2
=====ClO+5Cl-+3HO,B正确;若取少量无色溶液a于试管中,滴加稀HSO 后,发生
2 2 4
的反应为ClO+6I-+6H+===3I +Cl-+3HO,溶液呈黄色,C错误;根据B项分析可得碱
2 2
性条件下氧化性:Cl >KClO ,酸性条件下KClO 和HCl反应生成氯气,因此酸性条件下
2 3 3
氧化性:Cl<KClO,D正确。
2 3
9.[2024·龙岩联考] 中学常见的某反应化学方程式为X+Y―→M+N+HO(未配平,
2
反应条件已略去),下列叙述错误的是( )
A.若X、Y的物质的量之比为1∶4,且N是黄绿色气体,则该反应的离子方程式为
MnO +4H++2Cl-===Mn2++Cl↑+2HO
2 2 2
B.当N为氯碱工业的主要原料,M是造成温室效应的主要气体,则上述反应的离子
方程式一定为:CO+2H+===CO ↑+HO
2 2
C.若X是铁,Y是稀硝酸(过量),则X 与Y 反应的离子方程式为Fe+4H++
NO===Fe3++NO↑+2HO
2
D.若M、N为气体,且都能使澄清石灰水变浑浊,则将此混合气体通入溴水中,橙
色褪色,橙色褪色过程的离子方程式为SO +Br +2HO===4H++SO+2Br-
2 2 2
答案:B
解析:B中N为氯碱工业的主要原料,则N为NaCl,M是造成温室效应的主要气体,
M为CO ,应该是碳酸钠或碳酸氢钠与盐酸反应,如果是碳酸氢钠与盐酸反应,离子方程
2
式中应该是碳酸氢根,故B错误。
10.[2024·兰州市高三诊断考试]海洋中有丰富的食品、矿产、能源、药物和水产等资源,
下列说法正确的是( )
A.氯碱工业制碱的离子方程式:2Na++2Cl- +2HO=====H↑+Cl↑+2NaOH
2 2 2
B.第③步的反应可在直接加热的条件下实现
C.第⑤步、第⑥步中试剂分别可以选用SO 水溶液和稀硫酸
2
D.第②步中精盐水溶液中应先通入NH ,再通入CO
3 2
答案:D
解析:氯碱工业是指电解饱和 NaCl 溶液的工业,其反应的离子方程式为 2Cl-+
2HO=====Cl↑+H↑+2OH-,A项错误;MgCl 水解生成Mg(OH) 和HCl,直接加
2 2 2 2 2
热 HCl 挥发,促进水解平衡正向移动,无法得到无水 MgCl ,需在 HCl 气流中加热
2
MgCl ·6H O以抑制MgCl 的水解,B项错误;第⑤步中选用二氧化硫水溶液,其与溴水反
2 2 2
应生成硫酸和HBr,第⑥步中需通入氯气氧化HBr生成单质溴,不能使用稀硫酸,C项错
误;由于NH 的溶解度较大,CO 的溶解度较小,因此第②步中精盐水溶液中应先通入
3 2
NH ,形成氨的饱和NaCl溶液,再通入CO,D项正确。
3 2
11.[2024·浙江1月]工业上将Cl 通入冷的NaOH溶液中制得漂白液,下列说法不正确
2
的是( )A.漂白液的有效成分是NaClO
B.ClO-水解生成HClO使漂白液呈酸性
C.通入CO 后的漂白液消毒能力增强
2
D.NaClO溶液比HClO溶液稳定
答案:B
解析:NaClO水解生成的HClO具有漂白性,是漂白液的有效成分,A项正确;ClO-
水解的方程式为ClO-+H
2
O⇌HClO+OH-,漂白液呈碱性,B项错误;通入CO
2
后发生反
应:NaClO+CO +HO===NaHCO +HClO,HClO浓度增大,且HClO的氧化性更强,故
2 2 3
漂白液的消毒能力增强,C项正确;次氯酸不稳定,在光照条件下易分解,所以热稳定性:
NaClO>HClO,D项正确。
12.[2024·河北邯郸质检]ClO 是一种黄绿色、易溶于水的气体,是高效、低毒的消毒剂。
2
实验室以NH Cl溶液、盐酸和NaClO 溶液为原料,按照以下流程制取ClO ,下列说法正
4 2 2
确的是( )
A.电解时,阳极反应式为
NH+3Cl--6e-===NCl +4H+
3
B.电解过程中,混合溶液的pH逐渐减小
C.可用碱石灰除去ClO 中的NH
2 3
D.向溶液X中滴加AgNO 溶液,观察到沉淀生成,说明X中含有Cl-
3
答案:A
解析:电解时,Cl-在阳极放电生成NCl ,电极反应式为NH+3Cl--6e-===NCl +
3 3
4H+,A正确;电解过程的总化学方程式为NH Cl+2HCl=====NCl +3H↑,混合溶液的
4 3 2
pH逐渐增大,B错误;碱石灰不能除去NH ,C错误;向NCl 溶液中加入NaClO 溶液,
3 3 2
根据流程可知反应的化学方程式为6NaClO +NCl +3HO===6ClO ↑+NH ↑+3NaCl+
2 3 2 2 3
3NaOH,则溶液X中的主要溶质为NaCl和NaOH,所以检验其中所含Cl-时应先加HNO
3
酸化以除掉OH-,D错误。