文档内容
2019年广西桂林市中考化学试卷
一、选择题(共20小题.每小题2分,共40分.每小题只有一个选项符合题意)请将答案写在答题卡上.
1.(2分)垃圾分类回收是绿色新时尚,矿泉水瓶可归为( )
A.厨余垃圾 B.有害垃圾 C.其他垃圾 D.可回收垃圾
2.(2分)下列变化过程中,一定存在化学变化的是( )
A.木条折断 B.木条燃烧 C.玻璃破碎 D.石蜡融化
3.(2分)下列仪器中,可用于准确量取一定体积液体的是( )
A.量筒 B.试管 C.集气瓶 D.锥形瓶
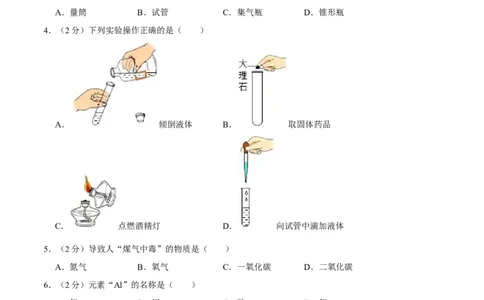
4.(2分)下列实验操作正确的是( )
A. 倾倒液体 B. 取固体药品
C. 点燃酒精灯 D. 向试管中滴加液体
5.(2分)导致人“煤气中毒”的物质是( )
A.氮气 B.氧气 C.一氧化碳 D.二氧化碳
6.(2分)元素“Al”的名称是( )
A.氯 B.铝 C.硅 D.氦
7.(2分)已知K O中O元素的化合价为﹣2,则K元素的化合价是( )
2
A.﹣1 B.0 C.+1 D.+2
8.(2分)下列物质能在纯氧中剧烈燃烧,火星四射的是( )
A.铁丝 B.红磷 C.氢气 D.蜡烛
9.(2分)下列物质不能用于实验室制取氧气的是( )
A.KMnO B.KClO C.KCl D.H O
4 3 2 2
第 1 页 / 共 7 页10.(2分)下列物品不是由有机合成材料制成的是( )
A.金戒指 B.塑料桶 C.人造羊毛毯 D.合成橡胶管
11.(2分)俗称“纯碱”的物质是( )
A.H SO B.HCl C.Na CO D.Cu(OH)
2 4 2 3 2
12.(2分)下列物质由阴阳离子构成的是( )
A.铜 B.氧气 C.金刚石 D.氯化钠
13.(2分)下列方法可将海水转化为淡水的是( )
A.蒸馏 B.静置 C.过滤 D.消毒
14.(2分)下列做法错误的是( )
A.加油站内严禁烟火
B.电器起火应立即用水灭火
C.炒菜时油锅起火可盖上锅盖灭火
D.发现火情应及时拨打119
15.(2分)下列关于物质用途的说法,错误的是( )
A.工业酒精可用于配制饮用酒
B.活性炭可用于防毒面具
C.氮气可用于制氮肥
D.食盐可用作调味品
16.(2分)如图所示的四种物质中,碱性最强的是( )
A.陈醋 B.橙汁 C.纯净水 D.肥皂水
17.(2分)《吕氏春秋》记载“金(即铜单质)柔锡(即锡单质)柔,合两柔则刚(即坚硬)”。这句话说明合金具
有的特性是( )
A.合金的熔点一般比其组分低
B.合金的硬度一般比其组分大
C.合金的抗腐蚀性一般比其组分强
D.合金的耐磨性一般比其组分好
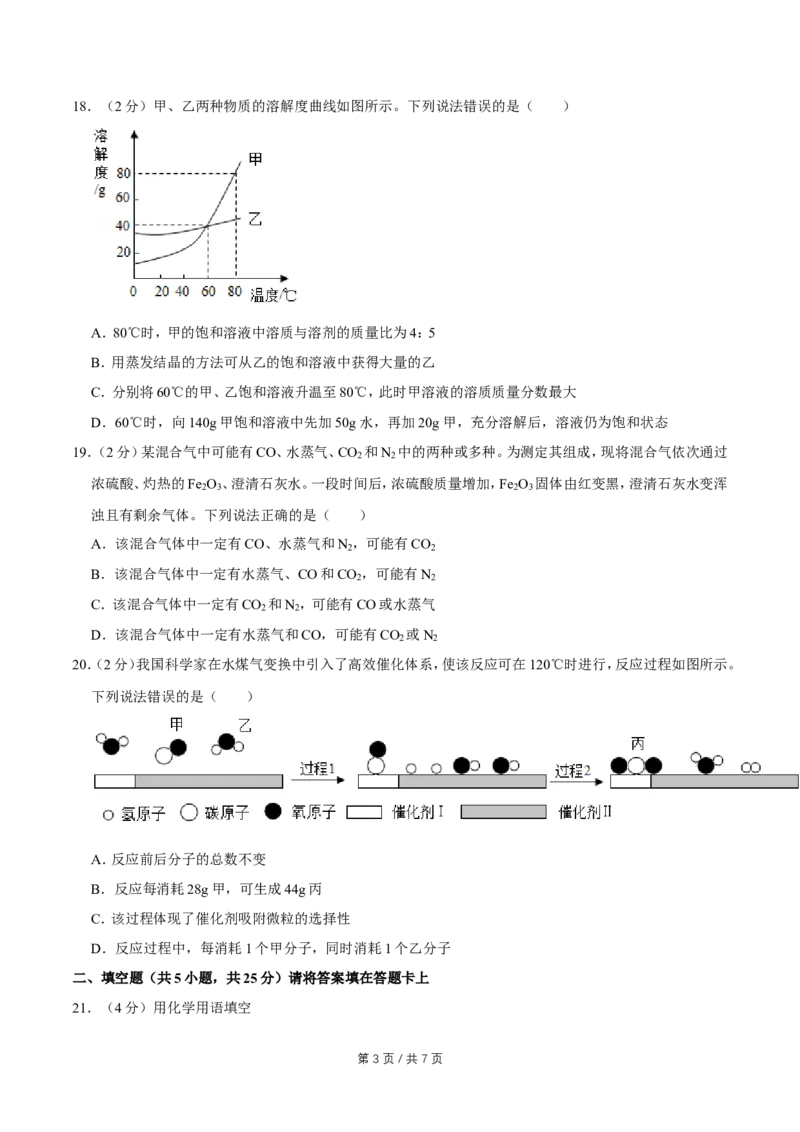
第 2 页 / 共 7 页18.(2分)甲、乙两种物质的溶解度曲线如图所示。下列说法错误的是( )
A.80℃时,甲的饱和溶液中溶质与溶剂的质量比为4:5
B.用蒸发结晶的方法可从乙的饱和溶液中获得大量的乙
C.分别将60℃的甲、乙饱和溶液升温至80℃,此时甲溶液的溶质质量分数最大
D.60℃时,向140g甲饱和溶液中先加50g水,再加20g甲,充分溶解后,溶液仍为饱和状态
19.(2分)某混合气中可能有CO、水蒸气、CO 和N 中的两种或多种。为测定其组成,现将混合气依次通过
2 2
浓硫酸、灼热的Fe O 、澄清石灰水。一段时间后,浓硫酸质量增加,Fe O 固体由红变黑,澄清石灰水变浑
2 3 2 3
浊且有剩余气体。下列说法正确的是( )
A.该混合气体中一定有CO、水蒸气和N ,可能有CO
2 2
B.该混合气体中一定有水蒸气、CO和CO ,可能有N
2 2
C.该混合气体中一定有CO 和N ,可能有CO或水蒸气
2 2
D.该混合气体中一定有水蒸气和CO,可能有CO 或N
2 2
20.(2分)我国科学家在水煤气变换中引入了高效催化体系,使该反应可在120℃时进行,反应过程如图所示。
下列说法错误的是( )
A.反应前后分子的总数不变
B.反应每消耗28g甲,可生成44g丙
C.该过程体现了催化剂吸附微粒的选择性
D.反应过程中,每消耗1个甲分子,同时消耗1个乙分子
二、填空题(共5小题,共25分)请将答案填在答题卡上
21.(4分)用化学用语填空
第 3 页 / 共 7 页(1)磷元素 。
(2)3个氮原子 。
(3)钠离子 。
(4)二氧化硫分子 。
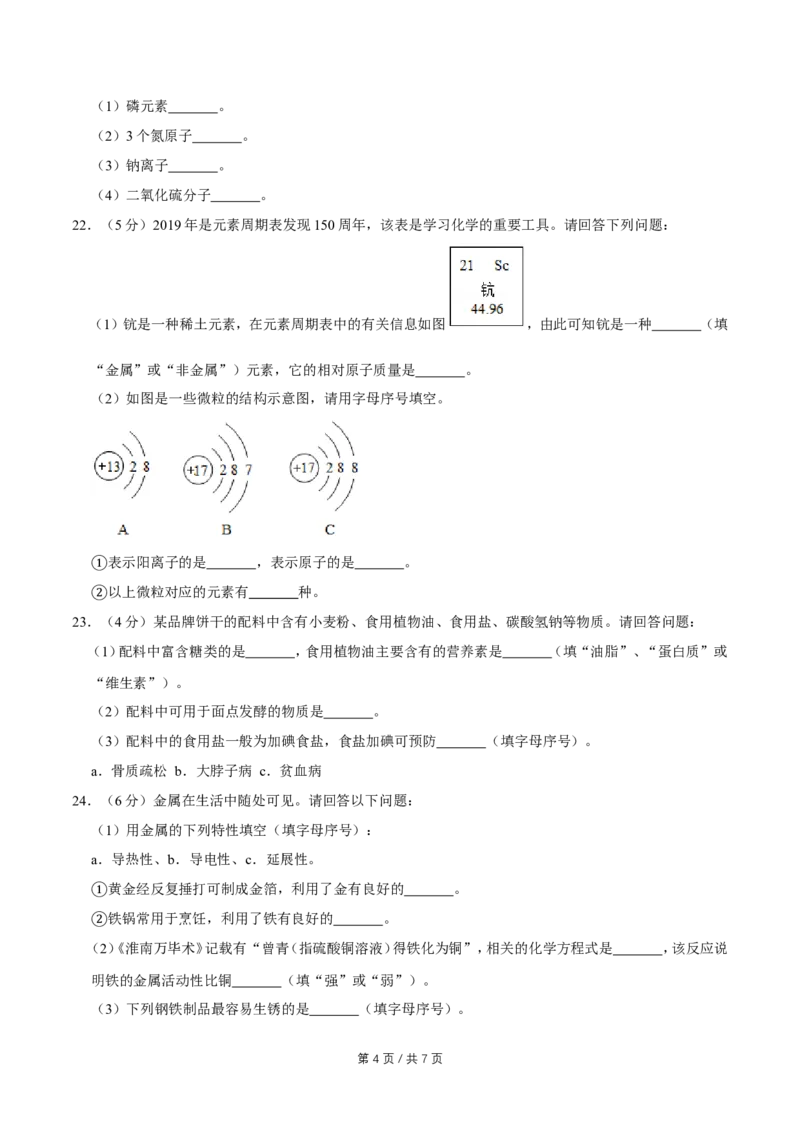
22.(5分)2019年是元素周期表发现150周年,该表是学习化学的重要工具。请回答下列问题:
(1)钪是一种稀土元素,在元素周期表中的有关信息如图 ,由此可知钪是一种 (填
“金属”或“非金属”)元素,它的相对原子质量是 。
(2)如图是一些微粒的结构示意图,请用字母序号填空。
表示阳离子的是 ,表示原子的是 。
①以上微粒对应的元素有 种。
23.②(4分)某品牌饼干的配料中含有小麦粉、食用植物油、食用盐、碳酸氢钠等物质。请回答问题:
(1)配料中富含糖类的是 ,食用植物油主要含有的营养素是 (填“油脂”、“蛋白质”或
“维生素”)。
(2)配料中可用于面点发酵的物质是 。
(3)配料中的食用盐一般为加碘食盐,食盐加碘可预防 (填字母序号)。
a.骨质疏松 b.大脖子病 c.贫血病
24.(6分)金属在生活中随处可见。请回答以下问题:
(1)用金属的下列特性填空(填字母序号):
a.导热性、b.导电性、c.延展性。
黄金经反复捶打可制成金箔,利用了金有良好的 。
①铁锅常用于烹饪,利用了铁有良好的 。
(②2)《淮南万毕术》记载有“曾青(指硫酸铜溶液)得铁化为铜”,相关的化学方程式是 ,该反应说
明铁的金属活动性比铜 (填“强”或“弱”)。
(3)下列钢铁制品最容易生锈的是 (填字母序号)。
第 4 页 / 共 7 页a.不锈钢杯子 b.涂油的自行车链条 c.切酸菜后没有洗干净的菜刀
25.(6分)含碳物质种类繁多。请回答下列问题:
(1)葡萄糖(C H O )中C、H、O原子的数目之比是 。
6 12 6
(2)石墨烯和金刚石均为碳单质,但导电性差异很大,原因是 (填字母序号)。
a.原子的排列方式不同 b.原子在不断运动 c.原子的体积很小
(3)乙醇(C H OH)是 (填“可再生”或“不可再生”)能源,乙醇完成燃烧的化学方程式是
2 5
。该反应中,化学能转变为 能。
三、简答题(共2小题,共13分)请将答案写在答题卡上.
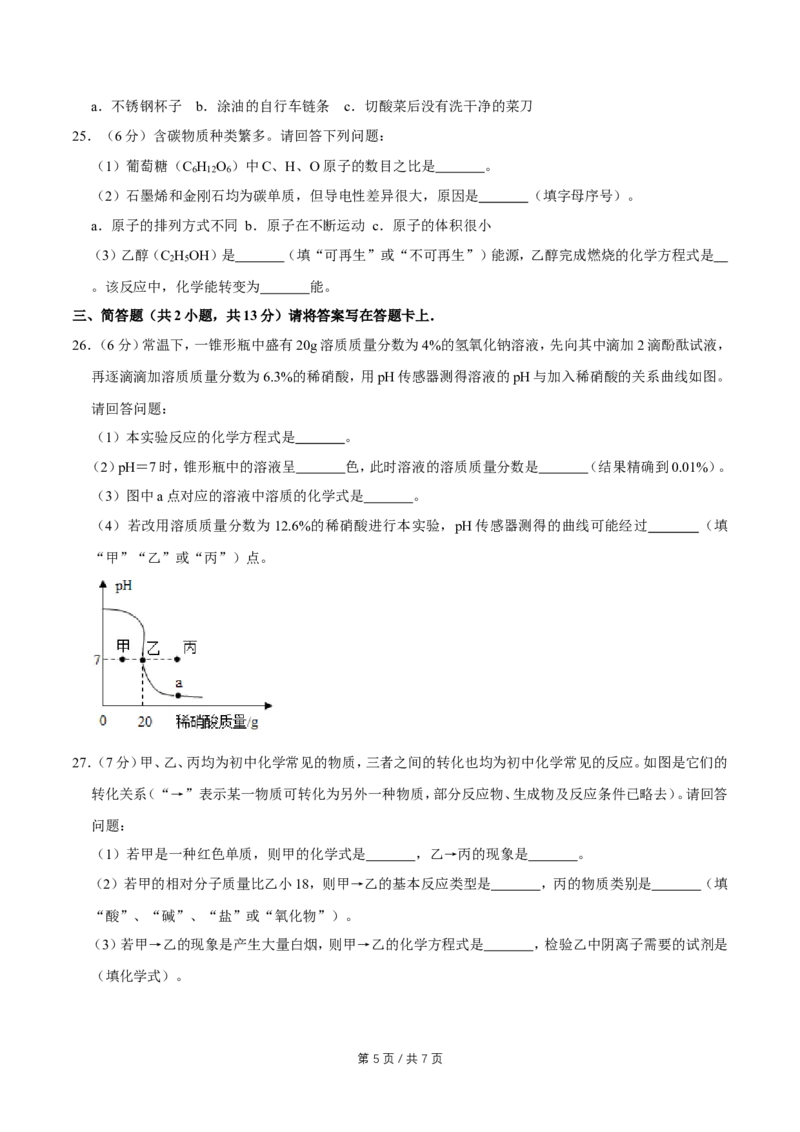
26.(6分)常温下,一锥形瓶中盛有20g溶质质量分数为4%的氢氧化钠溶液,先向其中滴加2滴酚酞试液,
再逐滴滴加溶质质量分数为6.3%的稀硝酸,用pH传感器测得溶液的pH与加入稀硝酸的关系曲线如图。
请回答问题:
(1)本实验反应的化学方程式是 。
(2)pH=7时,锥形瓶中的溶液呈 色,此时溶液的溶质质量分数是 (结果精确到0.01%)。
(3)图中a点对应的溶液中溶质的化学式是 。
(4)若改用溶质质量分数为12.6%的稀硝酸进行本实验,pH传感器测得的曲线可能经过 (填
“甲”“乙”或“丙”)点。
27.(7分)甲、乙、丙均为初中化学常见的物质,三者之间的转化也均为初中化学常见的反应。如图是它们的
转化关系(“→”表示某一物质可转化为另外一种物质,部分反应物、生成物及反应条件已略去)。请回答
问题:
(1)若甲是一种红色单质,则甲的化学式是 ,乙→丙的现象是 。
(2)若甲的相对分子质量比乙小18,则甲→乙的基本反应类型是 ,丙的物质类别是 (填
“酸”、“碱”、“盐”或“氧化物”)。
(3)若甲→乙的现象是产生大量白烟,则甲→乙的化学方程式是 ,检验乙中阴离子需要的试剂是
(填化学式)。
第 5 页 / 共 7 页四、实验探究题(共2小题,共16分)请将答案填在答题卡上
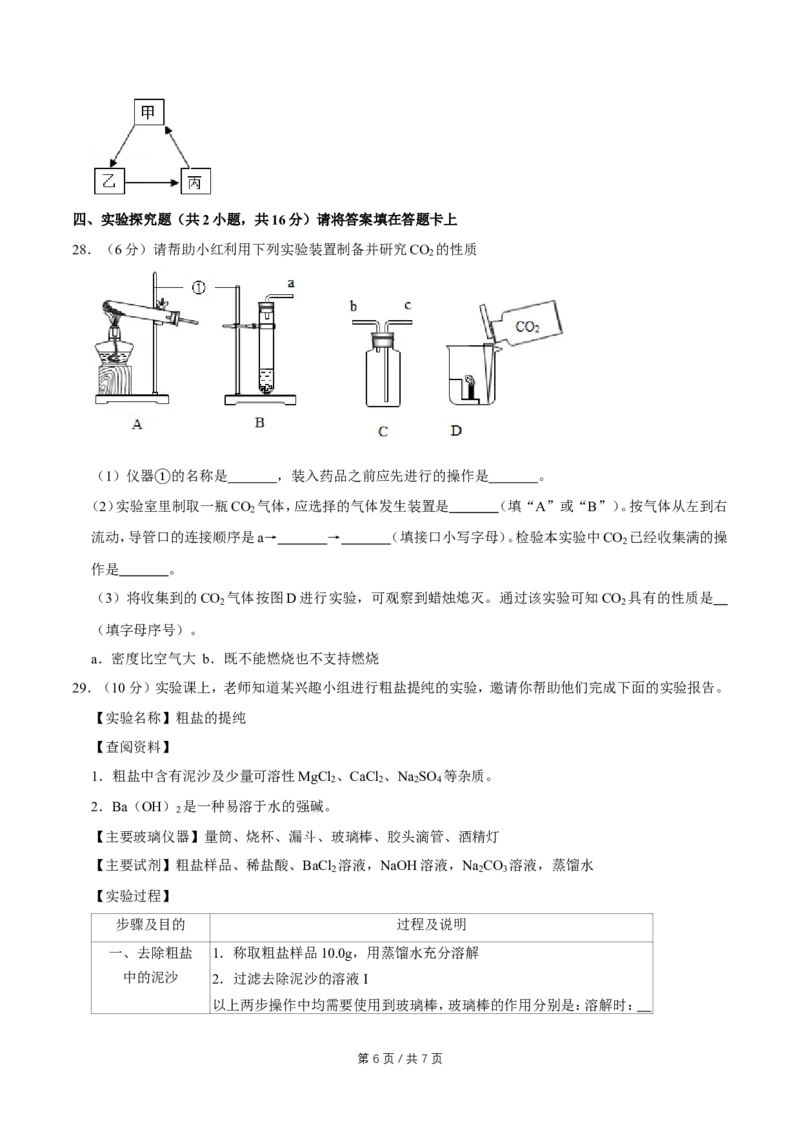
28.(6分)请帮助小红利用下列实验装置制备并研究CO 的性质
2
(1)仪器 的名称是 ,装入药品之前应先进行的操作是 。
(2)实验室①里制取一瓶CO
2
气体,应选择的气体发生装置是 (填“A”或“B”)。按气体从左到右
流动,导管口的连接顺序是a→ → (填接口小写字母)。检验本实验中CO 已经收集满的操
2
作是 。
(3)将收集到的CO 气体按图D进行实验,可观察到蜡烛熄灭。通过该实验可知CO 具有的性质是
2 2
(填字母序号)。
a.密度比空气大 b.既不能燃烧也不支持燃烧
29.(10分)实验课上,老师知道某兴趣小组进行粗盐提纯的实验,邀请你帮助他们完成下面的实验报告。
【实验名称】粗盐的提纯
【查阅资料】
1.粗盐中含有泥沙及少量可溶性MgCl 、CaCl 、Na SO 等杂质。
2 2 2 4
2.Ba(OH) 是一种易溶于水的强碱。
2
【主要玻璃仪器】量筒、烧杯、漏斗、玻璃棒、胶头滴管、酒精灯
【主要试剂】粗盐样品、稀盐酸、BaCl 溶液,NaOH溶液,Na CO 溶液,蒸馏水
2 2 3
【实验过程】
步骤及目的 过程及说明
一、去除粗盐 1.称取粗盐样品10.0g,用蒸馏水充分溶解
中的泥沙 2.过滤去除泥沙的溶液I
以上两步操作中均需要使用到玻璃棒,玻璃棒的作用分别是:溶解时:
第 6 页 / 共 7 页;过滤时: 。
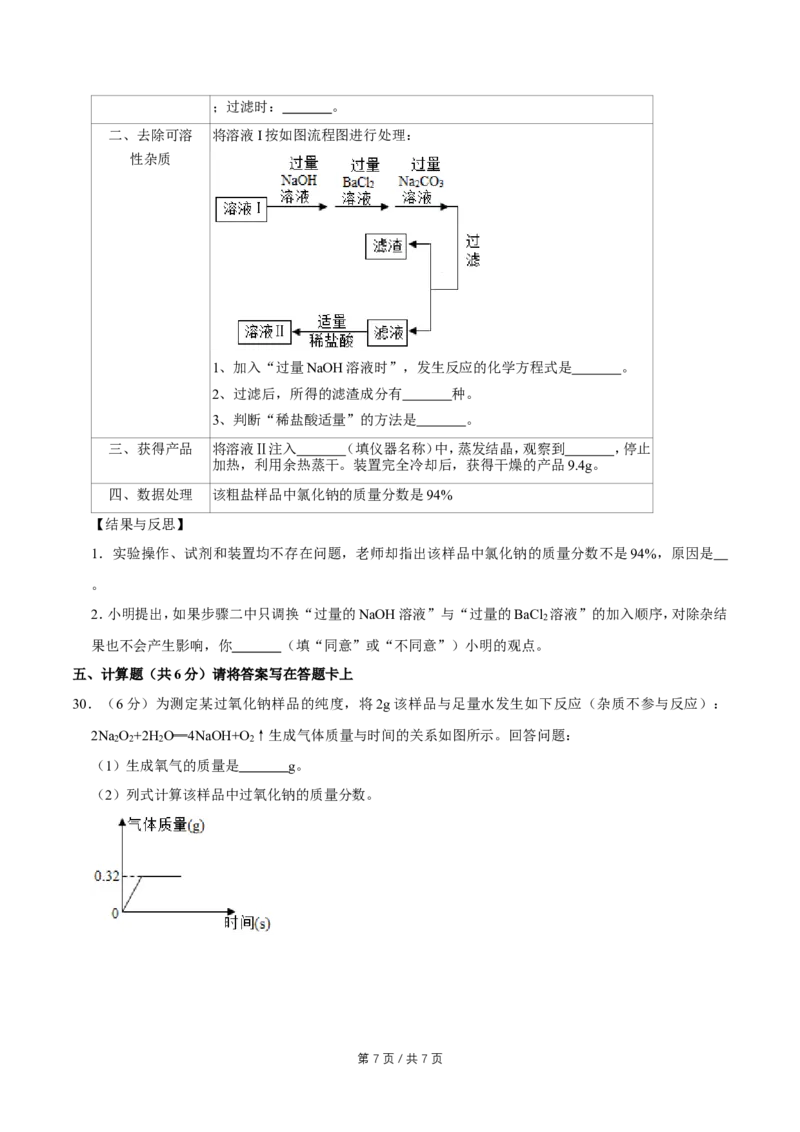
二、去除可溶 将溶液I按如图流程图进行处理:
性杂质
1、加入“过量NaOH溶液时”,发生反应的化学方程式是 。
2、过滤后,所得的滤渣成分有 种。
3、判断“稀盐酸适量”的方法是 。
三、获得产品 将溶液Ⅱ注入 (填仪器名称)中,蒸发结晶,观察到 ,停止
加热,利用余热蒸干。装置完全冷却后,获得干燥的产品9.4g。
四、数据处理 该粗盐样品中氯化钠的质量分数是94%
【结果与反思】
1.实验操作、试剂和装置均不存在问题,老师却指出该样品中氯化钠的质量分数不是94%,原因是
。
2.小明提出,如果步骤二中只调换“过量的NaOH溶液”与“过量的BaCl 溶液”的加入顺序,对除杂结
2
果也不会产生影响,你 (填“同意”或“不同意”)小明的观点。
五、计算题(共6分)请将答案写在答题卡上
30.(6分)为测定某过氧化钠样品的纯度,将2g该样品与足量水发生如下反应(杂质不参与反应):
2Na O +2H O═4NaOH+O ↑生成气体质量与时间的关系如图所示。回答问题:
2 2 2 2
(1)生成氧气的质量是 g。
(2)列式计算该样品中过氧化钠的质量分数。
第 7 页 / 共 7 页