文档内容
2011年高考理科综合(四川卷)化学试题
1.(2011四川高考)下列“化学与生活”的说法不正确的是
A.硫酸钡可用钡餐透视
B.盐卤可用于制豆腐
C.明矾可用于水的消毒,杀菌
D.醋可用于除去暖水瓶中的水垢
2.(2011四川高考)下列推论正确的
A.SiH 的沸点高于CH,可推测pH 的沸点高于NH
4 4 3 3
B.NH+ 为正四面体,可推测出PH+也为正四面题结构
4 4
C.CO 晶体是分子晶体,可推测SiO 晶体也是分子晶体,
2 2
D.CH 是碳链为直线型的非极性分子,可推测CH 也是碳链为直线型的非极性分子
2 6 3 8
3.(2011四川高考)下列说法正确的是:
A.分子晶体中一定存在分子间作用力,不一定存在共价键
B.分子中含两个氢原子的酸一定是二元酸
C.含有金属离子的晶体一定是离子晶体
D.元素的非金属型越强,其单质的活泼性一定越强
4.(2011四川高考)25 ℃在等体积的①pH=0的HSO 溶液,②0.05 mol·L-1的Ba(OH)
2 4 2
溶液,③pH = 10的NaS溶液,④pH=5的NHNO 溶液中,发生电离的水的物质的量之比是
2 4 3
( )
A.1∶10∶1010∶109 B.1∶5∶5×109∶5×109
C.1∶20∶1010∶109 D.1∶10 ∶104∶109
5.(2011四川高考)甲、乙、丙、丁四种易学溶于水的物质,分别由NH + 、Ba2+、Mg2
4
+、H+、OH-、Cl-、HCO - 、SO2-中的不同阳离子和阴离子各一种组成,已知:①将甲溶
3 4
液分别与其他三种物质的溶液混合,均有白色沉淀生成;②0.1 mol/l乙溶液中c(H+)>
0.1 mol/l;③向丙容器中滴入AgNO 溶液又不溶于稀HNO 的白色沉淀生成,下列结论不正
3 3
确的是
A.甲溶液含有Ba2+
B.乙溶液含有SO2-
4
C.丙溶液含有Cl-
B.丁溶液含有Mg2+
6.(2011四川高考)下列实验“操作和现象”与“结论”对应关系正确的是
操作和现象 结论
A 向装有Fe(NO) 溶液的试管中加入稀HSO ,在管口 HNO 分解成了NO
3 2 2 4 3 2
观察到红棕色气体
B 向淀粉溶液中加入稀HSO ,加热几分钟,冷却后再 淀粉没有水解成葡萄糖
2 4
加入新制Cu(OH) 浊液,加热,没有红色沉淀生成
2
C 向无水乙醇中加入浓 HSO ,加热至170°C产生的 使溶液褪色的气体是乙烯
2 4
气体通入酸性KmnO 溶液,红色褪去
4
D 向饱和NaCO 中通入足量CO 溶液变浑浊 析出了NaHCO
2 3 2 3
7.(2011四川高考)25°C和101kpa时,乙烷、乙炔和丙烯组成的混合烃 32 mL与过量
氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体的总体积缩小了 72
mL,原混合烃中乙炔的体积分数为
A.12.5% B.25% C.50% D.75%
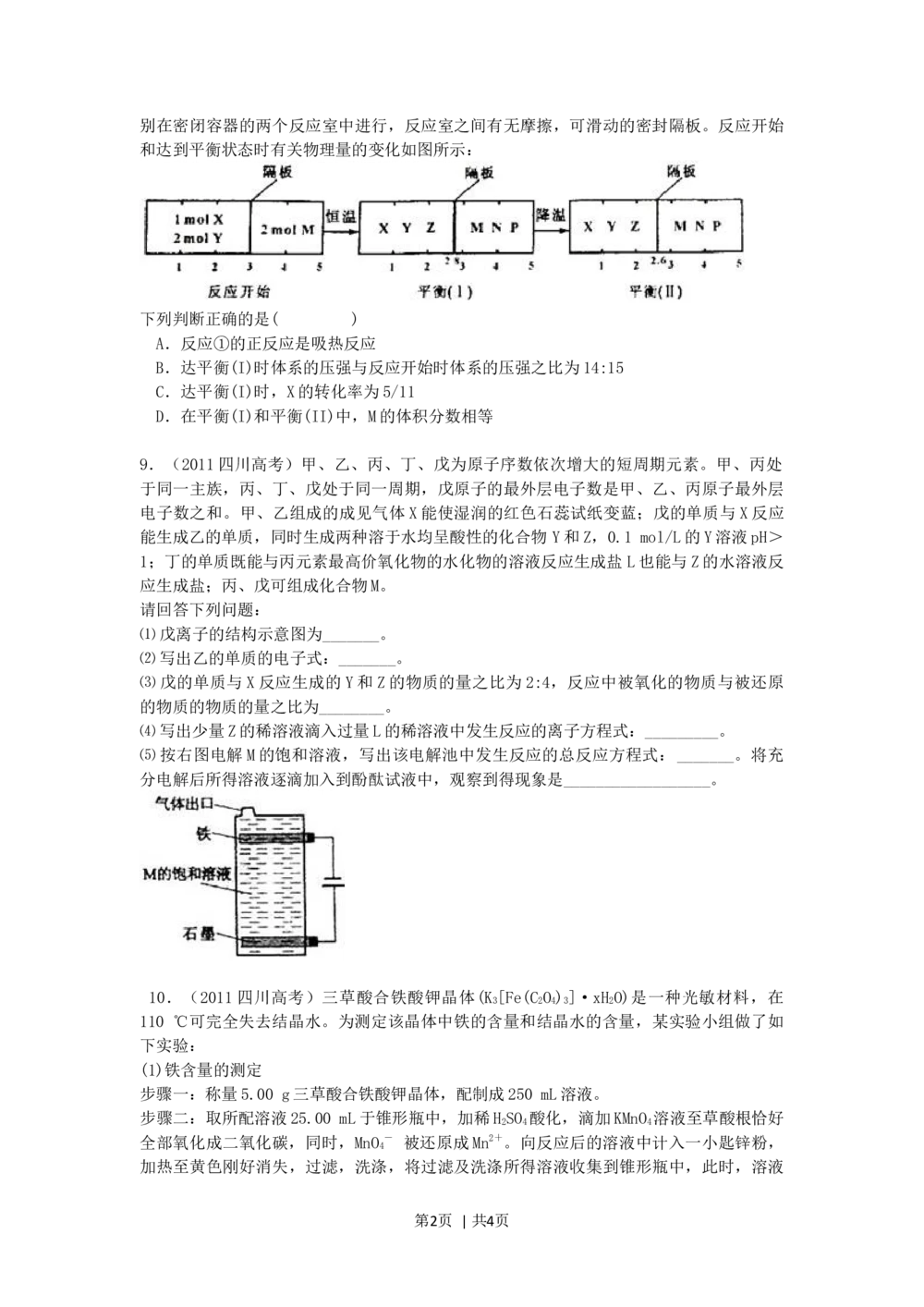
8.(2011四川高考)可逆反应①X(g)+2Y(g ) 2Z(g) 、②M(g) N(g)+p(g)分
第1页 | 共4页别在密闭容器的两个反应室中进行,反应室之间有无摩擦,可滑动的密封隔板。反应开始
和达到平衡状态时有关物理量的变化如图所示:
下列判断正确的是( )
A.反应①的正反应是吸热反应
B.达平衡(I)时体系的压强与反应开始时体系的压强之比为14:15
C.达平衡(I)时,X的转化率为5/11
D.在平衡(I)和平衡(II)中,M的体积分数相等
9.(2011四川高考)甲、乙、丙、丁、戊为原子序数依次增大的短周期元素。甲、丙处
于同一主族,丙、丁、戊处于同一周期,戊原子的最外层电子数是甲、乙、丙原子最外层
电子数之和。甲、乙组成的成见气体X能使湿润的红色石蕊试纸变蓝;戊的单质与X反应
能生成乙的单质,同时生成两种溶于水均呈酸性的化合物 Y和Z,0.1 mol/L的Y溶液pH>
1;丁的单质既能与丙元素最高价氧化物的水化物的溶液反应生成盐L也能与Z的水溶液反
应生成盐;丙、戊可组成化合物M。
请回答下列问题:
⑴戊离子的结构示意图为_______。
⑵写出乙的单质的电子式:_______。
⑶戊的单质与X反应生成的Y和Z的物质的量之比为2:4,反应中被氧化的物质与被还原
的物质的物质的量之比为________。
⑷写出少量Z的稀溶液滴入过量L的稀溶液中发生反应的离子方程式:_________。
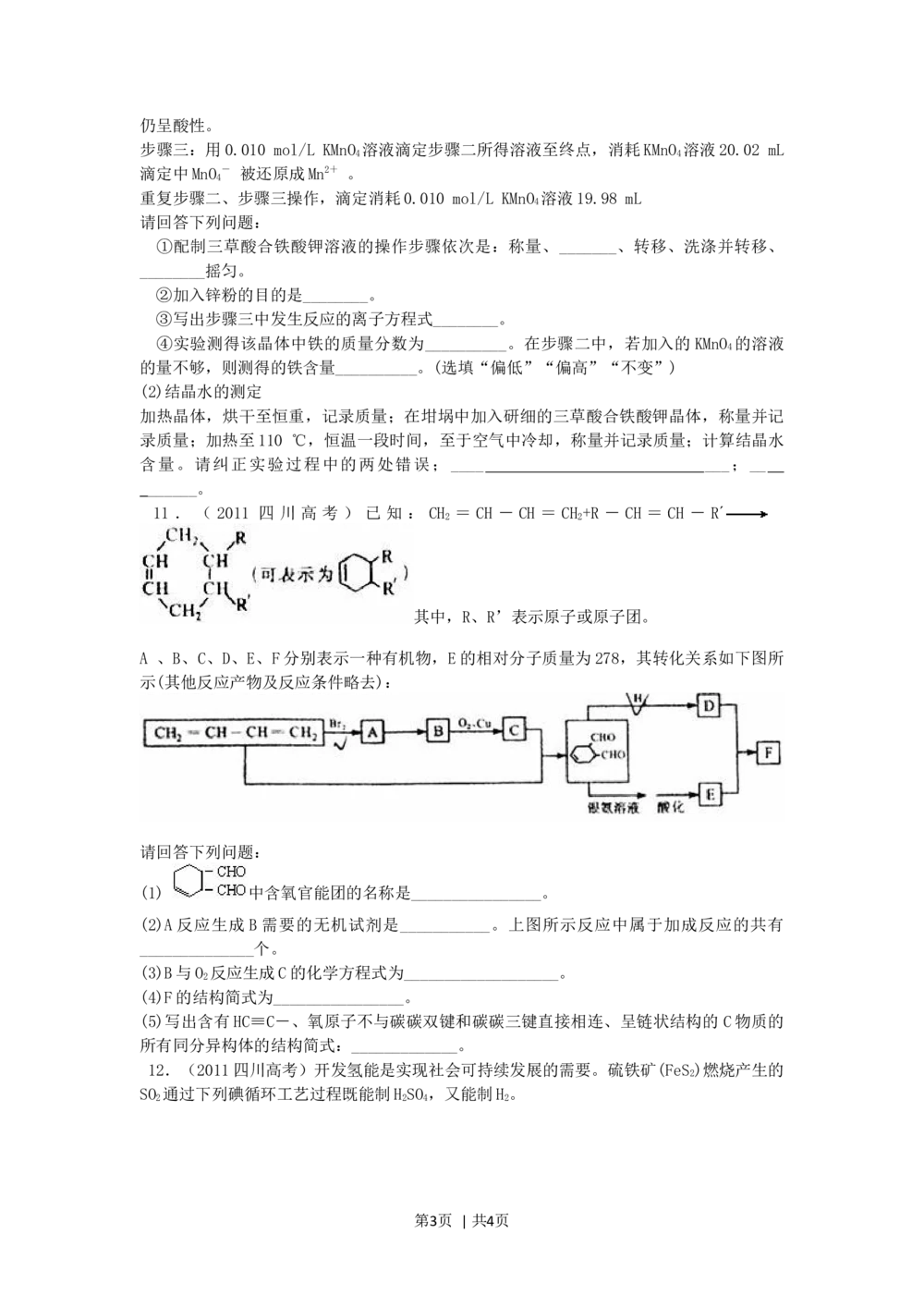
⑸按右图电解M的饱和溶液,写出该电解池中发生反应的总反应方程式:_______。将充
分电解后所得溶液逐滴加入到酚酞试液中,观察到得现象是__________________。
10.(2011四川高考)三草酸合铁酸钾晶体(K[Fe(CO)]·xHO)是一种光敏材料,在
3 2 4 3 2
110 ℃可完全失去结晶水。为测定该晶体中铁的含量和结晶水的含量,某实验小组做了如
下实验:
(1)铁含量的测定
步骤一:称量5.00 g三草酸合铁酸钾晶体,配制成250 mL溶液。
步骤二:取所配溶液25.00 mL于锥形瓶中,加稀HSO 酸化,滴加KMnO 溶液至草酸根恰好
2 4 4
全部氧化成二氧化碳,同时,MnO - 被还原成Mn2+。向反应后的溶液中计入一小匙锌粉,
4
加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液
第2页 | 共4页仍呈酸性。
步骤三:用0.010 mol/L KMnO 溶液滴定步骤二所得溶液至终点,消耗KMnO 溶液20.02 mL
4 4
滴定中MnO- 被还原成Mn2+ 。
4
重复步骤二、步骤三操作,滴定消耗0.010 mol/L KMnO 溶液19.98 mL
4
请回答下列问题:
①配制三草酸合铁酸钾溶液的操作步骤依次是:称量、_______、转移、洗涤并转移、
________摇匀。
②加入锌粉的目的是________。
③写出步骤三中发生反应的离子方程式________。
④实验测得该晶体中铁的质量分数为__________。在步骤二中,若加入的KMnO 的溶液
4
的量不够,则测得的铁含量__________。(选填“偏低”“偏高”“不变”)
(2)结晶水的测定
加热晶体,烘干至恒重,记录质量;在坩埚中加入研细的三草酸合铁酸钾晶体,称量并记
录质量;加热至110 ℃,恒温一段时间,至于空气中冷却,称量并记录质量;计算结晶水
含量。请纠正实验过程中的两处错误;____ ___;__
_______。
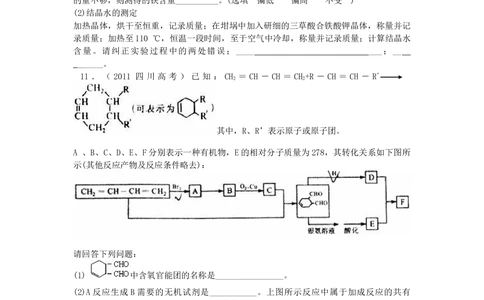
11 . ( 2011 四 川 高 考 ) 已 知 : CH = CH - CH = CH+R - CH = CH - R´
2 2
其中,R、R’表示原子或原子团。
A 、B、C、D、E、F分别表示一种有机物,E的相对分子质量为278,其转化关系如下图所
示(其他反应产物及反应条件略去):
请回答下列问题:
(1) 中含氧官能团的名称是________________。
(2)A反应生成B需要的无机试剂是___________。上图所示反应中属于加成反应的共有
______________个。
(3)B与O 反应生成C的化学方程式为___________________。
2
(4)F的结构简式为________________。
(5)写出含有HC≡C-、氧原子不与碳碳双键和碳碳三键直接相连、呈链状结构的 C物质的
所有同分异构体的结构简式:_____________。
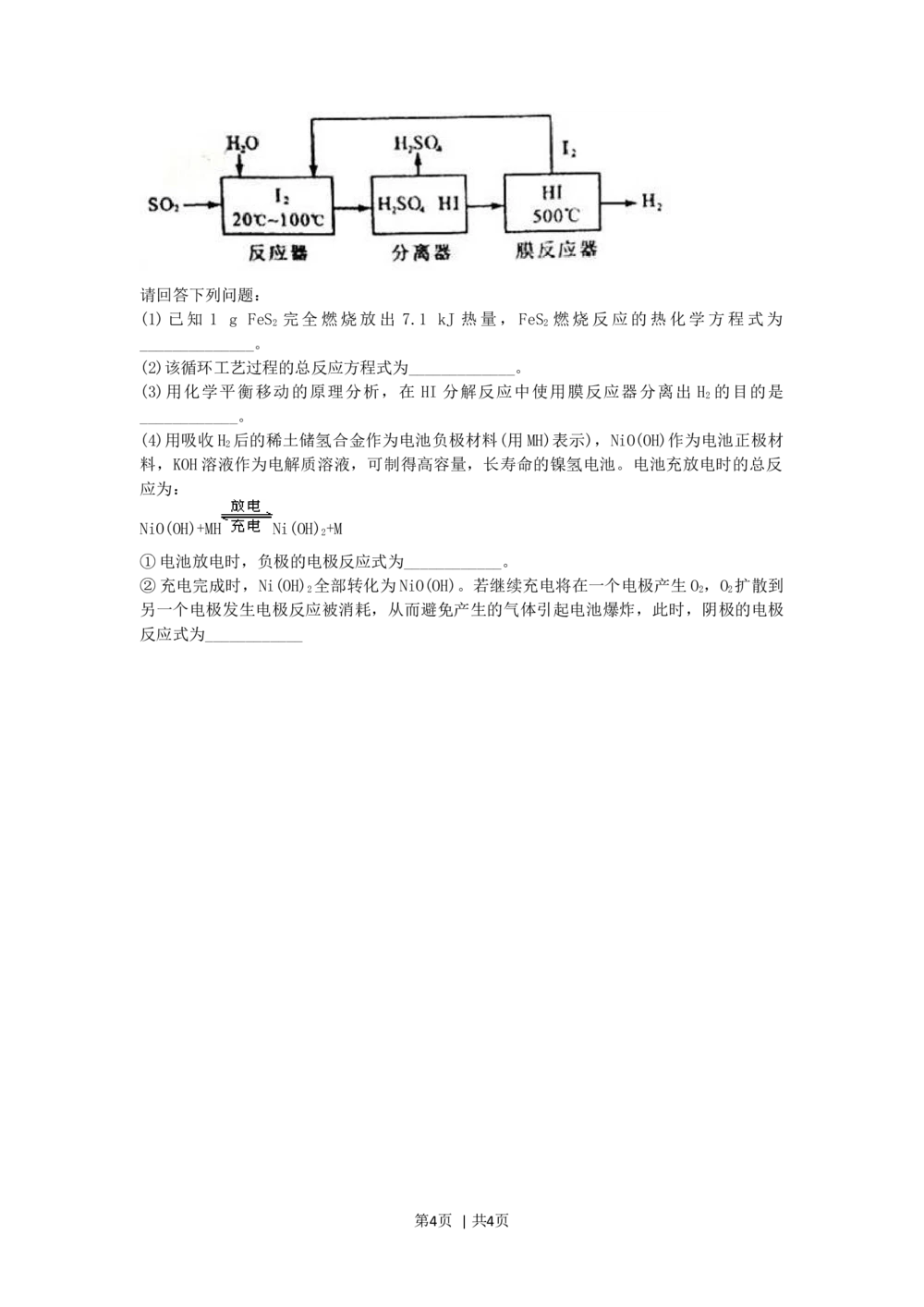
12.(2011四川高考)开发氢能是实现社会可持续发展的需要。硫铁矿(FeS)燃烧产生的
2
SO 通过下列碘循环工艺过程既能制HSO,又能制H。
2 2 4 2
第3页 | 共4页请回答下列问题:
(1)已知 1 g FeS 完全燃烧放出 7.1 kJ 热量,FeS 燃烧反应的热化学方程式为
2 2
______________。
(2)该循环工艺过程的总反应方程式为_____________。
(3)用化学平衡移动的原理分析,在 HI 分解反应中使用膜反应器分离出 H 的目的是
2
____________。
(4)用吸收H 后的稀土储氢合金作为电池负极材料(用MH)表示),NiO(OH)作为电池正极材
2
料,KOH溶液作为电解质溶液,可制得高容量,长寿命的镍氢电池。电池充放电时的总反
应为:
NiO(OH)+MH Ni(OH)+M
2
①电池放电时,负极的电极反应式为____________。
②充电完成时,Ni(OH) 全部转化为NiO(OH)。若继续充电将在一个电极产生O ,O 扩散到
2 2 2
另一个电极发生电极反应被消耗,从而避免产生的气体引起电池爆炸,此时,阴极的电极
反应式为____________
第4页 | 共4页